水提法生产左旋多巴的工艺研究及优化*
2021-12-03李学坚银江林袁经权赵小超黎永红张雯艳张桂珍
李学坚,银江林,袁经权**,苏 健,赵小超,黎永红,黄 艳,张雯艳,张桂珍
(1.广西中医药大学科学实验中心,广西南宁 530222;2.那坡康正天然植物提取有限责任公司,广西百色 533900;3.广西壮族自治区中医药研究院,广西南宁 530022)
0 引言
左旋多巴(L-dopa)收载于世界各国药典,在帕金森综合症的临床治疗中起十分重要的作用[1]。1961年Birkmayer发现L-dopa有抗帕金森综合症作用[2],1968年美国食品药品监督管理局(FDA)批准应用于临床,1973年上市销售,市场需求日渐增长。L-dopa的生产途径有化学合成法、生物酶催化法、生物发酵法和植物提取法。化学合成法因L-dopa和D-dopa手性拆分技术难度大,成本高,仅有欧洲、日本等发达国家采用;生物酶催化法和生物发酵法因技术不成熟,产量低,目前没有量产;植物提取法因原料丰富易得,工艺简单,逐步成为主流[3]。植物提取法最初以蚕豆荚皮、蚕豆及藜豆为原料,后多采用猫豆;工艺也从酸提-铅沉法[4]、稀醋酸法[5]发展到酸浸-离子交换法[6]。广西以其猫豆资源优势,近二十年逐渐成为世界L-dopa的主要产区[7],生产工艺为用稀HCl水溶液浸提,浸提液上001×7(732)阳离子交换树脂柱,将L-dopa富集于柱上;交换饱和后用水洗柱,再用浓氨水将L-dopa从柱上洗脱;洗脱液用HCl中和,减压浓缩,析出粗品;粗品用稀HCl溶液加热溶解至饱和,冷却析出结晶,过滤,烘干,即得L-dopa产品[8];用过的阳离子交换柱,须用NaOH溶液和HCl溶液再生才能用于下一次交换。在上柱、洗柱及柱再生工序有大量工艺废水产生;每生产1 kg L-dopa,可产生1.5-2.0 t高含淀粉、蛋白质、HCl和NaOH的废水,环保压力大,所有传统生产厂家因环境评价不合格而面临关停。目前国内外为解决L-dopa生产工艺排放黑臭废水的研究鲜有报道。中国学者大多着重于新技术、新手段的应用,如汪桂芳等[9]利用膜分离技术提高分离效果,杨卫华[10]采用重组酪氨酸酚裂解酶催化合成左旋多巴。波兰Polanowska等[11]为了环境保护和缩短工艺流程,尝试用0.2%醋酸水为溶剂从蚕豆中提取左旋多巴,但只是完成实验室提取试验,没有精制出产品,也没有进行工艺中试。
本研究摒弃传统工艺,创新性地开发一种新的生产工艺,虽然水的浓缩、蒸发量较大,但不产生含淀粉、蛋白质、HCl和NaOH的废水,能全面解决传统工艺的黑、臭、高COD工业废水问题,且产品得率、产品质量与传统工艺相当,可减少企业环保压力。
1 材料与方法
1.1 仪器
Alliance 2695型四元泵带紫外检测器高效液相色谱仪(Waters公司),GM705H型破壁料理机(上海飞利浦(中国)投资有限公司),HB43-S型水分测定仪(瑞士梅特勒-托利多仪器有限公司),DHG9246A型电热恒温鼓风干燥箱(上海精宏实验设备有限公司)。
1.2 材料
聚丙烯酰胺(PAM,非离子型,广州东歌化工科技有限公司);聚合氯化铝(PAC,巩义市碧波供水材料有限公司);HCl、NaOH和MgCl2(西陇科学股份有限公司);甲醇(Thermo Fisher);维生素C(VC,东营市华璇生物科技有限公司);单宁酸(广州市德晟化工有限公司);蒙脱石(粤江新材料(广州)有限公司);食品级95%酒精(广西崇左东亚糖业有限公司);含量测定用试剂为色谱纯,水为重蒸水;其余制剂为分析纯。猫豆(又名狗爪豆),经广西中医药大学韦松基教授鉴定为豆科藜豆属狗爪豆Mucunapruriens(Linn.) DC.var.Utilis (Wall.ex Wight) Bak.ex Burck的成熟、干燥种子[12]。
1.3 方法
1.3.1 工艺流程
常温下用含VC水将干猫豆打成水浆,加PAM,静置沉淀(第一次沉淀),滤取滤液;滤液加热煮沸,冷至室温,加PAM,静置沉淀(第二次沉淀),滤取滤液,浓缩,静置析出L-dopa粗品;滤取粗品,用pH值为3.5的HCl水溶液煮沸溶解至饱和,趁热滤取滤液,冷却,结晶析出L-dopa,滤取结晶,烘干得L-dopa原料药产品。
1.3.2 供试液制备方法
1.3.2.1 含VC水的制备
常温下操作,将1 g VC加入1 000 mL水中,充分搅拌使之完全溶解;用HCl调节pH值为4.5-5.0。
1.3.2.2 PAM溶液的配制
取1 g非离子型PAM加入到1 000 mL去离子水中,快速搅拌使之全部溶解。即配即用。与料液(水浆或滤液)混合时,要快速、充分地搅拌均匀。
1.3.2.3 猫豆水浆的制备
常温下操作,将含VC水和干猫豆一起放入破壁料理机中,不加热,转速7 500 r/min打浆10 min,得混悬状水浆。
1.3.3 L-dopa含量测定
按《欧洲药典》中提及的方法[13]进行。
1.3.4 澄清效果测定
1.3.4.1 澄清效果指标
在规定料液温度下操作;先将料液与沉淀剂快速、充分地搅拌均匀,再保温静置至规定时长,一次性倒入布氏漏斗,用2层Φ11 cm中速定性滤纸在-0.1 MPa真空度下抽滤10 min,测量滤液体积(VF)。
1.3.4.2 不同沉淀剂对澄清效果的影响
60 g猫豆,打成1 800 mL水浆,分成9等份,每份200 mL,分别与不同沉淀剂(各自预先溶于5 mL水)快速混匀,静置,沉淀1 h,抽滤,测量滤液体积(VF);取滤液测定L-dopa含量(C)。
1.3.5 基于猫豆原料的L-dopa转移率计算
L-dopa转移率T=(W产品×C产品)/(W原料×C原料)×100%,
式中:W产品为L-dopa产品质量;
C产品为L-dopa产品中L-dopa的含量;
W原料为猫豆原料的质量;
C原料为猫豆原料中L-dopa的含量。
2 结果与分析
2.1 操作温度对水浆沉淀澄清的影响
预试验结果表明,水浆温度超过65℃,无论加入何种沉淀剂,水浆均呈大粘度的稀薄液体,难以过滤。因此工艺全部在室温下操作,水浆温度22-28℃。
2.2 不同沉淀剂对水浆沉淀澄清的影响
数据表明,不添加沉淀剂的水浆难以自然沉淀;加入PAC和PAM的沉淀效果最好。添加熟石膏粉、MgCl2、明矾、蒙脱石、PAC,水浆中L-dopa含量降低,且添加明矾、蒙脱石、PAC的水浆颜色变深;其余添加沉淀剂对水浆中的L-dopa 含量没有影响(表1)。因此本工艺选用PAM作沉淀剂。
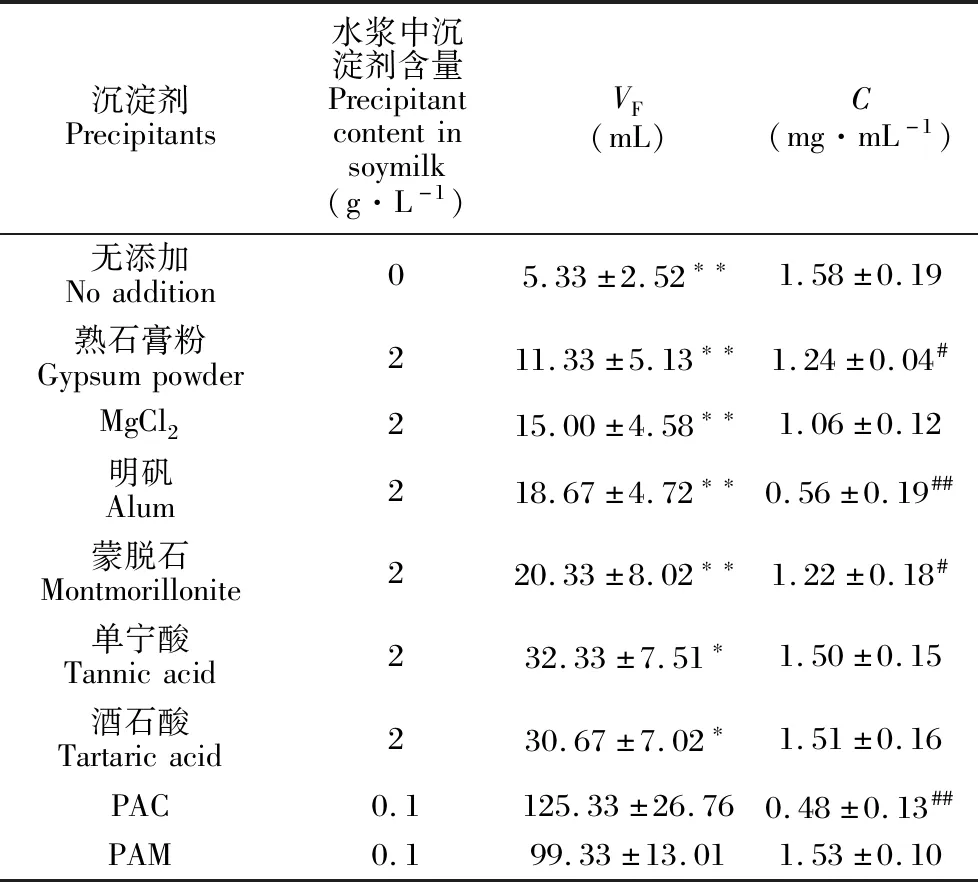
表1 不同沉淀剂对水浆沉淀效果的影响(x±s,n=3)Table 1 Effect of different precipitants on soymilk precipitation (x±s,n=3)
2.3 第一次沉淀工序的参数优选
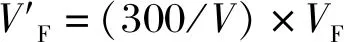

表2 第一次沉淀工序的因素和水平Table 2 Factors and levels of the 1st precipitation process
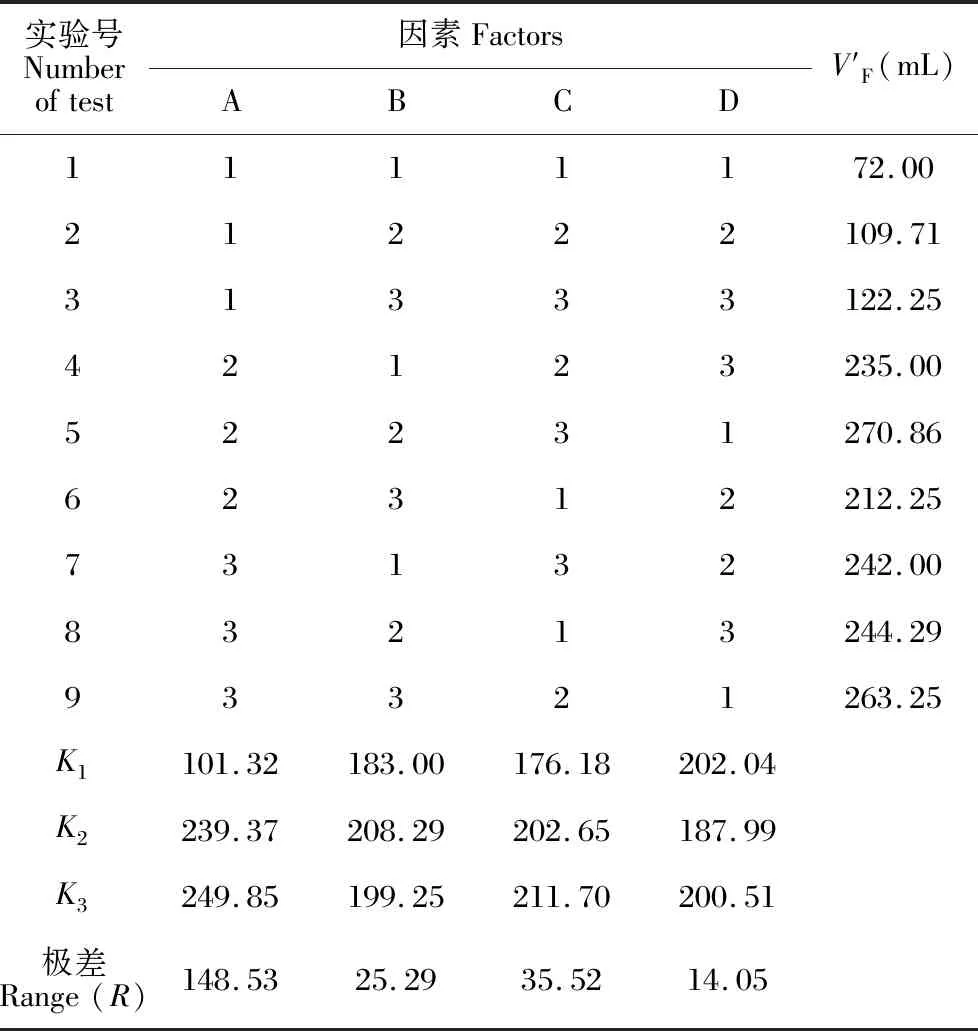
表3 第一次沉淀工序的试验设计与结果Table 3 Test design and results of the 1st precipitation process
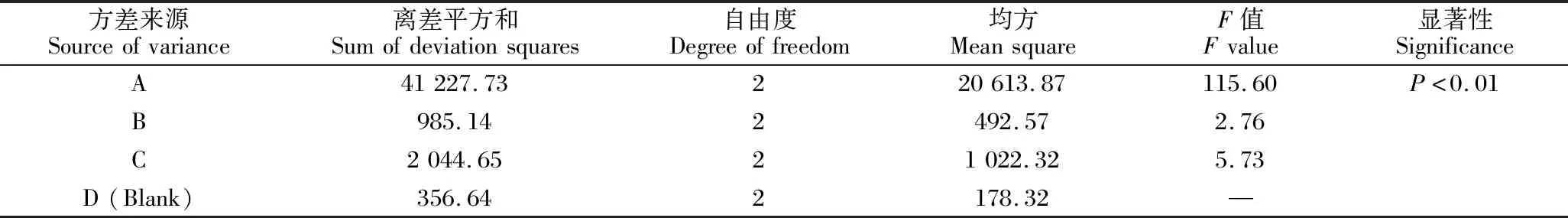
表4 第一次沉淀工序的方差分析Table 4 Variance analysis of the 1st precipitation process
极差分析显示,因素影响大小为A>C>B,结果提示选A3B2C3。方差分析显示,A有显著影响(P<0.01),B、C影响不明显(P>0.05)。对数据进行单因素分析,A1→A2变化明显(P<0.05),A2→A3变化不明显(P>0.05),拐点在A2,因此选A3较妥;B、C因素变化拐点不明显(P>0.05),可结合实际情况选择,越接近极差分析结果越佳。综合考虑,选择A3B2C2,即常温下操作,1 kg猫豆用35 L含VC水磨成水浆;1 L水浆加0.15 g PAM,快速、充分搅拌混合,常温静置1.5 h,即可进行过滤。
2.4 第二次沉淀工序的参数优选
采用L9(34)正交试验法。按第一次沉淀工序优化参数制备滤液,将滤液加热煮沸15-30 min,使水溶性蛋白和淀粉变性析出,冷却降温到所需温度。沉淀剂仍选用PAM,PAM在超过65℃的水中会出现分解,因此考察温度定为25-50℃。取煮沸后冷却降温的滤液9份,每份200 mL,按表5的用量和温度操作,加入PAM溶液,快速搅拌混匀,保温静置沉淀一定时间,抽滤,测量滤液体积(VF),结果如表6,方差分析结果如表7。

表5 第二次沉淀工序的因素和水平Table 5 Factors and levels of the 2nd precipitation process
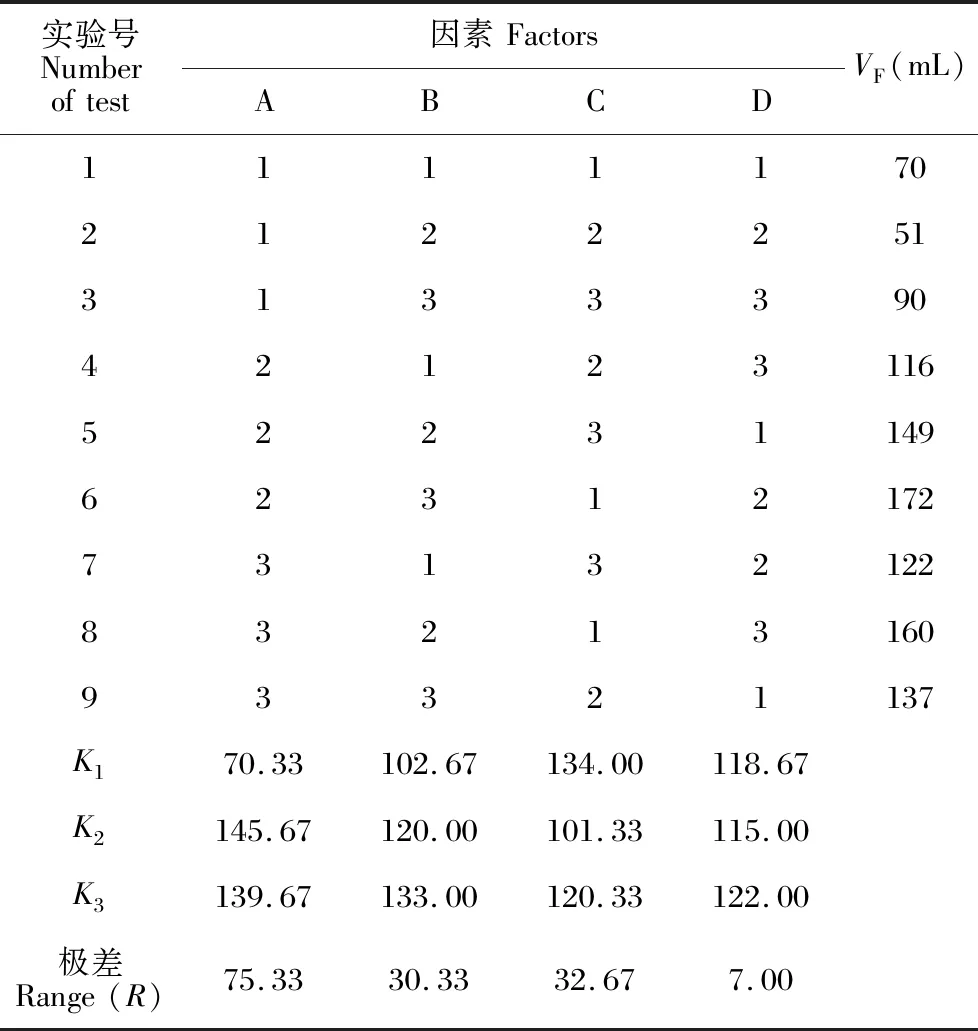
表6 第二次沉淀工序的试验设计与结果Table 6 Test design and results of the 2nd precipitation process

表7 第二次沉淀工序的方差分析Table 7 Variance analysis of the 2nd precipitation process
极差分析显示,因素的影响大小排序为A>C>B,应选A2B3C1。方差分析显示,A影响非常显著(P<0.01),C影响显著(P<0.05),B影响不明显(P<0.1)。对数据进行单因素分析,A1→A2变化明显(P<0.05),A2→A3变化不显著(P>0.05),拐点出现在A2,因此选A3较妥;B、C的变化拐点不明显(P>0.05)。综合考虑,选A3B3C1,即在室温(25℃)下操作,1 L滤液加0.1 g PAM,快速搅拌混合,静置2 h,即可进行过滤。
2.5 浓缩工序参数的优选
按第一、二次沉淀工序优化参数制备8 000 mL滤液,分为8等份,各自减压浓缩至不同体积,冷却至室温,静置6 h,滤取结晶,烘干,称重,含量测定,计算基于猫豆的L-dopa转移率,结果如表8。数据表明,当浓缩液体积是猫豆重量的2-2.5倍量时,L-dopa析出效果最好,过滤性亦佳。
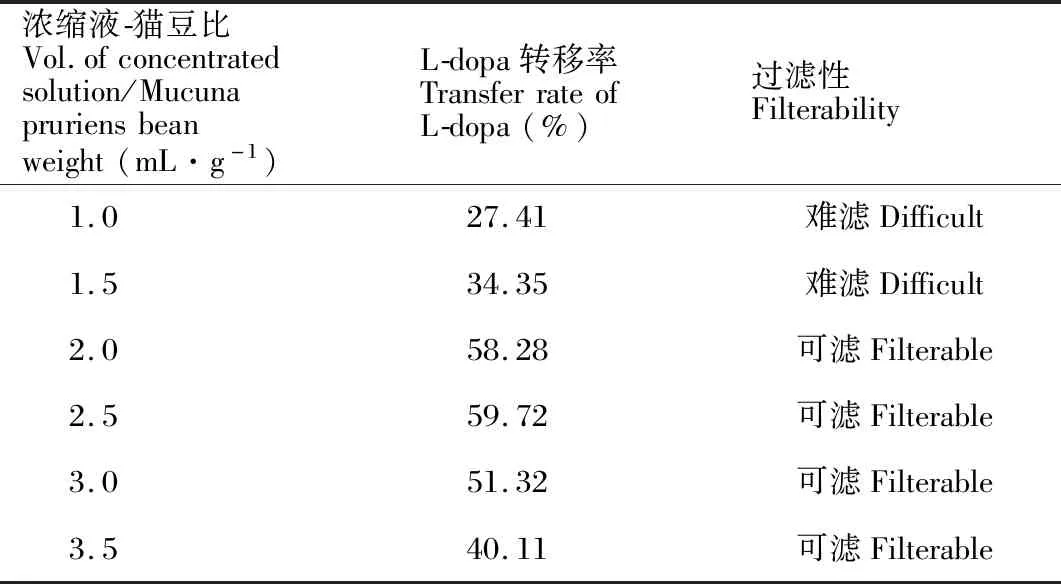
表8 浓缩程度对结晶的影响Table 8 Effect of concentration degree on L-dopa crystallization
2.6 精制方法研究
沿用传统工艺的成熟精制方法[14]。往耐酸容器中加入适量pH值为3.5的盐酸水溶液(预先溶有3%的VC),加热至沸,加入L-dopa粗品溶解至饱和,加入粗品质量4%的药用级活性炭粉,搅拌,保温40 min;趁热滤取饱和液,自然冷却至常温,析出结晶;滤取结晶,干燥后得到L-dopa产品。
2.7 工艺中试验证
将本工艺在广西那坡康正天然植物提取有限责任公司进行3批中试生产,产品按《欧洲药典》进行含量测定。结果如表9所示,工艺运行平稳,产品得率和产品质量与传统工艺相当,工艺只产生少量含HCl的工业废水。
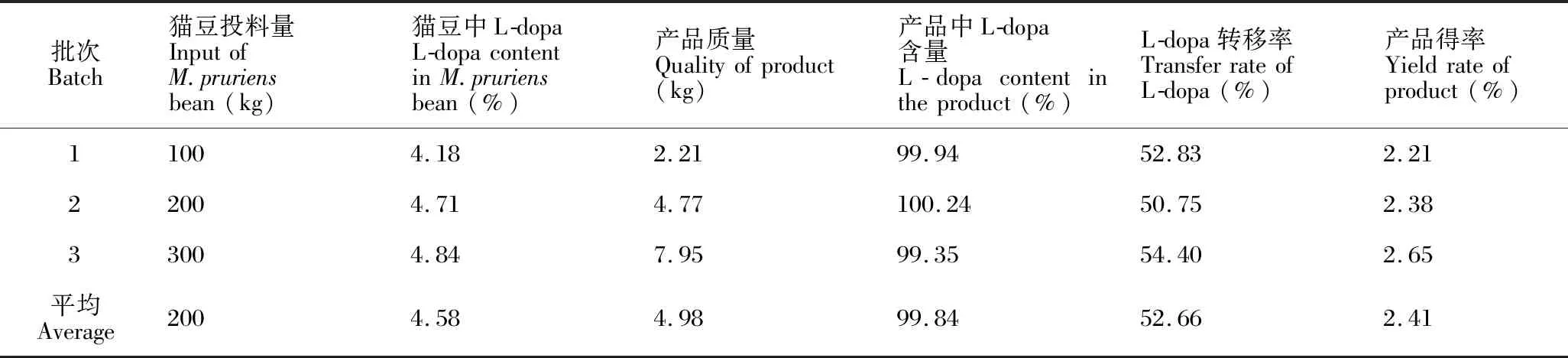
表9 中试生产结果Table 9 Results of trial-production
3 讨论
L-dopa不溶于乙醇、石油醚、乙酸乙酯等有机溶剂;在水中微溶,常温下600 mL水可溶解1 g[15]。预试验表明,猫豆其他成分对L-dopa有增溶作用,水中溶解度可超过3 mg·mL-1,因此只要有足量的水,猫豆磨成水浆10 min,豆中的L-dopa可溶解转移入水中。L-dopa易溶于酸水,但如用pH<3.5强酸水提取,会因强酸水溶解太多杂质而导致L-dopa无法从浓缩液中析出。
本工艺的技术难点在于尽可能减少提取液中的杂质和提高产品得率。工艺采用室温下水提、煮沸凝固析出水溶性淀粉和水溶性蛋白、加PAM沉淀剂等措施,目的是最大限度地减少提取液中的杂质。猫豆皮含有大量纤维,是第一次沉淀过滤的良好助滤材料,但形成的滤渣含水率较高,带走较多提取液;两次PAM沉淀过滤,累计损失约15%提取液,相当于损失约15%的L-dopa;浓缩析出粗品工序,有15%-20%的L-dopa残留于母液,造成L-dopa的重大损失。沉淀、过滤、析出粗品工序尚有待优化以提高L-dopa转移率,最终提高产品得率。
在浓缩析出L-dopa工序的母液中尚含有少量L-dopa,可通过加入乙醇析出。工厂实际将母液直接烘干成为低含量L-dopa产品出售,既避免黑臭工艺废水的产生,又省去防爆设备购置及防爆车间建设。
酪氨酸是L-dopa产品的相关物质之一,《欧洲药典》要求其含量≤0.5%,《美国药典》要求≤0.1%[16]。长期的生产数据表明,L-dopa结晶母液的pH值越接近中性,结晶中酪氨酸含量越低。本工艺全程控制pH值为5-6,经精制,产品中的酪氨酸含量很容易达到《中国药典》和《欧洲药典》要求,部分产品可达到《美国药典》要求。
PAM能与分散于水溶液中的悬浮颗粒架桥、附着结团,有极强的絮凝、沉淀作用,广泛应用于自来水生产、食品行业废水处理等领域[17]。工艺使用PAM作沉淀剂,可确保毒性安全。猫豆水浆加热至沸时,遇到MgCl2或熟石膏,水浆中的蛋白质可凝固成豆腐状,但过滤性不佳,滤饼含水率高,L-dopa损失大,因此没有进一步研究。
本工艺不产生黑、臭、高COD工业废水,每生产1 kg L-dopa,仅产生10-20 L含HCl工艺废水。试生产结果表明本工艺绿色环保,L-dopa产品得率可接受;沉淀滤渣可用于动物饲料或生产淀粉、蛋白质产品,猫豆资源可全部利用。浓缩工序的水蒸发量很大,将在后续研究中引进膜分离技术去除大部分水后再进行浓缩。此外,与猫豆同属的蚕豆,其叶、花、幼果、成熟种子和根中的L-dopa含量均很高,尤以鲜叶(22.4 mg·g-1)为最[18];作者后续研究将以叶、花、幼果和根为生产原料进行试验,探究新工艺的通用性和可行性。
4 结论
本研究开发的新生产工艺解决了传统工艺的黑、臭、高COD工业废水污染问题,且产品得率和产品质量与传统工艺相当,适合于工业化规模生产。
