基于CRISPR/Cas9的毛果杨PtrHBI1基因功能解析
2021-11-30王竹雯国艳娇周晨光姜立泉
王竹雯,国艳娇,李 爽,周晨光,姜立泉,李 伟
(林木遗传育种国家重点实验室(东北林业大学), 黑龙江 哈尔滨 150040)
木材是与人类生产生活息息相关的重要可再生资源[1-3]。木材的形成是复杂的、动态的、连续的[4],包括维管形成层细胞的分化、木质部细胞分化、次生细胞壁的积累和细胞程序性死亡[5-6]。转录因子在木材形成过程中起到关键调控作用[7]。
bHLH转录因子是植物中一个庞大的转录因子家族[8-10]。该基因家族在调控发育、胁迫响应、信号传导和次生生长方面起着重要作用[11-13],能够形成稳定、复杂的调控网络来提高植物的抗逆反应[14]。研究发现,AtHBI1参与拟南芥细胞伸长的信号调节,是油菜素内脂(BR)、赤霉素(GA)、温度和光信号通路下游细胞延伸的正向调节因子[15-17],其过表达植株的叶柄和下胚轴均伸长,且HBI1能和bHLH家族蛋白PRE1形成一个拮抗开关来影响光信号通路、温度和激素来调控细胞生长[18],而HBI1及其同源物的显性失活导致了细胞的矮化表型,表明HBI1作为中枢生长调控网络的关键节点,介导激素、环境和病原体信号的整合,在bHLH网络的反馈调节以及调节叶绿体功能和免疫应答方面发挥关键作用,在细胞延伸相关的激活基因中具有重要作用[19]。
继CRISPR/Cas9技术在哺乳动物细胞基因编辑应用之后,经过改造的CRISPR/Cas9载体也很快用于拟南芥、烟草、水稻、小麦、大豆和玉米等植物基因组的定向编辑研究[20-23]。2015年Fan等[24]率先将该系统应用在毛白杨(Populustomentosa)中的PtoPDS基因,获得了白化植株,自此CRISPR系统开始应用在树木中;Zhou等[25]首次对木质素合成途径中的关键酶基因4CLs进行敲除,获得的4CL1基因的突变体在木质素含量、紫丁香基木质素与愈创木基素之质量比(S/G)、浓缩单宁酸(原花青素)上均有着显著的降低,4CL2基因的突变体在浓缩单宁酸含量上有显著降低,这一结果为4CLs在木质素及类黄酮生物合成途径中的主要作用及功能冗余现象提供了遗传学证据。
本研究利用东北林业大学林木遗传育种国家重点实验室前期对毛果杨茎干中多种细胞类型进行的RNA-seq分析,获得了1个在形成层和木质部高表达的bHLH转录因子PtrHBI1,利用CRISPR/Cas9技术创制了毛果杨(Populustrichorcarpa)PtrHBI1基因突变体,通过对突变体的生长表型、组织切片观察及木材组分分析,初步解析PtrHBI1转录因子在木材形成过程中的功能,为创制适用于制浆造纸的林木优良品种提供新思路。
1 材料与方法
1.1 树木材料
树木材料均取自东北林业大学林木遗传育种国家重点实验室(本实验室)温室培养的野生型(WT)毛果杨,基因型为Nisqually-1。选取株高为(120 ± 5) cm的WT植株用于原位杂交,株高为(180 ± 20) cm的WT植株用于木质部原生质体转化,株高为(150 ± 5)cm的WT植株用于石蜡切片观察。
1.2 实验方法
1.2.1 毛果杨PtrHBI1基因的克隆、载体构建及亚细胞定位
1)PtrHBI1基因的克隆。通过PtrHBI1基因序列号(Potri.007G023600)在毛果杨网站中查找基因的完整转录组序列信息(https://phytozome.jgi.doe.gov/pz/portal.html),根据其上游与下游的序列信息设计特异性引物(见表1中PtrHBI1-1F、PtrHBI1-1R),以毛果杨木质部cDNA为模板进行基因克隆并连接pENTR/D_TOPO载体(life invitrogen),构建pENTR-PtrHBI1载体。利用热激法将连接液转化到大肠杆菌TOP10(本实验室保存),电泳检测获得阳性克隆后测序鉴定,与理论序列比对查看序列的准确性。利用Plasmid mini kit(Qiagen)质粒提取试剂盒对pENTR-PtrHBI1进行质粒提取,产物保存备用。
2)亚细胞定位。利用双酶切法构建亚细胞定位的瞬时表达载体pUC19-35S-PtrHBI1-GFP,PCR模板为pENTR-PtrHBI1,引物为PtrHBI1-2F、PtrHBI1-2R(表1),PCR反应体系、产物检测等步骤同上。参照东北林业大学林木遗传育种国家重点实验室姜立泉团队已发表的毛果杨木质部原生质体转化系统[26]瞬时转化pUC19-35S-PtrHBI1-GFP,激光共聚焦显微镜下观察结果,用以确定亚细胞定位情况。

表1 所用引物及序列
1.2.2 毛果杨PtrHBI1基因的原位杂交
原位杂交参考文献[27]的方法并根据本研究材料做适当改进。
1)毛果杨PtrHBI1基因探针制备。转录模板选取目的基因中150~200 bp且无poly A尾的非保守区域为转录模板。扩增引物为表1中PtrHBI1-3F、PtrHBI1-3R,正义探针转录模板为PtrHBI1-4F,反义探针转录模板为PtrHBI1-4R。
2)PtrHBI1基因原位杂交。经过多次实验发现供试材料第6茎节的切片形态最好且杂交后的组织较完整,因此选择毛果杨植株第6茎节进行后续实验。将毛果杨第6茎节进行固定液固定、组织脱水、浸蜡、包埋和切片。用半定量的方法估计特异探针的质量浓度,经过计算得出,PtrHBI1基因正义探针的质量浓度是25 ng/μL,PtrHBI1基因反义探针的质量浓度是25 ng/μL。原位杂交时,在黑暗的条件下光线会促进甲酰胺的电离作用影响杂交效果,原位杂交后,用显微镜观察杂交情况。
1.2.3 毛果杨PtrHBI1基因突变体的创制
1)构建pEgP237-U6-PtrHBI1gRNA-35S-Cas9载体。设计PtrHBI1基因gRNA的网站为http://crispr.hzau.edu.cn/CRISPR2/,遵循脱靶概率低于0.5、GC含量在50%左右的设计原则,合成gRNA的序列为表1中PtrHBI1-g-F、PtrHBI1-g-R,对gRNA进行引物复性。PCR产物稀释100倍。载体pEgP237-2A-GFP经BsaⅠ单酶切,与PtrHBI1的gRNA用T4 DNA连接酶连接,将连接产物利用热激法转化到TOP10大肠杆菌中,筛选阳性单克隆进行测序验证,后将阳性质粒pEgP237-U6-PtrHBI1gRNA-35S-Cas9转入GV3101农杆菌中,用于毛果杨的遗传转化。
2)毛果杨PtrHBI1基因突变体的创制。参照毛果杨快速遗传转化系统[28-29]进行。选择生长30 d左右健康的毛果杨无菌组培苗,切下第2~3节茎段,农杆菌侵染20 min后共培养48 h,用含有250 mg/L头孢霉素的无菌水浸泡清洗茎段,随后移至含有25 mg/L卡那霉素和250 mg/L头孢霉素的选择培养基上。生长25~30 d出抗性芽后,将抗性芽移至含有20 mg/L卡那霉素和125 mg/L头孢霉素的抗性芽生根培养基中。
3)突变体的鉴定。用pEgP237-2A-GFP上的F端引物M13F(表1)和PtrHBI1-g-R(表1)为引物,以待鉴定的植株的DNA作为模板PCR扩增约500 bp,连接pMD18-T(Takara)载体。取5 μL连接液进行大肠杆菌转化,随机挑取过夜培养的30个单克隆用引物M13F进行测序,使用DNAStar软件比对测序结果,鉴定编辑情况。
1.2.4 毛果杨PtrHBI1基因突变体的表型分析
1)突变体植株的表型观察。以野生型的毛果杨植株作为对照组,对生长60、90、120 d的突变体植株进行拍照,测量各个植株的生长指标,包括茎节数量、第8茎节长、地径以及株高。每个基因型选取3株树,重复测量3次,利用SPSS对各生长指标数据进行统计分析,用Sigma Plot 10.0软件作图。
2)石蜡切片观察。提前准备好西林瓶标记名称及日期,提前2 h左右配置石蜡切片的固定液并置于4 ℃冰箱预冷,对温室中生长至1.5 m左右苗高的突变体及野生型植株进行石蜡切片。收集材料时按照从上到下依次进行切割,选取第2、4、6、8、10茎节的中间区域,将每个茎段切成2 cm的厚度,切好的茎段立即放到装有预冷固定液的西林瓶里,每个西林瓶放7个左右茎段。固定好之后脱水、浸蜡,浸蜡4 d后进行包埋、切片,将用二甲苯脱蜡、酒精脱水后的切片用甲苯胺蓝水溶液染色,染色后的切片用树脂封片。用数字扫描显微成像系统M8和View Point Light 软件对毛果杨石蜡切片进行观察与统计学分析。野生型和每株转基因株系分别随机选3张第8茎节切片,每个切片随机选3个等比例区域,统计了单位面积(mm2)导管和纤维细胞数量及单个导管细胞孔径面积(μm2)。
1.2.5PtrHBI1基因突变体的木材组分分析
利用Klason酸水解法和高效液相色谱(HPLC)进行木质素及纤维素、半纤维素单糖含量测定[28]。分别选取3株4月苗龄的毛果杨野生型、ptrhbi1突变体植株作为实验材料,进行木材组分分析:将毛果杨茎段切下修剪成5 cm左右,剥掉树皮在室温下用90%(体积分数)丙酮浸泡2 d,室温下转入100%丙酮中培养14 d,每隔2 d更换1次新鲜的丙酮,晾干切片。用风干的茎段来测定木材组成(指标为酸不溶性木质素、酸可溶性木质素和单糖含量)和不同类型的木质素组成。
1.3 引物合成及测序
本研究全部的引物合成及测序服务均由吉林省库美生物科技有限公司完成(www.comatebio.com)。
2 结果与分析
2.1 毛果杨 PtrHBI1基因的原位杂交
实验室前期通过激光显微切割技术捕获了毛果杨野生型植株茎干不同类型的细胞,进行RNA-seq分析,结果显示,PtrHBI1在形成层、木质部和韧皮部细胞中具有不同的表达水平,其中在形成层细胞中的表达水平较高,其次是木质部(图1A)。对该基因进行毛果杨茎干原位杂交,结果如图1B和1C所示,PtrHBI1基因杂交信号集中于形成层和木质部,但在韧皮部也可观察到微弱的杂交信号,这与RNA-seq数据(图1A)中PtrHBI1基因的表达模式一致。通过对该基因的克隆及测序,获得了1 167 bp长度的CDS序列,用于后续研究。

A. RNA-seq数据中PtrHBI1基因在不同细胞类型的表达量(标准化FPKM值是指转录本丰度标准化为每千个碱基的转录每百万映射读取的片段数,误差线代表3个生物学重复的SE值)The transcript abundance of PtrHBI1 in RNA-seq data of different cell types (Normalized FPKM indicates normalized transcript abundances as fragments per kilobase of exon model per million mapped fragments. Error bars indicate one SE of three biological replicates); B.PtrHBI1基因的正义探针;C.PtrHBI1基因的反义探针。In situ mRNA localization of PtrHBI1. Digoxigenin-labeled sense PtrHBI1 RNA probe in B and digoxigenin-labeled antisense PtrHBI1 RNA probes in C(p.韧皮部phloem;ca.形成层cambium;x.木质部xylem)。图1 毛果杨PtrHBI1基因的表达模式Fig.1 Expression patterns of PtrHBI1 in Populus trichocarpa
2.2 PtrHBI1的亚细胞定位
利用毛果杨分化木质部原生质体转化系统,对PtrHBI1进行亚细胞定位,结果如图2所示,激光共聚焦显微镜下显示PtrHBI1定位在细胞核中。此结果表明PtrHBI1具有转录因子定位细胞核的一般特性。
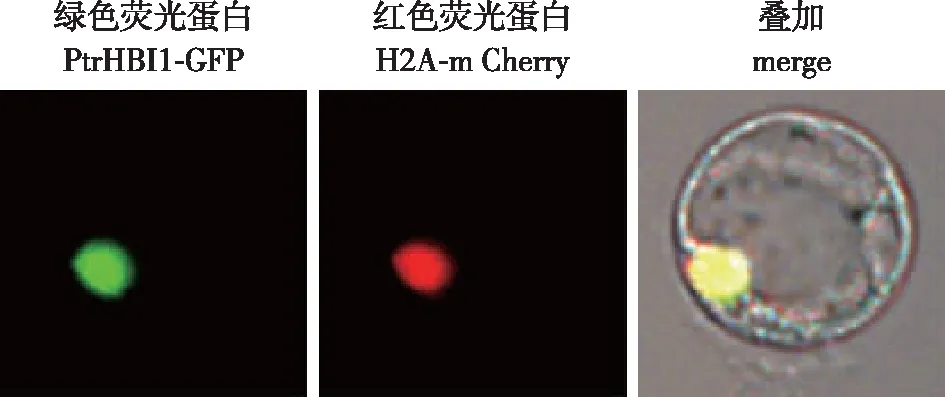
图2 毛果杨PtrHBI1基因亚细胞定位Fig.2 Subcellular localization of PtrHBI1 gene in P. trichocarpa
2.3 毛果杨PtrHBI1基因CRISPR突变体的获得
为了进一步研究PtrHBI1在木材形成过程中的功能,笔者采用CRISPR/Cas9基因编辑技术创制了毛果杨PtrHBI1基因功能缺失突变体。利用毛果杨快速遗传转化系统[26],经卡那霉素抗性筛选后,获得抗性植株(图3A—3C)。提取待鉴定的抗性植株叶片基因组DNA,使用载体引物M13F和PtrHBI1-g-R进行PCR扩增,结果如图3D所示,野生型(阴性对照,第3泳道)未扩增出条带,而2株抗性植株(4、5泳道)均扩增出与阳性对照(第2泳道)相同大小的条带,说明PtrHBI1重组质粒已经成功整合到毛果杨基因组中。

A. 愈伤组织分化诱导callus induction;B. 抗性芽诱导shoot induction;C. 抗性植株筛选the screening of the resistant plants;D. 转基因植株的PCR鉴定the PCR detection results(M. DNA marker DL2000; 1. ddH2O为模板的阴性对照negative control with ddH2O as PCR template; 2. pEgP237-U6-PtrHBI1gRNA-35S-Cas9质粒为模板的阳性对照 positive control with plasmid pEgP237-U6-PtrHBI1 gRNA-35S-Cas9 as PCR template; 3. 野生型毛果杨叶片DNA为模板的阴性对照negative control with leaf DNA of wild-type plant as PCR template; 4-5. 抗性植株叶片DNA为模板的样品sample with leaf DNA of kanamycin-resistant plant as PCR template)。图3 毛果杨转基因植株的获得Fig.3 Generation of P. trichocarpa transgenic plants
为了鉴定转基因植株的PtrHBI1基因编辑情况,提取转基因植株叶片DNA为扩增模板,参照毛果杨DNA序列,在包含gRNA位点的上下游共500 bp处设计引物PtrHBI1-5F、PtrHBI1-5R(表1),扩增目的片段DNA,加A尾后连接到T载体上,热激法转化大肠杆菌TOP10,每个植株挑取30个阳性单克隆进行测序,与野生型序列进行比对,结果如图4所示:获得1株ptrhbi1纯合突变体,其gRNA靶位点序列中缺失1个碱基“G”(图4A);造成PtrHBI1氨基酸序列翻译提前终止(图4B);另获得1株双等位突变体,其中一条等位基因缺失2个碱基,另一条等位基因缺失21个碱基(图4A),蛋白预测显示该突变体保留了典型的HLH结构域[30](图4B),表明该突变体可能仍具有PtrHBI1的功能。因此选取纯合突变体进行后续研究。

A. 等位基因编辑情况(红色“-”表示碱基缺失,“-21 bp-”表示缺失21个碱基)gene editing of alleles (The red short lines “-” represent deletion, “-21 bp-” represent 21 nucleotide deletion);B.被编辑基因的蛋白翻译情况预测(红色块区域表示缺失7个氨基酸) the prediction of amino acid sequence translation (The red short lines represent amino acid changed)。图4 毛果杨PtrHBI1基因编辑情况Fig.4 Gene editing of PtrHBI1 gene in P. trichocarpa
2.4 PtrHBI1突变体植株生长表型分析
为了分析PtrHBI1功能缺失后对树木的影响,首先对株高150 cm左右的ptrhbi1纯合突变体和野生型进行生长指标的测定,结果如图5所示。与野生型相比,ptrhbi1突变体植株的株高显著增高,茎节数、地径及第8茎节长度均有增加的趋势,表明PtrHBI1基因的功能缺失促进了植株的生长。
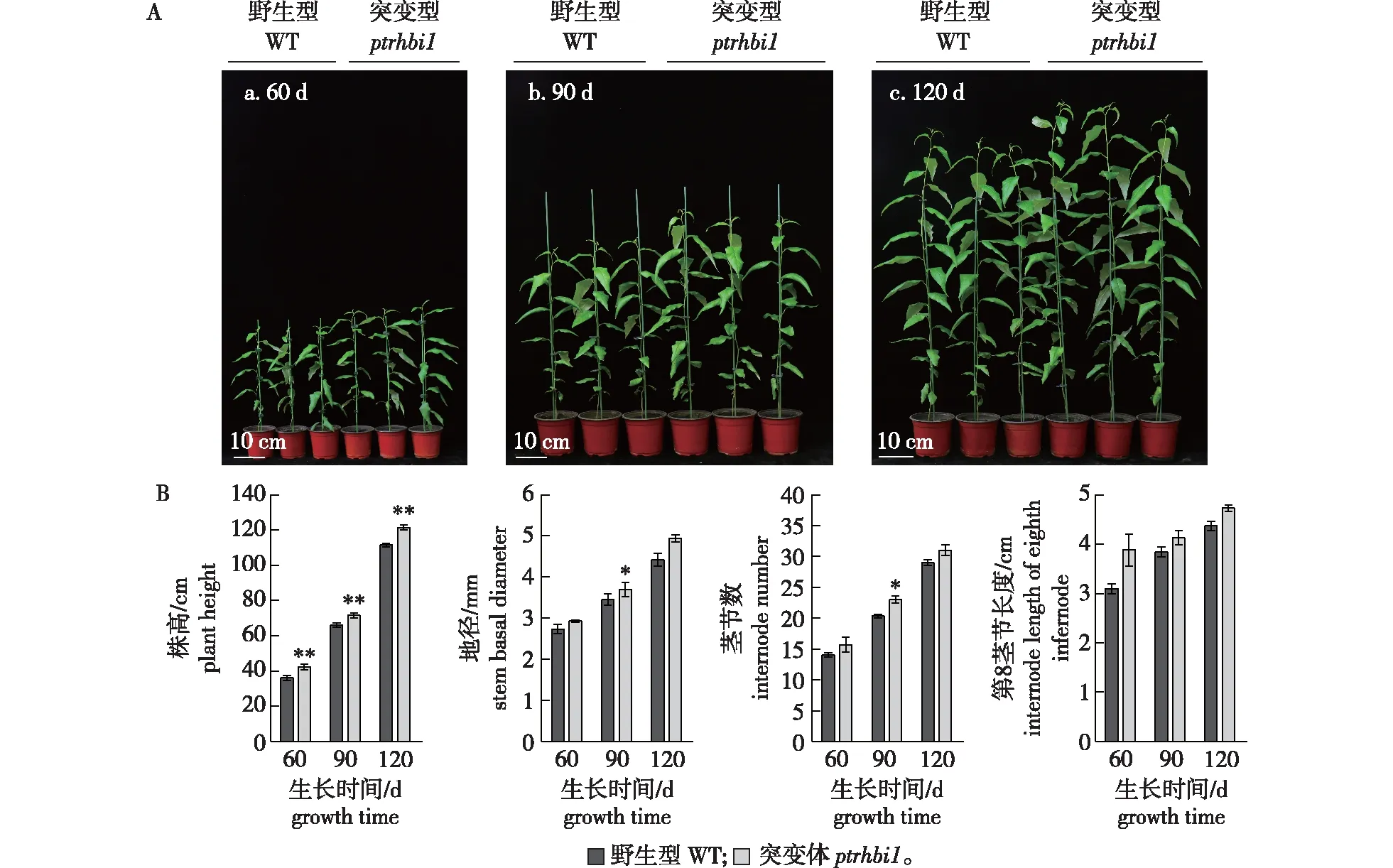
误差线代表3个生物学重复的SE值,*表示通过t检验,突变体与野生型植物各株系之间存在显著差异;*.P<0.05,**.P<0.01。下同。Error bars represent SE values of three independent experiments. Asterisks indicate significant differences between each line of the mutants and wild-type plants by Student’s t test. The same below.图5 毛果杨野生型和突变体植株生长表型分析Fig.5 Growthphenotype analysis of WT and ptrhbi1 mutants in P. trichocarpa
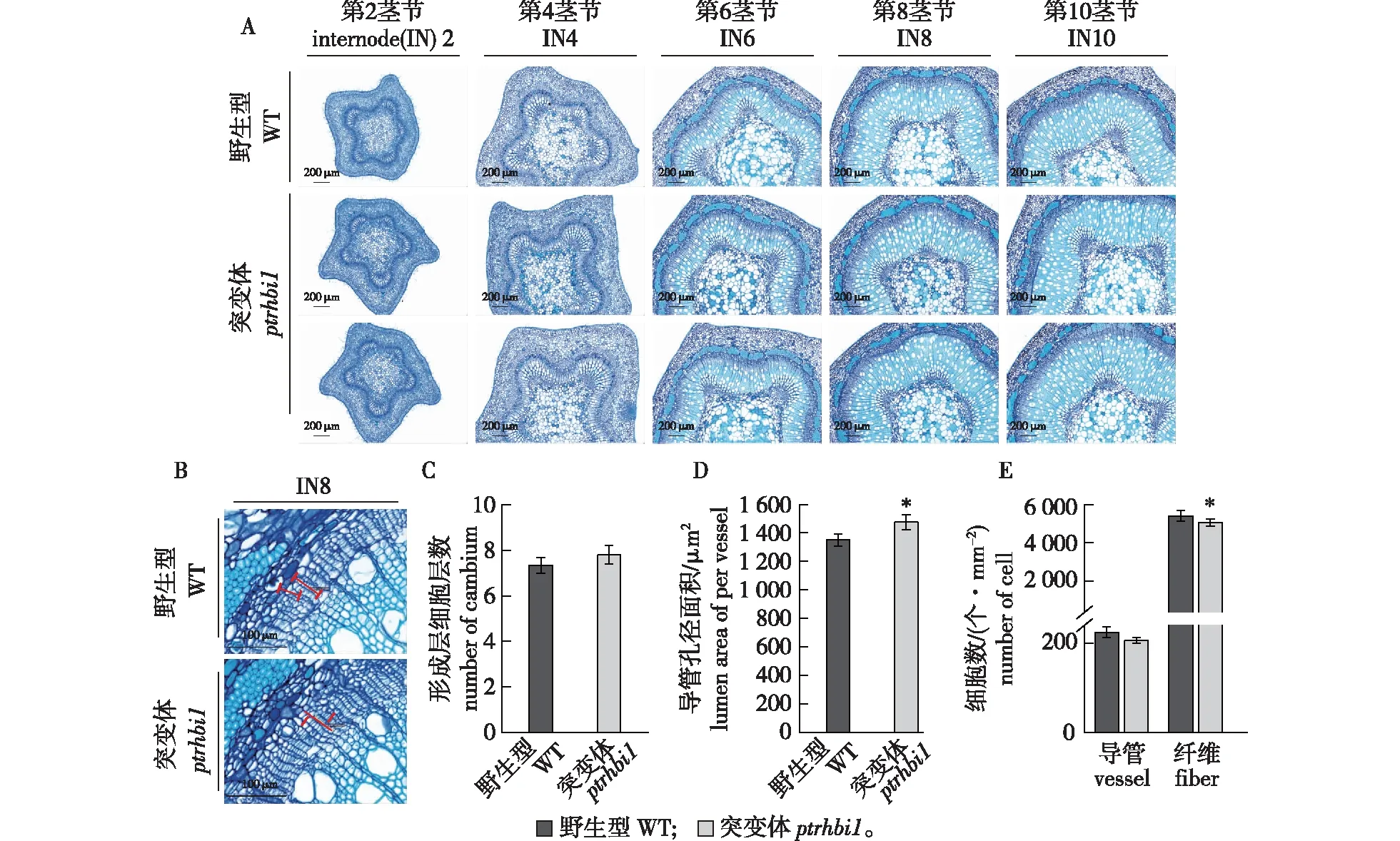
A. 野生型(WT)和突变体(ptrhbi1)毛果杨各茎节细胞形态观察(比例尺代表200 μm)morphologic observation of stem internodes of WT and ptrhbi1 (Bars=200 μm);B. 形成层细胞形态观察(红色线表示形成层区域,比例尺代表100 μm)morphologic observation of cambium cells (Red line showed cambium areas, Bars=100 μm);C. 单位面积细胞数目统计statistics analysis of number of cambium cell layer;D. 导管孔径大小统计statistics analysis of lumen area of per vessel;E. 形成层细胞层数统计statistics analysis number of cambium cell layer。图6 毛果杨野生型与ptrhbi1 突变体植株组织切片表型观察Fig.6 Paraffin section observation of WT and ptrhbi1 mutants
为了进一步解析PtrHBI1在杨树木材形成过程中发挥的功能,笔者通过石蜡切片技术及化学组织染色观察突变体茎横切面细胞形态,结果如图6所示,在ptrhbi1突变体植株中,形成层细胞的大小、形态、数量、细胞层数均没有明显变化(图6A—6C)。这一结果表明,PtrHBI1基因的功能缺失,并未对维管形成层的分化造成影响。除了形成层的表型,笔者也对ptrhbi1突变体植株木质部导管细胞和纤维细胞表型进行了观察,结果如图6A所示,各茎节中的导管和纤维细胞形态与野生型毛果杨没有差异。与野生型相比,ptrhbi1突变体植株中导管细胞孔径显著增大(图6D),纤维细胞的数量显著减少(图6E),导管细胞的数量没有改变。以上结果表明,PtrHBI1转录因子参与调控毛果杨木质部的发育过程。
2.5 ptrhbi1 突变体植株木材组分分析
通过以上实验结果可知PtrHBI1转录因子的功能缺失,影响了木质部细胞的发育,推测突变体的木材组分也会发生改变。因此,利用Klason酸水解法和HPLC分别对木质素、纤维素和半纤维素进行组分分析。木质素含量结果(表2)表明,ptrhbi1突变体植株的酸不可溶性木质素含量显著降低,酸可溶性木质素含量显著升高,总木质素含量变化不显著;紫丁香基木质素(S型木质素)、对-羟基苯基木质素(H型木质素)含量均显著降低,愈创木基木质素(G型木质素)含量显著升高,S/G比例显著降低。有报道指出木质部纤维细胞次生壁的木质素主要由S型木质素组成,而导管细胞次生壁主要由G型木质素组成[31-33],因此以上S型和G型木质素含量结果与ptrhbi1突变体植株纤维细胞数量减少、导管孔径变大的表型(图6D和6E)相一致。
此外,纤维素、半纤维素含量测定结果(表2)显示,ptrhbi1突变体植株中葡萄糖的含量显著增加,表明PtrHBI1基因的功能缺失促进纤维素的合成。综合以上结果,表明PtrHBI1转录因子在木质素合成及纤维素合成中发挥着调控作用。
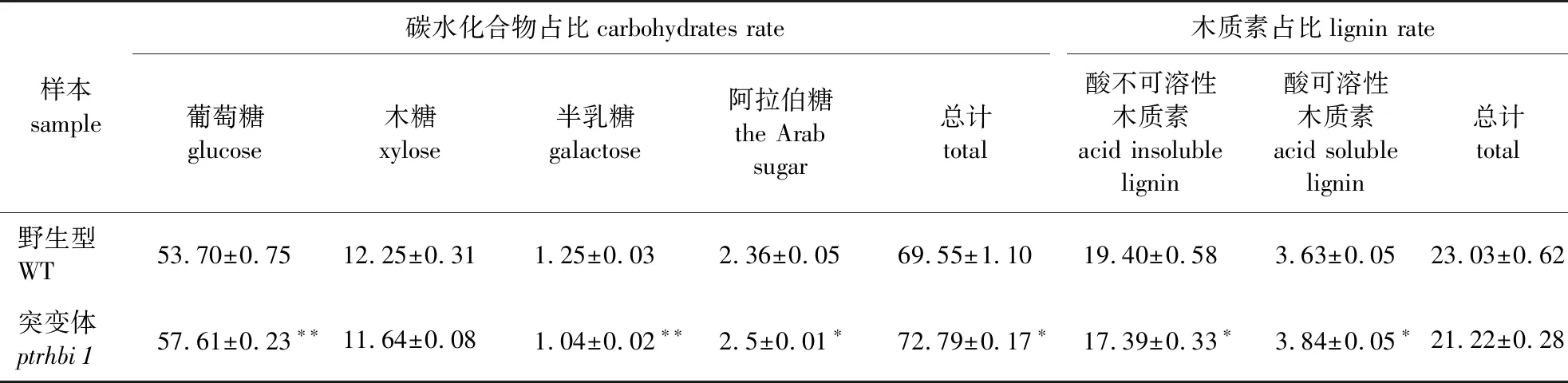
表2 毛果杨野生型与ptrhbi1 突变体植株木材组分占比

表3 毛果杨野生型与ptrhbi1 突变体植株木质素组分组成
3 讨 论
bHLH转录因子是植物中一个较为庞大的转录因子家族,调控众多复杂的生物学过程,广泛参与植物的生长发育和逆境响应[34]。本研究基于前期利用LCM捕获的毛果杨形成层、木质部和韧皮部细胞进行的RNA-seq数据分析,筛选得到1个在形成层和木质部表达的bHLH家族转录因子PtrHBI1,为了研究其具体功能,采用CRISPR/Cas9技术创制了PtrHBI1的功能缺失突变体,对突变体进行表型、组织切片及木材组分分析,发现PtrHBI1的功能缺失促进了植株的高生长,直接影响了木质部细胞的分裂分化,导致突变体木材纤维素含量增加、木质素S/G比例显著降低,揭示了PtrHBI1参与调控毛果杨的生长及次生木质部发育,为进一步解析植物次生木质部发育的复杂网络提供了新的线索。
毛果杨PtrHBI1与拟南芥的HBI1(AT2G18300)是同源基因[34]。对拟南芥HBI1的研究表明,HBI1作为植物生长调控网络的关键节点,通过介导激素、环境和病原体信号的整合,在植物生长和免疫之间的平衡中起关键作用[19]。在本研究中,毛果杨PtrHBI1的功能缺失显著提高了植株的高度,表明PtrHBI1在树木生长方面起到调控作用,这与拟南芥HBI1在植物生长中的功能相类似,但其在树木生长调控中的机制有待深入研究。通过对基于LCM技术的毛果杨木材细胞类型RNA-seq数据以及原位杂交的分析,确定了PtrHBI1在毛果杨茎干的维管形成层和木质部中高表达,因此推测该基因可能在维管形成层的分化上具有一定调控作用。但是对ptrhbi1突变体的各类型木材细胞统计分析发现,形成层的细胞数量及形态均没有显著变化,说明PtrHBI1的功能缺失并未对毛果杨维管形成层的分化造成影响。PtrHBI1又名PtrbHLH94,毛果杨bHLH家族进化分析显示PtrbHLH67(Potri.005G121900)与PtrHBI1在同一个进化分支[34],说明PtrbHLH67和PtrHBI1可能具有相似的功能,即存在功能冗余,单一敲除PtrHBI1基因功能可能不足以影响形成层的分化。这种对具有相近进化关系的其中一个基因进行编辑,而未出现相关表型的现象,也出现在以往的报道中[28]。
在被子植物中,木材细胞的次生细胞壁主要由厚壁组织细胞构成,这些细胞经过分化形成木质素、纤维素和半纤维素,其决定了木材的品质。对林产品工业来说,纤维素是纸浆和纸张生产的主要来源,木质素是糖化生产液体生物燃料的障碍[31,35],木质素的存在阻碍了纤维素纤维的提取。因此,获得高纤维素、低木质素含量的树种,对林产品工业以及生物能源行业具有重要意义。本研究通过对ptrhbi1突变体植株木材组分分析发现,其葡萄糖含量显著增加,碳水化合物含量显著提高,说明PtrHBI1的功能缺失促进了纤维素的合成,表明PtrHBI1基因可以作为利用分子育种技术进行木材材性改良的重要候选基因,对速生材的研究与定向培育起着重要的指导作用。双子叶植物的木质素主要由S型(syringyl)和G型(guaiacyl)木质素聚合而成[36-37]。普遍认为,木质部纤维细胞次生壁的木质素主要由S型木质素组成,而导管细胞次生壁主要由G型木质素组成[31-33]。木质素S/G比例的变化反应树木纤维细胞和导管细胞的数量或形态的变化,也是衡量制浆造纸木材的一个重要特性。研究表明,G型木质素会降低纸浆的产率,而S型木质素能提高纸浆的产率[37-39]。在杨树中过量表达木质素合成酶基因CAld5H增加了S/G木质素的比例,使得纸浆造纸效率大幅提高[40]。本研究中ptrhbi1突变体的S型木质素含量降低,同时G型木质素含量增加,使得S/G比例下降,表明PtrHBI1的功能缺失,不利于制浆造纸。近期研究发现,在不同类型的木质部细胞中抑制木质素的合成,S型和G型木质素分别在不同的转基因杨树中显著降低,并且特异降低纤维细胞木质素的转基因植株生物量增加,而针对导管细胞木质素抑制的结果则相反[33]。由此可见,基于PtrHBI1对纤维素和不同类型木质素含量的影响,若在特定木质部细胞类型中改变PtrHBI1基因的表达,可能会为创制利于制浆造纸树木品种策略提供参考。目前在细胞水平上改变木质素含量,仍需要对调控特定类型木质部细胞的转录因子进行挖掘。PtrHBI1的功能缺失,分别对纤维细胞和导管细胞的数量和孔径大小有显著影响,说明该转录因子调控毛果杨次生木质部细胞的发育,可能是在细胞水平进行木材改良的候选基因。
利用基因工程等技术进行林木遗传改良,选育产量更高、品质更优、抗逆性更强、适应性更广的林木品种用于生产,用更少的人工林面积生产更多的木材等林产品,以减少对天然林的依赖,是今后林木遗传育种的发展趋势和重点[38]。PtrHBI1参与调控毛果杨次生木质部发育过程,对植株的生长和木材形成具有重要的调控作用。PtrHBI1的基因功能缺失研究为创制适合于制浆造纸的优良树种提供了新思路。
