单孔胸腔镜联合颈部切口颈纵隔肿瘤切除术
2021-11-24王路汤磊刘丹钱鹏朱峰徐宁
王 路 汤 磊 刘 丹 钱 鹏 朱 峰 徐 宁
(安徽省胸科医院胸外科,合肥 230022)
颈纵隔肿瘤是指颈部肿瘤向胸腔生长延伸跨越胸廓入口进入纵隔,或纵隔肿瘤向上生长延伸跨越胸廓入口至颈部,同时占据纵隔及颈部[1]。颈纵隔肿瘤起源多种多样,常见的有甲状腺肿瘤、胸腺肿瘤、食管或气管肿瘤、淋巴管瘤、肺上沟瘤等[2]。多采用胸骨正中劈开或胸骨半蛤状切口行肿瘤切除术,但创伤大,不美观。借鉴宋帅林等[3]关于颈胸联合肿瘤的分度、吴跃煌等[4]关于胸骨后甲状腺肿的分度,杜国能等[5]根据CT扫描矢状面上将胸骨后甲状腺肿的分度,我们在影像学上将颈纵隔肿瘤分为三度:1度,肿瘤下界超过胸廓入口,但未达到主动脉弓切迹水平;2度,肿瘤下界达到或超过主动脉弓切迹水平,但未达到气管隆嵴水平;3度,肿瘤下界达到或超过气管隆嵴水平。2017年1月~2020年12月,我们对2度或3度颈纵隔肿瘤11例采取单孔胸腔镜联合颈部低领状切口行肿瘤切除,均获成功,报道如下。
1 临床资料与方法
1.1 一般资料
本组11例,男4例,女7例。年龄28~75(54.2±13.0)岁。刺激性咳嗽2例,胸闷、呼吸困难1例,其余8例为体检胸部CT检查发现颈纵隔占位。均行颈胸部增强CT检查,提示颈部及纵隔占位,跨越胸廓入口,无明显强化;右侧颈纵隔8例(图1、2),颈前纵隔3例;根据我们的颈纵隔肿瘤分度法,2度5例,3度6例;长径6.2~13.2 cm,平均9.8 cm。术前均行三维重建(图3)提示颈纵隔占位性病变,跨越胸廓入口。术前考虑甲状腺、胸腺来源可能,良性肿瘤可能性大。
纳入标准:①颈胸部增强CT诊断为颈纵隔肿瘤,根据我们的影像学颈纵隔肿瘤分度法为2度或3度;②三维重建提示肿瘤包膜完整,未侵犯心脏大血管、食管、气管等重要脏器,评估手术切除可能性大;③术前评估心肺功能可耐受单肺通气。
排除标准:①颈部和(或)胸部重大手术史,以及严重的脊柱畸形、心脏大血管变异等;②既往有胸膜炎或慢性脓胸胸膜增厚伴纤维板形成,经术前评估不能进行单孔胸腔镜手术;③严重的肝肾功能不全、冠心病、心绞痛、心肌梗死近期发作。
1.2 手术方法
双腔气管插管,静吸复合全身麻醉。先于侧卧位行单孔胸腔镜手术,再改平卧位行颈部低领状切口手术。
根据肿块所在位置决定左侧或右侧卧位及操作孔位置,一般选择腋前线第3、4肋间或腋中线第4、5肋间切口,长3~5 cm,置入胸腔镜探查胸腔内情况,肿瘤位置、大小、形态,包膜是否完整,有无浸润性生长以及活动度等。患侧肺萎陷,充分显露肿瘤,沿肿瘤包膜用电凝钩结合超声刀打开纵隔胸膜,松解肿瘤周围组织,保持瘤体包膜完整。如有滋养血管,予以游离结扎或Hem-o-lok结扎夹夹闭,超声刀离断。松解肿瘤时仔细辨认重要的血管神经,如迷走神经、喉返神经、锁骨下动脉、无名静脉、胸导管、气管及食管等,避免损伤,操作轻柔,以钝性分离为主,少用能量器械,将瘤体周围向胸廓入口处尽量松解,术侧颈纵隔肿瘤松解至该侧锁骨头以上平面,颈前纵隔肿瘤松解至甲状腺下动脉水平。留置胸腔引流管一根,逐层关闭胸腔。
改平卧位,肩部垫高,仰头过伸位,胸锁关节上1~2 cm沿皮肤纹理方向弧形切口,长6~8 cm,根据瘤体大小切口可适当延长。切开皮肤、皮下组织、颈阔肌,打开颈白线,显露气管、颈总动脉等组织,暴露颈纵隔肿瘤,用电刀、超声刀结合钝性分离,松解肿瘤周围。分离时注意保护喉返神经、迷走神经及血管等重要结构。待肿瘤松动后,将其提至颈部切口外(图4)。来源于甲状腺者,行单侧或双侧甲状腺全切术;非甲状腺来源者,完整切除瘤体。根据术中情况沿颈部切口方向放置1根或2根12F乳胶引流管(图5)。切除肿瘤常规术中冰冻病理检查,如为恶性,行胸腔镜下扩大根治,必要时改为胸骨正中劈开手术。
术后保持颈部及胸腔引流管引流通畅,胸腔引流<50 ml/d且无漏气,颈部引流<20 ml/d,予以拔除,无发热,生命体征平稳即可出院。出院3周后门诊复查胸片,如无异常,3个月后复查胸部CT。如行双侧甲状腺切除,术后口服左甲状腺素替代治疗,如行单侧甲状腺切除,术后3个月复查甲状腺功能决定是否补充左甲状腺素,均于内分泌科就诊。
2 结果
手术均顺利完成,无中转开放大切口手术。手术时间162~210(180.0±16.0)min,术中出血量10~30(19.1±7.01)ml,均未输血。术后胸腔引流量40~120(72.7±22.4)ml,胸腔引流管留置时间2~3 d;颈部引流量120~225(166.0±31.0)ml,颈部引流管留置时间3~4 d。术后住院时间3~8(4.6±1.4)d。术后病理:结节性甲状腺肿8例,胸腺囊肿1例,淋巴瘤1例,气管源性囊肿1例。1例右侧甲状腺切除术后第2天声音嘶哑,术后10天恢复正常。其他10例均未出现乳糜漏、喉返神经损伤、Hornor综合征等并发症。11例术后随访6~24个月,平均15个月,均无明显不适,颈胸部CT检查提示肿瘤无复发。
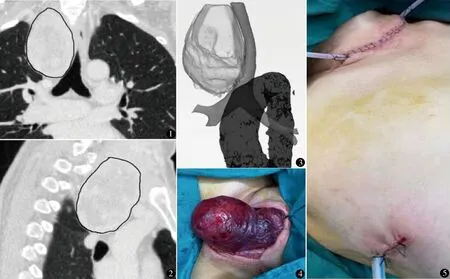
图1 术前CT矢状面提示右侧颈纵隔占位性病变,跨越胸廓入口,良性肿瘤可能性大,大小12.7 cm×6.2 cm×3.5 cm 图2 术前CT轴状面提示肿瘤下界达气管隆突,与脊柱界限清晰 图3 肿瘤、气管、主动脉三维重建,显示气管受压变形,未见心脏、大血管、气管等脏器受侵 图4 将肿瘤自颈部切口提出后完整切除 图5 颈部、胸部切口及引流
3 讨论
颈纵隔肿瘤并不少见,尤以胸骨后巨大结节性甲状腺肿居多,多见于右侧[6],单纯颈部切口难以完成手术,一直是胸外科的难题。既往多采用胸骨正中劈开、半蛤状切口等入路,但创伤大,术后疼痛剧烈,破坏胸廓完整性,对患者身心健康造成重大影响。目前单孔胸腔镜手术广泛开展,包括纵隔肿瘤切除、全胸腺扩大切除等术式已成常规。但颈纵隔肿瘤的微创治疗仅见数篇个案报告。Brichkov等[7]报道经颈部联合胸腔镜切除胸骨后巨大甲状腺肿7例;朱铁源等[8]报道6例颈部联合胸腔镜手术切除颈纵隔良性肿瘤,先行颈部切口手术,再更换体位行三孔胸腔镜手术;李彩连等[9]报道2例两孔胸腔镜联合颈部切口切除胸骨后甲状腺,与我们一样先行胸腔镜手术,再行颈部切口手术;张潜英等[10]报道5例颈部切口内镜辅助下胸骨后甲状腺切除。我们采用单孔胸腔镜联合颈部切口,手术视野能充分展现,操作空间足够,一旦出现不可避免的意外,亦方便随时迅速开胸扩大操作空间,保证手术的安全性和可操作性。
对于颈纵隔肿瘤,1度肿瘤多数可经颈部单一切口顺利娩出并切除,而2度及3度则需要联合颈部切口以外的胸部切口[5,11]。从11例影像资料来看,5例肿瘤下界达主动脉弓切迹水平,6例达气管隆嵴水平,单纯颈部切口难以切除,且肿瘤无明显外侵,良性肿瘤可能性大,术后病理亦证实了术前判断,故颈纵隔良性肿瘤或还没有浸润性生长的恶性肿瘤可以采用此术式,而浸润性生长的恶性肿瘤是否合适,尚有待进一步探讨。我们认为此类切口适应证有:①颈纵隔交界区肿瘤,单纯颈部切口或胸腔入路难以完成肿瘤切除,或不能完整切除,或手术重要操作在视野盲区;②术前影像检查提示肿瘤包膜完整,与周围组织无浸润性生长,或局部少许浸润尚能完整切除;③既往无胸腔手术、胸膜炎、胸部外伤等病史。
颈纵隔肿瘤组织来源多种多样,但其诊断及手术治疗存在一定的共性。本组3例肿瘤位于颈前纵隔交界区,单孔胸腔镜入路视野受到一定的限制,在双侧无名静脉之间向颈部操作视野欠佳,向颈部游离至甲状腺下动脉水平时,操作受到一定的限制。我们认为,此类患者可考虑行剑突下单孔胸腔镜向上游离,而且剑突下单孔胸腔镜联合颈部切口可避免体位改变,其可行性有待进一步探讨。颈纵隔肿瘤病理种类繁多,手术难度及风险均较大,术前应慎重评估,选择合适的术式及路径。本研究为回顾性的分析总结,并且手术例数少,尚有待扩大病例数量、随访术后并发症及远期生存质量等,以评估该手术的安全性、实用性以及远期疗效。
从本组有限的病例资料来看,单孔胸腔镜联合颈部低领状切口行颈纵隔肿瘤切除术安全、有效,可以推广。
