除去硅胶法制备氧化苦参碱分子印迹聚合物
2021-11-23陈光优胡光绒雷以柱田茂军
*陈光优 胡光绒 雷以柱 田茂军
(六盘水师范学院化学与材料工程学院 贵州 553004)
分子印迹技术是以模板分子为导向,设计和合成对某一种或某一类分析物具有特异性识别性能的分子印迹聚合物,分子印迹聚合物基体中存在大小、形状和功能等方面与目标分子相匹配的结合位点,因此分子印迹聚合物对目标分子具有高效结合性和独特的选择性[1-3]。从提出分子印迹概念后分子印迹技术就得到迅速发展[4],分子印迹技术广泛应用于色谱填料、固相萃取[5]、催化[6-7]和生物传感器等领域[8],在化学、医药学和天然药物的分离提取等方面具有十分乐观的应用前景。
氧化苦参碱(OMT),又名苦参素,是从豆科属植物苦参(Sophora flavescens Ait.)[9]中分离的具有生理活性的生物碱[10-11]。氧化苦参碱具有抗菌、杀虫、利尿、抗病原体、心肌缺血保护、免疫作用、抗乙肝病毒及抗肿瘤作用等功效[10-12]。本文以硅烷偶联剂(KH-550)修饰活化硅胶为载体,氧化苦参碱为模板分子,偶氮二异丁腈为引发剂,甲基丙烯酸为功能单体,乙二醇二甲基丙烯酸酯为交联剂制备氧化苦参碱表面分子印迹聚合物,洗脱模板分子从而获得具有与模板分子空间结构大小相匹配的氧化苦参碱表面分子印迹聚合物,用HF除去载体硅胶,即得除去硅胶分子印迹聚合物,用红外光谱对分子印迹聚合物进行表征,动态吸附实验、静态吸附实验和选择吸附实验考察分子印迹聚合物的吸附性能。
1.仪器与材料
(1)实验仪器
DF-101S型集热式恒温加热磁力搅拌器(上海聚昆仪器有限公司);AL204型电子分析天平(梅特勒-托利多仪器上海有限公司);TU-1901型双光束紫外可见分光光度计(北京普析通用仪器有限责任公司);HH-1型电动离心机(金坛市富华仪器有限公司);FTIR-7600傅立叶变换红外光谱仪(澳大利亚Lambda Scientific公司);80-2型多功能振荡仪(金坛市科析仪器有限公司)。
(2)实验试剂
氧化苦参碱(纯度98%,西安开来生物工程有限公司);苦参碱(纯度98%,西安开来生物工程有限公司);金雀花碱(纯度98%,西安开来生物工程有限公司);γ-氨丙基三乙氧基硅烷(KH-550,分析纯,南京创世化工助剂有限公司);氢氟酸(分析纯,上海申博化工有限公司);甲基丙烯酸(分析纯,天津市光复精细化工研究所);偶氮二异丁腈(化学纯,天津市光复精细化工研究所);乙二醇二甲基丙烯酸酯(分析纯,天津市光复精细化工研究所)。
2.方法与结果
(1)分子印迹聚合物的制备
①硅胶的活化
硅胶(80目)用浓盐酸浸泡48h,除去硅胶中的少量无机杂质,扩大比表面积使其孔穴分布更加均匀,有利于提高硅胶的吸附性能,蒸馏水洗涤至中性,100℃恒温干燥除去硅胶中部分化学吸附水和所有的物理吸附水。
②硅胶的硅烷化
称取50g活化硅胶于圆底烧瓶中,加入50mL硅烷偶联剂(KH-550)和50mL乙醇95%,在72℃水浴搅拌18h,用乙醇反复清洗,除去未反应完的偶联剂,70℃恒温干燥24h,即得硅烷化硅胶。
③分子印迹聚合物的制备
氧化苦参碱表面分子印迹聚合物(SMIP):称取1.000g氧化苦参碱(OMT)于250mL锥形瓶中,50mL甲醇溶解,加入30.4g硅烷化硅胶,超声脱气10min,加入5mL乙二醇二甲基丙烯酸酯(EDMA)、3mL甲基丙烯酸(MAA)、0.2g偶氮二异丁腈(AIBN),密封,52℃恒温搅拌48h,甲醇:乙酸(10:1)溶液洗涤,70℃恒温干燥24h,即得氧化苦参碱表面分子印迹聚合物。
空白表面分子印迹聚合物(SNIP):处理方法同氧化苦参碱分子印迹聚合物,只是没有模板分子氧化苦参碱。
除去硅胶氧化苦参碱分子印迹聚合物(NS-SMIP):干燥后的SMIP留2g备用外,余下用HF除去硅胶,70℃恒温干燥,即得去除硅胶的氧化苦参碱分子印迹聚合物。
除去硅胶空白表面分子印迹聚合物(NS-SNIP):处理方法同除去硅胶氧化苦参碱分子印迹聚合物。
(2)分子印迹聚合物的红外光谱表征
分子印迹聚合物红外光谱表征采用KBr压片,分辨率2cm-1,扫描范围450~4000cm-1。SMIP、OMT-SMIP和SNIP的红外光谱图见图1。由图1可知,3480cm-1是N-H伸缩振动特征吸收峰,3040cm-1是O-H伸缩振动特征吸收峰,2965cm-1是饱和C-H伸缩振动振动特征吸收峰,1722cm-1是酯的碳氧伸缩振动吸收峰,1611cm-1附近的峰是H-OH弯曲振动吸收峰,1488cm-1、1463cm-1是N-H弯曲振动吸收峰,1388cm-1是C-H弯曲振动吸收峰,1265cm-1是C-N伸缩振动吸收峰,1172cm-1、 962cm-1是Si-O的反对称伸缩振动吸收峰,757cm-1为Si-O对称伸缩振动吸收峰。

图1 SMIP(C)、吸附OMT-SMIP(B)和SNIP(A)的红外光谱
(3)分子印迹聚合物的吸附性能考察
①氧化苦参碱水溶液标准曲线
精确称取0.0300g的氧化苦参碱,蒸馏水溶解,100mL容量瓶定容,摇匀备用,即得浓度为300μg/mL氧化苦参碱标准溶液。准确移取标准溶液0.10mL、0.20mL、0.30mL、0.40mL、0.50mL、0.60mL、0.70mL、0.80mL、0.90mL和1.00mL稀释至10mL,即得浓度为3μg/mL、6μg/mL、9μg/mL、12μg/mL、15μg/mL、18μg/mL、21μg/mL、24μg/mL、27μg/mL和30μg/mL的标准待测液,蒸馏水作参比,紫外分光光度计在215nm处测定吸光度(A),以A-质量浓度(C)作图即得标准曲线,曲线方程为y=0.0194x+0.0789,r=0.9994,表明氧化苦参碱浓度在3.0~30μg/mL具有良好的线性关系。
②苦参碱水溶液标准曲线
精确称取0.0300g的苦参碱,蒸馏水溶解,100mL容量瓶定容,摇匀备用,即得浓度为300ug/mL苦参碱标准溶液。准确移取标准溶液0.10mL、0.20mL、0.30mL、0.40mL、0.50mL、0.60mL、0.70mL、0.80mL、0.90mL和1.00mL稀释至10mL,即得浓度为3μg/mL、6μg/mL、9μg/mL、12μg/mL、15μg/mL、 18μg/mL、21μg/mL、24μg/mL、27μg/mL和30μg/mL的标准待测液,蒸馏水作参比,紫外分光光度计在218nm处测定吸光度(A),以A-质量浓度以(C)作图即得标准曲线,曲线方程为y=0.0154x+0.1108,r=0.9994,表明苦参碱浓度在 3.0~30μg/mL具有良好的线性关系。
③金雀花碱水溶液标准曲线
精确称取0.0300g的金雀花碱,蒸馏水溶解,100mL容量瓶定容,摇匀备用,即得浓度为300μg/mL金雀花碱标准溶液。分别准确移取金雀花碱标准溶液0.10mL、0.20mL、0.30mL、0.40mL、0.50mL、0.60mL、0.70mL、0.80mL、0.90mL和1.00mL稀释至10mL,即得浓度为3μg/mL、6μg/mL、9μg/mL、 12μg/mL、15μg/mL、18μg/mL、21μg/mL、24μg/mL、27μg/mL和30μg/mL的标准待测液,蒸馏水作参比,紫外分光光度计在304nm处测定吸光度(A),以A-质量浓度以(C)作图即得标准曲线,曲线方程为y=0.03149x+0.0656,r=0.9991,表明金雀花碱浓度在3.0~30μg/mL具有良好的线性关系。
④动态吸附实验
称取100mg分子印迹聚合物于10mL离心试管中,分别加入浓度为30μg/mL、60μg/mL、90μg/mL、120μg/mL、150μg/mL、 180μg/mL、210μg/mL、240μg/mL、270μg/mL、300μg/mL的氧化苦参碱水溶液,震荡30min,离心,移取上层清液0.5mL稀释至10mL,以水作空白,在215nm处测定氧化苦参碱的含量,采用差减法来计算对氧化苦参碱的吸附量Q。

式中,Q为分子印迹聚合物的吸附量(mg/g);C为吸附后氧化苦参碱的浓度(μg/mL);C0为吸附前氧化苦参碱的浓度(μg/mL);W为分子印迹聚合物的质量(g);V为吸附溶液体积(mL)。
NS-SMIP和SMIP的动态吸附曲线见图2,图2可知NS-SMIP对氧化苦参碱的吸附量大于SMIP对OMT,分子印迹聚合物对OMT的吸附量在20min内都快速增加,在30min后吸附量基本接近饱和。这是由于分子印迹聚合物表面的孔穴比较浅从而有利于对OMT的吸附,因此在开始阶段分子印迹聚合物的吸附量速度非常快,当表面孔穴达到吸附饱和后,OMT再向分子印迹聚合物表面孔穴传质时,会受到阻碍,因而吸附速率会下降但在一段时间后就会达到吸附平衡。

图2 NS-SMIP和SMIP对OMT的动态吸附曲线
⑤静态吸附实验
称取100mg分子印迹聚合物于10mL离心试管中,加入浓度为300μg/mL的氧化苦参碱水溶液,震荡30min,离心,移取上层清液0.5mL稀释至10mL,以水作空白,在215nm处测定氧化苦参碱的含量,按公式(1)计算分子印迹聚合物的吸附量Q。
静态吸附曲线见图3,由图可知SMIP、NS-SNIP和SNIP对OMT的吸附量在浓度为120μg/mL达到最大值,随后吸附量达到平衡,NS-SMIP对OMT的吸附量在浓度为180μg/mL达到最大值。SNIP对OMT的吸附量明显小于SMIP吸附量,主要是由于SMIP与SNIP的表面空间结构有着明显差异而造成的,SMIP有着与OMT空间结构相匹配的孔穴,该孔穴对OMT分子有着独特的记忆功能,而SNIP表面存在的孔穴则是大小不一的各种结构,因此SNIP吸附量就小于SMIP。同理NS-SMIP对OMT的吸附量大于NS-SNIP对OMT的吸附量。NS-SMIP与SNIP的吸附量差值约为1.918mg/g,SMIP与SNIP的吸附量差值约为1.1mg/g,说明除去硅胶的分子印迹聚合物的吸附性能要强于未除去硅胶的分子印迹聚合物。

图3 NS-SMIP、NS-SNIP、SMIP和SNIP的静态吸附曲线
⑥选择性吸附实验
苦参碱(MY)和金雀花碱(CYT)的结构与氧化苦参碱(OMT)有一定的相似性,因此实验选用苦参碱和金雀花碱作为竞争对照底物,来分析分子印迹聚合物对氧化苦参碱的分子识别特性。氧化苦参碱(OMT)、苦参碱(MY)和金雀花碱(CYT)结构图见图4。
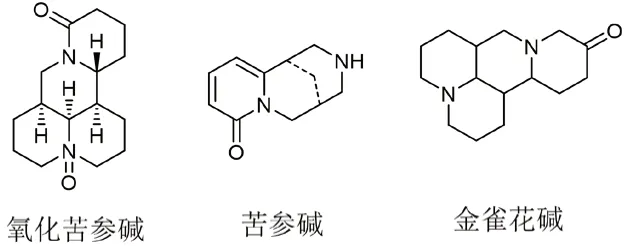
图4 氧化苦参碱、苦参碱及金雀花碱的化学结构
称取100mg分子印迹聚合物三份,于10mL的离心试管分别加入4mL浓度为300ug/mL氧化苦参碱(OMT)、苦参碱(MY)和金雀花碱(CYT)溶液,震荡30min,离心,移取上层清液0.5mL稀释至10mL,在215nm处测定氧化苦参碱(OMT)的吸光度,在218nm处测定苦参碱(MT)的吸光度,在304nm处测定金雀花碱(CYT)的吸光度,分别计算氧化苦参碱(OMT)、苦参碱(MY)和金雀花碱(CYT)的平衡浓度,按公式(1)计算分子印迹聚合物的吸附量Q。NS-SMIP和NS-SNIP的选择性吸附见图5,SMIP和SNIP的选择性吸附 见图6。

图5 NS-SMIP和NS-SNIP选择性吸附

图6 SMIP和SNIP选择性吸附
表1是NS-SMIP及NS-SNIP对OMT、MT及CYT的分配系数、 分离因子和相对分离因子的参数,表2是SMIP及SNIP对OMT、 MT及CYT的分配系数、分离因子和相对分离因子的参数。

表1 NS-SMIP和NS-SNIP对不同底物的选择性吸附参数

表2 SMIP和SNIP对不同底物的选择性吸附参数
由图5和图6可知NS-SMIP和SMIP对MT和CYT的吸附量明显小于OMT。而NS-SNIP和SNIP对三种底物的吸附量从总体来说差别不是很大。由表1和表2可看出NS-SMIP和SMIP对非目标分子的识别性是远低于目标分子,NS-SNIP和SNIP的选择性吸附能力要低于NS-SMIP和SMIP。这是因为NS-SMIP和SMIP对模板分子独特的匹配性,具有极高的选择特性。由表1可知NS-SMIP聚合物相对于苦参碱的分离因子(α)为1.3131,相对分离因子(α′)为1.2926,相对于金雀花碱的分离因子(α)为1.4049,且相对分离因子(α′)为1.3341。结果表明NS-SMIP具有良好的识别性以及特有的选择性,NSSMIP的选择性吸附能力要高于SMIP。
3.讨论
表面分子印迹技术是把模板分子的识别点建立模板材料的表面,洗脱后获得与模板分子空间结构和位点相匹配的表面分子印迹聚合物,表面分子印迹聚合物发展迅速,在各个领域中有着良好的发展前景。实验用表面分子印迹技术来制备氧化苦参碱表面分子印迹聚合物,用HF除去硅胶制备氧化苦参碱分子印迹聚合物,动态吸附实验、静态吸附实验和选择性吸附实验考察分子印迹聚合物的吸附性能。结果表明除去硅胶分子印迹聚合物对氧化苦参碱的吸附性能要强于未除去硅胶的分子印迹聚合物。除去硅胶分子印迹聚合物对氧化苦参碱分子具有良好的识别性以及独特的选择性,且除去硅胶分子印迹聚合物的这些特性要比未除去除硅胶分子印迹聚合物的明显。
