晚期非小细胞肺癌患者纤维蛋白原、D-二聚体与表皮生长因子受体-酪氨酸激酶抑制剂疗效的关系
2021-11-23钱晓涛胡格苏杰李蔷薇徐秀理
钱晓涛,胡格,苏杰,李蔷薇,徐秀理
中国科学院合肥肿瘤医院肿瘤综合治疗中心,合肥 230031
肺癌治疗已进入精准医学时代,进展日新月异。以表皮生长因子受体-酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitor,EGFR-TKI)为代表的分子靶向药,显著改善了非小细胞肺癌患者的预后,提高了患者生活质量,但其无进展生存期(progressive-free survival,PFS)仅10~12个月,且最终不可避免地会产生耐药。筛选出与TKI疗效及耐药有关的生物标志物,是临床亟待解决的问题。近年来,越来越多的研究显示,凝血功能异常,尤其是纤维蛋白原(fibrinogen,FIB)、D-二聚体(D-dimer,D-D)与肿瘤的发生发展、预后有密切关系,但其与EGFR-TKI疗效的关系尚不明确。本研究拟就此问题进行初步的探讨与分析,现报道如下。
1 资料与方法
1.1 一般资料
收集2018年1月1日至2020年12月30日就诊于中国科学院合肥肿瘤医院进行EGFR-TKI治疗的晚期非小细胞肺癌患者的病历资料。纳入标准:①经病理学检查确诊为非小细胞肺癌,包括鳞状细胞癌、腺癌、腺鳞癌,分期为ⅢB~Ⅳ期;②驱动基因检测证实为EGFR敏感突变,包括19DEL、L858R;③年龄>18岁,体能状况评分0~2分,生存期>3个月;④心肺功能、肝肾功能正常;⑤心电图正常,血红蛋白(hemoglobin,HGB)>80 g/L,白细胞计数(white blood cell,WBC)>4×10/L,血小板计数(platelet,PLT)>80×10/L;⑥临床资料完整;⑦签署靶向治疗同意书。排除标准:①EGFR基因突变不明或者野生型;②对TKI过敏或者不能耐受的严重不良反应,如皮疹、贫血、消化道反应、间质性肺炎等;③伴有其他肿瘤;④依从性差或者临床资料不全。根据纳入、排除标准,共纳入44例晚期非小细胞肺癌患者,其中男性26例,女性18例;年龄39~86岁,中位年龄64岁;有吸烟史10例,无吸烟史34例;腺癌43例,鳞状细胞癌1例;19外显子缺失突变22例,L858R突变19例,其他少见突变3例;确诊时发生脑转移18例;一线TKI治疗32例,二线治疗12例,其中吉非替尼28例,厄洛替尼4例,埃克替尼7例,阿法替尼1例,阿美替尼1例,奥西替尼3例;局部放疗(脑、肺、骨)30例,未行放疗14例;TKI治疗前FIB≤498 mg/dl 28例,>498 mg/dl 16例,D-D>0.55 μg/ml 25例,≤0.55 μg/ml 19例;末次随访时D-D≤0.55 μg/ml 14例,>0.55 μg/ml 30例,FIB≤498 mg/ml 36例,>498 mg/dl 8例。
1.2 研究方法
1.2.1 标本采集 清晨抽取空腹静脉血5 ml,置于含3.8%枸橼酸钠抗凝剂的专用试管中,3000 r/min离心10 min,留取上层血清,分别采用免疫比浊法和凝血酶固定法检测D-D、FIB水平。正常参考值范围:FIB≤498 mg/dl,D-D≤0.55 μg/ml。
1.2.2 治疗方法 EGFR敏感突变患者选用以下任一靶向药:吉非替尼250 mg,每天1次;厄洛替尼150 mg,每天1次;埃克替尼125 mg,每天3次;阿法替尼40 mg,每天1次;阿美替尼110 mg,每天1次;奥西替尼80 mg,每天1次。对于脑转移患者,优先推荐三代TKI。
1.2.3 疗效评价 依据实体瘤疗效评价标准1.1版分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、稳定(stable disease,SD)和进展(progressive disease,PD)。PFS定义为自治疗开始至疾病进展的时间。
1.2.4 观察指标及研究内容 基线资料包括:血常规、肝肾功能、癌胚抗原(carcinoembryonic antigen,CEA)、凝血功能、胸腹部CT、头颅MRI等。治疗开始后每2~3个月复诊,评价疗效,动态监测上述指标。研究内容:①比较FIB水平(分为≤498 mg/dl组和>498 mg/dl组)、D-D水平(分为>0.55 μg/ml组和≤0.55 μg/ml组)与 PFS 的关系;②动态监测D-D、FIB的水平,评估其与TKI耐药的关系。
1.3 随访
入组44例患者均通过门诊、住院以及电话的方式随访。随访患者一般情况、有无药物不良反应以及生存情况,随访截止时间为2021年2月1日。
1.4 统计学分析
采用Graphpad Prism 9.0软件进行统计分析。采用Kaplan-Meier法绘制生存曲线,并进行Logrank检验;价值分析采用受试者工作特征(receiver operating characteristic,ROC)曲线,计算ROC曲线下面积(area under the curve,AUC)、灵敏度、特异度、约登指数;以P<0.05为差异有统计学意义。
2 结果
2.1 PFS 分析
随访截至2021年2月1日,中位随访时间18个月。44例患者中有30例患者出现病情进展,14例病情尚稳定。FIB≤498 mg/dl组患者中位PFS为13.2个月,明显长于>498 mg/dl组患者的7.0个月,差异有统计学意义(HR=0.36,95%CI:0.15~0.86,P<0.01)(图 1)。D-D≤0.55 μg/ml组患者的中位PFS为23.0个月,长于>0.55 μg/ml组患者的8.0个月,差异有统计学意义(HR=2.80,95%CI:2.13~6.40,P=0.03)(图2)。
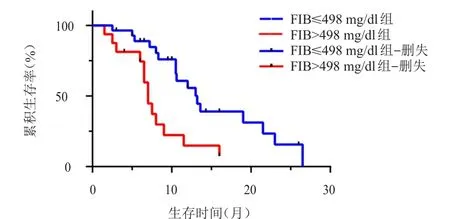
图1 FIB≤498mg/dl组(n=36)和>498mg/dl组(n=8)患者的PFS曲线
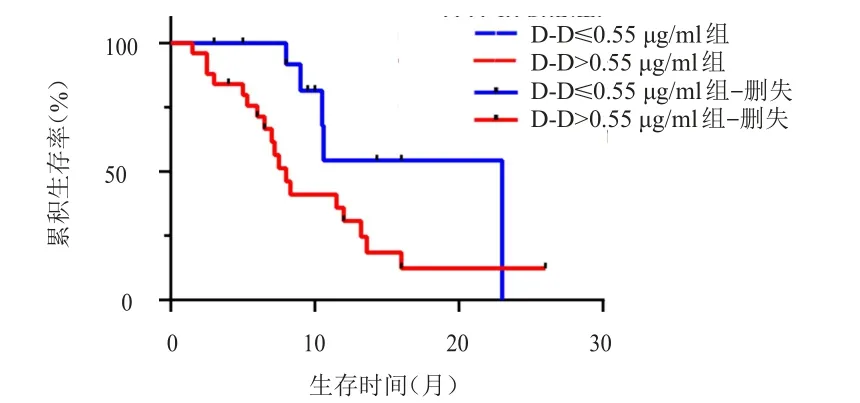
图2 D-D>0.55μg/ml组(n=30)和≤0.55μg/ml组(n=14)患者的PFS曲线
2.2 D-D、FIB水平预测TKI耐药的价值分析
对末次随访时D-D、FIB水平与病情状态进行分析发现,D-D>0.55 μg/ml有30例,其中PD 27例,SD 3例;D-D≤0.55 μg/ml有14例,其中PD 4例,SD 10例。FIB>498 mg/dl有8例,其中PD 6例,SD 2例;FIB≤498 mg/dl有36例,其中PD 25例,SD 11例。绘制ROC曲线,评估D-D、FIB水平预测TKI耐药的价值。结果显示,D-D水平与TKI耐药的一致性较高,能较好地预测TKI耐药的发生,AUC=0.83,P<0.01,灵敏度为87.1%,特异度为76.9%,诊断符合率为84.1%,约登指数为0.64;FIB水平与TKI耐药的一致性较差,AUC=0.52,P=0.82(图3)。

图3 D-D、FIB水平预测TKI耐药的ROC曲线
3 讨论
FIB是肿瘤基质的主要成分,在恶性肿瘤细胞周围形成保护屏障,使恶性肿瘤细胞能逃避内源性防御机制的损伤。研究发现,FIB与肿瘤的转移密切相关。FIB通过p-蛋白激酶B(protein kinase B,PKB,又称AKT)/p-雷帕霉素靶蛋白(mechanistic target of rapamycin kinase,MTOR)途径显著促进细胞迁移和侵袭,促进肿瘤上皮-间充质转化等恶性生物学行为。FIB与成纤维蛋白生长因子-2和血管内皮生长因子相互作用,促进肿瘤细胞生长和血管生成。
研究表明,胰腺癌、胃癌、肺癌、食管癌、乳腺癌、肾癌等肿瘤,FIB 水平是生存的独立预后因素。龚晶等探讨236例晚期非小细胞肺癌患者一线化疗与血浆FIB状态及预后的相关性,结果显示,FIB正常组和升高组总生存时间分别为20.8个月和15.1个月(P<0.01)。另一项回顾性分析结果显示,高FIB组、低FIB组患者的中位PFS分别为142天和204天,中位总生存时间分别为317天和427天,差异均有统计学意义(P<0.01)。Cox风险比例模型显示,FIB升高是影响PFS和总生存时间的独立因素。对于可切除非小细胞肺癌,有研究发现,相比较于正常组,术前FIB、D-D高水平组患者无复发生存(recurrencefree survival,RFS)、5年生存率均更差。
目前,凝血功能与EGFR-TKI疗效的相关性研究国内外报道很少。本研究发现,FIB≤498 mg/dl组患者中位PFS为13.2个月,明显长于>498 mg/dl组患者的7.0个月。D-D是纤维蛋白的主要酶解产物之一,是凝血和纤溶系统的重要组成部分。D-D升高患者预后更差,PFS明显缩短。FIB、D-D水平可能是TKI疗效的预测指标。本研究分析D-D水平与TKI耐药的关系,结果显示,D-D水平预测TKI耐药的灵敏度、特异度、诊断符合率均较高。D-D升高与EGFR-TKI耐药有关,D-D水平正常则提示病情稳定。D-D水平对于TKI耐药、病情进展可能有一定预测作用。
综上所述,本研究提示,FIB、D-D可能是肺癌靶向治疗较敏感的生物标志物,对疗效有较好的预测作用。相比较于影像学检查,更加简单易行,且价格低廉,有一定的临床意义。同时,降低D-D、FIB水平,改善血液高凝状态,可能是防治TKI耐药的一个重要策略。本研究不足之处为样本量较小、回顾性分析,需要大样本研究进一步验证。
