锂电池中固体电解质界面研究进展
2021-11-22杨毅闫崇黄佳琦
杨毅,闫崇,黄佳琦,*
1北京理工大学材料学院,北京 100081
2北京理工大学前沿交叉科学研究院,北京 100081
1 引言
2019年,诺贝尔化学奖授予了三位对锂离子电池发展做出卓越贡献的杰出科学家John B.Goodenough、M. Stanley Whittingham和Akira Yoshino。自1991年商业化锂离子电池问世以来,因其能量密度高、充放电循环稳定、安全性高等优点,逐步应用于各类电子产品与电动汽车中1–8。随着大众对手机、笔记本电脑等电子产品的应用需求增加,以及对电动汽车续航能力的要求,促使锂离子电池不断朝高比能、高安全性、高充电速率、低成本等方向发展9–14。为满足这些发展目标,科研人员不断开发出更先进的电极材料和电解液,电极材料在提升电池的能量密度方面发挥着关键作用,而电解液在增强电池的循环稳定性方面扮演重要角色。
电解质的加入会在电极表面产生电极/电解质界面,目前关于“界面”与“界面膜(层)”的定义比较模糊,界面一词是作为描述相变界的专业术语,而有界面的存在就会产生界面自由能,引发物质在界面吸附,形成界面膜(层);另外,若两相接触后在界面发生化学或电化学反应,其反应产物会存在于两相界面上,且产物性质会明显与两相不同,即形成界面膜(层)。在电池首次充放电过程中,电解液组分与电极在液固界面上发生氧化还原反应,反应产物在电极表面堆积形成钝化层,该钝化层就是电极/电解质界面膜。电极/电解质界面的稳定性对于电池的循环性能及寿命十分重要15,一方面,界面膜形成阶段会消耗部分锂离子(Li+),造成电池容量损失;另一方面界面膜具有离子导通、电子绝缘性质,可以保障锂离子的快速迁移及阻止电解液组分的持续分解,同时也防止溶剂分子共嵌入对电极材料造成不可逆的破坏。
通常来说,在负极表面形成的界面膜被通称为固体电解质界面(solid electrolyte interphase,缩写为SEI),而在正极表面的界面膜被通称为正极电解质界面(cathode electrolyte interphase,缩写为CEI),SEI与CEI被统称为电极电解质界面膜(electrode electrolyte interphase,缩写为EEI)16–18,而EEI的结构组成会影响电极的离子传输过程和电池充放电稳定性19,20。近年来,研究人员通过实验与理论计算相结合的方式对SEI和CEI的形成机理、组成与结构、离子传输方式、界面优化调控等方面进行了详细研究,并在基础研究和应用研究领域取得了重要突破。
虽然当前领域内针对于SEI的研究已经取得一定进展,但受限于SEI的自身稳定性和复杂性、纳米尺度下的有限研究方法等因素,SEI的结构和成分认知及准确调控策略还处于初级阶段。
本文综述了在液态电解质环境下锂离子和锂金属电池等二次电池体系SEI的最新研究进展,重点展开讨论了以下几个关键问题:(1)在首次充放电时,电极/电解质界面有何过程发生?(2)对于界面膜来说,SEI的组成与结构是怎样的?(3)电极/电解质界面形成后,锂离子如何穿过界面膜到达电极表面的?(4)如何调控及改善SEI,以优化电池性能?
2 界面形成机制
在锂离子电池充电阶段,Li+从正极脱出通过电解液与隔膜到达负极,同时正极电势升高,负极电势降低,电池电压升高;而在电池放电阶段,Li+从负极返回到正极,降低电池的电压。随着电池电极表面的电势的升高/降低,电解液组分与电极之间也发生着电化学反应,其固相氧化/还原产物堆积在电极/电解液之间产生一层界面膜,是一种多相混合物。而该界面膜能在允许锂离子的传导的同时隔绝电子的传输。
对于石墨负极来说,随着负极表面电势的不断下降,其表面的多种组分(阳离子、溶剂、阴离子、添加剂、痕量水)发生竞争反应,并还原产生SEI,还原反应的顺序与速率取决于各组分的还原电位、浓度、反应活化能等因素。图1展示了石墨表面SEI的形成过程,An等21认为石墨表面大多数的还原反应发生在0.8–0.2 V (vs. Li/Li+),还原反应产生的有机/无机的不溶性产物沉积在石墨电极表面,可溶性产物则扩散到电解液中;如果SEI尚未完全形成,负极电位继续下降到0.2 V (vs. Li/Li+)以下时,溶剂分子与Li+形成的溶剂化基团会共嵌入石墨层间,如果共嵌发生过多,将诱发产生石墨的剥离;对于碳酸丙烯酯(PC)溶剂来说,在0.9 V(vs. Li/Li+)以下时,PC就会共嵌入石墨层间甚至引发石墨的剥离,对电池负极的稳定性造成不可逆损失。

图1 石墨表面SEI形成过程示意图21Fig. 1 Schematic of the SEI formation process on graphite surface 21.
2.1 界面膜形成过程
Liu等22采用电化学石英晶体微天平(EQCM)、微分电化学质谱仪(DEMS)和原子力显微镜(AFM)原位监测高定向热解石墨(HOPG)表面SEI的形成过程。如图2a,b所示,采用循环伏安法(CV)从开路电位(3.0 Vvs. Li/Li+)扫描到0.0 V (扫速为1.0 mV·s-1),并将该过程分为四个阶段。图2a显示,第II、III阶段出现明显的还原峰,对应LiF的生成和电解液中有机组分的还原;图2b的原位AFM图象显示,在电压2.0 V下降到0.91 V时,此阶段可以发现石墨表面产生不规则的岛状沉积,对应LiF的生成;而在0.91到0.74 V阶段,溶剂分子与Li+形成的溶剂化结构共嵌入石墨层间;0.74到0.62 V阶段内,共嵌入石墨中的初始溶剂化鞘层中的碳酸乙烯酯(EC)开始发生还原,沉积的颗粒开始大量增多并且进行聚集,表明SEI开始形成;电压在0.62 V以下时,共嵌入的溶剂分子不断被还原,SEI的厚度不断增加;在随后的正扫阶段,电压上升到0.3 V以上时,SEI中部分有机组分发生再氧化,形成Li2O。

图2 (a)石墨负极表面SEI形成过程中的电位与质量变化曲线22;(b)电位变化过程中石墨负极表面的原位AFM图像22Fig. 2 (a)Curve of potential and mass change during the formation of SEI on graphite cathode surface 22;(b)In situ AFM image of graphite cathode surface during potential change 22.
电池在充放电循环过程中,正/负极不断经历电位的上升和下降,图3a展示了电解液在电极表面被氧化还原的能级示意图。其中图中μA与μC分别表示负极和正极的电化学势,电解液的电化学稳定窗口即其最低未占据分子轨道(LUMO)与最高占有分子轨道(HOMO)的能级差。Goodenough等23认为当μA位于电解液的LUMO能级之上时,电解液组分将会发生还原分解,若μC低于电解液的HOMO能级,将会氧化电解液。对于锂离子电池来说,常用的有机电解液多为碳酸盐类,其氧化电位约为4.7 V (vs. Li/Li+),还原电位为1.0 V (vs.Li/Li+),但Li+插入石墨层间则发生在0.25至0 V (vs.Li/Li+)之间32,明显低于电解液的还原电位;因此在充电阶段石墨电极电位低于1.0 V (vs. Li/Li+)后,电解液发生还原分解,其中不溶的产物则逐渐沉积在石墨表面形成SEI。虽然这一反映正/负极界面膜形成机制的模型被广泛使用,但是电解液组分的电化学稳定窗口和其HOMO与LUMO的能级差并不一致,如图3b所示,一方面HOMO与LUMO能级是为研究独立分子的电子质而提出,而由于溶剂分子之间的相互作用会对溶剂的氧化还原电位产生影响,导致HOMO能级偏移可达4.0 eV,因此需要注意表述的严谨性24。
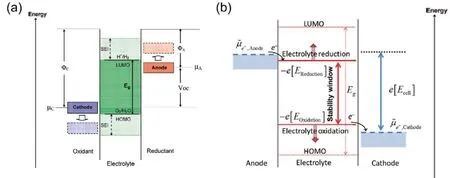
图3 (a)电解质在电极表面发生氧化/还原反应的能级示意图23;(b)对电解质稳定性与正/负极电位和HOMO和LUMO能级关系的修正模型24Fig. 3 (a)Energetics of the formation of the anode and cathode SEI layers under electroreduction and electro-oxidation conditions 23; (b)Correct notation for the negative and positive potential limits for the electrolyte stability, and the energy levels of HOMO and LUMO 24.
借助分析仪器可以通过信号的反馈监测界面演化过程,但是该如何从更微观的视角去揭示界面形成的机理?近期的研究发现电极表面初始双电层结构中的行为对于界面形成影响较大,即发生在内亥姆霍兹层的离子特性吸附和锂离子的溶剂化行为将会共同影响电解质界面的形成,如图4a所示,发生在电极表面的离子特性吸附的氧化还原将决定界面初始的化学组成和结构,而溶剂化结构则参与影响界面的动态演变过程,两者相互耦合共同影响界面的稳定性25,26。

图4 (a)循环前后电极/电解质界面演化示意图28;(b)双电层模型的发展历程30Fig. 4 (a)The schematic diagram of the interface formation before and after cycling 28; (b)The development models of electric double layers 30.
2.2 内亥姆霍兹层的离子特性吸附
当电极与溶液发生接触时,电极中的锂金属原子有失去电子变成离子并离开电极表面的趋势。对于锂这一活泼性金属来说,表面的锂离子将会离开电极表面进入电解液中,使得锂金属电极表面带负电荷,在电极与溶液界面瞬间产生电势差;同时电解液组分受到静电吸引和本身热运动的影响,在两者达到平衡时会在电极/电解液界面处形成双电层27,28。
双电层这一概念在1853年被von Helmholtz提出并且模型化,经过Gouy、Chapman和Stern的改进被大家所认可29。如图4b所示,Stern将双电层分为紧密层(Compact Layer)与扩散层(Diffusion Layer);其中紧密层又包括内亥姆霍兹层(Inner Helmholtz Plane)与外亥姆霍兹层(Outer Helmholtz Plane)30。在电极初始状态的内亥姆霍兹层中,存在着溶剂分子和阴离子的特性吸附;同时被内亥姆霍兹层有限的空间所限制,内亥姆霍兹层中无法容纳溶剂化基团。在外亥姆霍兹层中不存在特性吸附现象,但是存在溶剂化结构的基团;亥姆霍兹层是特性吸附离子、溶剂化基团等反应底物距离电极最近的地方,也是初始阶段溶液中的离子和电子在三相界面处发生氧化/还原反应的主要场所。
Yan等25认为双电层中的特性吸附现象可能仅存在于电池首次循环前,循环后它将会被电子绝缘的电极/电解液界面所替代,作为架接电极和电解液体相的重要桥梁,电极表面内亥姆霍兹层中初始状态下的离子特性吸附将直接关联电极/电解液界面的氧化还原反应,影响界面结构和化学成分。电极表面初始状态下的特性离子吸附对界面调控的研究也逐渐被报道31–37,通过调控亥姆霍兹层中的特性吸附物种构建稳定界面已取得不错效果,但需要进一步探究更多影响特性吸附的因素,例如阴离子和溶剂分子的电子给体数(Donor Number),电解质介电常数和吸附粒子的空间位阻等因素都将会影响电极表面特性吸附的结果,同时需要更深入的研究去挖掘它们之间的关系。
从1924年Gouy-Chapman-Stern模型的提出和发展促进了现代电化学的进步,同时也面临着一些挑战。新材料体系和新型复杂电池体系的应用过程中发现的现象很难去用经典模型和理论去完美解释。因此对双电层更深层次的认识、理解和拓展对调控电极/电解液界面反应有重要意义。
2.3 溶剂化结构
锂离子电池的性能与其界面的物理/化学状态密切相关,而界面物理/化学状态深受电解质的影响。除了特性吸附之外,Li+的溶剂化结构是影响电极/电解质界面的另一个重要因素。大量的研究主要集中在溶剂化结构与石墨负极9,38–42、硅负极43–45、锂金属负极46–52等表面SEI的关系;CEI与LiCoO253、LiMn2O454,55、LiFePO456–59、LiNixCoyMn1-x-yO260等正极材料的关系。
从界面形成过程来说,电解液体相的溶剂化结构对于电极/电解质界面膜的形成影响显著,已有的研究进展表面在低浓度电解液中,锂离子容易与强极性的溶剂分子形成溶剂化结构,而阴离子被排除在溶剂化鞘层之外;但在高浓度电解液中,阴离子则更容易进入到溶剂化鞘层中。这些参与到溶剂化结构中的电解液组分尤其是进入内溶剂化层的成分将会参与到EEI的形成,从而影响电解质界面膜的结构、成分、离子导率和厚度等61–71。
在稀溶液中环状溶剂分子相比于链状溶剂分子和阴离子来说,在与阳离子(Li+、K+、Na+、Al3+等)进行配位时更易形成环状溶剂分子主导的溶剂化结构40。对于低浓度电解液体系(LHE)来说,Li+会与强极性的溶剂分子形成溶剂化结构,而大多数阴离子则被排除在溶剂化鞘层之外9;当采用高浓电解质体系(HCE),阴离子有更多机会进入到初始溶剂化鞘层中65–67,如图5所示。在形成SEI过程中,如果电解液的浓度较低时,溶剂分子将会被先还原;而在高浓度电解液中,更多阴离子进入溶剂化鞘层中,将会被优先还原分解,而由阴离子主导形成的含无机组分较多的SEI具有更快的离子传输速率64。

图5 稀电解液和超浓电解液中所形成不同溶液化结构的示意图66Fig. 5 Schematics of the solution structure in dilute and superconcentrated electrolytes 66.
阴离子主导的界面化学可以让更多的阴离子参与界面膜的形成过程,以获得优良的电池性能。Yao等9成功地制备了一种弱溶剂化电解质(WSE),实现了在低盐浓度下于电解液中形成大量离子对和聚合体,在低浓度盐条件下让更多的阴离子参与到溶剂化鞘层中;因WSE的溶剂化结构在石墨电极上形成了独特的阴离子衍生的电极界面,实现了电池快速充电和长期稳定循环的性能。他们通过第一性原理来揭示溶剂化结构中阴离子和溶剂分子对锂离子的竞争配位,为未来新电解质的开发设计提出了新思路。
3 SEI组成与结构模型
SEI是负极/电解液界面处电解液组分发生还原分解并沉积在负极表面所形成的一层薄膜,其厚度通常在几个纳米到几百纳米之间。领域内对SEI的化学组成和结构的研究呈现出百家争鸣的态势72–74,因为温度、电解液体系、电池循环/化成条件、电极的表面活性等因素均能对SEI的成分和结构产生影响。
从1970年开始,人们开始关注负极表面的膜结构和组成75;1977年,Dey等76尝试去表征锂表面形成的物质;1979年Peled等77提出SEI的马赛克模型;到1999年Aurbach等78提出SEI的层状模型。目前马赛克模型和层状模型是两种描述SEI的主要模型。
在马赛克型的SEI中,电解液组分发生还原生成的有机产物和无机产物随机地分布在电极表面79,80,如图6a所示。而这种在电极表面上,形如马赛克般的非均质结构将影响Li+的传输路径81,因为Li+总是沿着迁移速率快的通道进行移动,由于沿不同SEI组分的迁移速率不一样,很难在锂金属负极实现Li+的均匀化沉积/脱出过程,而这也将引起锂枝晶和死锂的产生。

图6 (a)用多种有机/无机组分来描述SEI的马赛克模型示意图77;(b)SEI层状结构模型示意图82;(c)石墨表面SEI形成过程的示意图22Fig. 6 (a)The traditional mosaic model to describe the SEI with multiple organic/inorganic components 77; (b)Schematic diagram of SEI layered structure model 78; (c)Schematic diagram of SEI formation process on graphite surface 22.
对于SEI的层状模型来说,电解液组分还原产物较为均匀的分布在电极表面形成层状结构,如图6b所示,一般来说其由低氧化态的无机内层(例如LiF、LiO2、LiCO3、LiOH等)和高氧化态的有机外层(例如ROCO2Li、ROLi等)组成82。在SEI的初始形成阶段,电解液组分先被还原为有机产物,距离电极表面较近的组分随后进一步还原为较为稳定的无机物,此无机物层极大地影响了SEI的电子绝缘性能81–84。
SEI组分的还原过程如图6c所示22,在界面形成初期,电解液的组分逐渐被还原成沉积到石墨表面形成SEI的有机组分,随后随电位下降,还原分解得到的有机组分进一步还原,形成LiF、Li2O、Li2CO3、Li2S等84,85。
4 基于电极界面的Li+传输
电极/电解液界面的SEI与CEI在经过一系列复杂的反应形成后,其含有的有机/无机组分为后续Li+的传输构建了从电解液通往电极表面的道路。对于充电过程来说,Li+首先经历脱溶剂化这一过程,随后通过SEI到达电极表面得到电子。Li+的脱溶剂化行为及通过界面的传输与电池的循环性能、快充能力甚至是安全性密切相关86,87。
4.1 脱溶剂化
如图7所示,溶剂化的Li+在穿过SEI前需要完全脱去它的溶剂化鞘层,然后在多晶态的SEI中进行固相扩散87,88,如图7所示。脱溶剂化过程被认为是限制锂离子电池石墨负极快充性能的重要因素89,而溶剂化作用环境和SEI的性质都会影响脱溶剂化过程的自由能。

图7 锂离子脱溶剂化和随后在多晶态SEI与石墨层间的扩散过程示意图87Fig. 7 Li ions undergo the desolvation and subsequent diffusion process to across the polycrystalline SEI 87.
电化学阻抗谱(EIS)通常被用来研究Li+的脱溶剂化过程,Ogumi等63采用EIS研究不同电解液体系下Li+在石墨负极表面的传输活化能,发现裸Li+和溶剂化的Li+活化能分别为25和53–59 kJ·mol-1,意味着Li+在嵌入石墨前的脱溶剂化过程能垒较大,过程相对缓慢。
SEI的化学性质同样影响Li+的脱溶剂化过程,Xu等90认为理想的SEI不仅在物理意义上是足够薄的,而且也应具有一定的化学性,可以催化Li+快速打破溶剂化鞘层,以实现脱溶剂化过程的快速完成。
4.2 传输方式
关于Li+在SEI中的扩散方式,目前主要有两种观点,一种是Li+通过空位、间隙或者是晶界进行扩散;另一种观点是来自电解液中的Li+进入SEI中,挤压SEI组分中原有的Li+,使其在SEI中进行扩散。
SEI中的不同组分对于Li+有着不同的迁移能垒91,例如Li3N的扩散势垒最低(0.007–0.038 eV),这可以解释富含Li3N组分的SEI中Li+的迁移速率较快。而对于LiF、Li2CO3和Li2O等物质,其晶界周围对Li+来说是优良的通道。Shi等92认为,Li+穿过SEI的过程可以分为两个机制,第一阶段是Li+可以通过电解液浸润SEI外层疏松多孔的有机层进行SEI的外层扩散;第二个阶段是在内层Li2CO3等无机层的碰撞扩散。
5 电极/电解质界面膜的调控
电极/电解液界面膜对电池的性能有重要影响,对于理想的界面来说应该具有以下的要求:(1)具有稳定的物理/化学性质,同时具有高度的电子绝缘性和快速且均匀的锂离子选择通过性;(2)具有一定的机械强度和弹性,既能适应电极材料的体积变化,又能在循环过程中保持结构的稳定性;(3)具有高度致密性,抑制溶剂分子热力学腐蚀反应和共嵌入反应等。为了实现这些要求,许多研究者从电解液添加剂、电流密度、温度及电极表面改性等角度进行了研究。
5.1 电解液添加剂
Aurbach等93通过试验证实电解液中添加碳酸丙烯酯(VC)可以在碳负极表面生成聚烷基碳酸锂化合物,而该化合物可以抑制共嵌行为的发生,从而提高SEI的稳定性。Brown等94通过透射电镜发现氟代碳酸乙烯酯(FEC)的分解可产生独特的LiF纳米结构,如图8a所示,而且LiF的生成可以实现均匀的锂沉积和脱出过程,利于电池循环性能的提升;而Pritzl等95发现在LiNi0.5Mn1.5O4(LNMO)/石墨软包电池充电34 min后,VC开始在LNMO正极表面氧化分解,而且由于VC在正/负极表面氧化/还原分解成膜,使得电池的阻抗增加,循环性能变差。Aspern等96设计了两种磷烷分子(PFPOEPi和PFPOEPi-1CF3)作为电解液添加剂。他们通过理论和实验结果表明,所设计的磷烷分子在正极表面进行分解并发生聚合反应参与CEI的形成,如图8b所示,而且证实该过程是由化学反应控制;另外由于CF3基团的引入,降低了所形成的CEI的厚度,但导致电池电荷转移阻抗显著增大,降低了电池循环的稳定性。除了上述介绍的添加剂外,1,3-二氧戊环(DOL)97,98、三氟代碳酸丙烯酯(TFPC)99、氟醚(HFE)100,101等电解液有机添加剂也会对界面膜性能产生影响。Ding等102还通过降低Cs+阳离子添加剂的浓度将其还原电势降低到Li+的标准还原电位以下,实现Cs+在循环过程中不被消耗;同时由于Cs+在金属锂上的附着,在锂负极表面形成致密的正电屏蔽层,如图8c所示,可以形成一个自愈的锂沉积过程,实现对锂沉积形貌的调控。

图8 (a)FEC分解产生的独特的LiF纳米结构极大地提高了Li的循环性94;(b)磷基添加剂在NMC111电极表面的分解机理示意图96;(c)特殊阳离子添加剂(Cs+)形成自愈锂沉积的屏蔽层示意图102;(d)不同条件下结构均匀性和机械强度对SEI失效时间的影响示意图106;(e)90和25 °C时SEI的形成过程示意图108Fig. 8 (a)The unique LiF nanostructure generated by FEC decomposition contributes to greatly enhanced Li cyclability 94;(b)Postulated decomposition mechanism of phospholane-based additives on NMC111 electrode surface 96;(c)Additives with specific cations (Cs+)to serve as a screening layer for self-healing Li deposition 102;(d)Influence of structural uniformity and mechanical strength on SEI failure time under differentoperating conditions 106; (e)The SEI formation mechanisms at 90 and 25 °C 108.
5.2 电流密度
Dollé等103发现电流密度对界面膜的组成影响十分显著,在电流密度较低时,Li2CO3首先形成,而ROCOOLi在电极放电结束前才开始形成;在较高的电流密度下,SEI只含有Li2CO3却没有ROCOOLi的生成。Ota等104采用色谱-质谱研究碳负极表面SEI形成过程发现,在较高电流密度时,SEI的无机组分先于有机组分形成;而在较低电流密度条件下,SEI的有机组分首先形成,这与Dollé的研究结果不同,但应注意到两者所用的电解液也是不同的。
同时,电流密度也会影响SEI结构的稳定性105和均匀性,如图8d所示,Shen等106通过模拟计算认为当SEI的弹性模量达到3.0 GPa后,通过低电流密度条件得到的均匀SEI结构对于电池性能来说更加重要。
5.3 温度
温度对界面层组分有明显影响,Stetson等107研究了硅负极表面的SEI演变情况,研究发现温度升高将会使得SEI有机组分发生溶解导致其厚度变薄,同时界面阻抗也发生了下降。Hou等108采用一种耐高温电解液研究锂金属全电池在90 °C下的工作状况,发现在90 °C下锂盐和溶剂会发生不完全的分解,如图8e所示,导致SEI中无机组分含量下降,形成更多不稳定的中间体,与在25 °C下循环的电池相比,SEI中无机组分的减少和不稳定中间体增加引起其结构非均匀性增加和阻抗的上升。Yan等109研究了温度对石墨负极表面SEI的影响,研究发现在高温下电极与溶剂分子反应活性增加,电解液组分会发生副反应并且产生气体,导致电极/电解质界面不稳定性增加;在低温时,形成的SEI具有较低的离子导率,使得组装的全电池首次库伦效率仅有17%;而在室温下形成的SEI则具有很好的离子导率和电子绝缘性。
5.4 杨氏模量与压力
SEI的形成受电解液、电极材料、电池循环条件等因素影响,同时SEI的机械特性与其组分和结构密切相关。Shin等110研究了SEI的弹性与其本身化学组成和结构的依赖性,实验与理论计算结果表明,SEI内层无机组分的杨氏模量明显高于外部的有机/聚合物层,同时研究发现内层无机成分的弹性与晶体结构密切相关,比如晶体相的LiF和Li2CO3的杨氏模量均高于两者的非晶相组分;研究结果表明虽然SEI的外层有机/聚合物组分的杨氏模量低于内层,但是致密的无机组分主导的内层将很难承负极材料循环过程中的体积变化,易导致SEI的结构发生破裂;反而弹性较好的外层组分能承受负极在嵌/脱锂过程中的体积变化。对于石墨负极来说,其在充放电过程中体积变化较小;而硅负极或锂金属负极则由于其在充放电时巨大的体积膨胀及SEI的不稳定性,限制了两者的实际应用,因此,在减少硅负极/锂负极体积膨胀和缓解应力工作方面有一定研究进展111–113,此外,从SEI的柔韧性出发,可以通过改变电解液组分或化成条件,形成柔韧性较好的SEI组分并将其利用于充放电过程中体积形变较大的负极材料,比如金属锂和硅负极。
Louli等114采用实时压力测量法分析5种402035型软包电池在循环中的压力进行分析,将负极SEI生长情况和电池性能关联起来,研究发现在循环过程中电池在充电阶段体积发生膨胀,内部压力增加,放电时则相反;进一步研究发现负极活性材料发生不可逆体积膨胀将会引起不可逆的压力增长,这也将导致SEI发生破裂后继续生长,尤其是含有硅的负极SEI显著增长,消耗更多的锂,造成电池容量的下降;而且实验结果证实电池的容量损失率与压力增长率之间存在线性关系,即电池的压力增长越快其容量损失率越大。
5.5 电极表面改性
根据SEI的形成过程和机理,人们采用掺杂、预处理、包覆等方法对电极表面进行改性,以优化界面膜的性能。Cheng等115提出“植入式SEI”的概念,通过将锂金属在精心设计的三元电解液中预循环后,在锂表面构建了一层极其稳定的SEI,并且该SEI在醚基和碳酸盐基电解液中均可以与硫和LiNi0.5Co0.2Mn0.3O2正极形成很好的兼容性。
Yan等116提出了混合导体中间相(MCI)的概念,利用氟化铜溶液预处理锂金属得到含LiF/Cu的MCI保护膜,如图9a所示;由于MCI膜具有高的杨氏模量和充足的LiF/Cu晶界,在提升离子导率的同时也促进了锂在界面的优先存储,抑制了枝晶的产生。利用MCI膜的上述优点,组装的LiNi0.5Co0.2Mn0.3O2/Li全电池可以稳定400次充放电循环。An等117利用紫外光(UV)处理石墨负极,增加了石墨表面氧的含量,利于后续形成较薄的SEI,提高电池容量保持率的同时也降低了电荷转移阻抗。关于人工SEI,Zheng等118制备了一种高杨氏模量的非晶态碳纳米球薄膜,其在电池循环过程中可以很好适应电极的体积变化,而且SEI促进了对新沉积锂的钝化以抑制锂枝晶的产生。通过非晶态碳纳米球的包覆,锂金属电池在1.0 mA·cm-2的电流密度和1.0 mAh·cm-2的沉积容量条件下实现99%左右的库伦效率,而且电池寿命保持150次循环以上。为阻止电解液对锂金属负极进行腐蚀,实现锂的均匀沉积和无锂枝晶出现,Yan等119通过将锂板浸入氟代碳酸乙烯酯(FEC)中,在金属锂负极表面上构建了离子导通且致密的双层界面膜,最外层(顶部)的界面膜含有机组分,内层(底部)界面膜则富含无机组分,通过AFM对双层界面进行扫描,如图9b,发现外部有机组分层的杨氏模量约为0.6 GPa,对界面膜进行深入穿透,发现杨氏模量高达7.0 GPa,则对应内部的无机层。

图9 (a)通过LiF/Cu界面缓冲锂离子浓度和重新分布离子通道,以调控锂沉积过程原理图116;(b)界面的AFM图像和杨氏模量分布图119Fig. 9 (a)Buffering the concentration of Li ions and redistribute the ionic channels by LiF/Cu interface for dense and smooth Li deposition 116; (b)AFM topography image and Young's modulus distribution diagram of protected Li surface 119.
6 结论与展望
本文对近期关于界面的相关研究进展进行了综述,主要聚焦于界面的形成、界面描述模型和界面的调控。其中,内亥姆霍兹层中的离子特性吸附和外亥姆霍兹层中的溶剂化结构两种主要的行为对于界面化学来说至关重要,但需要更深入的研究来说明其中的关联。关于描述界面膜的模型,马赛克模型和层状模型作为两种主流观点常被用来描述SEI有机组分和无机组分的分布规律。随后讨论了基于SEI的Li+传输方式,包括脱溶剂化和SEI中的固相迁移,并阐述了可能的迁移途径和能垒。为了实现高性能、长循环的工作电池目标,人们对于界面的调控进行了大量的研究,在本文中也进行了相关的总结。
尽管人们对于电池界面的研究取得了一定的成果,但是需要继续探索电极/电解液界面深层的机制。从18世纪Galvani发现生物电以来,电化学已经发展了两个多世纪,如今越来越多的领域涉及到电化学,也促进了电化学学科的快速发展,但现在对于电池中各个现象的认识仍受限于电化学的发展,需要新的理论来指导探索未知的方向,未来的研究中以下几个问题希望能被重点关注和研究:(1)离子特性吸附与溶剂化结构与界面性质之间存在着怎样的联系?(2)如何更科学地描述Li+在界面处的传输过程,包括对SEI的结构和成分构建新的认识;(3)开发更先进的表征技术,从原子/分子的尺度精确追踪界面的形成、演化规律和离子传输途径,为已有现象提供更直接的解释和证据。
为了解决上述问题,需要多个学科的研究人员一起努力,提供先进的观点和独到的见解,相信在不断的合作和努力下,对电池内部界面行为规律和调控方面的理解有更大进步。
