紫衫烷类与蒽环类药物用药顺序不同对乳腺癌新辅助化疗疗效影响的meta分析
2021-11-20丁波泥钱立元文言广
邱 佳,丁波泥,钱立元,吴 唯,文言广
(中南大学湘雅三医院乳甲外科,长沙 410013)
在乳腺癌新辅助化疗中较常使用蒽环类和紫杉烷类药物,但临床医师很少关注这2种药物的用药顺序不同对疗效是否有影响。通常是先使用蒽环类药物再使用紫杉醇类,这种给药顺序似乎只是因为蒽环类药物首先被引入临床实践中,但并没有任何生物学理由可以证明这种给药顺序是标准的[1]。为探讨紫衫烷类与蒽环类药物用药顺序不同对乳腺癌患者新辅助化疗疗效的影响,本文对既往相关的临床研究进行了meta分析,现报道如下。
1 资料与方法
1.1 研究对象
将Pubmed、Cochrane 图书馆、Embase 数据库、中国知网(CNKI)、万方医学网等数据库中检索的比较紫衫烷类与蒽环类药物用药顺序对乳腺癌疗效影响的相关文献作为研究对象。本研究已在INPLASY上注册(编号:INPLASY202040134),可在inplasy.com上全面获取(http://doi.org/10.37766/inplasy2020.4.0134)。
1.2 纳入标准
(1) 研究类型为随机对照试验、新辅助化疗中比较紫衫烷类与蒽环类药物用药顺序对乳腺癌疗效影响的文献、全文等;(2)研究对象为乳腺癌患者;(3)暴露因素为紫衫烷类药物与蒽环类药物顺序或逆序用药,具体剂量及疗程不限定; (4)研究主要结局为总生存率(OS)、无病生存率(DFS)及病理完全缓解率(PCR),次要结局为保乳率、客观缓解率(ORR)、疾病控制率(DCR)及3~4级不良反应发生率。
1.3 排除标准
(1)重复文献;(2)非新辅助化疗;(3)非随机对照试验;(4)给药方案为联合方案,如紫杉烷类药物(包括紫杉醇、多西他赛)、阿霉素联合环磷酰胺(TAC)方案;(5)给药方案中同时包含内分泌治疗及放疗;(6)无结局指标或结局指标不符合标准的文献;(7) 非中、英文文献。
1.4 文献检索
采用自由词和主题词结合的方式检索Pubmed、Cochrane、Embase、中国知网(CNKI)、万方医学网等数据库,收集符合纳入标准的研究。英文检索词为Breast Cancer、Taxoids、Anthracyclines、randomized controlled trial等,中文检索词为乳腺癌、紫衫烷类药物、蒽环类药物、用药顺序等。检索时间为建库至2020年4月。
1.5 文献质量评估
按照Cochrane评价手册的系统评价评估标准5.1.0版本推荐的“偏倚风险评估工具”评价纳入研究的偏倚风险,如果存在分歧,则根据第3方研究人员意见予以决定。
1.6 文献资料提取
由2名研究人员对文献是否符合纳入标准进行评估,并提取相关数据。对文献纳入和提取数据有质疑者由第3名研究人员评估并通过讨论达成一致。对OS与DFS等数据,若文中提及危害比(HR),风险比(RR) 及95%可信区间(95%CI)则运用TIERNEY[2]等提供的Calculations Spreadsheet计算ln(HR)和SE[ln(HR)],若文章中未提供则运用Engauge Digitizer 12.1提取生存曲线数据,再运用上表计算ln(HR)和SE[ln(HR)]。
1.7 统计学处理
采用Revman5.3软件进行数据分析。以OS、DFS、PCR、保乳率、ORR、DCR、3~4级不良反应发生率为效应指标。采用RR及其95%CI为效应分析统计量。各纳入研究异质性检验采用CochraneQ检验,计算I2值。若研究间无统计学异质性(I2≤50%且P>0.10),选择固定效应模型进行meta分析;若存在统计学异质性(I2>50%或P≤0.10)则采用随机效应模型进行meta分析,同时对其异质性来源进行分析,无法解决或无法判定异质性来源时采用随机效应模型进行分析,必要时采用敏感性分析判断结果的稳定性,无法合并的指标采用描述性分析。以P<0.05为差异有统计学意义。
2 结 果
2.1 文献检索结果
初步检索出文献3 695篇,最终纳入符合标准的相关文献10篇[3-12],文献筛选流程见图1。累计总样本为1 956例,观察组(T→A组)982例,对照组(A→T组)974例。纳入文献基本资料见表1。文献质量评估结果见图2。
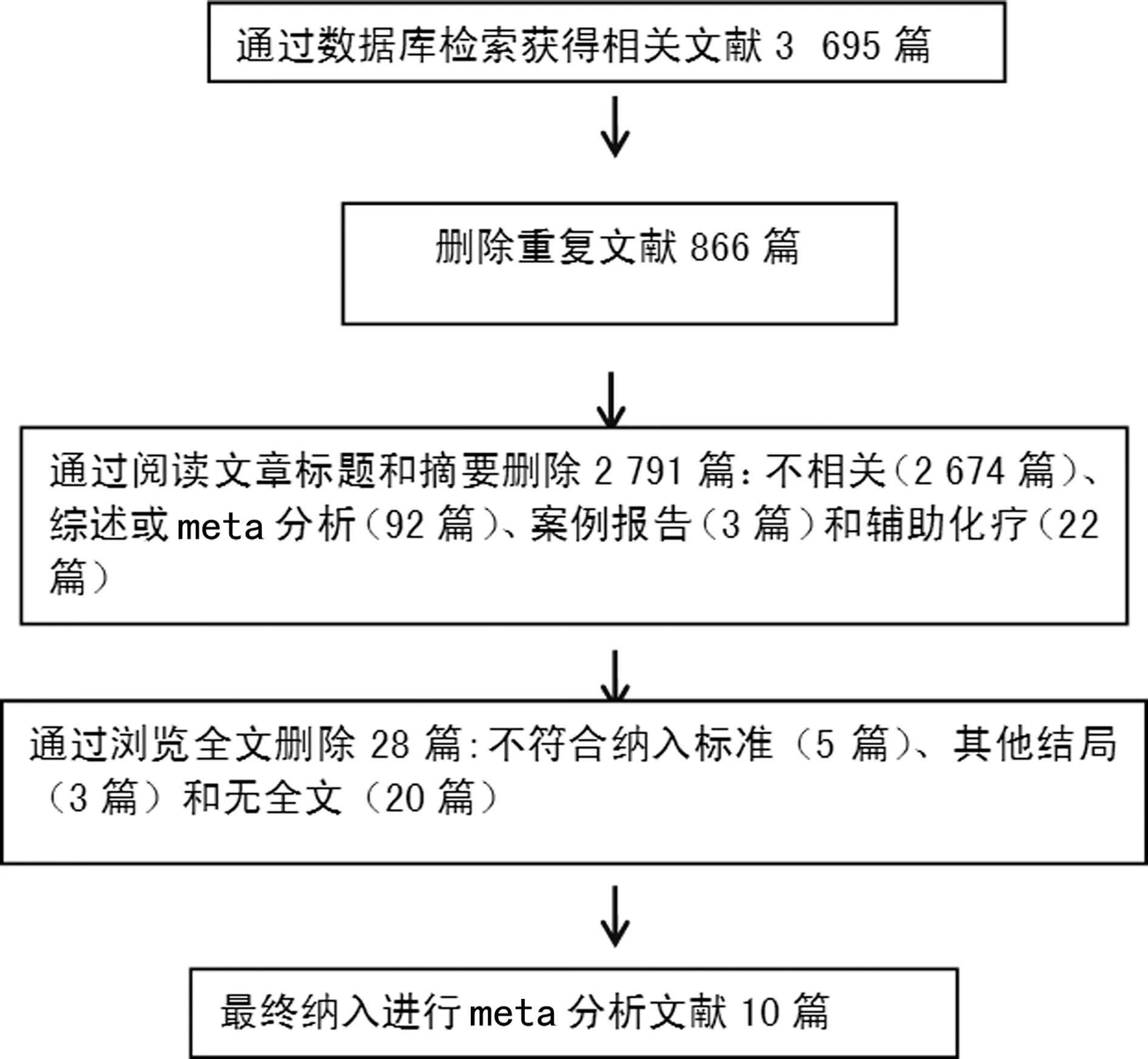
图1 文献筛选流程
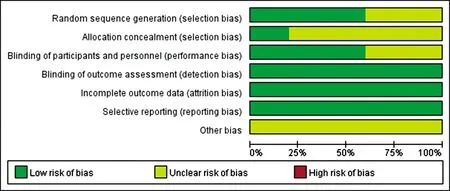
图2 纳入研究质量及偏倚风险评价
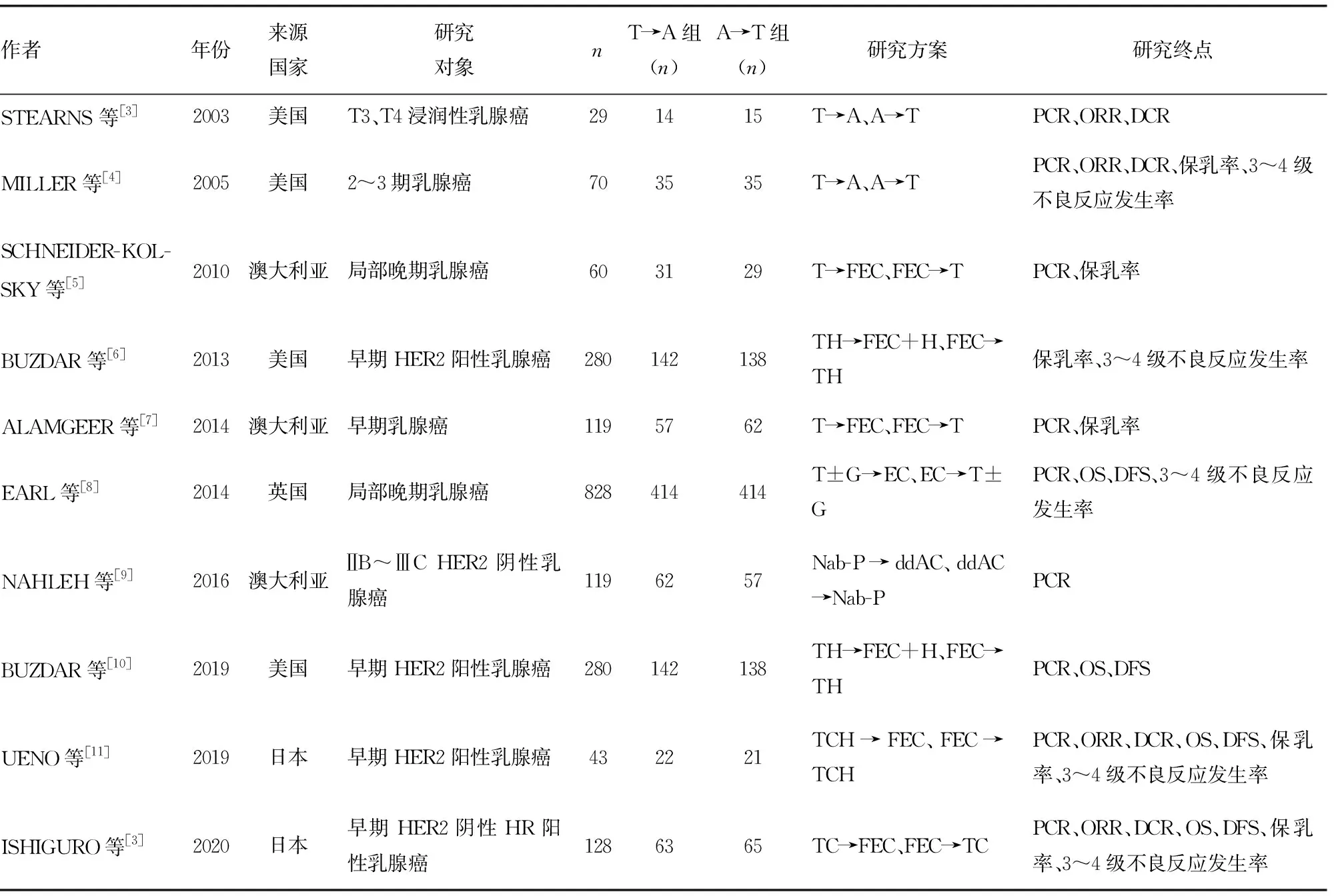
表1 纳入文献基本资料
2.2 meta分析结果
2.2.1预后
预后指标包括5年OS、DFS,效应指标采用HR表示。研究间无统计学异质性(I2=0%,P=0.64),选择固定效应模型进行meta分析。T→A组患者5年OS、DFS与A→T组比较,差异均无统计学意义(P=0.91、0.87),见图3。
2.2.2临床疗效
临床疗效指标包括PCR、ORR、DCR、保乳率及3~4级不良反应发生率。3~4级不良反应发生率包括骨髓抑制、消化系统反应及其他不良反应。效应指标采用RR表示,除中性粒细胞减少的研究间存在统计学异质性(I2=75%,P=0.02)采用随机效应模型进行meta分析外,其余指标的研究间无统计学异质性(I2≤50%,P>0.10),选择固定效应模型进行meta分析。两组患者PCR、ORR、DCR、保乳率比较,差异均无统计学意义(P=0.26、0.71、1.00、0.81)。在3~4级不良反应中T→A组患者更易发生白细胞减少,差异有统计学意义(P=0.000 01);两组患者其余3~4级不良反应比较,差异均无统计学意义(P>0.05),见表2。
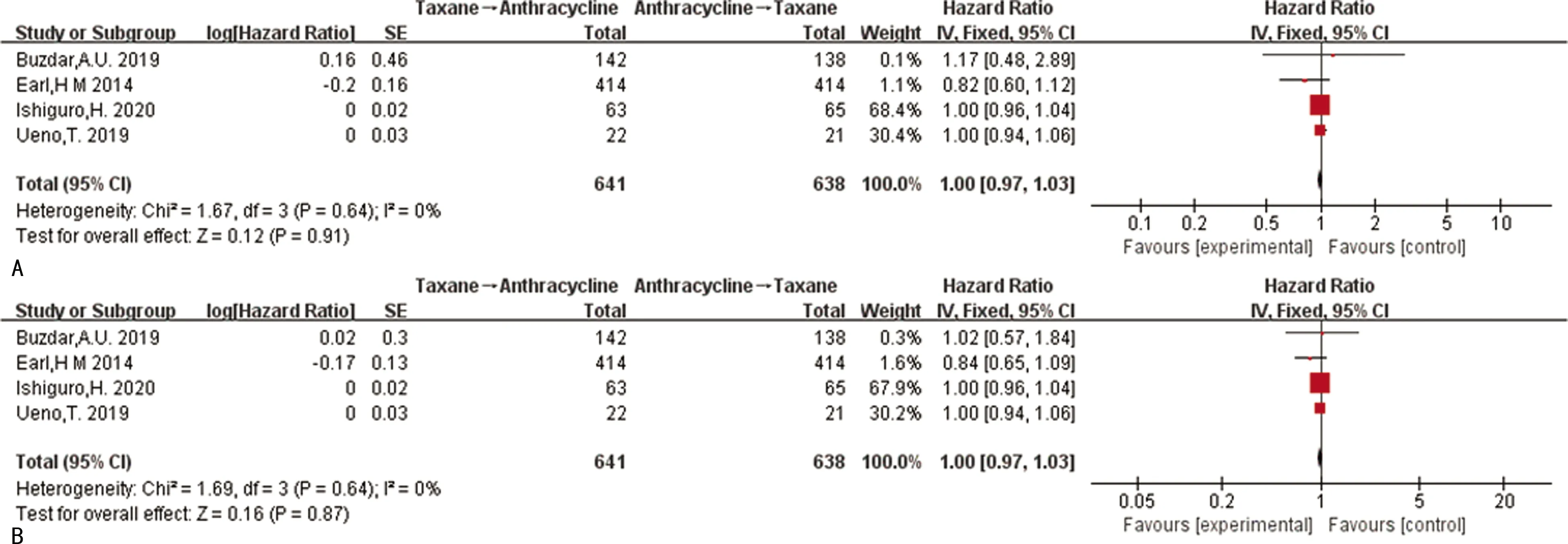
A:接受T→A组患者与接受A→T组患者的OS比较;B:接受T→A组患者与接受A→T组患者的DFS比较。
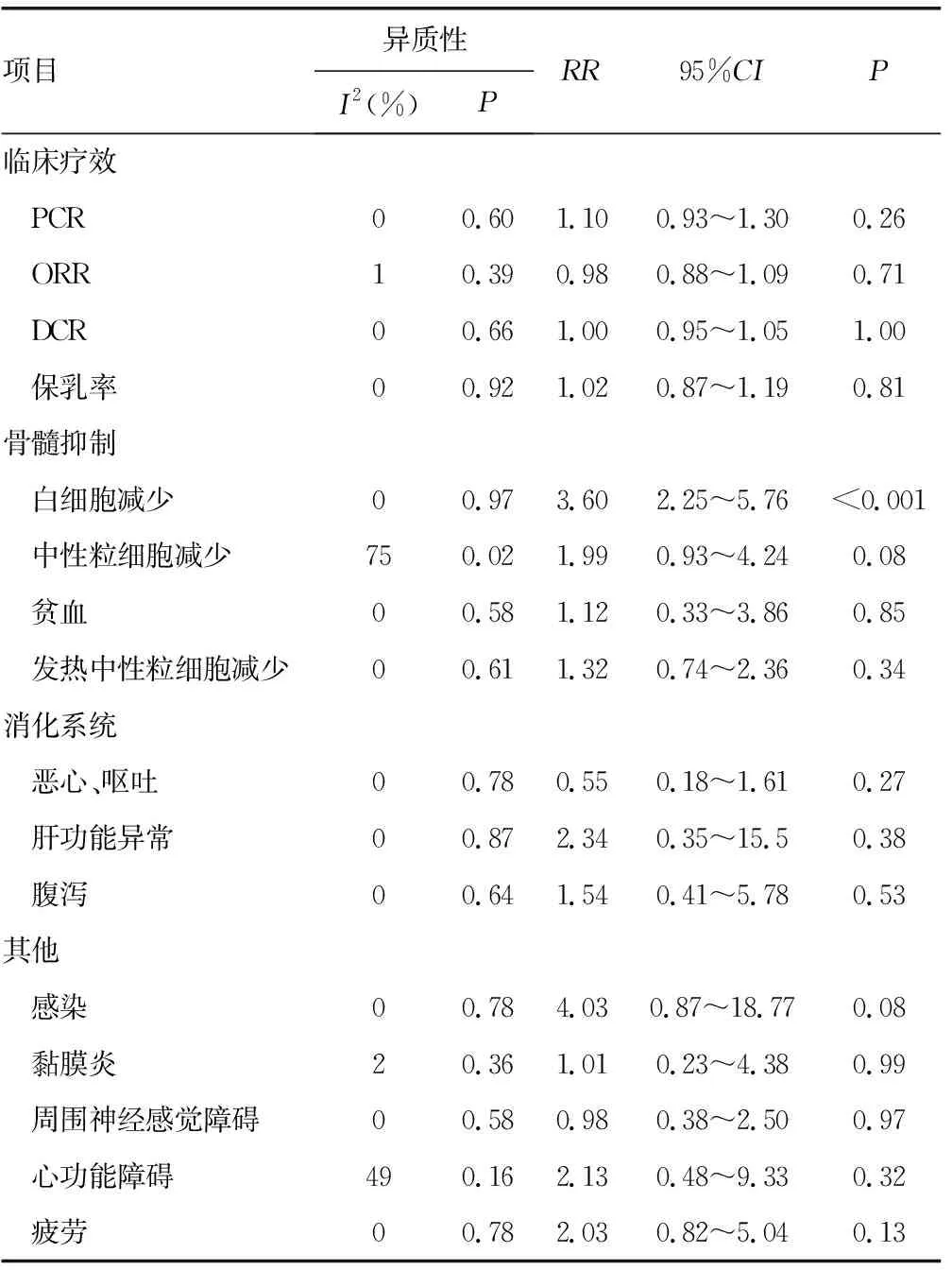
表2 两组患者临床疗效比较
2.2.3亚组分析
本研究旨在讨论紫杉烷类药物和蒽环类药物的使用顺序的不同是否会影响乳腺癌患者新辅助化疗的疗效,由于本研究纳入的文献大部分的给药方案均使用了其他药物,如氟尿嘧啶、曲妥珠单抗等,为探究这些药物是否会对结果产生影响,对结局指标PCR、ORR、DCR进行了亚组分析。两组患者PCR、ORR、DCR比较,差异均无统计学意义(P>0.05),且各亚组研究间不存在异质性,见表3。
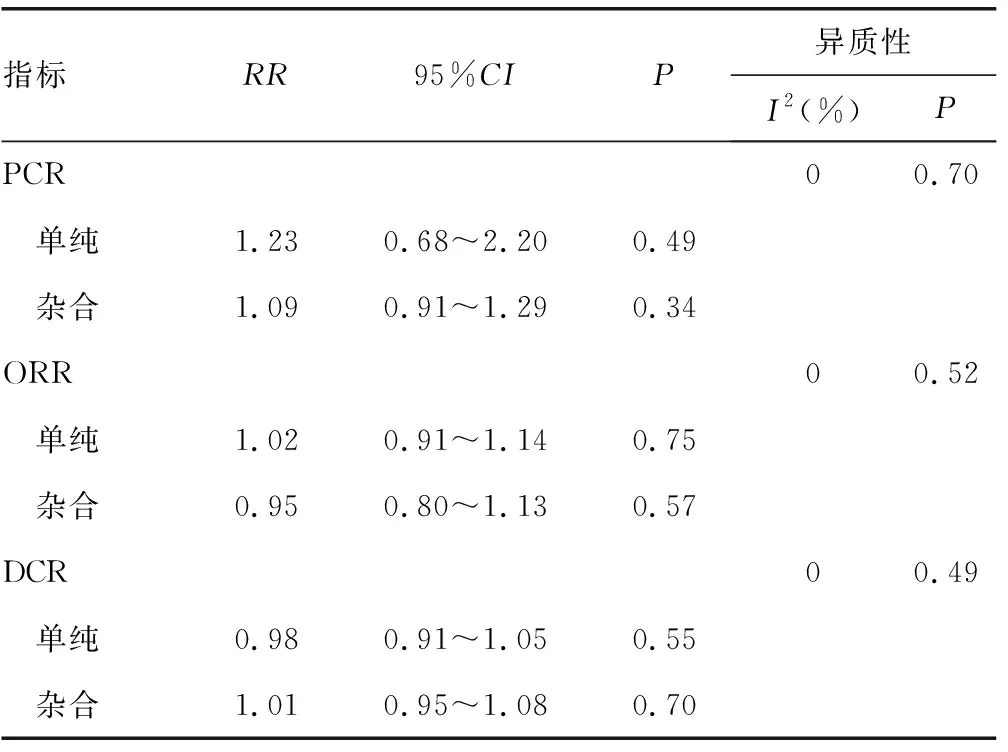
表3 PCR、ORR、DCR亚组分析
2.3 异质性分析
中性粒细胞减少的研究间存在统计学异质性(I2=75%,P=0.02),进行敏感性分析探讨其异质性来源,结果在剔除ISHIGURO等[12]研究后两组比较,差异仍无统计学意义(P>0.05),且RR、95%CI、P值均无明显变化,但异质性较前明显下降,见表4。
2.4 发表偏倚分析
对结局指标纳入研究数量大于5项者进行发表偏倚研究,以PCR、保乳率为指标绘制漏斗图。可见所有点全部落于漏斗内,各点基本对称分布,提示发表偏倚较小,见图4、5。
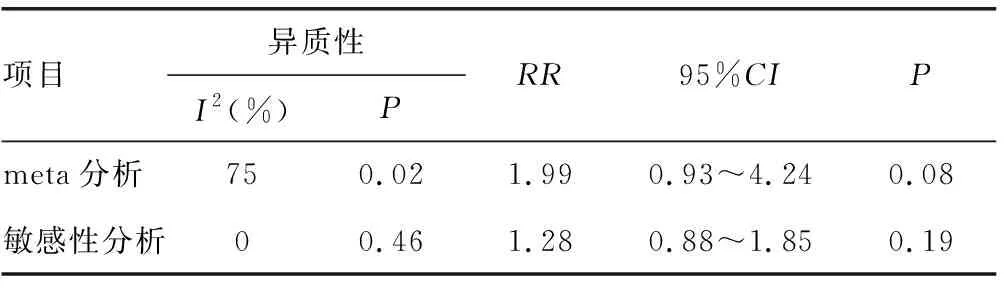
表4 两组患者中性粒细胞减少率比较的敏感性分析
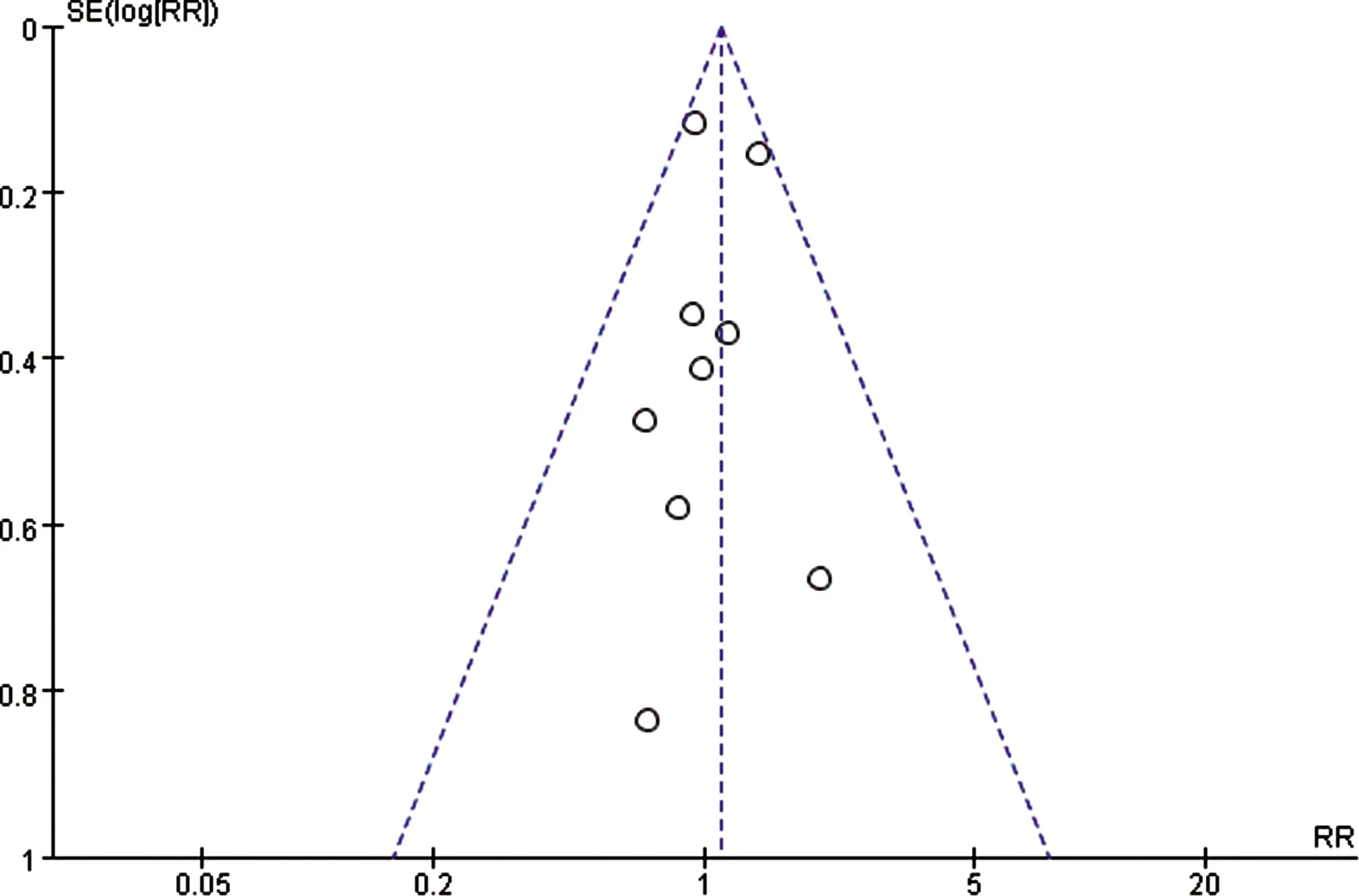
图4 两组间PCR漏斗图

图5 两组间保乳率漏斗图
3 讨 论
3.1 乳腺癌化疗药物给药顺序理论基础
乳腺癌新辅助化疗临床多采用2种以上药物,其中最常用的为蒽环类和紫衫烷类药物。蒽环类药物主要作用机制是对RNA、DNA合成进行干扰,抑制拓扑异构酶活性,为细胞周期非特异性类药物[13]。紫衫烷类药物是稳定微管的药物,能与微管蛋白结合并引起有丝分裂抑制,从而遏制了细胞分裂及增殖,属于细胞周期特异性类药物[14]。联合用药可能会因为药物之间的相互作用或抗癌药物作用的周期特异性对化疗的疗效和毒性产生影响,因此,正确的给药顺序是促进肿瘤合理用药的重要组成部分。化疗方案的给药顺序应遵循以下3个原则:(1)相互作用原则,如紫杉醇和顺铂,顺铂会延缓紫杉醇的排泄,加重不良反应的发生,联用时需先给予紫杉醇。(2)细胞动力学原则,生长较慢的实体瘤处于增殖期的细胞较少,G0期细胞较多,先用周期非特异性药物杀灭一部分肿瘤细胞,使其进入增殖期再用周期特异性药物;而生长较快的肿瘤应先用周期特异性药物大量杀灭处于增殖期的细胞减少肿瘤负荷,再用周期非特异性药物杀灭残存的肿瘤细胞。(3)刺激性原则,化疗开始时静脉的结构稳定性好,药液渗出机会较小,对周围组织的不良刺激也较小,应先用刺激性大者[15]。乳腺癌属非惰性肿瘤,根据给药顺序原则应先用周期特异性药物再使用周期非特异性药物,以达到最好的疗效。因此,可能T-A的用药顺序更能提高疗效。
3.2 本研究结果分析
本研究共纳入符合标准的相关文献10篇[3-12],累计样本量1 956例,对既往已发表的有关蒽环和紫衫烷类用药顺序不同对乳腺癌新辅助治疗的疗效影响的研究进行了meta分析。结果显示,无论是否伴有其他药物,如氟尿嘧啶、曲妥珠单抗等,使用T→A顺序的乳腺癌患者OS、DFS、PCR、保乳率、ORR、DCR与使用A→T者比较,差异无统计学意义(P>0.05);而3~4级不良反应中,T→A组患者更易发生白细胞减少差异有统计学意义(P=0.000 01);两组患者其余3~4级不良反应比较,差异均无统计学意义(P>0.05)。各组森林图显示,T→A组患者PCR、保乳率均具有优于A→T组的趋势,可能与化疗方案的给药顺序原则有关,但差异均无统计学意义(P>0.05),分析原因:(1)目前能收集到有关用药顺序的研究大多为小样本随机试验,样本量不大;(2)另外高PCR主要发生在激素受体(HR)阴性的乳腺癌患者中,而HR阳性患者PCR很低[16]。本研究纳入的10篇文献中研究对象超过一半为HR阳性患者,T→A组患者中HR阴性247例,A→T组患者中HR阴性255例,从病理分子分型来看,A→T组比T→A组更易达到较高的PCR,可能是两组的差异未达到统计学意义的原因。
本研究对中性粒细胞减少率中存在的异质性进行了亚组分析发现,不管是从药物剂量、疗程,还是从种族、样本量等方面分析均未能探及异质性来源,故对其进行了敏感性分析,发现在剔除ISHIGURO等[12]研究后异质性较前明显下降(表4)。回顾这篇文献发现其研究对象为HER2阴性患者,而另外2篇是HER2阳性患者,可能是造成异质性来源的主要因素。
3.3 本研究的优势与局限性
以往已有探讨蒽环类和紫杉类用药顺序的研究,但目前仅有1篇系统性综述[17]且未进行meta分析,其余研究[1,18]仅对文献进行了分类性描述,与之前研究不同的是本研究着重关注了新辅助治疗领域,并纳入了更多新近发表的文献,故具有一定的开拓性。但由于相关的随机试验资料不多,纳入分析的文献病例数较少,尤其不良反应方面存在一定发表偏倚,因此,本研究未根据患者肿瘤大小、分期、年龄等因素进行亚组分析。
综上所述,乳腺癌新辅助化疗患者给予蒽环类联合紫衫烷类药物治疗时T→A与A→T之间的疗效对比未见明显优势,考虑到T→A组患者更易发生白细胞减少,因此,在临床治疗中可选择A→T的给药顺序。由于文献数目有限,仍期待有更多的大型随机对照试验对紫衫烷类与蒽环类药物用药顺序不同是否对乳腺癌患者疗效产生的影响进一步研究,为蒽环和紫衫烷类药物的最佳用药顺序提供更有力的证据支持。
