血清sMFAP4水平对下肢闭塞性动脉硬化患者支架植入术后6个月再狭窄的预测价值
2021-11-20张名林史键山金桂云
张名林 史键山 邓 堂 孙 刚 金桂云
海南医学院第一附属医院介入血管外科,海南 海口 570102
下肢闭塞性动脉硬化(arteriosclerosis obliterans,ASO)是一种下肢缺血性疾病,以动脉粥样硬化性增厚、失去弹性和动脉壁内侧钙化为主要临床特征,导致下肢动脉硬化性狭窄或阻塞[1-2]。目前,对于药物治疗效果不佳的下肢ASO患者,介入治疗是主要手段之一。然而介入治疗后血管再狭窄一直是个难题,同时也增加了二次手术的风险[3]。微纤维相关蛋白4(microfibrillar-associated protein 4,MFAP4)是一种寡聚细胞外间质蛋白,属于纤维蛋白原相关结构域(fibrinogen-related domain,FReD)超家族成员,主要位于心脏和全身动脉细胞外间质纤维中[4]。除了C端FReD,MFAP4结构还包含一个N端精氨酸-甘氨酸-天门冬氨酸序列,具有整合素结合和激活能力。此外,MFAP4以可溶性形式存在于循环体液中,并且血清可溶性MFAP4(soluble microfibrillar-associated protein 4,sMFAP4)被认为与心血管疾病、肺部疾病及肝硬化等有关。本研究旨在探讨血清sMFAP对于下肢ASO患者接受介入治疗后发生血管再狭窄中的预测作用,一方面为血管再狭窄的发生提供新的生物标志物,另一方面也为下肢ASO术后再狭窄机制的研究提供新的靶点,现报道如下。
1 对象与方法
1.1 研究对象
选取2019年4月至2020年11月海南医学院第一附属医院收治行支架植入手术的268例下肢ASO患者为研究对象。所有患者Rutherford分期均为Ⅲ~Ⅵ期。纳入标准:(1)诊断标准符合《下肢动脉硬化闭塞症诊治指南》[5],下肢出现麻木、无力、凉、间歇性跛行及静息痛或缺血性溃疡、坏疽,缺血肢体远端动脉搏动减弱甚至消失,踝肱指数<0.9,趾肱指数<0.7;(2)经计算机体层血管成像(computed tomography angiography,CTA)确诊;(3)首次接受治疗者。排除标准:(1)合并大动脉炎、急性血栓形成等血管疾病或因其他原因引起血管狭窄者;(2)既往有下肢外伤、下肢手术史、近期服用抗血小板或激素类药物者;(3)恶性肿瘤或其他严重的全身性疾病,如肾功能或肝功能不全者。本研究获得医院伦理委员会审核通过,所有患者签署知情同意书。
1.2 治疗
所有患者取仰卧位,进行常规手术消毒,然后使用1%利多卡因进行局部麻醉。健侧股动脉采用Seldinger法穿刺,静脉注射肝素3000 U,每小时追加1000 U。通过对患肢血管造影检查确定血管狭窄位置、范围、程度及侧支循环及流出道状态,采用经皮球囊扩张血管成形术对病变部位进行球囊扩张,然后植入支架,支架长度需完全覆盖病变部位,采用数字减影血管造影(digital subtraction angiography,DSA)进行确认。血管管腔狭窄≤10%,并且未出现手术并发症及遗留明显血管夹层即可判定为手术成功。术后6个月内口服氯吡格雷75 mg/d并长期口服阿司匹林 100 mg/d;同时术后常规给予他汀类、血管紧张素转化酶抑制剂类药物。
1.3 血清sMFAP4检测
在术前和术后12 h分别采集空腹血样,2000 r/min离心20 min,将获得的上清储存于-80℃冰箱中待检测,使用前进行单次热融循环处理。采用均相酶联免 疫分析(amplifed luminescent proximity homogeneous assay,AlphaLISA)法在384孔微量滴定板上检测血清sMFAP4。按照说明,将MFAP4单克隆抗体(HG-HYB 7-14)与AlphaLISA受体磁珠偶联,对MFAP4单克隆抗体HGHYB 7-18通过(+)生物素-N-羟基琥珀酰亚胺酯标记修饰与AlphaLISA链霉亲和素包被的供体磁珠结合。反应混合物在室温下孵育1 h,然后加入链霉亲和素包被的供体磁珠使最终浓度达到40 mg/ml,再将滴定板在黑暗室温环境下孵育30 min,最后使用AlphaScreen技术在 EnVision多功能酶标仪上检测492 nm处的光密度值。除标准品及质量控制品进行4次实验,其余均为2次,接受重复样本协方差≤10%,组内及组间变异系数分别为8.7%和9.5%。
1.4 随访预后
所有患者均于术后1个月、3个月、6个月时进行CTA复查,再狭窄定义为支架内或支架两端5 mm内血管管腔狭窄率≥50%。根据再狭窄情况将患者分为再狭窄组及非再狭窄组。对于多发性血管狭窄患者,如果上述部位有大于50%的血管狭窄,则计入再狭窄组。再狭窄严重程度(%)=(B-A)/A×100%,其中A是手术中植入支架后DSA确认的狭窄区域的最小管腔面积,B是术后6个月末狭窄区域的最小管腔面积。对于多发性血管狭窄的患者,采用分度值来表示再狭窄的严重程度。再狭窄的严重程度分为四级:Ⅰ级为<20%;Ⅱ级为20%~40%;Ⅲ级为大于40%且小于60%;Ⅳ级为>60%。
1.5 统计学方法
应用SPSS 19.0软件对数据进行统计学分析,采用Kolmogorov-Smirnov进行正态性检验,正态分布资料以(±s)表示,组间比较采用两独立样本t检验,组内比较采用配对t检验;多组间比较采用单因素方差分析;计数资料以n(%)表示,组间比较采用χ2检;采用Spearman秩相关系数进行相关性分析。术后6个月再狭窄的影响因素分析采用Logistic回归分析。采用受试者工作特征(receiver operating characteristic,ROC)曲线确定最佳截断点、灵敏度、特异度和曲线下面积(area under the curve,AUC);P<0.05为差异有统计学意义。
2 结果
2.1 临床特征比较
268例下肢ASO患者行介入治疗后,再狭窄患者56例,非再狭窄患者212例。两组患者性别、体重指数、吸烟史、饮酒史、高血压比较,差异无统计学意义(P>0.05);再狭窄组患者年龄、合并冠心病、糖尿病、高脂血症、Rutherford分期为Ⅴ~Ⅵ期的患者比例高于非再狭窄组患者,差异有统计学意义(P<0.05)。(表1)
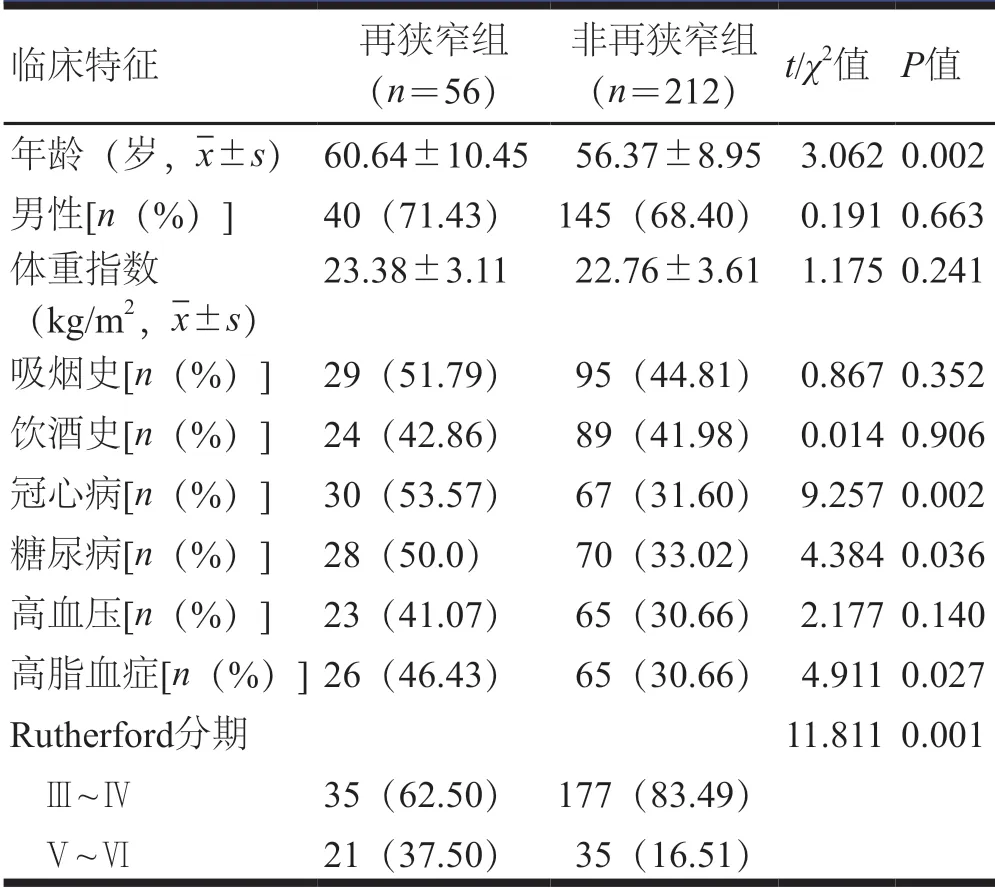
表1 两组患者临床特征比较
2.2 血清sMFAP4水平比较
术前,两组患者sMFAP4水平比较,差异无统计学意义(P>0.05);术后12 h,两组患者血清sMFAP4水平均高于介入术前,且再狭窄组患者血清sMFAP4水平高于非再狭窄组患者,差异有统计学意义(P<0.05)。(表2)
表2 两组患者血清sMFAP4水平比较(U/L,±s)
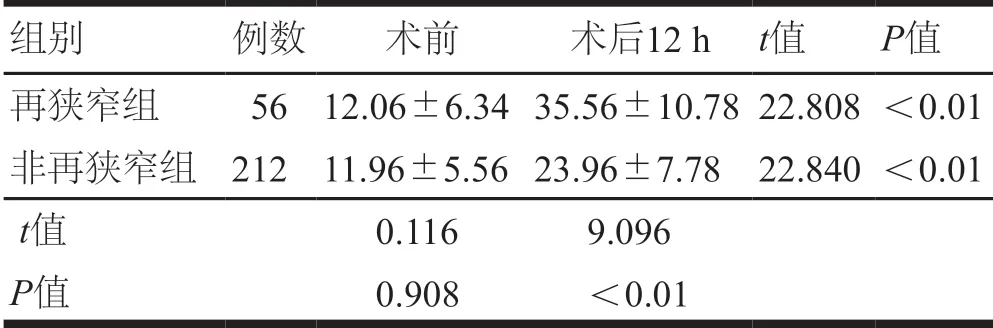
表2 两组患者血清sMFAP4水平比较(U/L,±s)
组别 例数 术前 术后12 h t值 P值再狭窄组 56 12.06±6.3435.56±10.7822.808<0.01非再狭窄组 212 11.96±5.5623.96±7.78 22.840<0.01 t值 0.116 9.096 P值 0.908 <0.01
2.3 血清sMFAP4水平与再狭窄严重程度相关性分析
术前,不同再狭窄严重程度分级患者的血清sMFAP4水平比较,差异无统计学意义(P>0.05);术后12 h,不同再狭窄严重程度分级患者的血清sMFAP4水平比较,差异有统计学意义(P<0.01)(表3)。术后血清sMFAP4水平与再狭窄的严重程度呈正相关(r=0.764,P<0.01)。
表3 手术前后不同再狭窄严重程度患者的血清 sMFAP4水平比较(U/L,±s)
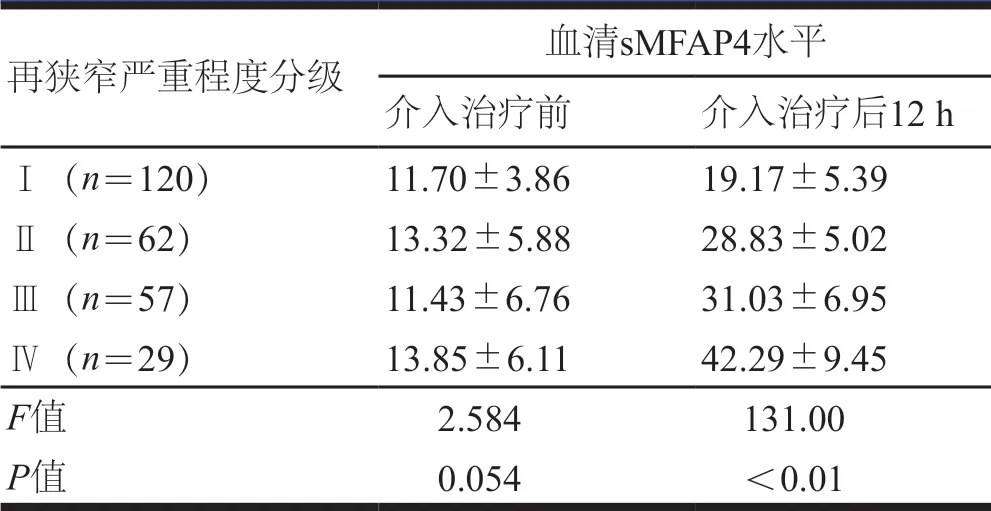
表3 手术前后不同再狭窄严重程度患者的血清 sMFAP4水平比较(U/L,±s)
再狭窄严重程度分级 血清sMFAP4水平介入治疗前 介入治疗后12 hⅠ(n=120) 11.70±3.86 19.17±5.39Ⅱ(n=62) 13.32±5.88 28.83±5.02Ⅲ(n=57) 11.43±6.76 31.03±6.95Ⅳ(n=29) 13.85±6.11 42.29±9.45 F值 2.584 131.00 P值 0.054 <0.01
2.4 术后6个月再狭窄影响因素的多因素分析
将年龄、合并冠心病、糖尿病、高脂血症、Rutherford分期为Ⅴ~Ⅵ期和介入治疗后12 h血清sMFAP4水平升高作为自变量,术后6个月再狭窄为因变量,进行Logistic回归分析,结果显示,合并冠心病、Rutherford分期为Ⅴ~Ⅵ期、术后12 h血清sMFAP4水平升高是术后6个月再狭窄的独立危险因素(P<0.05)。(表4)
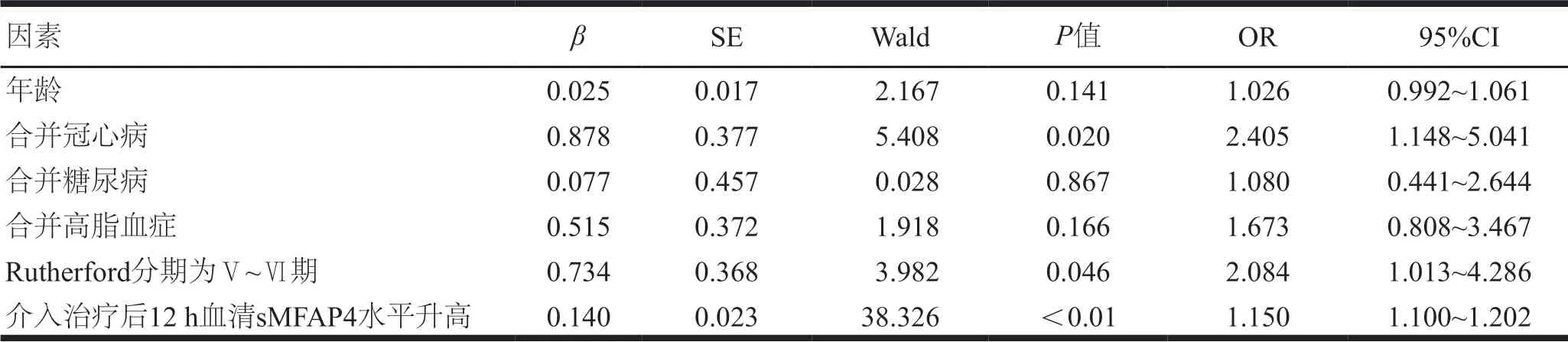
表4 术后6个月再狭窄影响因素的多因素分析
2.5 血清sMFAP4水平预测术后6个月再狭窄的临床价值
血清sMFAP4水平预测术后6个月再狭窄ROC曲线显示,最佳截断值为33.1 U/L,AUC为0.810(95%CI:0.742~0.877),灵敏度和特异度分别为64.3%和88.7%,约登指数为0.53。
3 讨论
介入手术是治疗下肢ASO的主要手段[6],如周围动脉疾病(peripheral artery disease,PAD),虽然血管内支架植入术作为新兴腔内治疗手段可一定程度上弥补球囊成形术的不足,但PAD患者支架植入术后仍存在较高的再狭窄风险[7]。虽然已证实血管内支架植入术改善下肢ASO患者血流动力学,但仍有部分患者在术后发生再狭窄[8]。支架内再狭窄的病理机制复杂,包括患者本身的动脉粥样硬化进展、支架植入时引起斑块重建、血管内膜持续受压造成的平滑肌细胞增生及迁移、细胞外基质大量形成或炎性细胞因子释放、术后抗凝治疗不充分等造成[9-10]。此外,本研究结果显示合并冠心病、Rutherford分期为Ⅴ~Ⅵ期是术后6个月再狭窄的独立危险因素。
MFAP4为纤维蛋白原相关蛋白超家族一种36 kD的细胞外基质糖蛋白,主要位于富含弹性纤维的部位和所有组织的血管内,可参与体内血管平滑肌增生、新生内膜形成和血管重塑。研究显示,其可以导致血清sMFAP4水平增加,还参与了肝脏纤维化、气管重构、慢性阻塞性肺疾病等疾病过程[11-13]。Christensen等[14]报告了sMFAP4在类风湿性关节炎患者血清和滑膜液中普遍升高,且随访7年,血清sMFAP4水平升高与三种心血管事件和(或)危险因素呈正相关。这可能是因为血管平滑肌细胞是血清sMFAP4蛋白分子的主要来源,促炎因子可导致血管平滑肌细胞活化,进一步促进sMFAP4的释放,而血清MFAP4水平升高也反映了动脉壁对脉动压力的脆弱性增加。此外,Wulf-Johansson等[15]发现稳定型冠心病患者血清sMFAP4水平普遍低于急性心肌梗死或不稳定型心绞痛患者及无冠状动脉钙化者,表明当内膜和中层钙化时,血管平滑肌细胞的MFAP4合成可能会受到抑制。
基于以上研究结果,血清sMFAP4可能与下肢ASO患者支架植入术后再狭窄的病理机制相关,本研究结果显示,术后12 h血清sMFAP4水平对于下肢ASO患者支架植入术后6个月内再狭窄的危险因素,且具有一定预测价值。再狭窄组患者术后血清sMFAP4水平显著高于非再狭窄组患者,血清sMFAP4水平与再狭窄严重程度也呈正相关。这可能是因为血管床重塑和(或)缺血导致组织破坏并进一步促进细胞外间质蛋白分子的大量释放,包括sMFAP4进入血液循环,而随着血清sMFAP4水平持续升高,会促使血管平滑肌细胞活化、增殖,从而致使血管狭窄、弹性纤维聚集等。
综上所述,支架植入术后6个月发生再狭窄的ASO患者血清sMFAP4水平升高,且与术后再狭窄的严重程度呈正相关,因此sMFAP4为术后再狭窄的独立危险因素和潜在的预测标志物。
