八种评分系统对肝硬化失代偿期患者短期预后的预测价值
2021-11-19杨继敏刘中亮
祝 强 杨继敏 刘中亮
首都医科大学密云教学医院消化内科,北京 101500
肝硬化每年以5%~7%的速度从代偿期发展到失代偿期[1],代偿期中位生存期为10~12年,失代偿期中位生存期为2~4年,终末阶段常出现慢加急性肝衰竭(ACLF)和肝硬化急性失代偿(AD),表现为多器官功能衰竭和短期高死亡率[2]。在过去的三十年中已经提出了许多评分来预测肝硬化的预后,但在进行临床现场决策时适用性通常令人不满意。因为单个患者与评分所基于的平均患者群体不同,所处疾病阶段差异、不同地区流行病学差异等。本研究拟对 MELD、MELD-Na、AIMS65、GBS、CTP、mDF、ABIC、CLIF-C ADs[3-8]八种评分系统进行比较,辨别适合本地区预测短期预后的评分系统。
1 资料与方法
1.1 一般资料
选取2015年1月至2020年7月首都医科大学密云教学医院收治的227例肝硬化失代偿期患者资料。根据入院后28 d随访结果分组。A组(未输血好转组,n=145),男83例,女62例,年龄52~78岁;B组(输血好转组,n=50),男33例,女17例,年龄52~82岁;C组(临床死亡组,n=32),男18例,女14例,年龄54~82岁。纳入标准:符合《肝硬化诊治指南(2019更新)》[9]中的诊断标准。排除标准:肝癌或其他恶性肿瘤;肝脏或其他器官移植史;HIV感染者;合并其他严重疾病;临床资料严重缺失者。
1.2 方法
1.2.1 观察指标 患者入院24 h内的实验室指标以及年龄、肝性脑病等。肝性脑病的诊断及分级以《肝硬化肝性脑病诊疗指南》为标准[10]。以临床死亡及输血事件为主要研究终点。
1.2.2 八种评分系统介绍 MELD[5]公式=3.78 ln[bilirubin(mg/dl)]+11.20 ln(INR)+9.57 ln[creatinine(mg/dl)]+6.431× 病 因。 病 因 为 胆汁性或酒精性为0,其他为1;低危:≤14分,中危:15~18分,高危:>18分。MELD-Na[8]公式 =MELD+1.32×(137-Na)-[0.033×MELD×(137-Na)]。血清钠≤125 mmol/L者按125 mmol/L计算,≥137 mmol/L者按137 mmol/L计算。AIMS65[4]根据Alb、INR、神志改变、收缩压、年龄计算,总分为5分。GBS根据收缩压、血尿素氮、Hb、脉搏、黑便、晕厥、肝脏疾病、心力衰竭计算,<6分为低危,≥6分为中高危。CTP[5]根据肝性脑病(级)、腹水、TBil、INR、Alb计算,A级:5~6分,B级:7~9分,C级:≥10分。mDF[5]公式=4.6(patient's PT-reference PT)+total bilirubin(mg/dl)。≥32分,短期死亡率高。ABIC[5]公式=(age×0.1)+[serumbilirubin(mg/dl)×0.08]+[serumcreatinine(mg/dl)×0.3]+(INR×0.8)。A 级:< 6.71,B级:6.71~ 8.99,C级:≥ 9.0。CLIF-CADs[7]公式 =10×[0.03×Age{years}+0.66×ln(Creatinine{mg/dl})+1.71×ln(INR)+0.88×ln(WBC{109cells/L})-0.05×Sodium{mmol/L}+8]。分数越高,预后越差。
1.3 统计学处理
采用SPSS 25.0及MedCalc 19.4统计学软件进行统计分析。正态分布计量资料以()表示,依方差不同采用ANOVA检验和Kruskal-Wallis H检验;组间比较采用χ2检验。测算ROC来比较八种评分的预测价值,使用delong法比较AUC值间的差异。P<0.05为差异有统计学意义。
2 结果
2.1 三组各观察指标比较
三组年龄、性别、脉搏比较差异无统计学意义,见表1。病因(酒精性肝硬化、乙型肝炎/丙型肝炎、混合性、隐源性肝硬化、其他)构成比较差异无统计学意义(P>0.05),见表2。C组的WBC、TBil、血尿素氮、血肌酐、INR、PT、腹水和肝性脑病评分水平高于A组,收缩压、Hb、Na、Alb水平低于A组(P<0.05),结果显示在肝硬化不同阶段,观察指标具有不同的权重。

表1 三组各观察指标比较

表2 三组患者病因构成比较[n(%)]
2.2 三组风险分级比较
三组对八种评分产生的风险分级比较,差异有统计学意义(P<0.05),显示八种评分在不同阶段预测存在偏差,见表3~4。

表3 三组CTP、GBS、MELD、MELD-Na风险分级比较
2.3 三组八种评分比较
C组八种评分高于A组和B组(P<0.001);B组 GBS、AIMS65、CTP高于A 组(P< 0.05),见表 5。
表5 三组八种评分比较(,分)

表5 三组八种评分比较(,分)
注:与B组比较,aP<0.05;与A组比较,bP<0.05;与C组比较,cP<0.05
组别 n GBS AIMS65 mDF MELD MELD-Na CTP CLIF-C ADs ABIC所有病例 227 9.26±4.26 1.66±1.24 12.44±21.73 11.32±7.47 13.19±7.81 8.71±2.48 49.71±12.65 10.78±4.95 A 组 145 7.59±3.57a 1.28±1.15a 7.36±12.05 9.93±5.86 11.69±6.42 8.05±2.16a 49.92±10.89 9.80±3.16 B 组 50 11.74±3.37c 1.92±1.07c 11.75±13.93c 10.09±5.65c 12.04±6.39c 8.76±2.22c 50.01±9.13c 10.04±3.00c C 组 32 12.91±4.27b 2.94±0.95b 36.56±41.72b 19.49±10.80b 21.77±10.01b 11.63±2.15b 61.89±17.19b 16.38±8.97b F/H值 42.99 47.04 38.79 29.04 31.62 35.54 31.92 30.72 P值 <0.001 <0.001 <0.001 <0.001 <0.001 <0.001 <0.001 <0.001
2.4 八种评分对短期临床预后的预测价值
在本研究中CTP评分预测临床死亡价值最高(AUC=0.864);其余评分的AUC在0.824~0.758间,见图1。八种评分预测输血事件的价值有限,GBS的AUC值为0.727,其余评分的AUC值在0.585~0.464间,见图2。

图1 八种评分预测临床死亡的ROC曲线(C组)
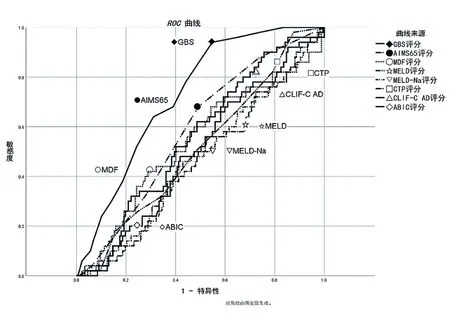
图2 八种评分预测输血的ROC曲线(B组)
2.5 八种评分系统的AUC值差异比较
C组中CTP的预测价值优于CLIF-C ADs、GBS(Z=2.045、2.073,P< 0.05),见图 3。B 组 中GBS的预测价值优于ABIC、AIMS65、CLIF-C ADs、mDF、CTP、MELD(Z=4.297、3.016、3.716、3.026、3.810、3.830,P< 0.05),见图 4。

图3 预测临床死亡的AUC值比较(C组)

图4 预测输血的AUC值比较(B组)
3 讨论
肝硬化进入失代偿阶段将演变为伴有多器官、多系统功能障碍的全身性疾病,患者往往发展为肝移植或死亡[11]。临床医师需要识别出患者的临床特征并进行预后分析,有利于改善失代偿期管理。

表4 三组mDF、ABIC、CLIF-C ADs、AIMS65风险分级比较
年龄是可预测生存的变量,本研究中年龄在三组间比较差异无统计学意义,考虑可能与本地区医疗干预不足及流行病学特征等有关。种族、性别和病因不是导致死亡的独立危险因素。血清Na+是死亡的独立预测因子[12],与本研究结果一致。
八种评分在肝硬化不同阶段的预测存在偏差。因观察指标不同或权重变化、个体生物学变异性和流行病学、检测方法等因素影响,各地区对于评分系统认可度不一。本研究通过比较八种评分在三组间的预测差异,显示在预测28 d死亡率时,CTP评分诊断价值最高(AUC=0.864);其余评分的AUC为0.824~0.758;对各评分AUC差异进行比较时显示CTP的预测价值优于CLIF-C ADs、GBS(Z=2.045、2.073,P< 0.05),与凡小丽等[3]研究结果相符。有研究显示[13]在预测3个月的死亡率时MELD评分优于CTP评分。可能的原因是在短期预测中反映循环系统恶化的指标所占权重更大。CTP包含2项循环状态指标(腹水和肝性脑病)、MELD包含1项循环状态指标(血肌酐)、MELD-Na包含2项循环状态指标(血肌酐和Na),但考虑Na不足以替代腹水和肝性脑病对循环状态的评估作用。在本研究中观察到MELD-Na能识别出MELD评分低的患者中隐藏的高危人群。如果将CTP的肝性脑病替换为AIMS65中的精神状态,则两者在5项指标中重叠3项。如果将mDF的PT时间延长替换为CTP中的INR,则CTP是在mDF基础上的拓展评分。在本研究中,CLIF-C ADs评分的预测表现中等,考虑其对没有慢加急性肝衰竭背景的肝硬化急性失代偿患者预测更准确[7]。ABIC和MELD之间有3项指标重叠。ABIC没有包含病因,但纳入年龄,在本研究中的预测效果介于MELDNa和MELD之间。
在本研究中八种评分对输血事件预测价值均有限,与马佳丽等[14]研究结果相符,其中GBS优于其他评分;AIMS65预测临床死亡时优于GBS,预测输血时劣于GBS,与Koichiro等[4]的研究结果相符。
各评分系统有不同优缺点,如MELD及MELDNa重复性好,已取代CTP用于分配肝脏供体的优先顺序[15];但其结果需要复杂计算,实用性差,且低估合并腹水患者的死亡风险[16]。临床医师希望识别出患者的临床特征,并进行充分的风险分级以制订最佳治疗策略,希望未来有新技术可以提供更好的支持。
