基于七元瓜环衍生物的毛细管气相色谱柱的制备及分离性能研究
2021-11-19董美玉冉金凤王莎莎
董美玉,冉金凤,王莎莎,董 南
(贵州大学 化学与化工学院,贵州 贵阳 550025)
毛细管气相色谱(gas chromatography)是一种高分辨率的分析方法。固定相的选择性和有效的色谱柱制备方法是影响色谱柱高分离效率的两个主要因素[1]。瓜环是继杯芳烃(calixaren)、冠醚(crown ether)、环糊精(cyclodextrin)之后备受瞩目的一类新型大分子化合物,它拥有疏水性的内部空腔和环绕空腔两端端口的羰基氧原子,可以通过空腔疏水作用、离子-偶极作用、氢键等与不同种类的分子发生主客体相互作用[2-3]。瓜环本身的结构也是惰性的,具有良好的化学和热稳定性。良好的物理化学性质和优异的分子识别能力使瓜环很早就进入了色谱工作者的视野。2004年刘思敏等[4]首次将全羟基取代六元瓜环与硅胶键合,制备成亲水性液相色谱固定相,成功分离了多种生物碱。NAGARAJAN等[5]将全羟基取代六元瓜环与烯丙基溴化合物反应得到的烷基化衍生物键合到硅胶上应用于液相色谱固定相。李来生等[6-7]以全羟基取代六元瓜环和七元瓜环分别作为气相色谱填充柱的固定相,成功分离烷烃、卤代烃、醇、酮、胺等以及一些芳香族异构体,但是色谱柱效较低(863~936 N/m),色谱峰型较宽、对称性不好。齐美琳等分别采用六、七、八元瓜环和瓜环聚合物利用静态法制备了一系列的毛细管气相色谱固定相[8-10],分离了非极性的多环芳烃、中等极性的酯、酮、较强极性的醇、胺类等,也可较好分离Grob试剂和不同极性化合物组成的混合物。我们课题组采用合成的全羟基取代五元瓜环或单羟基取代七元瓜环,以溶胶-凝胶化学键合的方式制备了毛细管气相色谱固定相[11]。此固定相涂层的均匀性、化学稳定性较涂渍法有所改善,因此制得的色谱柱的柱效和分离选择性得到了进一步提高。
为了进一步提高色谱柱的选择性,拓展瓜环在气相色谱固定相方面的应用范围,丰富固定相的种类,在本文中将单羟基七元瓜环进一步衍生为4-乙烯苄氧基七元瓜环,与端羟基聚二甲基硅氧烷一起作为固定相,溶胶-凝胶法制备一种新型的毛细管气相色谱柱并对色谱柱的色谱性能及分离选择性进行研究。
1 实验部分
1.1 仪器与试剂
岛津Solution气相色谱仪(日本);PX-85ZH 分析天平(上海奥斯豪有限公司);VORTEX-5-漩涡混合器(海门市其林贝尔仪器制造有限公司); TGL-16C 高速离心机(上海安亭仪器厂);UC-6H加热型超声波清洗器(上海泰坦科技科技股份有限公司);弹性石英毛细管柱(10 m×0.25 mm,河北永年县锐沣色谱器件有限公司)。
γ-缩水甘油醚氧丙基三甲氧基硅烷(KH-560)、三氟乙酸(TFA)、端羟基聚二甲基硅氧烷(OH-PDMS)、甲基三甲氧基硅烷(MTMOS)和含氢硅油(PMHS)均购自上海Aladdin公司;分析纯二氯甲烷(上海申博化工有限公司);色谱级甲醇(天津市科密欧化学试剂有限公司);单羟基七元瓜环((HO)1Q[7])实验室自制。
1.2 4-乙烯苄氧基七元瓜环的合成和分离
在100 mL的两口烧瓶中加入500 mg单羟基七元瓜环((HO)1Q[7])、5 mL 二甲基甲酰胺(DMF)和30 mL 二甲基亚砜(DMSO),持续搅拌直至单羟基七元瓜环溶解。在氮气的保护下将反应体系冷却至0 ℃,加入850 mg NaH,搅拌反应2 h。随后向反应液中加入210 uL的4-乙烯基苄氯,移除反应液的冰浴,让其自然恢复到室温并继续反应8 h。反应结束后,用适量乙醚沉淀反应液,减压抽滤后再用甲醇反复抽滤洗涤3次,最后得到白色产物,产率为60%。C51H50N28O151H NMR (400 MHz, D2O),δ(ppm):7.4 (d, 2H), 7.2 (d, 2H), 6.6 (m, 1H), 5.67 (brm, 12H), 5.30 (brm,14H), 5.15 (d, 2H), 4.4(s, 1H), 4.3(d, 2H), 4.15(d, 2H), 4.08(m, 12H)。
1.3 毛细管色谱柱的制备
弹性石英毛细管柱的预处理:首先取10 m内径为0.25 mm的弹性石英毛细管柱,用N2将5 mL的二氯甲烷压入并浸泡10 min,通氮气将柱内的溶液推出且继续通氮气15 min使其干燥。然后将1.0 mol/L的NaOH溶液推入毛细管柱浸泡30 min,蒸馏水沥洗至中性,再用0.1 mol/L的HCL溶液沥洗毛细管柱中和未被冲洗干净的NaOH溶液,用蒸馏水洗净至中性,最后弹性石英毛细管柱在氮气的保护下120 ℃干燥2 h。
毛细管色谱柱的制备:在分析天平上称取20 mg 4-乙烯苄氧基七元瓜环倒入5 mL 聚乙烯塑料管中,依次加入TFA(95%)300 μL、CH2CI2700 μL、OH-PDMS 300 μL、MTMOS 50 μL、PMHS 50 μL、KH-560 100 μL,在涡旋振荡器上混匀5 min,再放入高速离心机中以12 000 r/min的转速离心5 min,取出上清液的溶胶-凝胶溶液作为色谱柱的固定相。在氮气作用下将此上清液缓缓推入预处理好的毛细管内,直至溶胶-凝胶固定相充满整根色谱柱。将两端密封, 溶胶-凝胶溶液在柱内保持15 min,然后通氮气将溶胶-凝胶溶液推出管外,在氮气保护下静置1 h,让涂层干燥并与石英毛细管内壁发生键合。将该柱放入气相色谱仪,一端接气化室,另一端放空,在氮气保护下进行程序升温老化。首先在初温40 ℃以1 ℃/min升温至150 ℃保持360 min,再以同样的速率升温至280 ℃保留240 min进行固化,即完成了端羟基聚二甲基硅氧烷/4-乙烯苄氧基七元瓜环(PDMS/4-VBOQ[7])毛细管气相色谱柱的制备。
2 结果与讨论
2.1 色谱柱的柱效和极性
在柱温为100 ℃,载气为1 mL/min流速的条件下用萘测量色谱柱的柱效,其值为1 231 N/m,表明色谱柱有较高的柱效。
麦氏(McReynolds)常数是评价固定相极性和选择性的重要指标。在120 ℃测定该色谱柱的麦氏常数,并与商用色谱柱SE-54和OV-1701的固定相进行比较,结果如表1所示。

表1 PDMS/4-VBOQ[7]固定相的麦氏常数及平均极性(120 ℃)Tab.1 McReynolds constants and average polarity of the PDMS/4-VBOQ[7] column (120 ℃)
PDMS/4-VBOQ[7]固定相的总极性为607,平均极性为121,根据麦氏常数三级分度法,ΔΙ平均<100为弱极性固定相,100~400为中等极性固定相,400以上为极性固定相,因此PDMS/4-VBOQ[7]属于中等极性固定相,介于弱极性SE-54柱与中等极性OV-1701柱之间。5种探针化合物在PDMS/4-VBOQ[7]色谱柱上的流出顺序是正丁醇(Y′)>硝基丙烷(U′)>吡啶(S′)>2-戊酮(Z′)>苯(X′),表明在PDMS/4-VBOQ[7]色谱柱上Y′(氢键作用-质子给予和接受体)和U′(偶极作用,电子接受体)的作用力比较强。
2.2 色谱柱的分离重现性
色谱柱的分离重复性是保证色谱柱分析数据准确可靠的重要参数。本文对PDMS/4-VBOQ[7]色谱柱的日内重复性、日间重复性和色谱柱之间的重现性进行了考察,结果见表2。

表2 PDMS/4-VBOQ[7]色谱柱的精密度考察Tab.2 Precision investigation of PDMS/4-VBOQ[7] column
从表2中可以看出,该色谱柱的日内精密度RSD小于0.14%,日间RSD小于0.33%,不同色谱柱之间重复性的RSD小于0.65%,表明该自制色谱柱精密度高、重现性好,可用于实际样品的测定。
2.3 Grob试剂的测试
Grob试剂在色谱技术中有着广泛的作用,是目前应用最广泛的评价固定相色谱分离性能的综合试剂。它由不同极性、不同官能团、不同酸碱的化合物组成,既可评价色谱的分离性能,还可体现色谱柱表面的活性和吸附特性。图1是Grob试剂在自制色谱柱上的分离色谱图。从图中可看出,PDMS/4-VBOQ[7]色谱柱对Grob试剂的12个组分都有很好的分离效果,且峰型尖锐对称,表明该色谱柱具有较好的惰性,对各类化合物都有较好的分离选择性。其中2,3-丁二醇的色谱峰拖尾,表明其与固定相之间的作用力较强,可能是由醇羟基与4-乙烯基苄氧七元瓜环之间的氢键作用导致。2,6-二甲基苯胺(216 ℃)比2,6-二甲基苯酚(203 ℃)后流出,表明固定相显酸性,对碱性组分有一定的吸附作用。
2.4 分离选择性的研究
选取一些常见的较难分离的芳香位置异构体,探讨自制毛细管柱的分离情况。毛细管柱对位置异构体的分离因子α、保留因子k′ 和分离度R如表3所示。
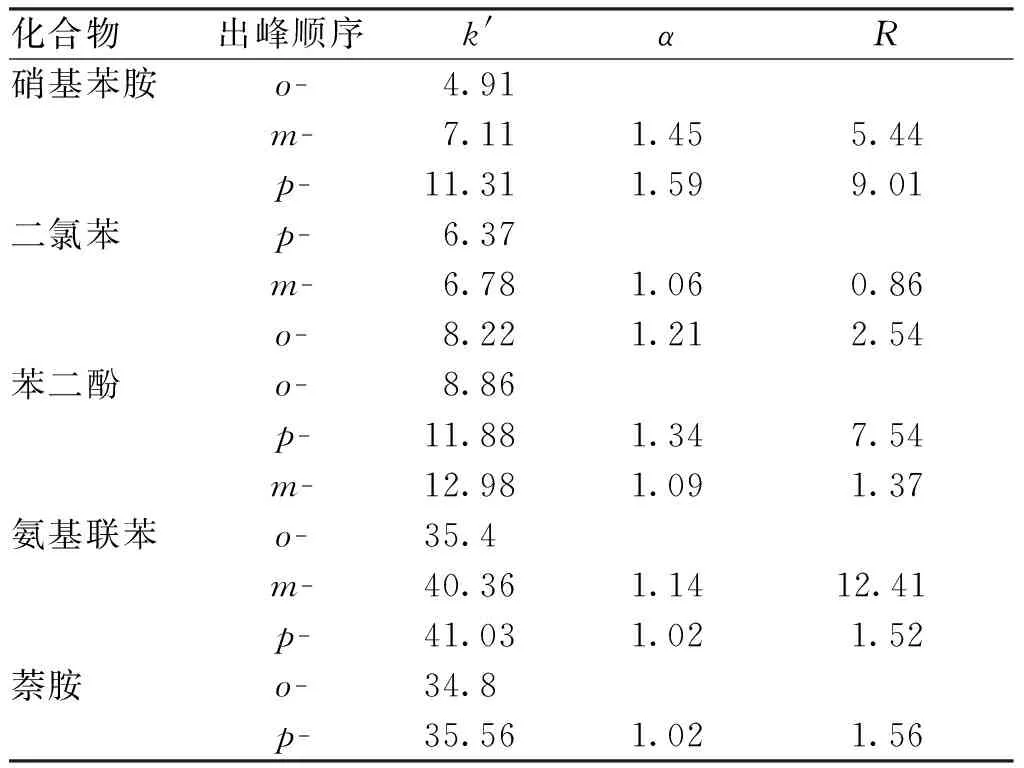
表3 异构体在 PDMS/4-VBOQ[7]色谱柱上的分离因子α、保留因子 k′和分离度RTab.3 The separation factor α, retention factor k′ and separation degree R of isomers on PDMS/4-VBOQ[7] column
从表中可以看出,无论是对极性还是弱极性的芳香位置异构体,自制色谱柱都有较好的分离效果,说明在瓜环上键合苯基有利于对芳香位置异构体的分离。另外,对正构烷烃、酮类、酯类以及醇类混合物在柱长10 m的自制色谱柱上分别进行分离,色谱图如图2~5。由图可见,自制PDMS/4-VBOQ[7]色谱柱不仅对各类化合物均有较好的分离选择性,而且分离效率高。
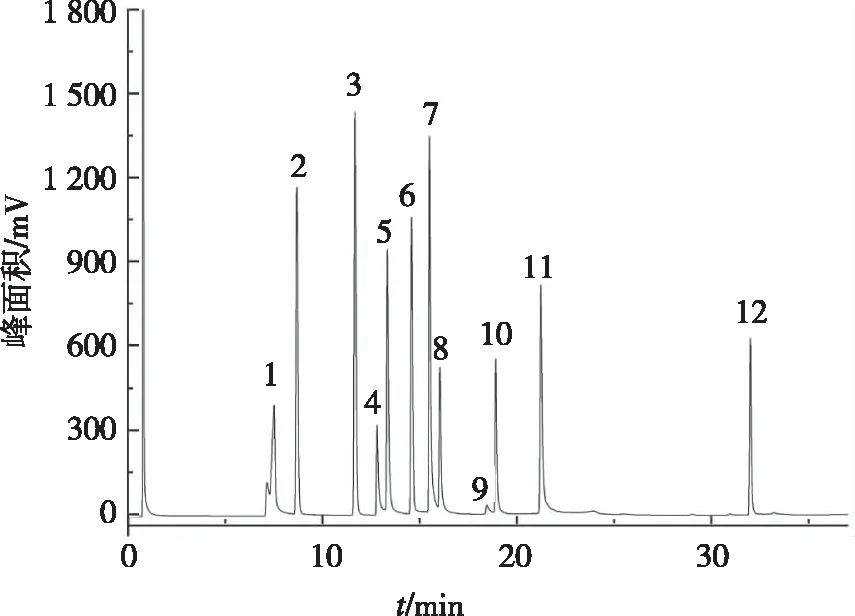
分离条件:柱温40℃ (1 min) 然后5 ℃/min 升到 220 ℃。进样口温度为250 ℃;FID 检测器温度为280 ℃;分流进样比为50 ∶1;载气为高纯N2;载气流速为1 mL/min。 色谱峰:1—2,3-丁二醇;2—葵烷;3—十一烷;4—壬醛;5—正辛醇;6—2,6-二甲基苯酚;7—2,6-二甲基苯胺;8—2-乙基己酸;9—二环己胺;10—葵酸甲酯;11—十一酸甲酯;12—十二酸甲酯。图1 PDMS/4-VBOQ[7] 色谱柱分离Grob试剂的色谱图Fig.1 Chromatography of Grob reagents separation on the PDMS/4-VBOQ[7] column
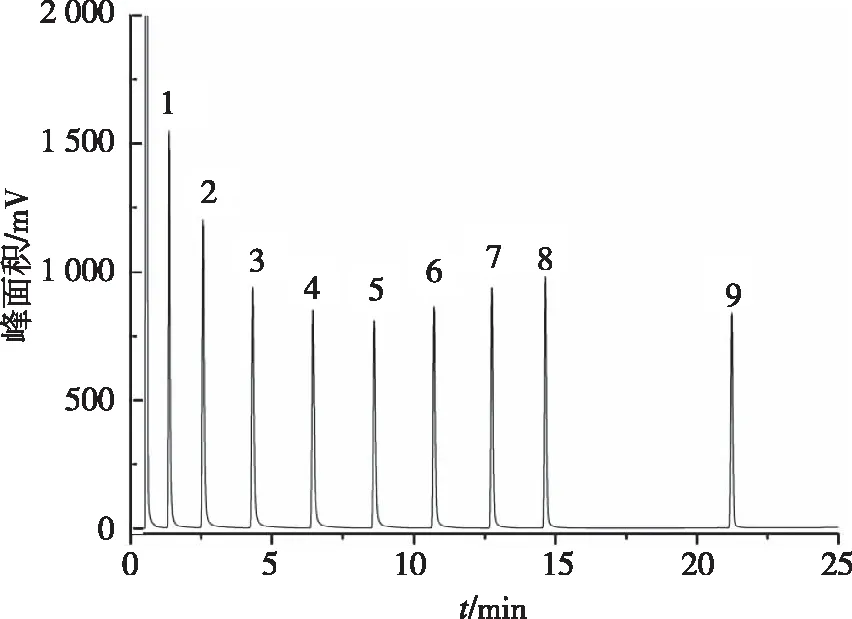
分离条件:40 ℃(1 min)然后7 ℃/min 升到250 ℃保持10 min。进样口温度为250 ℃;FID 检测器温度为280 ℃;分流进样比为50 ∶1;载气为高纯N2;载气流速为1 mL/min。 色谱峰:1—正庚烷;2—正辛烷;3—正壬烷;4—正葵烷;5—正十一烷;6—正十二烷;7—正十三烷;8—正十四烷;9—正十八烷。图2 PDMS/4-VBOQ[7]色谱柱分离正构烷烃的色谱图Fig.2 Chromatogram of n-alkanes separarion on the PDMS/4-VBOQ[7] column

分离条件:70 ℃(1 min)然后6 ℃/min 升到220 ℃保持10 min。进样口温度为250 ℃;FID 检测器温度为280 ℃;分流进样比为50 ∶1;载气为高纯N2;载气流速为1 mL/min。 色谱峰:1—乙酸丁酯;2—己酸乙酯;3—庚酸甲酯;4—辛酸甲酯;5—水杨酸甲酯;6—葵酸甲酯;7—十一酸甲酯;8—十二酸甲酯。图3 PDMS/4-VBOQ[7]色谱柱分离酯类的色谱图Fig.3 Chromatogram of esters separarion on the PDMS/4-VBOQ[7] column
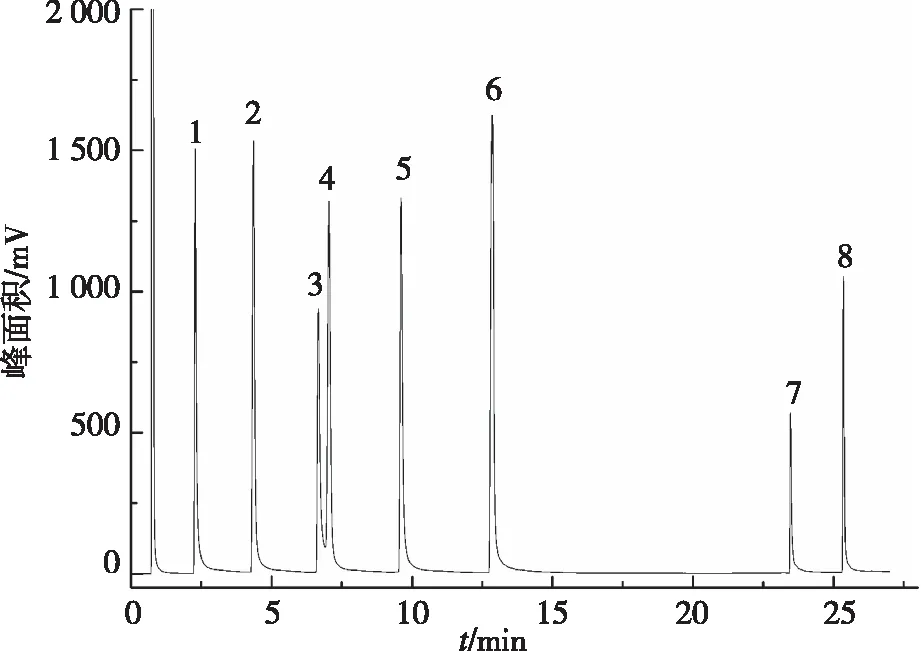
分离条件:40 ℃(1 min)然后5 ℃/min升到110 ℃保持1 min,以12 ℃/min升到230 ℃保持5 min。进样口温度为250 ℃;FID 检测器温度为280 ℃;分流进样比为50 ∶1;载气为高纯N2;载气流速为1 mL/min。 色谱峰:1—2-戊酮;2—环戊酮;3—2-庚酮;4—环己酮;5—2-辛酮;6—苯乙酮;7—苯甲酮;8—二苯乙酮。图4 PDMS/4-VBOQ[7]色谱柱分离酮类色谱图Fig.4 Chromatogram of ketones separarion on the PDMS/4-VBOQ[7] column

分离条件:40 ℃(1 min)然后8 ℃/min升到220 ℃。进样口温度为250 ℃;FID 检测器温度为280 ℃;分流进样比为50 ∶1;载气为高纯N2;载气流速为1 mL/min。 色谱峰:1—正己醇;2—环己醇;3—正庚醇;4—正辛醇;5—2-苯乙醇;6—正葵醇;7—十一醇;8—十二醇。图5 PDMS/4-VBOQ[7] 色谱柱分离醇类的色谱图Fig.5 Chromatogram of alcohol separarion on the PDMS/4-VBOQ[7] column
3 结论
采用溶胶-凝胶法制备了端羟基聚二甲基硅氧烷/4-乙烯苄氧基七元瓜环新型毛细管气相色谱柱。该色谱柱分离选择性好、分离效率高,既可分离非极性化合物、极性化合物、较难分离的芳香位置异构体,也可较好分离Grob 试剂的混合物。这些实验结果表明瓜环衍生物在气相色谱固定相方面有很大的应用潜力。
