基于分子印迹技术的中药成分绿色分离研究进展
2021-11-18刘显银邱模昌
刘显银,邱模昌
(江西医学高等专科学校,江西 上饶 334000)
中医药在全世界传统医学领域有着最完整和标准化的理论体系,迄今为止,中医药的疗效已被全世界广泛认可[1]。中药由许多复杂的成分组成,包括有效成分、无效成分和有毒成分,中药有效成分的高效提取分离成为改善中药内在质量和临床疗效的关键。传统溶剂分离会带来一定的安全和环境压力,因此,开发一种基于环保和高效的中药活性成分绿色分离新方法越来越迫切[2]。目前,针对中药成分分离,除传统的大孔树脂吸附技术外,超临界流体萃取、高速逆流色谱、膜分离、泡沫分离等技术的应用也越来越广泛。1931年,Polyakov制备了具有特异性吸附能力的硅胶,并首次提出“分子印迹”的概念,其通过预先设计的具有功能基团的聚合物,特异性识别目标分子[3-4]。目前,已开发出的MIPs广泛用于对映体分离[5-7]、分析化学[8-10]、电化学和仿生传感器[11-13]、药物传递[14-15]、生物技术[16]、食品安全[17-18]及环境科学[19-20]等领域。在中医药传统理论与现代研究领域,分子印迹理论与技术还被用于探讨中药质量标志物研究[21]、中药“十八反”配伍禁忌[22]、中药炮制共性技术[23]、金(山)银花纷争[24]等重大中医药理论。分子印迹技术最大的优势在于特异性结合,与中药成分分离理论有着明显的技术共性,近年来,将MIPs用于中药成分分离取得了显著的成效。本文综述了MIPs近年来的技术进展,并对其在中药成分绿色分离中的应用进行了探讨和展望,以期为该技术在中药领域的应用提供参考。
1 分子印迹技术概述
1.1 技术原理
在制备MIPs的过程中,模板分子首先与功能单体依靠官能团之间的聚合力形成主客体复合物。然后通过交联剂交联聚合或者引发剂引发单体聚合,形成高交联的刚性聚合物,最后将模板分子洗脱或解离得到MIPs。MIPs有模板分子空间结构和相应的结合位点,对模板分子具有特异选择性[25]。MIPs设计理念最初来源于生物学的受体-配体结合理论,由于其类似“锁匙”的仿生学设计,因此,MIPs最大的特征为识别专一性。根据结合形式的不同,形成MIPs的聚合力可分为共价键、非共价键、半共价键、离子间作用力和金属配位等类别[26]。不同类别聚合力在亲和力、选择性、吸附动力学及重现性方面有一定差异。MIPs形成原理如图1所示。
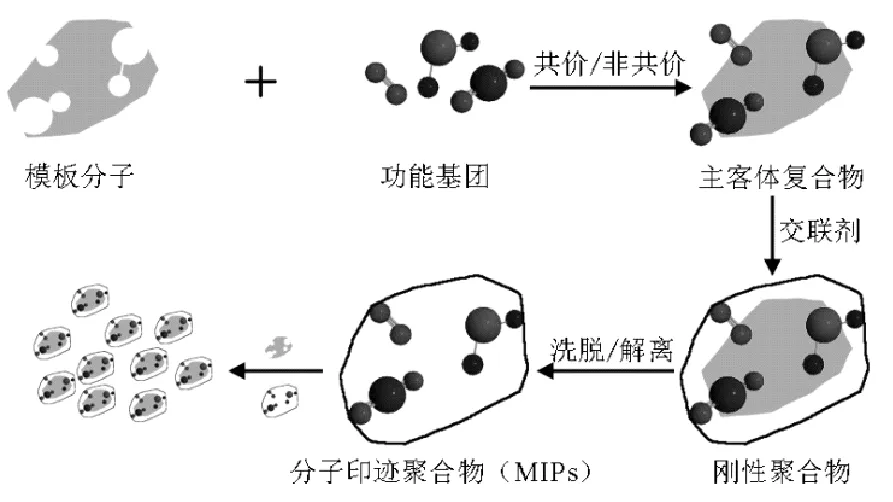
图1 分子印迹技术原理
1.2 常用材料
在MIPs的制备中,模板分子和功能单体往往具有特异性,根据目标产物的不同而选择不同的模板分子和功能单体。交联剂和引发剂的选择则需要根据模板分子、功能单体以及反应体系的温度、酸碱性及水相/有机相组成进行适当的筛选。交联剂是MIPs制备中关键的材料,适宜的交联剂可以保持聚合物的机械稳定性以维持特异的分子识别能力,同时对MIPs颗粒的粒径、表面均匀性具有一定的影响,通常采用高交联度的材料作为交联剂。偶氮二异丁腈(AIBN)是分子印迹聚合物中最常用的自由基引发剂,作为油溶性的偶氮引发剂,可溶于大部分反应体系引发自由基的链反应,反应稳定,副反应少[27]。常用的交联剂和引发剂见表1。

表1 分子印迹聚合物常用交联剂和引发剂
1.3 制备方法
根据制备MIPs的材料性质和模板分子结构特征的不同,MIPs的制备方法可以有多种选择。从直观上根据模板分子在聚合物基质中嵌入方式的差异,可将制备方法分为三维分子印迹(3D)和二维分子印迹(2D)或表面印迹。根据MIPs形成过程所经历的中间状态不同,三维分子印迹又可细分为本体聚合法、悬浮聚合法、乳液聚合法、沉淀聚合法、溶胶-凝胶法。表面印迹根据模板分子和聚合物材料发生聚合的位置不同,又可以分为自上而下(top-down)和自下而上(bottom-up)两种制备方法[28]。根据载体形成聚合物空腔过程的差异,表面印迹的制备方法又可以分为牺牲载体法、聚合加膜法和化学接枝法[29]。
随着化学工业和材料科学的发展,分子印迹技术与新技术、新材料的不断结合,MIPs的制备理论和实践也得到了进一步的优化和提升。硼亲和策略与分子印迹技术中相结合,通过pH值调控可逆共价结合,实现硼酸盐与顺式二醇物质的结合、解离,有利于模板分子的印迹与去除[30-31]。离子液体是指由有机阳离子和无机或有机阴离子组成,在室温或者接近室温状态下完全呈液态的物质。离子液体可以作为溶剂、致孔剂、模板、功能单体等参与MIPs的制备,提高体系的溶解性及功能单体与模板分子间的结合能力[32]。采用温敏型材料制备的温敏型MIPs[33]以及采用pH值敏感材料制备pH敏感型MIPs也成为当前的研究热点[34]。常见的MIPs制备方法的工艺流程及优缺点见表2。

表2 常用的MIPs制备方法的工艺流程及优缺点
2 在中药成分分离中的应用
中药化学成分复杂,各成分化学结构及性质差异较大,以化学成分为物质基础的中药药理药性研究是中医药现代化系统工程的重点内容。与其他分离技术相比,无论是对于单一成分还是对一类结构类似物的有效部位的分离,分子印迹技术都显示出独特的优势,各种分离技术对比见表3。近年来,分子印迹技术还被用于中药有毒成分的分离而发挥减毒增效的作用。基于药效功能基团研究的不断发展,分子印迹技术还可用于新的活性成分筛选。

表3 不同中药分离技术对比
2.1 有效成分的分离
中药有效成分的富集为药物的结构鉴定、活性筛选、制剂制备等提供基础,对目标分子的特异性吸附能力是MIPs最重要的指标。Yu等[58]将质量比为1∶4的红景天苷和丙烯酰胺溶于7mL二甲基甲酰胺溶液中超声30 min,加入一定量的EGDMA和AIBN,室温下氮气保护搅拌30min后迅速升温至60 ℃,持续反应24 h得到聚合物。聚合物用甲醇-乙酸回流(9∶1,V/V)索氏提取,除去红景天苷模板分子。对MIPs性能研究表明,随着红景天苷的浓度从3 mg·L-1增加到100 mg·L-1,MIPs对红景天苷的吸附能力由180μg·L-1提高到1 260μg·L-1。除了吸附能力,MIPs的稳定性至关重要。Bi等[59]将笼型聚倍半硅氧烷(POSS)加入到聚合体系中,无机POSS分子在MIPs中起骨架支撑作用,增大MIPs的比表面积和孔隙率,从而增加其吸附能力,同时增大MIPs结构的稳定性。为了使MIPs具有快速的吸收动力学,高选择性和更高结合能力,在制备过程中引入磁性物质制备的磁性MIPs取得了很好的效果。外加磁场使MIPs与体系发生快速分离,最大程度保护了MIPs结构完整性,同时由于其粒径较小,具有较大比表面积,因此具有较高的吸附容量[60]。除了针对单一成分具有较好的识别和分离能力,MIPs同样可以用于分离中药的一类或几类化学成分即有效部位。有效部位往往具有相同或者相近的理化性质,反映其结构上有特征性的相似基团,即可为模板分子的选择提供依据,制备相应的MIPs。MIPs对目标成分分离效率主要采用最大吸附容量、方法回收率、印迹因子、分离因子及提取物纯度等指标进行描述。近5年MIPs用于中药有效成分分离统计见表4。
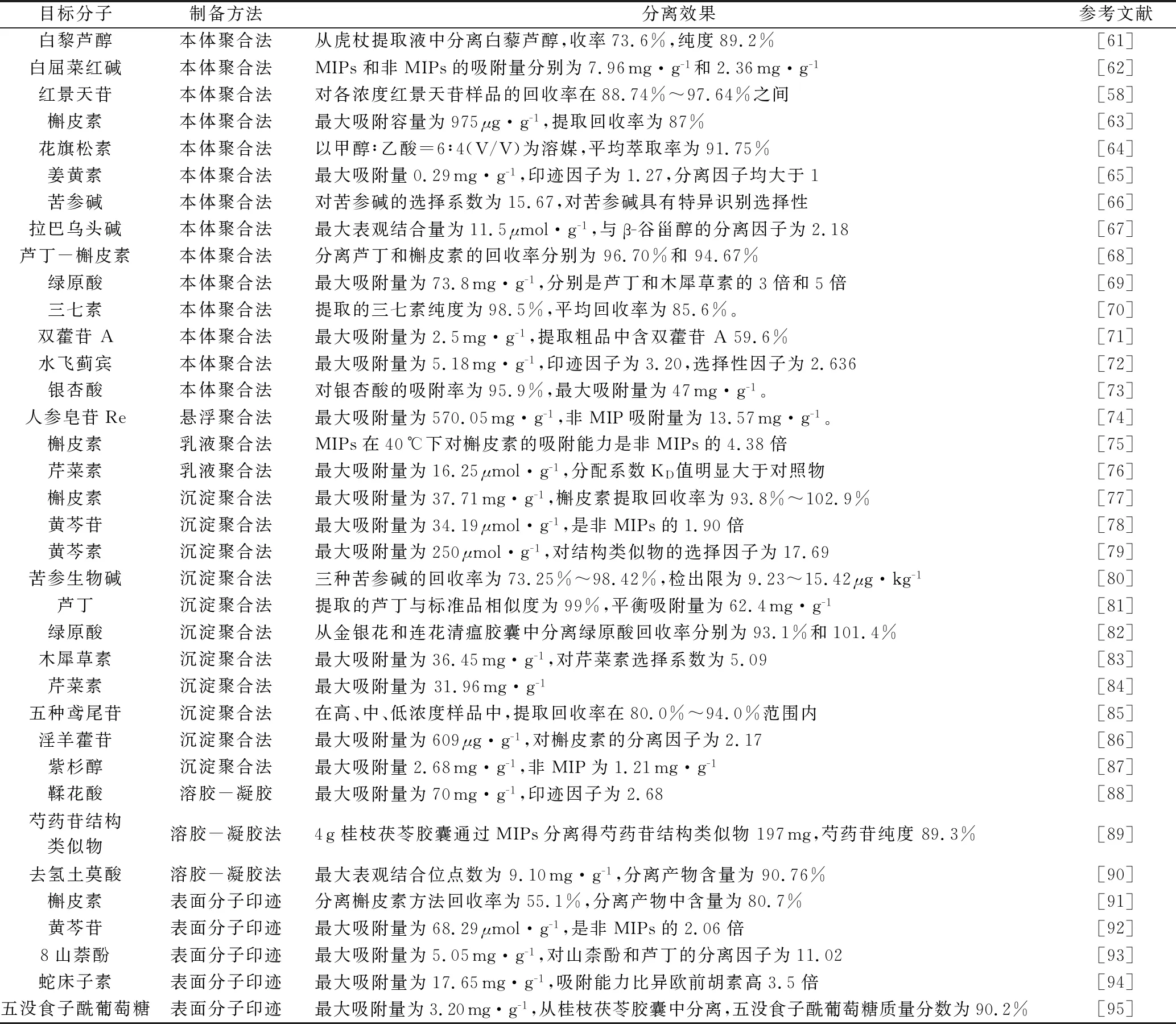
表4 近5年(2015-2020)MIPs用于中药有效成分分离统计
2.2 有效成分的筛选
中药有效成分或有效成分群药理作用筛选是阐明中药药效物质基础的关键性工作。分子印迹技术运用于活性成分筛选有多种形式,目前有一些探索性研究。Xie等[96]运用“敲除”理念,采用毛蕊异黄酮作为模板分子,制备了能特异性识别黄芪中黄酮类化合物的MIPs,与固相萃取技术结合,特异性“敲除”黄芪中黄酮类成分,获得黄芪提取物组、黄酮“敲除”组、黄酮组,对比三者的心肌细胞保护作用。结果表明在细胞毒性实验、活性氧实验和线粒体膜通透性实验中,黄酮“敲除”组显示出与提取物组相同的心肌细胞保护作用,黄芪中黄酮类成分与心肌细胞保护作用无明显相关性。Chen等[97]制备了不同的MIPs,分离出热毒宁注射液中七种咖啡酸及其类似物,并将成分进行组合,研究组合物对脂多糖诱导的小鼠单核巨噬细胞白血病细胞(RAW264.7)中前列腺素E2生物合成的抑制作用。结果表明在一定范围内,不同组合物可以产生协同的抗炎作用,但当浓度过高时,则产生拮抗作用,可能与不同成分相互竞争靶蛋白有关。采用分子印迹技术对中药活性成分及相互间药效作用机制的探讨,为中药有效成分药理活性筛选提供新思路。MIPs“敲除”活性筛选流程见图2。

图2 MIPs“敲除”活性筛选流程
2.3 有毒成分的分离
有毒中药理论是传统中医药理论的重要组成部分,现代中药药理和毒性效应及其两者的关系转换研究已经成为中医药研究的关键科学问题,也是制约中医药学科发展的瓶颈。随着中药毒理学研究的不断发展,对有毒中药中毒性成分的确证、分离,从而达到减毒增效的目的,成为中药研究的热点。马兜铃酸广泛存在于马兜铃以细辛属的中药中[98]。有研究表明马兜铃酸与肝癌的发生有“决定性关联”[99],因此,开发一种快速检测和分离中药中马兜铃酸的方法很有必要。Li等[100]采用分子印迹聚合技术功能化的磁性碳纳米管(MCNT@AAI-MIPs)除去中药中的马兜铃酸。首先通过溶剂热法合成了功能化磁性碳纳米管并在乙醇和水存在下,将模板分子与功能单体苯基三甲氧基硅烷(PTMOS)进行自组装。以正硅酸乙酯(TEOS)为交联剂,在功能化磁性碳纳米管上涂覆马兜铃酸MIPs膜即得MCNT@AAI-MIPs。将2 mg MCNT@AAI-MIPs混悬于2 mL马兜铃酸乙腈溶液中(50μg·mL-1),孵育一定时间(6~30 min)后,通过外部磁场分离吸附马兜铃酸的MCNT@AAI-MIPs,通过高效液相色谱法检测分离后混悬液中马兜铃酸的含量计算吸附容量。吸附于MCNT@AAI-MIPs中的马兜铃酸通过大量的乙腈超声解吸附。通过溶胶-凝胶法制备的分子印迹纳米复合材料对马兜铃酸的吸附容量达到18.54 g·mg-1,15 min可达到吸附动力学平衡,印迹因子为3.17,检测限和回收率都表明采用该技术可以高效地从中药中分离出马兜铃酸。MCNT @AAI-MIPs合成步骤见图3。何首乌作为传统的中药,其肝毒性和肾毒性问题近年来引起了广泛的关注[101-102]。有研究表明,大黄素类衍生物是何首乌中主要的毒性成分,其在大鼠体内可引起严重的代谢紊乱而诱发肝脏毒性[103]。孙挺[104]采用超声辅助提取法,获得有效成分二苯乙烯苷含量较高,而毒性成分大黄素、大黄素甲醚含量低,进一步以大黄素和大黄素甲醚为模板制备MIPs,用于从提取物中除去大黄素和大黄素甲醚,达到“脱毒”的目的。该方法大黄素和大黄素甲醚去除率均为100%,二苯乙烯苷的保留率在(88.49±2.09)%以上,达到减毒增效的目的。近年来,随着对中药毒性成分的认识和研究不断深入,明确中药毒性的物质基础,进一步实现减毒增效已经成为研究的热点。中药毒效关系与中药多成分、多途径、多靶点的整体性密切相关,不同种属、产地、加工方式及炮制对中药毒性成分均可能产生影响,将分子印迹技术应用于中药毒性成分研究,实现微量成分的分离和检测,有助于进一步明确中药毒效关系。
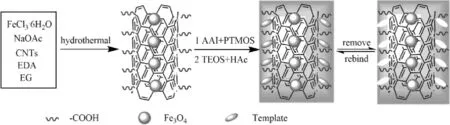
图3 MCNT@AAI-MIPs的合成步骤
2.4 代谢成分分离
中药体内代谢化学研究对阐明中药的有效性,探讨有效成分的作用原理,解释中药复方配伍的合理性具有重要意义,为新的活性成分的发现、新药合成及新的前体药物的研制提供可贵的理论和实践依据;此外,也是中药成分药代动力学和生物利用度研究的基础和前提。但是,由于中药成分复杂,每种单一成分含量较低,因此,代谢物的发现、提取和鉴定是中药体内代谢的研究难点,分子印迹技术由于其高识别能力和高选择性,在中药体内代谢成分分离方面显示出一定优势。Cai等[105]采用人参皂苷Rb1为模板分子,制备了相应的磁性MIPs,并将其用于大鼠粪便中人参皂苷代谢物的特异性识别和选择性富集。MIPs显示出快速分离、吸附能力强、高选择性以及快速结合动力学等特征。此外,结合线性离子阱与Orbitrap傅立叶扫描质谱法,确定或初步确定了26种原人参二醇组和32种原人参三醇组人参皂苷代谢物。Yang等[106]分别以多聚腺苷和大黄素-8-O-b-D-葡萄糖苷为模板分子制备了两种MIPs,将其应用于大鼠血浆中虎杖提取物代谢产物的分离和富集,获得17种茋类化合物和19种蒽醌类化合物。由于单组分含量低,体内代谢过程复杂,中药代谢成分分析通常依赖于高精度检测方法,对于微量甚至痕量代谢成分的分析有一定局限性。将分子印迹技术引入中药代谢成分研究,在代谢成分特异性选择和高效富集方面有着显著的优势。
3 展望
分子印迹技术用于中药成分的分离是现代物理化学手段在中医药现代化系统工程中的有益尝试,已经取得了一定的理论和实践成果,但由于分子印迹技术发展时间不长,在中医药学科中的应用仍然存在很多问题。首先目前所制备的 MIPs主要采用非极性材料,识别的目标分子以疏水性为主,对于亲水性目标分子的选择性存在一定障碍。在水相反应体系中,水分子与模板分子竞争从而削弱或破坏模板分子与功能单体之间的非共价作用力,进一步限制了MIPs在中药成分分离中的应用,急需克服。其次,MIPs与目标分子的结合速率还比较低,工业化制备MIPs可能存在均匀性差的弊端,快速高效的结合和解离还存在一定的技术壁垒,难以满足工业化需求。再者,大多数功能单体只适用于小分子物质,对于生物大分子如蛋白质、酶,如何保证MIPs形成规则的可容纳生物大分子的腔室结构以及在结合和解离过程中生物大分子的稳定性,尚需进一步探索。另外,分子印迹技术往往使用大量的有机试剂,不符合绿色化学的发展理念,因此,采用绿色技术和替代试剂也是研究的重点。随着生物技术、电子技术、合成手段和现代分析检测手段的迅猛发展,MIPs的合成、表征方法和理论系统将日臻完善,MIPs作为一种对目标分子高选择性的新技术,对中药活性物质的特异性分离有着明显的优势。将该技术应用于中药活性物质的分离,不仅具有深刻的理论意义,还具有广泛的应用前景。
