H4GeW12O40/TiO2催化合成乙酸正戊酯
2021-11-16陈飘王红吕宝兰杨水金
陈飘,王红,吕宝兰,杨水金
(湖北师范大学 化学化工学院,湖北 黄石 435002)
乙酸正戊酯在化工生产、木材工业、皮革工业以及塑料纺织工业[1]等领域具有重要作用.通常该类化合物是在浓硫酸的催化下以冰乙酸和正戊醇为原料通过酯化反应合成,但该反应产率低,副反应多而且设备腐蚀严重,不是理想的实验方案.在不断寻找新的催化剂以改进该类化合物的合成下开发了固体超强酸[2],氧化亚锡[3],硫酸铈铵[4],磺化硅胶[5],硫酸氢钠[6],固载杂多酸等催化剂[7],它们对酯化反应能起到催化作用.但以上方法也存在催化剂回收困难等不足,因而很难进一步开发应用[8].以固体杂多酸盐TiSiW12O40/TiO2为代表的催化剂[9]对于该反应同样具有良好的催化效果.锗钨酸作为一种固体超强酸,具有Keggin结构,催化活性高,工艺流程简单[10]等优点,但纯的锗钨酸本身存在的缺陷限制了它的广泛使用,为进一步提高对它的利用率,通常可将杂多酸负载在多孔材料上[11].作者发现催化剂H4GeW12O40[12-14]对酯化反应催化活性,但考虑到锗钨酸易溶解,回收困难,而二氧化钛性质优良,因而尝试用催化剂H4GeW12O40/TiO2合成乙酸正戊酯来探究其催化效果.
1 实验部分
1.1 催化剂H4GeW12O40/TiO2的制备
H4GeW12O40[15]:50 mL60 ℃热水中加入13.6 g钨酸钠、13.4 g的氧化钨后成为绿色浑浊液,120 ℃搅拌沸腾,再分别加入0.8 g的氧化锗、1.3 g碳酸钠,搅拌下加热回流2 h.在回流1 h后明显观察到溶液颜色变浅,回流2 h后颜色褪去,溶液变成澄清透明.缓慢滴加15 mL浓盐酸后回流15 min.静置冷却,滤去底部少量的绿色沉淀物,用无水乙醚萃取两次后,于培养皿中自然晾干即得H4GeW12O40·13H2O,然后70 ℃下在干燥箱中干燥12 h.
1.2 TiO2的制备
一边搅拌,一边将6.6 mL钛酸正丁酯中慢慢地逐滴加到65 mL蒸馏水中,搅拌30 min,并于180℃条件下水热反应持续10 h,冷却至室温得到白色沉淀.经抽滤洗涤3次,自然沉降2次后,在70 ℃下烘干,研细即得二氧化钛粉末.
1.3 H4GeW12O40/TiO2的制备
称取一定量的锗钨酸和二氧化钛于盛有一定量水的150 mL的圆底烧瓶中,保持沸腾状态回流2 h.蒸干后再煅烧.
2 结果与讨论
2.1 催化剂的表征
2.1.1 三种催化剂的红外光谱图
H4GeW12O40,TiO2,H4GeW12O40/TiO2的红外光谱图如下.
由图1看出,在979 cm-1(Ge—O)、886 cm-1(W=O)、764cm-1(W—O—W)处出现特征吸收峰与文献[16]报道一致,可确定合成物为Keggin型杂多酸H4GeW12O40.H4GeW12O40/TiO2的主要特征吸收峰为980 cm-1,保持着H4GeW12O40的Ge—O键的吸收峰.
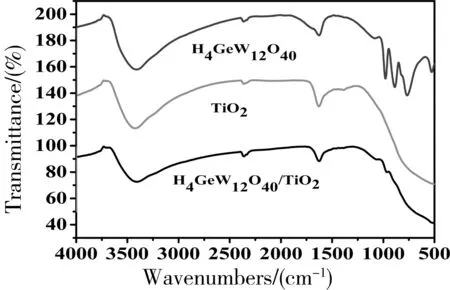
图1 H4GeW12O40/TiO2,TiO2,H4GeW12O40的红外光谱图Figure 1 Infrared spectra of H4GeW12O40/TiO2,TiO2,H4GeW12O40
2.1.2 催化剂的XRD光谱图
图2为H4GeW12O40,TiO2,H4GeW12O40/TiO2的XRD光谱图.
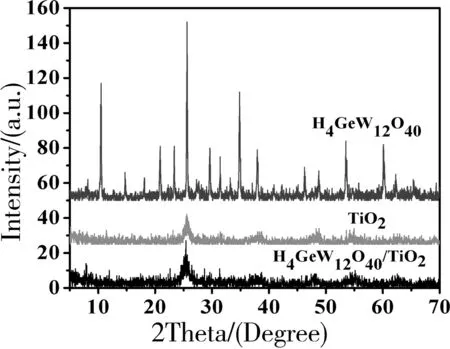
图2 H4GeW12O40,TiO2和H4GeW12O40/TiO2 的XRD光谱图Figure 2 XRD spectra of H4GeW12O40,TiO2 and H4GeW12O40/TiO2
由图2可知,H4GeW12O40在2θ为10°、25°、35°处出现强的特征衍射峰,在2θ为46~60°内也出现衍射峰,TiO2在2θ为25°出现锐钛矿衍射峰,H4GeW12O40/TiO2在2θ为25°出现特征衍射峰,并且比TiO2衍射峰宽和强度更强,说明H4GeW12O40更好的分散在载体TiO2上.
2.2 反应条件的优化
2.2.1反应物用量比对收率的影响
固定催化剂与带水剂用量和反应时间不变,将乙酸用量定为0.2 mol,通过调整反应物的用量比,来探究产物的收率随反应物用量比的变化.
由表1可知,随着反应物用量比的逐渐增大,产物的收率先是呈现上升趋势,达到最高产率后,又随反应物用量比的增加而呈现下降趋势.由表1中的数据可以看出,当正戊醇与冰乙酸的物料比为1.35∶1时,产物的最高收率为95.7%,故将此时的物料比称作反应物的最佳用量比.

表1 产物收率随反应物用量比的变化表Table 1 The change table of product yield with reactant dosage ratio
2.2.2 催化剂用量对收率的影响
当醇酸摩尔比为最佳比,保持带水剂的用量和反应所持续的时间不变时,改变催化剂用量,探究产物收率随催化剂用量的变化.
由表2可知,随着催化剂用量逐渐增大,产物收率先增加后又降低,当催化剂的使用量与反应物总的质量呈现0.5%的关系时,产物的收率达到最大值,此后,再增加催化剂用量,收率反而减小.故确定当催化剂的用量为参与反应的物质的总质量的0.5%时,是最佳的.

表2 产物收率随催化剂用量的变化表Table 2 The change table of product yield with the amount of catalyst
2.2.3 反应时间对收率的影响
当带水剂量固定、催化剂量不变,且在反应物的最佳配比下,改变反应时间,探究产物收率随反应时间的变化关系.
由表3可知,在45 min到75 min之间,反应所持续的时间加长,产物的收率呈现上升的趋势,过了75 min后继续增加反应时间,则产物的收率下降,所以可将75 min作为该反应所需要的最佳反应时间.

表3 产物收率随时间的变化表Table 3 Change of reaction yield with time
2.2.4 产物的收率随带水剂使用量的变化
当催化剂用量为最佳、反应所需的时间为最佳时间75 min,且在反应物的最佳配比下,反应时间和催化剂用量最佳时,改变带水剂环己烷的用量,探究产物收率随带水剂用量的变化关系.
由表4可知,当带水剂体积为8 mL时产物的最高收率为95.7%.此时的用量就是带水剂的最佳用量.

表4 产物收率随带水剂用量的变化表Table 4 Product yield varies with the amount of water agent
综合表1、2、3、4可知,在正戊醇与冰乙酸的物料比为1.35∶1时,在上述的几种优化条件下进行乙酸正戊酯的催化合成,其收率可高达95.7%.且在该优化条件下平行三次实验,实验收集沸程范围为130 ℃以上,实验收率分别为95.7%,94.6%,94.2%,平均收率为94.8%.
2.2.5 几种催化剂催化同一反应时的活性比较
表5列出了氧化亚锡[3],硫酸钛[17],以及H4GeW12O40/TiO2催化合成乙酸正戊酯的数据.
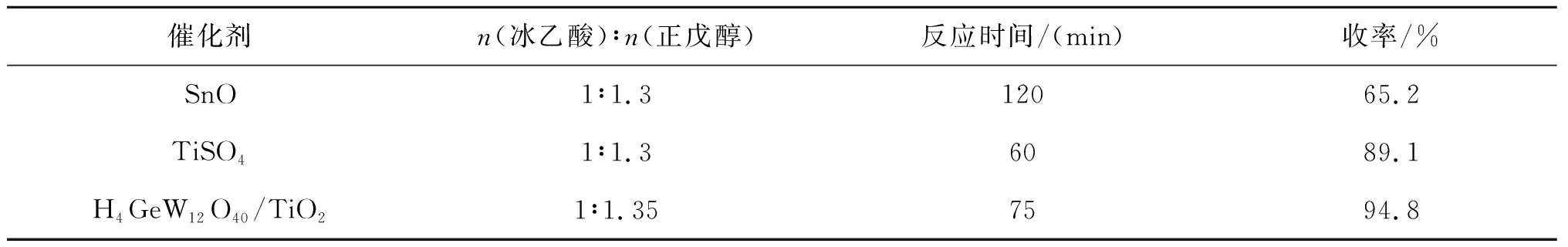
表5 各催化剂催化活性差异表Table 5 The difference in catalytic activity of each catalyst
由表5可知H4GeW12O40/TiO2催化合成乙酸正戊酯时,可以有效缩短反应所需要的时间,提高产物的收率,催化效果比其他两种的要好.
2.2.6 催化产物的IR表征
3 结 论
在乙酸正戊酯的合成中,H4GeW12O40/TiO2体现了良好的催化活性,乙酸用量为0.2 mol,当n冰乙酸:n正戊醇=1∶1.35,催化剂用量与参与反应的反应物总质量呈现0.5%的关系时,用取8 mL环己烷作为带水剂,反应75 min后可使乙酸正戊酯的收率高达95.7%.所以H4GeW12O40/TiO2对于合成乙酸正戊酯有较大的实用性.
