一种新型联苯双子季铵盐缓蚀剂的合成及性能研究
2021-11-13童欣张光华张万斌刘晶韩小倩王哲王艳蒙冯鹏超
童欣,张光华,张万斌,刘晶,韩小倩,王哲,王艳蒙,冯鹏超
(1.陕西科技大学 陕西省轻化工助剂重点实验室,陕西 西安 710021;2.陕西科技大学 陕西省轻化工助剂化学与技术协同创新中心,陕西 西安 710021)
在油田开采过程中,酸洗液对提高原油产出量至关重要,因此盐酸对油管及设备的腐蚀也随之增加[1-2],为减少酸对此类金属的腐蚀,加入缓蚀剂是最简单有效的防腐方法[3-4]。基于之前的研究得出[5-7],咪唑啉类缓蚀剂具有经济高效等优点,但其制备复杂,反应温度高,具有一定的安全隐患。大部分的缓蚀剂都含有杂原子(N,O,S,P),杂环及不饱和键,且双子季铵盐缓蚀剂的缓蚀效率更高,所以本文以绿色环保的甲基丙烯酸二甲氨基乙酯作为原料合成一种新型双子季铵盐,且目标产物中N,O上的孤对电子,可与金属上的空d轨道形成配位键,增大缓蚀剂的吸附能力[8-11],从而提高缓蚀率。双子季铵盐相比于单离子季铵盐[12],还具有很好的水溶杀菌的作用。
1 实验部分
1.1 试剂与仪器
甲基丙烯酸二甲氨基乙酯、联苯二氯苄、浓盐酸(质量分数37%)、无水乙醇、丙酮、乙醚均为分析纯。
VERTEX-80型傅里叶变换红外光谱仪;ADVANCEⅢ 600 MHz型核磁共振波谱仪;PARSTATMC型电化学工作站。
1.2 缓蚀剂的合成
BDMA的合成:将甲基丙烯酸二甲氨基乙酯(3.14 g,20 mmol) 和丙酮(15 mL) 加入三口烧瓶中振摇,再将联苯二氯苄(2.51 g,10 mmol)用15 mL 丙酮溶解后,逐滴加入到三口瓶中,在55 ℃的水浴锅中反应8 h,完成季铵化反应。再利用减压蒸馏分离出丙酮,剩余粗产物经乙醚洗涤、干燥,最终得到产物BDMA,产率82.36%。BDMA的制备路线如下:

1.3 失重测试
将样品Q235钢(50 mm×10 mm×2 mm)依次用水、丙酮、乙醇清洗,干燥后称重。分别在30,40,50,60 ℃下,将样品钢在含有不同浓度BDMA的1 mol/L HCl溶液中浸泡4 h,再清洗、干燥、称重。计算腐蚀速率和缓蚀率。
1.4 电化学实验
25 ℃下,以辅助电极Pt电极,参比电极(SCE)饱和甘汞电极[13]和工作电极(WE)Q235钢片组成三极电极。电化学阻抗谱(EIS)测试是在105~10-2Hz频率范围内,交流振幅为10 mV的开路电势(OCP)下进行的,在每次测试之前,将电极浸入溶液中1 h以达到稳定状态,使用ZSimpWin软件分析了阻抗数据。每次扫描后都要更换溶液和工作电极,对每个实验条件进行3~4次测量,以估计重复性,相对标准偏差小于5%[14]。
1.5 表面分析
用砂纸将Q235钢片打磨,直至上面无任何划痕为止,再分别把钢片浸泡在不含缓蚀剂,和含有100 mg/L BDMA 的1 mol/L 盐酸中1 h,用AFM观测其表面形貌,扫描频率为2 Hz。
1.6 量子化学计算
量子化学计算是采用计算化学中的Material Studio 8.0软件将产物用3D的模型画出来,并计算出分子模型,通过分子模型的分析来进一步通过解释分子结构与机理的关系。
2 结果与讨论
2.1 BDMA的结构表征
BDMA的红外吸收光谱见图1。


图1 BDMA的红外光谱图Fig.1 FTIR spectra of BDMA
由图2可知,BDMA的核磁共振氢谱(溶剂为 D2O)。图中,δ4.70的峰是溶剂D2O。δ1.85的峰是与双键相连的—CH3的6个H,δ3.05 的峰是氮上4个—CH3的12个H,δ3.64 的峰是与氮相连的α位—CH2—的4个H,δ4.42 的峰是与苯环相连的—CH2—的4个H,δ4.52 的峰是与氧相连的—CH2—的4个H,δ5.25~5.27 和δ5.78~5.81的峰是双键末端的2个H,δ5.62和δ6.01的峰是双键末端的2个H,δ7.35~7.47的峰是苯环上的4个 H,δ7.47~7.52的峰是苯环上的4个H,通过1H NMR和FTIR验证了BDMA的分子结构。

图2 BDMA的1H NMR谱图Fig.2 1H NMR spectra of BDMA
2.2 失重实验
图3为不同温度和浓度下,Q235钢片在盐酸中浸泡4 h的缓蚀率结果。样品的腐蚀速率(Vcorr)和缓蚀率(η)可由下列公式得出。
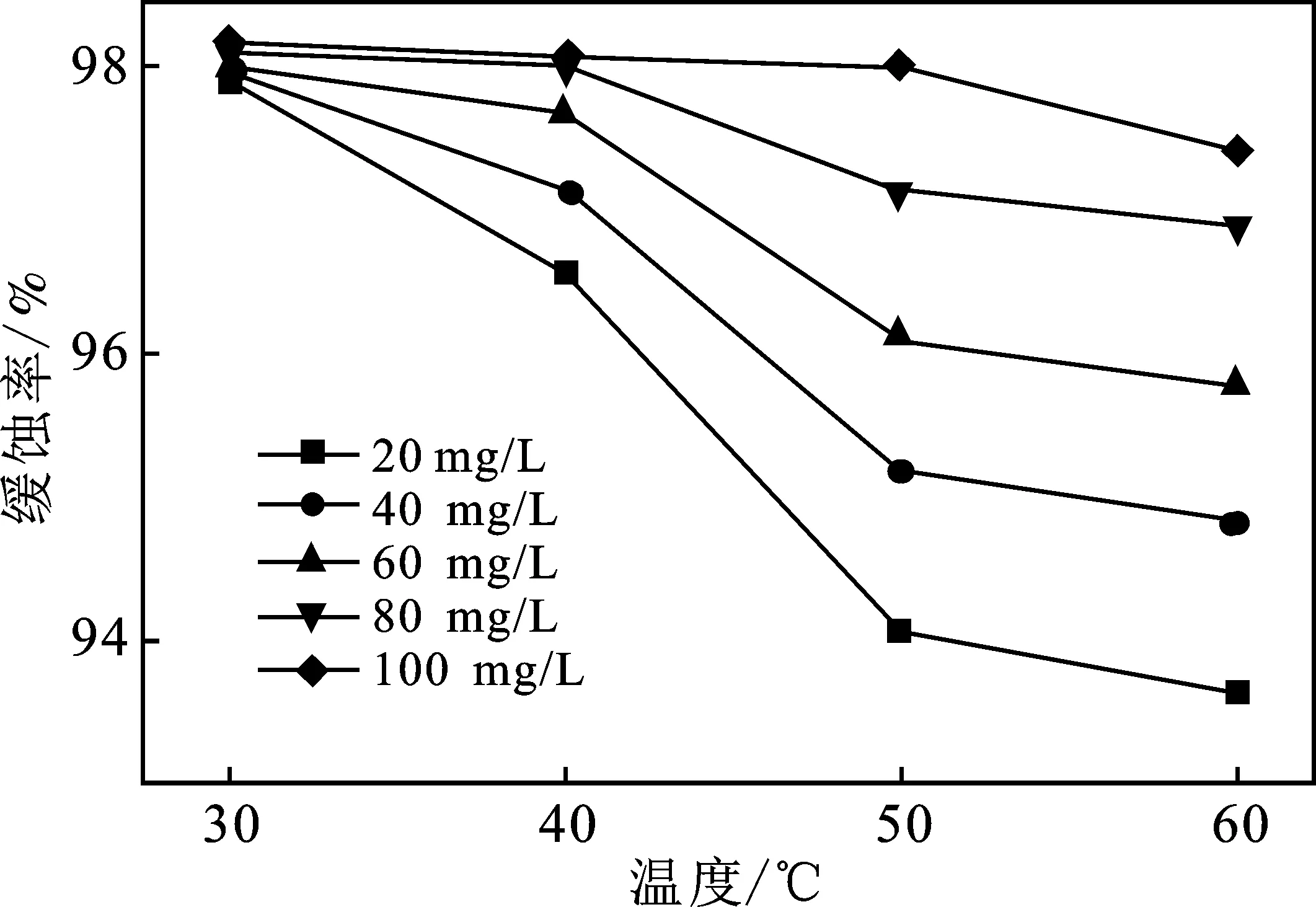
图3 BDMA的缓蚀率结果图Fig.3 Results of BDMA’s corrosion inhibition rate
V=Δm/st
(1)
η=(v0-v)/v0×100%
(2)
根据缓蚀率图3可知,相同温度下,BDMA浓度与缓蚀率成正比,伴随BDMA浓度的增加,缓蚀剂分子在Q235钢片表面的吸附量和覆盖率逐渐增大,阻隔了酸和金属的接触,导致腐蚀速率减小。相同的浓度下,随着温度的上升,缓蚀率有所下降,这是因为在较高温度下反应速率加快,且使BDMA吸附在Q235钢片表面的部分分子脱落,从而降低了缓蚀率。30~60 ℃的缓蚀率均可达到97%以上,可知 BDMA在较高的温度下仍可牢固的吸附在Q235钢片表面。在30 ℃时,20~100 mg浓度的缓蚀剂的缓蚀率均可达到97.5%以上,这说明BDMA具有优异的缓蚀效果。
2.3 电化学测试
在25 ℃,用电化学阻抗谱(EIS)测试盐酸对Q235钢的腐蚀。在空白样品和含有BDMA的酸溶液中的Nyquist图以及等效电路图模型见图4。

图4 BDMA浓度对Q235钢的Nyquist曲线的影响Fig.4 The influence of BDMA concentration on the Nyquist curve of Q235 steel
由图4可知,曲线均呈近似半圆形状,未添加和添加了缓蚀剂的阻抗谱中的形状并未改变,说明缓蚀剂只是改变了反应的活性而不改变腐蚀的性质,腐蚀主要与溶液和电极界面处的电荷转移有关[15]。随着缓蚀剂的浓度增大,半圆的半径增大,这证明缓蚀剂分子在Q235钢表面形成了一层保护膜且膜逐渐紧密,减少了酸和金属的接触,使缓蚀率增加。
图5和表1示出了25 ℃下,低碳钢在1 mol/L盐酸中不存在和存在BDMA时的Tafel曲线。当BDMA加入到溶液中时,腐蚀电位(Ecorr)向正方向移动,阳极和阴极反应都被抑制。BDMA应属于优先抑制阳极腐蚀过程的混合型缓蚀剂。BDMA的加入导致腐蚀速率降低,这解释了阳极和阴极Tafel曲线向较低电流密度大范围位移的原因。这一现象表明,阳极金属溶解和阴极析氢反应通过金属表面缓蚀剂分子的覆盖而受到抑制[16]。同时,随着浓度的增加,这些过程的抑制作用更加明显。BDMA溶液中阴、阳极Tafel曲线的形状相对于空白溶液几乎没有变化,即反应的机理不受缓蚀剂的影响[17]。
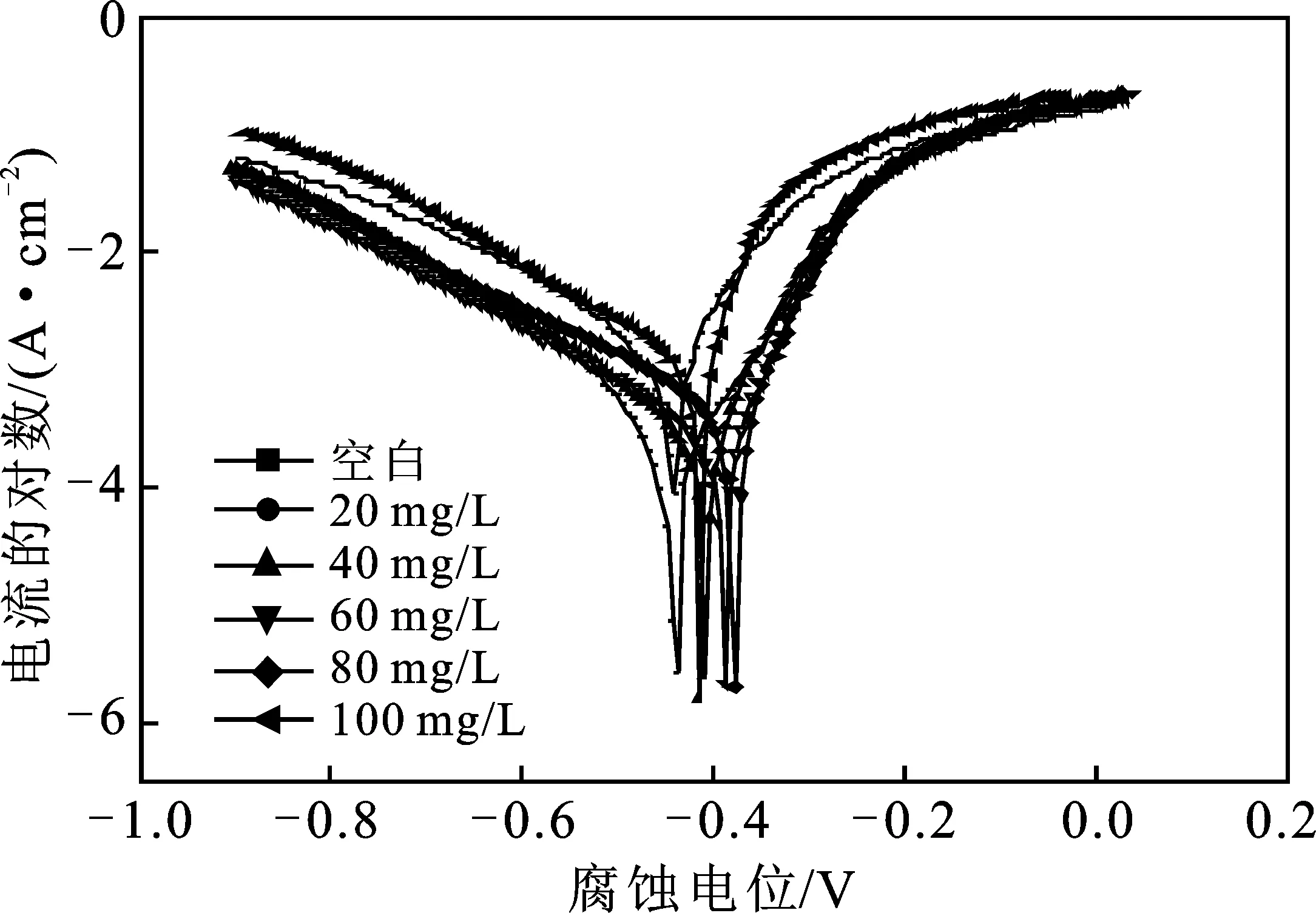
图5 BDMA浓度对Q235钢的极化曲线的影响Fig.5 Influence of BDMA concentration on the polarization curve of Q235 steel
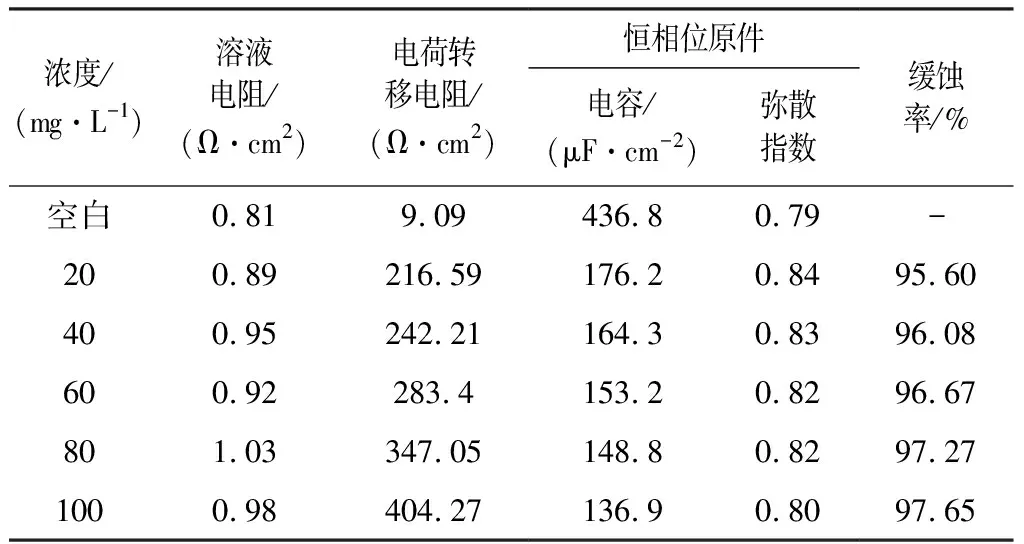
表1 电化学测试对应的阻抗参数Table 1 Impedance parameters corresponding to electrochemical test
2.4 吸附等温线
吸附等温线是对BDMA在金属表面的吸附行为的进一步表征,相关参数由Langmuir吸附等温式计算。
c/θ=1/Kads+c
(3)
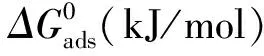
(4)
式中,55.5 (mol/L)为水的摩尔浓度;R[8.314 J/(mol·K)]为气体常数;T(K)为热力学温度。
根据缓蚀率数据分析,用c/θ对c作图,结果见图6。该图中相关系数接近于1,符合朗格缪尔等温式,且属于单分子层吸附,有效的阻隔了酸性介质。

图6 温度对 BDMA的Langmuir拟合曲线的影响Fig.6 The influence of temperature on the Langmuir fitting curve of BDMA
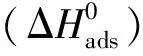
(5)
(6)
式中,X是积分常数。
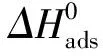

图7 BDMA在1 mol/L HCl中的lnKads与1/T图Fig.7 Diagram of lnKads and 1/T of BDMA in 1 mol/L HCl

表2 温度对BDMA的吸附参数的影响变化Table 2 The influence of temperature on the adsorption parameters of BDMA
2.5 活化能
通过公式得活化能(Ea,kJ/mol),可进一步解释BDMA在Q235钢表面的吸附行为:
vcorr=Aexp(Ea/RT)
(7)
式中,vcorr[mg/(cm2·h)]为腐蚀速率;A[mg/(cm2·h)]为指前因子;R[8.314 J/(mol·K)]为气体常数;T(K)为热力学温度。
下图是不同浓度BDMA,1 mol/L盐酸中的Arrhenius图。与空白样中的Ea相比,加入缓蚀剂的Ea较大。Ea与腐蚀速率成反比,是因为缓蚀剂在钢片表面吸附成膜[19],阻隔了酸与钢片的接触,腐蚀速率减缓,从而起到优异的缓蚀效果。通常,Ea在40~800 kJ/mol 区间内属于化学吸附,所以BDMA在钢片表面的吸附主要为化学吸附。
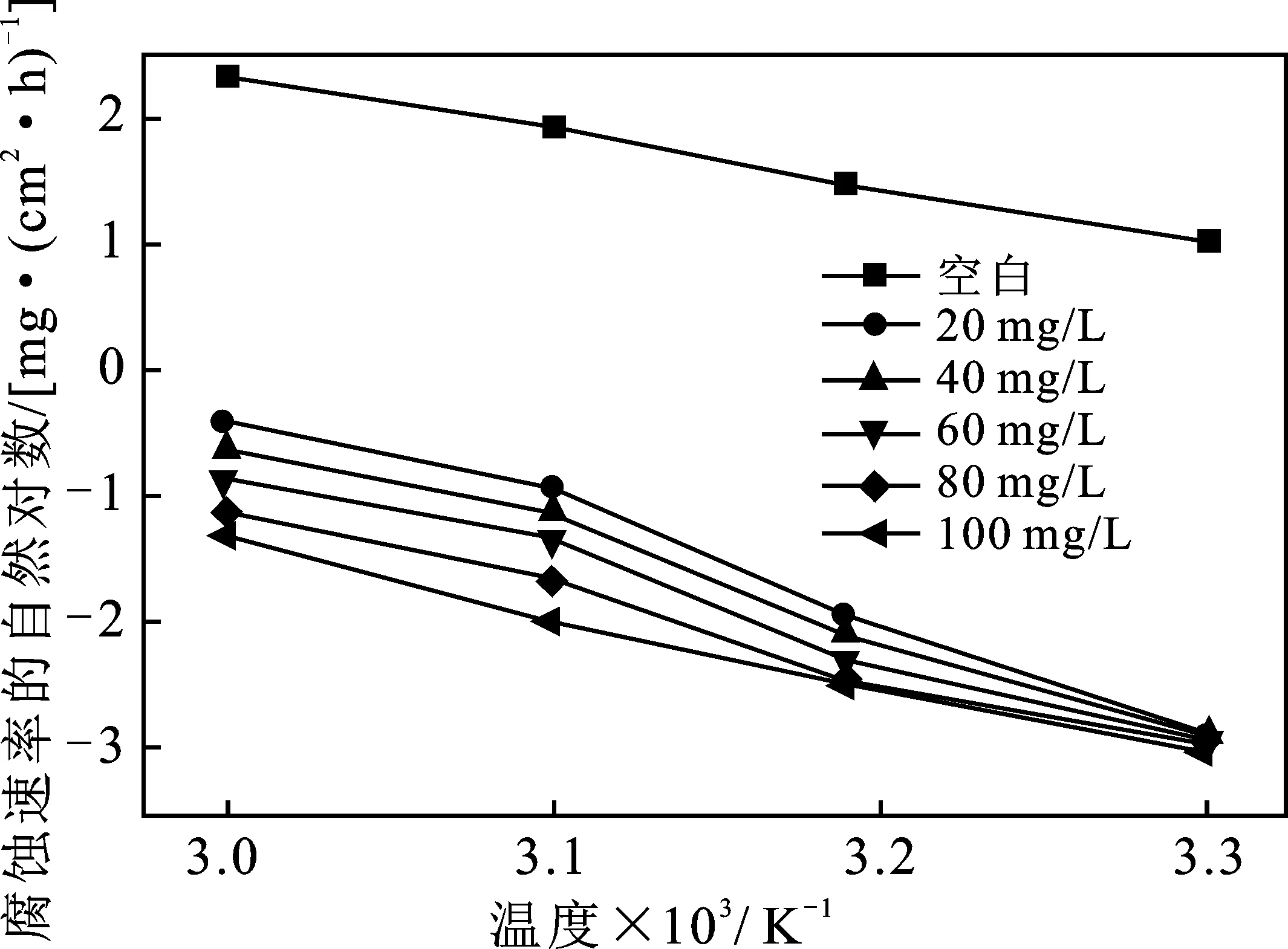
图8 浓度对BDMA Q235钢上Arrhenius的影响Fig.8 Effect of concentration on Arrhenius on BDMA Q235 steel
2.6 腐蚀形貌分析
图9为Q235钢分别在有或无BDMA的盐酸溶液中浸泡1 h后的三维形貌和相图,其中(a)为未腐蚀前的样品,Q235钢表面较为平整,可清晰的看到砂纸打磨过的痕迹,表面粗糙度是30.4 nm;(b)是浸泡在1 mol/L盐酸溶液中的样品,由于H+对钢片的腐蚀,图中有很多腐蚀过的痕迹,出现了不同程度的凹陷和凸起,表面粗糙度增至121 nm;(c)为浸泡在含100 mg/L BDMA的盐酸溶液中的样品,表面的凹陷和凸起明显变得相对平滑,腐蚀痕迹明显减少,此时表面粗糙度为36.2 nm。上述结果表明BDMA分子能够吸附在Q235钢表面,BDMA在金属表面形成保护层将酸和金属隔开,阻止腐蚀。
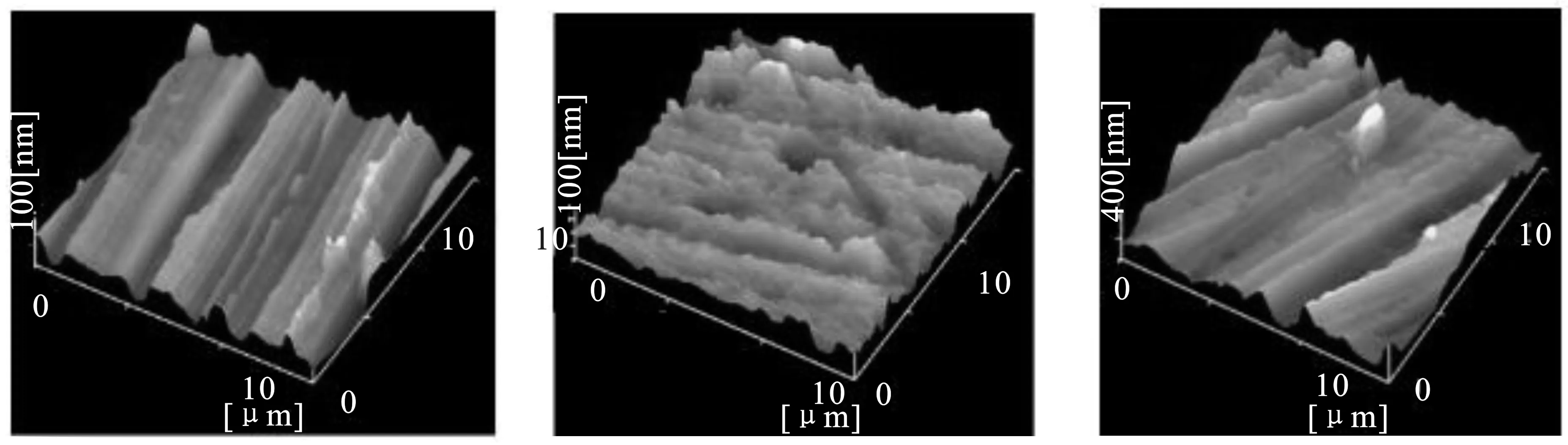
图9 不同介质下Q235钢的AFM图Fig.9 AFM diagram of Q235 steel in different media

2.7 量子化学计算
由前线轨道理论可知[20],HOMO轨道是指最高占据分子轨道即为提供电子的能力,EHOMO的值与给低能级和空轨道提供电子的能力成正比。LOMO轨道是指最低占据分子轨道即为接受电子的能力,ELOMO值与EHOMO相反,其值越低,越易接受电子[21]。从图中我们可以看出在该结构中分子的右侧含双键和氧原子的附近给电子的能力较高,中间含苯环附近接受电子的能力较高,表明该缓蚀剂的具备得电子和失电子的能力。使BDMA牢固的吸附在金属表面,缓蚀效果更佳。ΔE是HOMO和LOMO轨道之间的能量间隙,化学反应是由于电子在能级上面的跃迁产生,所以间隙越近,化学反应越易进行[22],由表中可以看出,该缓蚀剂的ΔE为1.57,所以发生反应较为容易。

图10 BDMA的优化分子结构和前线轨道能量分布Fig.10 Optimized structure(A),HOMO(B) and LUMO(C) distributions of BDMA

表3 BDMA在不同温度下的吸附参数Table 3 Frontier orbital energies of BDMA
3 结论
本文以甲基丙烯酸二甲氨基乙酯和联苯二氯苄为联结基,成功的制备出了一种具有水溶性的双子季铵盐缓蚀剂(BDMA)。通过其他的测试方法对BDMA在1 mol/L HCl中对Q235钢的缓蚀性能进行更深一步的解释。结果表明,BDMA能够明显的抑制钢表面的腐蚀,在低温下的缓蚀率比高温下更加优异,这是因为在高温下BDMA会在钢表面发生脱附。通过对其阻抗和极化参数的分析,得出BDMA在钢片表面形成了一层膜,抑制金属与酸的接触,从而起到保护金属的作用,且BDMA符合Langmiur吸附等温式,主要为化学吸附。量子化学计算表明该缓蚀剂上有很多的吸附位点,可以使缓蚀剂牢固的吸附在金属表面。这些测试都表明该缓蚀剂具有优异的缓蚀性能,且该缓蚀剂工艺简单,应用广泛,易于保存。
