气相色谱法测定葡萄酒中甜蜜素的条件优化
2021-11-13邹大松向雅洁邹昌新
邹大松,向雅洁,邹昌新
(1.公安县公共检验检测中心,湖北 荆州 434300 ;2.松滋市公共检验检测中心,湖北 松 滋 434200;3.松滋市刘家场镇畜牧兽医技术服务中心,湖北 松滋434217;4.松滋市农业农村局,湖北 松滋 434200)
甜蜜素的化学名称为环己基氨基磺酸钠,化学式为C6H11NHSO3Na,于1937 年被Sveda 发现。由于其甜度远高于蔗糖,于是早在1950 年就被当作食品甜味剂推广使用[1-4]。但是关于甜蜜素作为食品添加剂使用是否对人体有害这一课题在国际还没有定论,部分国家全面禁止食品中添加甜蜜素,还有部分国家则是严格限量控制食品中的甜蜜素含量。最新的文献资料表明,甜蜜素当作食品添加剂来使用被人体吸收后,会给人体骨细胞正常运转带来负面影响,尤其是经常摄入富含甜蜜素的食品会对人体(尤其是排毒能力差老幼群体)肝脏系统造成不良影响。
葡萄酒是用新鲜的葡萄或葡萄汁经完全或部分发酵酿成的酒精饮料,因其营养价值较高、口感独特、酒精含量相对白酒要低,故广受消费者的青睐。近年来,随着人们对食品安全的日渐关注,相关部门加强了对食品卫生安全的监管,要求各生产企业严格按照国家标准控制食品中的各种添加剂用量,并不定期抽检,曝光了一些不法行为。例如,2019 年河南工商部门对登封市美真宜商贸有限公司崇高路店销售的马峪川甜红葡萄酒进行检测,查出甜蜜素含量超出国家限量标准。
目前测定食品中甜蜜素含量的方法很多,主要有气相色谱法、液相色谱法、薄层色谱法、重量法等[5-8]。研究采用气相色谱法测定葡萄酒中甜蜜素含量,对样品前处理条件进行了优化,以期为同类样品的甜蜜素分析测定提供参考。
1 材料与方法
1.1 试验材料
1.1.1 试验仪器Agilent 7890B 气相色谱仪,带FID的检测器,美国安捷伦公司;UPH 超纯水机,成都优普公司;GZX-101-1-BS 电热恒温鼓风干燥箱,深圳博泰公司;UMV-1 涡旋振荡器,北京优晟公司;204E 天平,规格0.000 1 g,美国梅特勒托利多公司。
1.1.2 试验试剂甜蜜素标准溶液,BW12371-1,含量1 000 mg/mL,北京万佳首化生物科技有限公司;硫酸,优级纯,中国医药集团有限公司;亚硝酸钠,分析纯,中国医药集团有限公司;氢氧化钠,分析纯,中国医药集团有限公司;正庚烷,分析纯,中国医药集团有限公司;氯化钠,分析纯,中国医药集团有限公司;葡萄酒(市场购买),275 mL,酒精含量3.5%,香港新动力公司。
1.2 试验方法
1.2.1 标准溶液配置将1 000 mg/mL 甜蜜素标准溶液的母液按照GB5009.97—2016[9]中的方法配制成为0.5、1.0、2.0、5.0、10.0 mg/L 的梯度标准溶液,备用。
1.2.2 葡萄酒样品前处理及条件优化(1)水浴除酒精和二氧化碳:用天平准确称取25.0 g 葡萄酒样品到烧杯中,先用氢氧化钠溶液(40 g/L)将葡萄酒样品的pH 调至7~8;置于60℃水浴中处理30 min,以去除葡萄酒中的酒精与二氧化碳;将水浴后的葡萄酒放置到常温,用超纯水定容到50 mL,备用。(2)衍生化反应:分别向去除酒精和二氧化碳的葡萄酒溶液中加入5.0 mL 正庚烷、2.5 mL 亚硝酸钠溶液(50 g/L)以及2.5 mL 硫酸溶液,水浴反应30 min;加入2.5 g 氯化钠,采用涡旋混合器充分混匀;高速离心分层后取上清液待测[10-14]。该研究重点优化了葡萄酒样品衍生化反应的条件,包括硫酸浓度(50、100、150、200、250 g/L)、水浴温度(10、20、30、40、50℃)和涡旋振荡时间(20、40、60、80、100、120 s),得出最佳衍生化反应条件。
1.2.3 色谱参数参考GB5009.97—2016 中色谱条件相关参数,使用DB-1 弱极性毛细色谱柱。检测器选择为FID;分流进样,分流比为30 ∶1;进样口温度230℃;进样量体积为1 μL;色谱柱选择程序升温,先以5℃/min 的速度从65℃升温至85℃,然后以18℃/min 的速度升温至220℃,在220℃下保持10 min。
1.2.4 方法验证(1)精密度检验:将同1 次葡萄酒样品连续使用气相色谱检测7 次,考察方法的精密度。(2)加标回收率检验:在葡萄酒样品中分别加入100、150 及200 μL 10.00 mg/mL 的甜蜜素标准溶液,按照优化后的衍生化反应条件进行衍生化,然后上机检测,考察样品的加标回收率。
2 结果与分析
2.1 衍生化反应条件优化
2.1.1 最佳硫酸浓度从图1 可以看出,当硫酸浓度在在50~150 g/L 区间内,甜蜜素的峰面积与硫酸浓度呈正相关性,即随着硫酸浓度的升高,峰面积增加;当硫酸浓度在150~250 g/L 区间内,甜蜜素的峰面积呈缓慢下降趋势;当硫酸浓度为150 g/L 时,检测到的甜蜜素峰面积最大。葡萄酒样品处理中加入硫酸的目的是让衍生化反应处于有利的酸性环境,同时硫酸能促进葡萄酒样品中的亚硝酸钠反应为亚硝酸,并为衍生化反应带来羟基促进最终产物的合成[15]。试验结果显示,当硫酸浓度为150 g/L 时,最有利于甜蜜素衍生反应的进行。
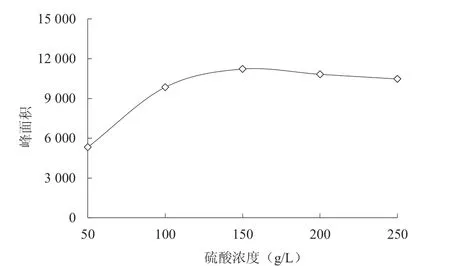
图1 不同浓度硫酸处理甜蜜素的峰面积
2.1.2 最适水浴温度由图2 可知,甜蜜素的峰面积与水浴温度呈正相关性,即随着水浴温度的升高,甜蜜素的峰面积增加;尤其当水浴温度从10℃上升到30℃时,甜蜜素峰面积增加显著,而当水浴温度由30℃上升到50℃时,甜蜜素峰面积增加值趋于稳定。葡萄酒样品衍生化反应的原理是甜蜜素在酸性环境下先生成环己胺,然后环己胺与亚硝酸反应结合为重氮盐,但是重氮盐在温度较高时容易自我分解生产氮气[16]。在试验过程中,当温度达到30℃及以上时,重氮盐的结构不稳定,产生大量气体,温度越高反应越剧烈,导致葡萄酒样品的溶液随着气体产生形成飞溅,造成样品中甜蜜素含量的部分损失。因此,葡萄酒样品前处理法中衍生化反应的最适水浴温度为30℃。
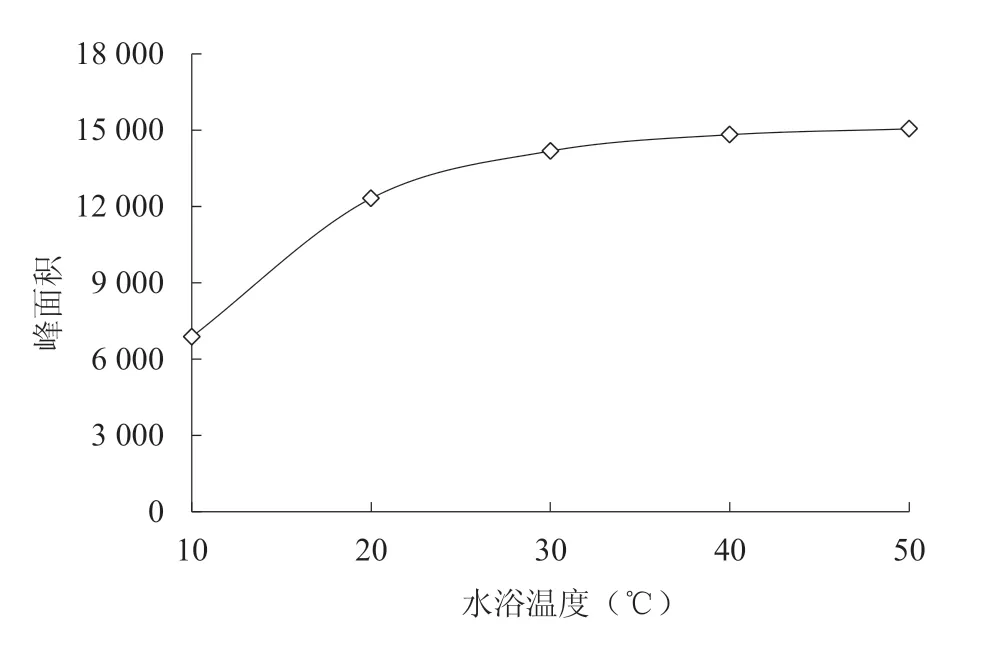
图2 不同水浴温度处理甜蜜素的峰面积
2.1.3 最佳涡旋振荡时间从图3 可以看出,甜蜜素峰面积与涡旋振荡时间呈正相关性,即随着涡旋振荡时间的延长,峰面积增加;当涡旋振荡时间在20~80 s 范围内时,峰面积与涡旋振荡时间的相关性较为明显,涡旋振荡处理80 s,甜蜜素的峰面积最大;而当涡旋振荡时间在80~120 s 区间时,峰面积与涡旋振荡时间的相关性趋于平稳[17]。在实际操作过程中,从节约时间与节省资源的角度考虑,以涡旋振荡处理80 s,最有利于甜蜜素衍生化反应的进行。
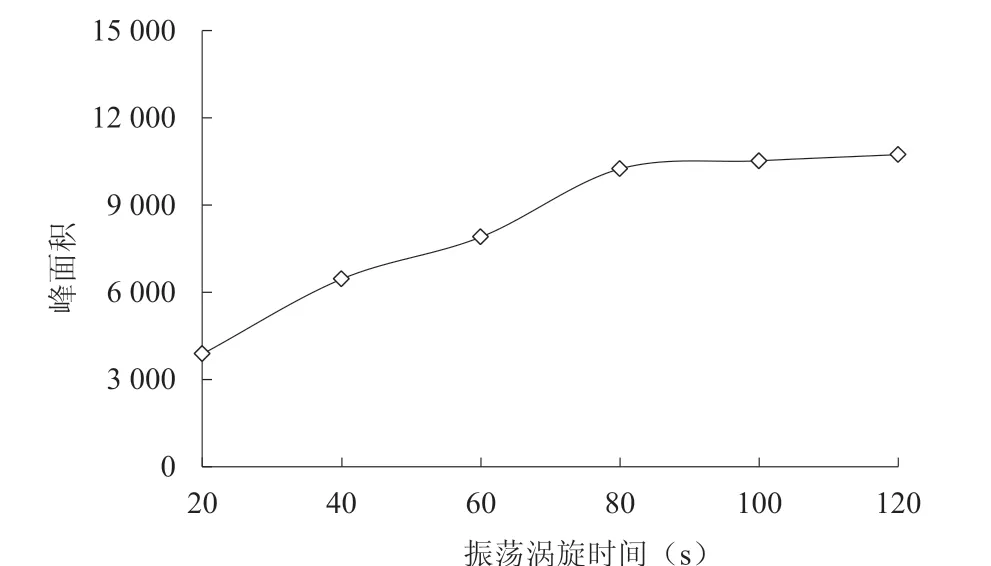
图3 不同涡旋振荡时间处理的甜蜜素峰面积
2.2 标准曲线及色谱图
如图4 所示,该检测方法的标准曲线方程为y=5 220.3x+ 989.03,R2=0.999 6 >0.995,可以满足试验要求。衍生化反应条件优化后,葡萄酒样品中的甜蜜素色谱峰如图5 所示,各物质的分离度较好,不存在相互干扰,且峰型完整,甜蜜素的保留时间为5.387 min。
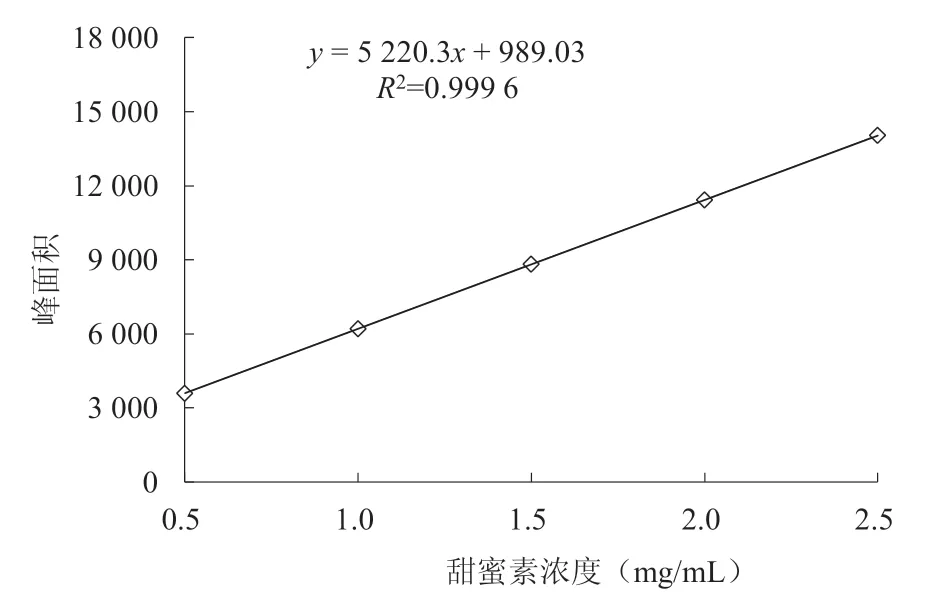
图4 甜蜜素标准曲线

图5 葡萄酒样品的甜蜜素色谱图
2.3 精密度检验
精密度试验结果显示,7 次测定的峰面积平均值为10 837.6,标准偏差为475.4,相对标准差为4.4%,小于5%,表明该检测方法满足试验要求。
2.4 加标回收率检验
由表1 可知,甜蜜素的回收率在90%~110%之间,符合试验要求。
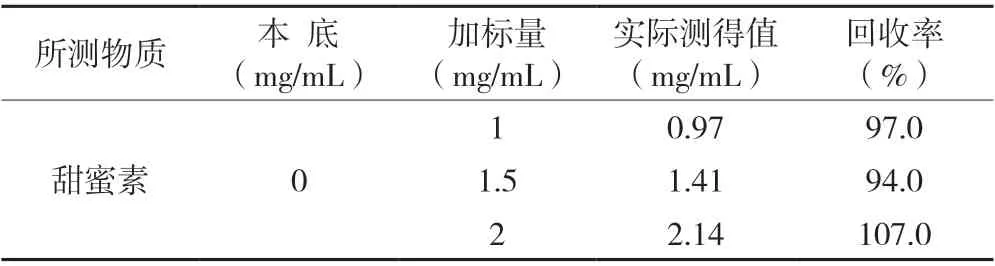
表 1 甜蜜素的加标回收率检验结果
3 结 论
由于供试葡萄酒样品种类较为单一,所有样品中测得的甜蜜素含量均低于仪器与方法的检出限,为了便于研究的开展,采用样品加标法[18-20]在购买的葡萄酒样品中加入了10.00 mg/mL 甜蜜素标准溶液200 μL。
该研究以葡萄酒样品中的甜蜜素为对象,参考GB5009.97—2016 中的仪器配置、试验条件、前处理法以及衍生法的相关要求,优化了衍生化反应中的硫酸浓度、水浴温度和涡旋振荡这3 个参数。结果表明:葡萄酒样品中甜蜜素的最佳衍生化反应条件为硫酸浓度150 g/L、水浴温度30℃、涡旋振荡时间80 s,采用气相色谱法获得的标准曲线为y=5 220.3x+ 989.03,R2=0.999 6 >0.995;对同1 样品进行7 次测定,峰面积的平均值为10 837.6,标准偏差为475.4,相对标准差为4.4%,小于5%,加标回收率在90%~110%之间,表明该研究建立的葡萄酒中甜蜜素含量的气相色谱检测方法重现性好、精密度高,符合分析检测要求,可应用于同类样品的甜蜜素分析检测。
