血液透析对行经皮冠状动脉介入治疗的患者合用阿司匹林及氯吡格雷抗血小板聚集的影响
2021-11-13王亚辉杨滨
王亚辉 杨滨,2
(1.山西医科大学,山西 太原 030001; 2.山西医科大学第二医院心血管内科,山西 太原 030001)
近年来,慢性肾脏病(chronic kidney disease,CKD)在全世界的发病率急剧增加,约为13.4%[1],大多数CKD患者进展到终末期肾病(end-stage renal disease,ESRD),心血管疾病是ESRD患者死亡和发病的主要原因,约占ESRD患者死亡率的45%,而其中20%的死因是急性冠状动脉综合征导致的[2]。对于这些患者,可通过经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)来实现血运重建,但支架内血栓形成是PCI后不可避免的问题,双联抗血小板治疗阿司匹林和氯吡格雷是减少支架内血栓形成的标准治疗[3]。ESRD患者需要长期进行血液透析(hemodialysis,HD)治疗,有研究表明HD患者的抗血小板治疗效果不佳,普遍存在治疗后血小板高反应性(high on-treatment platelet reactivity,HPR)。HPR指同一种抗血小板药物在不同患者所产生的不同抗血小板效应,其中经治疗后血小板反应性仍较高者(即血小板功能检测提示血小板活性抑制不足),血栓事件发生风险可能较高[4]。然而关于HD患者如何合理应用抗血小板治疗的研究是有限的,目前尚无相关指南依据。
通过光学方法检测血小板的功能是测定血小板聚集度的传统“金标准”。AggRAM血小板聚集仪检测原理即为光学方法检测,在特定的连续搅拌条件下于富含血小板血浆中加入诱导剂时,由于血小板发生聚集,悬液的浊度就会发生相应的改变,光电池将浊度的变化转换为电讯号的变化,在记录仪上予以记录,根据聚集曲线可计算出血小板聚集程度和时间。乏血小板血浆源自同一份样品聚集率为100%(无漂浮的血小板),通过检测乏血小板血浆的吸光度可测量除血小板外的其他因素产生的光散。
1 资料与方法
1.1 临床资料
本研究为回顾性研究,纳入2020年1月—10月于山西医科大学第二医院住院的临床确诊CKD合并冠心病的HD患者23例,男性17例,女性6例。所有患者都具有完整病历且经美国海伦娜AggRAM血小板聚集仪监测血小板聚集率。记录患者年龄、性别、吸烟史和既往病史等资料,收集患者住院期间相关实验室化验指标包括血小板、血红蛋白、血清肌酐、丙氨酸氨基转移酶和N末端脑钠肽前体等,根据国际肾脏病指南推荐使用肾小球滤过率计算公式(CKD-EPI)计算肾小球滤过率[5]。
纳入标准:患者均根据诊断标准和治疗指南诊断为冠心病(包括稳定型心绞痛、不稳定型心绞痛或急性心肌梗死)[6],所有患者成功行PCI,同时诊断为CKD 5期(肾小球滤过率均<15 mL/min)[7],定期接受持续性HD治疗(3~4次/周,每次4 h以上)。
排除标准:(1)血小板计数>450×109/L或<100×109/L;(2)口服抗凝或其他抗血小板药物者;(3)凝血异常;(4)严重贫血、感染和甲状腺功能亢进等。
1.2 治疗方法
所有患者均规律口服阿司匹林片(拜耳医药保健有限公司,规格:100 mg)100 mg,1次/d;氯吡格雷(波立维,赛诺菲制药,规格:75 mg)75 mg,1次/d。其他治疗包括血管紧张素转化酶抑制剂/血管紧张素Ⅱ受体阻滞剂、β受体阻滞剂、钙离子拮抗剂、他汀类和质子泵抑制剂等一线治疗药物。
1.3 观察项目及检查方法
1.3.1 血小板聚集率的测定及分析
HD前(HD当天,口服双联抗血小板治疗后HD前)及HD后(透析后2 h内)抽取患者静脉全血3 mL,采用美国海伦娜公司的AggRAM血小板聚集仪检测HD前后的血小板聚集率,采用花生四烯酸(arachidonic acid,AA)和腺苷二磷酸(adenosine diphosphate,ADP)两种不同的诱导剂诱导血小板聚集,以AA诱导的血小板聚集率检测阿司匹林,以ADP诱导的血小板聚集率检测氯吡格雷。将ADP诱导的血小板聚集率>55%定义为HPR,≤55%为血小板低反应性(low on-treatment platelet reactivity,LPR)[8]。
1.3.2 主要心血管不良反应
通过门诊复查和电话进行随访,记录出院后6个月内主要心血管不良事件(major adverse cardiovascular events,MACE)发生情况。MACE主要包括心源性死亡、复发心绞痛、急性心肌梗死和心力衰竭等。
1.4 统计学处理

2 结果
2.1 纳入患者的临床和实验室特点
本研究共调查23例患者,根据ADP诱导后的血小板聚集率分为氯吡格雷治疗后HPR组和LPR组,对HD患者出现HPR进行单因素分析,详细的临床和实验室特征见表1,两组患者在高脂血症、肾小球滤过率方面比较,差异有统计学意义(P<0.05),年龄、性别、吸烟史、高血压史、糖尿病史、血小板、血红蛋白、血清肌酐、丙氨酸氨基转移酶和N末端脑钠肽前体等方面比较,差异无统计学意义(P>0.05)。由于他汀类药物、质子泵抑制剂和钙离子拮抗剂也经过肝脏P450酶代谢,可能与氯吡格雷存在竞争性结合,但在本研究中表明这些药物与HD患者治疗后血小板反应性之间没有相关性(P>0.05)。

表1 HD患者的临床和实验室特征
2.2 HD前后血小板聚集率检测结果比较
经AA诱导的HD前后血小板聚集率分别为7.7%±6.9%和13.2%±8.6%,HD后经AA诱导的血小板聚集率明显升高,HD降低了阿司匹林的疗效(P<0.01),见图1。

图1 经AA诱导后HD前后的血小板聚集率
经ADP诱导的HD前后血小板聚集率分别为32.0%±17.2%和40.6%±19.0%,HD后经ADP诱导的血小板聚集率明显升高,HD降低了氯吡格雷的疗效(P<0.01),见图2(上述具体数据见表2)。
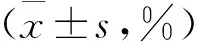
表2 HD前后血小板聚集率比较
HD前6例(26.1%)患者ADP诱导的血小板聚集率>55%,HD后出现9例(39.1%)患者ADP诱导的血小板聚集率>55%,HD后增加了13%的患者出现HPR。
2.3 HPR组与LPR组MACE发生率比较
为期6个月的随访结果显示,HPR组发生MACE 3例(再发心绞痛1例,急性心力衰竭1例),发生率为22.2%,LPR组发生MACE 1例(急性心力衰竭1例),发生率为7.1%,HPR组MACE发生率明显高于LPR组,但差异无统计学意义(P>0.05),见表3。

表3 HPR组与LPR组MACE发生率比较
3 讨论
本研究发现HD后患者血小板聚集率明显升高,表现出很高的HPR发生率,降低阿司匹林和氯吡格雷的抗血小板疗效,其中高脂血症和肾小球滤过率升高与HPR发生相关。在HD患者中,HPR患者的MACE发生率明显高于LPR患者,但无统计学意义。
CKD是PCI术后不良心血管结局、复发性缺血事件和不良预后的危险因素。CKD患者在接受PCI的人群中所占比例越来越大,占急性冠状动脉综合征患者的40%[9]。研究表明,CKD尤其是HD患者对氯吡格雷治疗的抗血小板反应降低,且常表现出HPR,同本次研究的结果一致。ADAPT-DES研究纳入了8 582例(其中85例患者进行维持性HD)PCI术后给予阿司匹林和氯吡格雷抗血小板治疗的患者,对所有患者进行血小板功能检测及2年的结果分析,得出近2/3的HD患者服用氯吡格雷后出现HPR,HD和HPR均与药物洗脱支架植入后2年的不良预后独立相关[10]。Alexopoulos等[11]在经过氯吡格雷抗血小板治疗的HD患者中观察到很高的HPR患病率,85例HD患者中,70例(82.4%)显示HPR;同样在Htun等[2]的研究中,HD患者也表现出非常高的HPR患病率,31例HD患者中有10例(32.3%)表现出对阿司匹林低反应,14例(45.2%)患者表现出对氯吡格雷低反应,而且HD治疗后氯吡格雷低反应性的患者增加了6.5%。而HD降低阿司匹林与氯吡格雷抗血小板效果的机制目前尚不明确。
笔者考虑影响HD患者抗血小板治疗效果及出现高HPR患病率的潜在机制包括肾功能不全、HD本身及药物生物利用度差(包括活性代谢物可能的HD清除)等。相关研究表明肾功能不全患者的基线血小板活化显著增加,对双联抗血小板治疗的反应减弱,并且有证据表明,无论是否存在糖尿病,肾小球滤过率本身的严重降低是氯吡格雷维持剂量下高残留血小板反应性的重要决定因素[12-13]。在笔者的研究中肾小球滤过率升高也为出现HPR的危险因素。HD患者表现出增强的血小板反应性与血液暴露于HD回路本身也有很大关系,在HD过程中,人工表面可以激活血小板和白细胞,血小板大量活化,可能伴随着血小板聚集和血小板-白细胞相互作用[14];而且HD在一定程度上导致血小板更新增加,这也可能导致HPR[15]。HD降低氯吡格雷的治疗效果也应该考虑到氯吡格雷复杂的代谢过程,氯吡格雷是一种前药,只有15%才能代谢成为活性药物发挥作用,生物利用度较差,并且活性代谢物通过肾排出,可能在HD过程中被去除。Small等[16]的研究表明,ESRD患者在60 mg普拉格雷剂量治疗后,普拉格雷活性代谢物水平会低于肾功能正常的患者,氯吡格雷和普拉格雷都是一种前药,笔者考虑这也可能适用于氯吡格雷。
笔者的研究表明HD会降低阿司匹林和氯吡格雷的疗效,并且使用氯吡格雷后HD患者有较高的HPR发生率,这将会导致HD患者血栓事件的风险增加,因此需对出现HPR的HD患者选择更有效的个体化抗血小板治疗方案。有研究指出低剂量替格瑞洛(90 mg,1次/d)比氯吡格雷能更好地抑制HD患者的血小板[17]。最近一项日本的研究纳入了38例HD患者,通过分别给予氯吡格雷和普拉格雷并在HD前后评估血小板反应性,得出给予普拉格雷(3.75 mg,1次/d)在HD前后均比氯吡格雷(75 mg,1次/d)能更好地抑制血小板聚集[18]。在PIANO-2 CKD试验中,对于HD患者,与75 mg/d或150 mg/d的氯吡格雷相比,联用西洛他唑200 mg/d可增强对血小板活化的抑制作用,降低HPR发生率[19]。总之,目前的研究表明通过将氯吡格雷改为替格瑞洛或普拉格雷,或者辅助使用西洛他唑可改善HD患者HPR发生率。
综上所述,HD患者具有非常高的HPR发生率,需要更多的研究来评估HD患者出现HPR的影响因素,以及其他抗血小板药物的潜在优势。本研究的局限性是:单中心研究样本量少,未纳入患者的基因信息,未随访及观察患者的预后。对于HD降低阿司匹林与氯吡格雷的抗血小板治疗疗效及出现高HPR发生率的影响因素尚需高质量、大样本、长随访期的临床研究,明确血小板功能检测在指导HD患者抗血小板治疗中的价值,确立HPR统一的血小板功能检测方法及标准,从而对HD患者实施个体化、有效的抗血小板治疗方案。