胸腺肿物的影像诊断思维
2021-11-12复旦大学附属华山医院静安分院
复旦大学附属华山医院静安分院
梁宗辉 主任医师、硕士生导师
吴娟 解骞 舒政 邓晓飞 梁宗辉
病例资料患者,男,49 岁,体检发现纵隔肿物2 周入院。入院查体:神清,气平,锁骨上淋巴结未及肿大,双肺呼吸音清,心率80 次/分,律齐,未及杂音,腹软,肝脾肋下未及,神经系统检查未见异常。无既往史。实验室检查未见异常。
影像表现:CT 增强示前纵隔胸腺区域结节,大小约18 mm×29 mm,可见分叶,平扫29 HU,增强后57 HU,周围结构清晰,包膜完整。两肺门及纵隔未见明显肿大淋巴结。考虑胸腺瘤可能(图1a,1b)。MR 增强示前纵隔胸腺区结节样异常信号,呈分叶状,大小约18 mm×29 mm,T1WI呈等信号,T2WI 呈高信号,DWI 呈稍高信号,边界较清楚,信号尚均匀,增强后呈中度强化,与周围血管界限清晰,两侧肺门及纵隔未见明显肿大淋巴结。考虑胸腺瘤可能大(图1c~1f)。

图1 a)胸部CT 平扫示前纵隔胸腺区分叶状软组织密度影,大小约18 mm×29 mm,密度均匀,平扫CT 值约29 HU;b)增强后动脉期病灶呈均匀轻中度强化,CT 值约57 HU;c)MR T1WI 示病灶呈等低信号,包膜薄而连续;d)T2WI 示病灶呈均匀高信号;e)DWI 示病灶信号稍增高;f)增强后动脉期显示病灶轻中度均匀强化
手术记录:达芬奇机器人辅助胸腔镜下全胸腺切除术。术中探查:3 cm×2 cm×2 cm 实性肿块,包膜完整,无外侵;左右纵隔胸膜、左右肺、心包、左右膈神经、胸骨、胸壁及周围血管探查无粘连外侵。术中行纵隔肿瘤切除加全胸腺切除,无肿瘤残留,无淋巴结清扫。
病理结果(图2):肉眼所见,前纵隔灰黄肿物3 cm×3 cm×2 cm,质中,界不清。免疫组化示:CK(+)、VIM(+)、SALL 4(')、Syn(+)、CgA(+)、CD56(+)、Ki'67(20%+)、CD5(')。结论:(前纵隔胸腺肿瘤)非典型类癌,伴点灶状坏死,大小3 cm× 3 cm×2 cm,核分裂像约3 个/2 mm2。送检“左侧第6 组”淋巴结0/1 枚,未见肿瘤转移。送检A“3a 组淋巴结”镜检为少量胸腺组织。
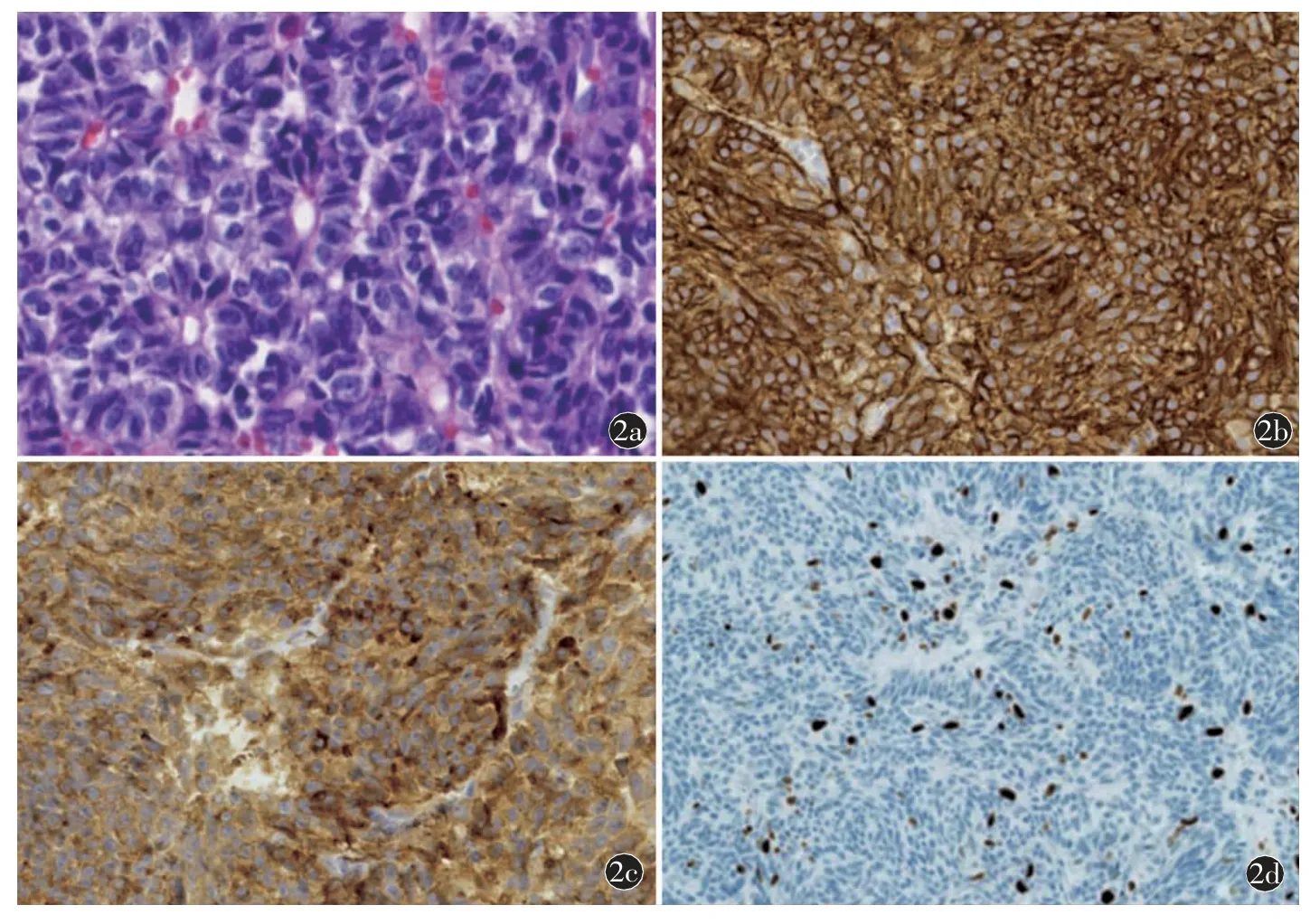
图2 a)H'E 染色光镜下细胞学检查显示癌细胞排列呈巢状(200×);b)ChgA(+)(200×);c)CD56(+)(200×);d)Ki'67(20%+)(200×)
讨论胸腺组织具有特殊性,起源于内中外三个胚层细胞,因此会发生胸腺瘤、胸腺癌、神经内分泌肿瘤(neuroendocrine tumors,NETs)等多种细胞起源的肿瘤[1]。胸腺NETs 发病率低,约占纵隔肿瘤的2%~4%,占所有NETs 的0.4%[2]。2015 年WHO 胸腺肿瘤遵循肺部分类策略,把胸腺NETs 分为典型类癌(typical carcinoids,TC)(低级)、非典型类癌(atypical carcinoids,AC)(中级)、大细胞神经内分泌癌和小细胞癌(高级)[2]。其中典型类癌和不典型类癌统称为胸腺类癌(thymic carcinoid,ThC)[2]。ThC起源于胸腺的Kulschitsky 细胞即嗜铬细胞,属前肠源类癌,1972 年从NETs 中分离出来[2]。ThC 罕见,年发生率约百万分之一,好发于男性,男女比例约3∶1,平均发病年龄约50岁[3]。不典型类癌较典型类癌多见,占所有NETs 的40%~55%,恶性程度更高,侵袭能力更强[3]。
临床上,约30%ThC 患者没有症状,常于体检中偶然发现;部分患者表现为不典型局部症状,如咳嗽、胸痛、上腔静脉阻塞和呼吸困难等;约50%患者出现与激素分泌过多有关的症状[4],包括5'羟色胺分泌引起的类癌综合征,异位促肾上腺皮质激素分泌引起的Cushing 综合征,生长激素释放激素分泌引起的肢端肥大症;约25%患者在I 型多发性内分泌肿瘤(multiple endocrine neoplasm,MEN)综合征基础上发生[2]。ThC 伴发Cushing 综合征易发生肾上腺增生或肾上腺肿瘤,而伴有MEN'I 型易发生甲状旁腺增生或甲状旁腺瘤[5],临床上容易误诊,因此影像学发现和诊断ThC 对临床正确治疗显得尤为重要。
影像上,ThC 一般发生在前纵隔胸腺区,少部分位于下纵隔,甚至后纵隔,主要由于胸腺异位所致。ThC 呈类圆形、分叶状或不规则形软组织肿块,肿块越大,形态越不规则,包膜越不完整,坏死囊变及钙化出血越多见,侵袭性越强。大部分ThC 发现时已经晚期,表现为巨大的前纵隔肿块,呈偏心性生长,局部突向肺内,与周围组织分界不清,有时包绕侵犯血管或向血管间隙生长,甚至向锁骨上、纵隔或肺门旁淋巴结转移[6]。本例中肿块位于胸腺区,缺乏恶性征象,唯有分叶状外形提示侵袭性可能,此征象或许与肿瘤早期发现有关。ThC 平扫CT 密度与胸壁肌肉类似,增强后轻'中度强化,CT 值增高约20~40 HU,与本例相符。有文献报道部分ThC 肿块内可见细丝状或线状明显强化征象,对于诊断有提示作用[6,7]。MR 信号在T1WI 呈低信号,T2WI 呈高信号,增强后不均匀异质性强化。增强后肿块内网状隔膜样强化是ThC 的强化特点,对诊断具有提示价值[7]。ThC 由于生长抑素受体的过度表达,生长抑素类似物奥曲肽单光子发射计算机断层扫描(single photon emission computed tomography,SPECT)功能检查诊断该疾病的敏感度和特异度较高[3],但有研究显示SPECT'CT 奥曲肽扫描并不比增强CT 或MRI 扫描检测到更多病变,且并非所有ThC 都表达生长抑素受体,所以常规奥曲肽扫描主要用于切除后的监测[3]。本例术后SPECT'CT 检查显示术区生长抑素受体阴性。
病理上,ThC 主要依靠HE 染色与免疫组化检查进行诊断。肉眼观肿瘤为大小不等的圆形、卵圆形或分叶状肿块,有或无包膜,切面灰白,质韧。光镜下肿瘤细胞小,大小一致呈卵圆形,巢状或菊花样排列,细胞浆呈嗜酸性,细胞核在TC 与AC 中表现不一致。TC 细胞核轻中度异型,有丝分裂<2 个/2 mm2,无坏死;而AC 细胞核高度异型,有丝分裂<2 个/2 mm2,有坏死,或2~10 个/2 mm2,有或无坏死[3]。2 mm2最高活性区域的有丝分裂个数和是否合并坏死是区分TC 与AC 的最重要的组织学标准。免疫组化中,嗜铬粒蛋白A(chromogranin A,ChgA)、突触素(synaptophysin,Syn)、神经细胞黏附分子(CD56)和神经特异性烯醇化酶(neuron specific enolase,NSE)四种神经内分泌标记物中的两种及以上表达阳性[8]。最近研究表明,Ki'67 是NETs 亚分类的重要标志物,对鉴别典型/非典型类癌的临界值为7.5%,敏感度和特异度分别为91.4%和100%[8]。
第八版TNM 分类分期推荐使用国际肺癌研究协会(International Association for the Study of Lung Cancer,IASLC)和国际胸腺恶性肿瘤协作组织(International Thymic Malignancy Interest Group,ITMIG)联合提出的循证胸腺恶性肿瘤分期系统,胸腺瘤、胸腺癌和胸腺类癌共用一个TNM 分期[9]:T1a:肿瘤包裹或延伸到前纵隔脂肪中,T1b:纵隔胸膜直接受累;T2:侵入心包;T3:侵犯至肺、头臂静脉、上腔静脉、胸壁或膈神经;T4:侵犯主动脉、心包内肺动脉、心肌、气管或食管。N1:胸腺前结节;N2:胸部深处或颈部淋巴结。M1a:胸膜或心包结节;M1b:肺实质内结节或远处器官转移。新的TNM 分期系统用于适应证和分期治疗的判断,也可作为一个潜在的预后预测模型[4]。
对于可根治性切除的ThC 患者应尽快安排手术治疗,但在术前应控制功能综合征。以前的ThC 切除术不推荐淋巴结切除,但新TNM 分期系统建议术中应进行局部淋巴结清扫。由于ThC 预后不良,对伴有MEN'I 的年轻男性,尤其是具有侵袭性胸腺肿瘤家族史的患者,在进行初次或复发性甲状旁腺切除术时,可进行预防性胸腺切除。对于治疗后的局部复发患者,仍建议根治性手术切除。对于晚期R0 患者或R1~2 切除术患者,建议行射频或冷冻消融术的同时进行放疗和/或全身治疗,包括生长抑素类似物如奥曲肽和兰瑞肽疗法、达卡巴嗪/替莫唑胺或基于奥沙利铂的细胞毒性化疗、依维莫司靶向治疗、肽受体放射性核素疗法和干扰素α等[4]。ThC预后较差,5年或10年生存率分别为28%~72%和26%~60%。患者生存率主要与肿瘤大小,切除的完整性以及TNM 分期分类相关[4]。
影像诊断思维诊断胸腺肿物首先需要定位,与其他脏器不同,正常胸腺组织40 岁时退化成脂肪[10],故胸腺肿物的定位需遵循纵隔肿物的定位思路。纵隔肿物的分布遵循一定的规律,临床上有多种分区法用于指导纵隔病变的鉴别诊断。但唯有常用的三分区法能较好的涵盖胸腺可能发生的病变,其他分区法会分割胸腺病变发生的范围。根据三分区法,绝大多数胸腺病变位于前纵隔,当肿物较小时容易定位,当肿物较大时需综合位置以及与心脏、大血管的关系进行判断肿物起源于前纵隔还是侵犯至前纵隔。前纵隔包括胸骨后方,心包、主动脉和头臂血管前方,胸廓入口下方和横膈上方。此例病灶较易定位于前纵隔。
此例肿物表现为实性肿块,均匀中度强化,炎性病变可以排除,考虑肿瘤性病变或其他类似肿瘤的良性病变。对于前纵隔原发性肿瘤而言,影像诊断需要判断肿瘤的起源,良恶性以及与周围脏器的关系,帮助临床指导治疗方案的选择。这需要综合肿块大小、形态、密度、强化方式、有无囊变坏死、有无周围侵犯及淋巴结转移和有无合并内分泌异常等信息进行判断。
前纵隔肿瘤根据不同起源分为[10]胸腺恶性肿瘤(约35%),淋巴瘤(约25%),甲状腺及甲状旁腺肿瘤(约15%),良性畸胎瘤(约10%),恶性生殖细胞瘤(精原细胞瘤约4%,非精原细胞瘤约6%)和其他少见病变如脂肪瘤/脂肪肉瘤(约5%)。胸腺瘤是前纵隔最常见的原发性肿瘤,根据2015 年WHO 分类分为低风险胸腺瘤(A 型、AB 型和B1型)和高风险胸腺瘤(B2 型和B3 型)[11]。低风险胸腺瘤倾向于轮廓规则的实性结节,可伴有坏死囊变,包膜完整,较少发生周围侵犯以及淋巴结和远处转移;高风险胸腺瘤倾向于轮廓不规则的实性肿块,包膜完整或不完整,坏死、囊变及淋巴结转移多见[11]。MR 可以清晰显示胸腺瘤的包膜是否完整及肿瘤内的纤维间隔(低风险胸腺瘤典型征象)对鉴别出低风险胸腺瘤具有较高价值[11]。胸腺癌与ThC侵袭性高于胸腺瘤,大血管侵犯多见,其他征象重叠,鉴别困难。值得注意的是重症肌无力在AB 型、B1 型和B2 胸腺瘤中特别常见,因此若重症肌无力患者合并前纵隔肿瘤,则可诊断胸腺瘤[11]。ThC还需与胸腺高级别NETs鉴别,虽然NETs 亚型之间影像学特征无明显差异,但肿瘤侵袭性不同,鉴别主要依靠病理学特征[2]。此病例表现为前纵隔包膜完整中度强化的实性结节,影像学征象倾向于低风险胸腺瘤和ThC 中少见的侵袭性较低的典型类癌,临床指标无指导价值,诊断出不典型类癌比较困难。
淋巴瘤好发于年轻患者,约50%纵隔淋巴瘤伴有发热、体重减轻和盗汗等症状,可伴有血清乳酸脱氢酶升高。淋巴瘤患者常发生纵隔、下颈部或腋窝淋巴结肿大,其中内乳淋巴结肿大与淋巴瘤的诊断有很强的相关性[11]。淋巴瘤通常推挤包绕血管,但不会侵犯血管,增强后轻中度强化,坏死少见,很少出现心包及胸膜结节样转移,鉴别相对容易[10]。甲状腺肿瘤一般不位于前纵隔,只有胸内甲状腺肿时需要鉴别,可以看到与甲状腺相连,值得注意的是纵隔甲状腺肿并不总是与甲状腺相连,但会表现出相似的影像学特征[10]。异位纵隔甲状旁腺肿瘤常表现为有或无钙化的小软组织病变,与甲状旁腺功能亢进有关[10]。
生殖细胞瘤分为畸胎类和非畸胎类肿瘤。良性畸胎瘤常见于年轻患者,因含有脂肪、液体、钙化(包括骨和牙齿样成分)等特殊成分而较好鉴别。非畸胎类包括精原细胞瘤和非精原细胞瘤,影像表现与ThC 鉴别困难[6]。精原细胞瘤好发于年轻男性,容易发生肺转移,胸腔积液少见。约10%患者合并血清β'HCG 稍升高[10]。非精原细胞瘤好发于40 岁以下男性或女性,90%患者血清AFP 或β'HCG 水平显著升高,对鉴别诊断具有很大意义[10]。脂肪瘤与脂肪肉瘤内含有脂肪,鉴别比较容易,部分乏脂脂肪肉瘤鉴别也较困难。
此例良性征象较多,也需要与一些良性病变,如胸腺囊肿、胸腺增生等鉴别。胸腺囊肿主要呈囊性密度和信号,虽然有时由于蛋白含量较高而类似实性病灶,但增强后不会强化。胸腺增生包括真性增生、滤泡型增生与淋巴上皮涎腺炎样增生三种类型。大部分胸腺增生影像表现为弥漫性对称性增大,部分表现为结节状或体积较大肿块与肿瘤鉴别困难,MR 化学位移技术可以鉴别,原理是非肿瘤性胸腺组织内散在分布微脂肪[10]。
综上所述,ThC 发病率低,好发于中年男性,多以偶然发现或不典型症状就诊,影像表现为实性肿块,可发生囊变坏死,增强后轻中度强化,部分病例内可见线状或隔膜样强化。肿块较小时与低风险胸腺瘤难鉴别,良性征象较多;肿块较大时与高风险胸腺瘤或胸腺癌难鉴别,侵袭性征象较多。值得注意的是,在诊断前纵隔肿瘤时,除了典型生殖细胞瘤和典型淋巴瘤,需想到ThC,建议患者进一步检查神经内分泌指标;同样,遇到Cushing 综合征、MEN'I型或其他神经内分泌异常的患者需排除胸腺ThC。