新型鸭坦布苏病毒病亚单位疫苗安全性评价
2021-11-10王善辉
王善辉
(江苏省徐州生物工程职业技术学院动物工程学院,江苏 徐州 221006)
鸭坦布苏病毒病是由鸭坦布苏病毒(Duck tem⁃busu virus,DTMUV)引起的鸭出血性卵巢炎[1,2]。自2010年4月在我国发生以来,迅速传播到河北、山东、江苏、安徽、浙江、福建等省份,给我国鸭养殖业带来严重的经济损失。临床主要表现为雏鸭神经症状甚至死亡,产蛋鸭产蛋率急剧下降等,产蛋率可从90%迅速下降至10%,甚至停产[3]。发病率为60%~100%,死亡率为5%~30%[4]。剖检可见卵巢变性、萎缩,主要病变特征是雏鸭肝脏有白色针尖状坏死灶等[5]。DTMUV属于黄病毒科、黄病毒属、恩塔亚病毒群成员,病毒基因组为长约10 990 nt的单股正链RNA,编码3个结构蛋白和7个非结构蛋白[6]。其中,E蛋白具有良好的免疫原性,是鸭坦布苏病毒的主要保护性抗原。其表面存在大量的抗原表位,可诱导机体产生中和抗体[7]。
疫苗免疫是预防该病流行、传播的有效手段。新型鸭坦布苏亚单位疫苗研制项目组前期预测并合成DTMUV的E基因的融合表位蛋白(TBE),采用杆状病毒表达系统表达了该融合表位蛋白,研制出一种新型鸭坦布苏病毒病重组亚单位疫苗[8]。为探明该重组亚单位疫苗的安全性和保护性,本试验将3批次实验室疫苗制品分别以高、中、低剂量组免疫7日龄雏鸭;并以高剂量免疫200日龄产蛋鸭。通过对免疫鸭食欲、精神状态、注射部位观察及体重增加情况的监测及对产蛋鸭的产蛋量与孵化率进行统计以评价疫苗的安全性,攻毒保护试验评价疫苗的保护性,旨在为疫苗进一步扩大临床试验打下基础。
1 材料与方法
1.1 疫苗、毒株及动物
按照王善辉等[9]提供的方法在实验室制备3批次的DTMUV病重组亚单位疫苗,批号分别为20201020、20201110、20201120。DTMUV病商品活疫苗(WF100株)购自齐鲁动物保健品有限公司;DTMUV JSXZ株由徐州生物工程职业技术学院动物工程学院微生物学实验室分离保存;SPF鸡胚购自济南赛斯家禽科技有限公司;樱桃谷雏鸭、产蛋鸭购自徐州市睢宁县某养鸭场,经检测不含抗DTMUV的母源抗体。
1.2 分组及免疫
1.2.1 雏鸭免疫将550只7日龄樱桃谷雏鸭随机分成11组,50只/组,其中1~9组分别为高、中、低剂量的重组亚单位疫苗免疫组,第10组为商品活疫苗(WF100株)免疫组,第11组为非免疫对照组,注射磷酸盐缓冲液1.5 mL/只。重组亚单位疫苗免疫组经颈部肌肉注射疫苗,1、4、7组免疫0.5 mL/只,2、5、8组免疫1.0 mL/只,3、6、9组免疫1.5 mL/只。商品疫苗组肌肉注射(0.5 mL/只)。首免2周后加强免疫。相同条件下,将各组鸭分开隔离饲养。

表1 分组及免疫剂量
1.2.2 产蛋鸭免疫200日龄樱桃谷产蛋鸭250只,随机均分成5组,50只/组,其中1~3组为重组亚单位疫苗免疫组,分别注射3批疫苗,1.5 mL/只;第4组为商品活疫苗免疫组,第5组为非免疫对照组,各组鸭分开隔离饲养。
1.3 安全性检测
1.3.1 雏鸭全身及注射部位反应免疫后观察1~3周雏鸭的精神状态与采食情况。各免疫组及对照组随机取5只免疫鸭,剖检观察疫苗吸收情况,即疫苗注射部位是否有疫苗颗粒,是否出现红肿、出血及炎性渗出等病变。免疫后28 d每组分别随机抽取20只免疫鸭及非免鸭称重,比较其对增重的影响。
1.3.2 产蛋鸭产蛋量与孵化率记录产蛋鸭免疫后30 d内的产蛋数量,并进行标记。比较免疫鸭与非免疫种鸭同期产蛋数。从产蛋鸭免疫后4~6 d内每组随机抽取80枚入孵蛋,统计孵化率。
1.4 雏鸭免疫攻毒保护试验
首免后28 d,于免疫组随机抽取10只鸭,肌肉注射200 U/只(1ELD50病毒量为1 U)的DTMUV JSXZ株。分离血清用于病毒分离。经卵黄囊途径接种6日龄SPF鸡胚,每胚0.1 mL。24~72 h死亡的鸡胚按照王永娟等[10]建立的方法,通过RT-PCR法检测E基因,阳性胚判为DTMUV感染死亡鸡胚。只要有1枚鸡胚感染,即判定这只鸭病毒分离阳性,为发病鸭。记录发病鸭数量,并计算各组疫苗的保护率。
2 结果与分析
2.1 雏鸭食欲、精神状况及注射部位观察
首次免疫后连续观察21 d,免疫雏鸭与非免疫鸭采食、精神状况均正常,未见任何全身不良反应。检查免疫鸭注射部位(每组随机取出5只鸭),所有免疫鸭均未见局部出血、渗出、水肿及肉芽肿块或肿胀等病变。剖检可见高剂量组个别免疫鸭在注射部位有少量微小疫苗颗粒存在,其余鸭对疫苗全部吸收良好。
2.2 雏鸭体重增长情况
由表2可见,首免后28 d时,3批次疫苗的高、中、低剂量组免疫鸭和非免疫鸭的体重无明显差异,重组亚单位疫苗免疫没有影响雏鸭体重。

表2 首免后28 d各组鸭平均体重
2.3 产蛋鸭的产蛋量与孵化率
产蛋鸭免疫后,每天统计各组鸭产蛋数量,连续统计30 d。结果(表3)显示,产蛋量在免疫后第4天开始下降,下降2~3个百分点,然后逐渐恢复,到第10天已经基本恢复到同组鸭免疫前的产蛋率。且在种鸭免疫后4~6 d内每组随机抽取80枚入孵蛋,统计孵化率,经比较免疫组与对照组无明显差异。说明疫苗对免疫后30 d内产蛋鸭的产蛋率和免疫后4~6 d入孵蛋的孵化率无明显影响。

表3 免疫种鸭的产蛋及孵化情况
2.4 攻毒保护试验
雏鸭在首免后28 d攻毒,观察15 d。非免疫组10只鸭均出现明显的食欲不振、排绿色粪便、后期则出现瘫痪等症状,其中4只死亡。剖检显示病鸭肝脏、脾脏、腺胃、脑膜有出血、坏死等病变;商品活疫苗免疫组10只鸭未出现临床症状,保护率为100%。1、4、7组分别有3只鸭出现食欲不振、排绿色粪便等轻微症状,15 d后症状基本消失,其保护率均为70%;低剂量免疫组和非免疫组所有发病鸭体内都分离到DTMUV。中、高剂量重组疫苗免疫组鸭未出现临床症状,剖检未见异常,均未分离到DTMUV,保护率均为100%。结果表明,3个批次的重组亚单位疫苗都能够很好地保护免疫雏鸭免受DTMUV的攻击,达到与商品活疫苗相同的保护效果(表4)。
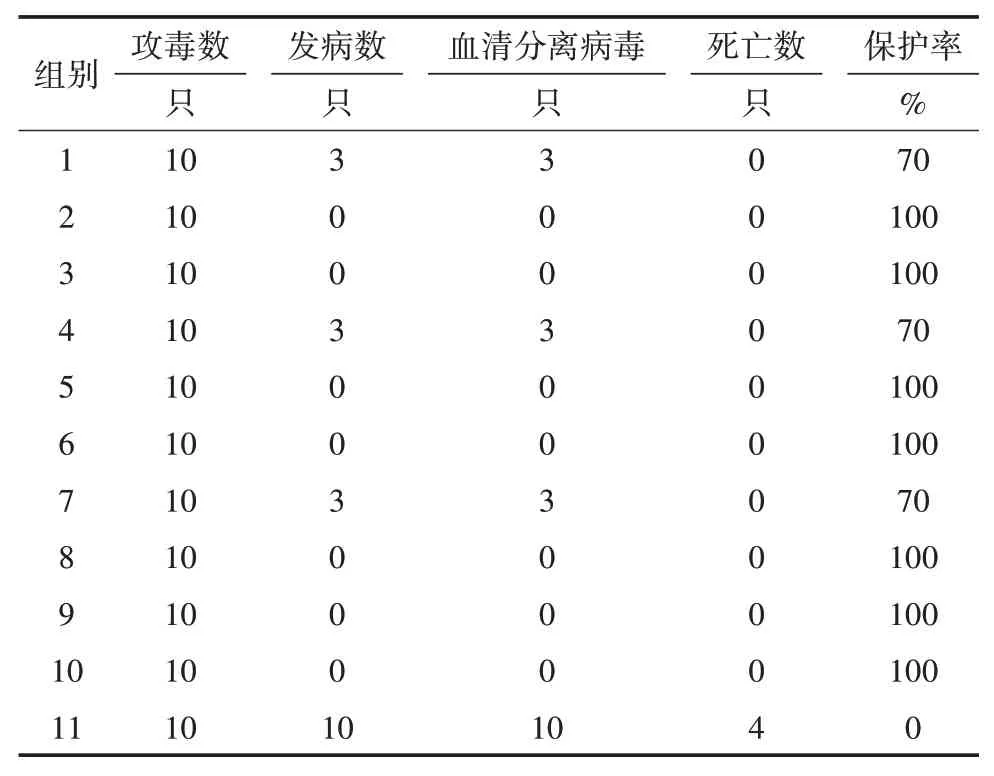
表4 雏鸭免疫后DTMUV攻毒试验结果
3 小结与讨论
为检测新型鸭坦布苏亚单位疫苗研制项目组前期研制的鸭坦布苏病毒病重组亚单位疫苗的安全性,试验将3个批次的实验室疫苗制品按高、中、低3个剂量组分别免疫9组7日龄雏鸭,设商品活疫苗对照组及非免疫对照组。通过观察免疫鸭食欲、精神状态、注射部位病变及体重增加情况来评价疫苗的安全性。
安全性试验结果显示,免疫鸭食欲、精神状态均正常,注射部位未见明显病变,体重增长情况与非免疫组鸭一致。产蛋鸭免疫后,每天统计各组鸭产蛋数量,连续统计30 d,结果显示,产蛋量在免疫后第4天开始下降,下降2~3个百分点,然后逐渐恢复,到第10天已经基本恢复到同组鸭免疫前的产蛋率。在种鸭免疫后4~6 d内每组随机抽取80枚入孵蛋,统计孵化率,结果发现免疫组与对照组无明显差异,说明疫苗对免疫后30 d内产蛋鸭的产蛋率和免疫后4~6 d入孵蛋的孵化率无明显影响。
攻毒保护试验结果显示,低剂量组保护率为70%,中、高剂量组与商品活疫苗组的保护率均为100%,非免疫对照组雏鸭均表现为典型的DTMUV感染症状,其中4只死亡。说明重组亚单位疫苗能够很好地保护免疫鸭免受DTMUV的攻击,达到与商品活疫苗相同的保护效果。以上结果表明,该重组亚单位疫苗具有良好安全性及保护性。本研究为该疫苗的进一步扩大临床试验及推广应用打下了一定的基础。
