乙酸乙酯合成条件的优化研究
2021-11-09李学章
*李学章
(云南工贸职业技术学院 云南 650300)
乙酸乙酯是一种用途广泛的精细化工产品,具有优异的溶解性、快干性,广泛用于涂料、合成橡胶、粘合剂、乙基纤维素等生产过程中。也是制药工业和有机合成的重要原料,因此对于乙酸乙酯产率的研究方案尤为重要。目前合成乙酸乙酯的方法[1]主要有直接酯化法(原料为醋酸和乙醇,浓硫酸为催化剂直接酯化,再经中和、水洗、除杂、干燥、蒸馏得到成品)、乙醛缩合法(催化剂为烷基铝,用乙醛缩合反应生成醋酸乙酯)、加成反应法(乙烯与醋酸催化作用下,发生加成反应而生成醋酸乙酯)、氧化制取法(丁烷氧化制取乙酸时副产乙酸乙酯)。
1.实验原理

此反应是可逆的,为了有利于乙酸乙酯的生成,实验合成中采用了无水乙醇过量的方法,使反应向生成酯的方向进行,即使反应向右进行[2]。
2.实验仪器与药品
仪器:标准回流装置1套、标准蒸馏装置1套、DZTW型电子调温电热套、2WAJ阿贝折射仪。
药品:实验所用试剂均为化学纯。
3.实验方法
在三颈烧瓶中,加入5mL无水乙醇,再慢慢加入一定体积的浓硫酸,使其混合均匀,并加入几颗沸石。三颈瓶一侧口插入温度计,另一侧口插入滴液漏斗,中间口安装一蒸馏装置。在滴液漏斗中加入15mL无水乙醇和10mL冰醋酸,混合均匀。用电热套加热,当温度升至100℃左右,自滴液漏斗慢慢滴入其余的混合液,维持反应温度在110~125℃之间。滴加完毕后,继续加热,直至温度升高到130℃不再有馏出液为止。
慢慢向粗产品中加入饱和碳酸钠溶液至无二氧化碳气体放出,酯层用pH试纸检验呈中性。移入分液漏斗中,充分振摇后静置,分去下层水相。酯层用饱和食盐水洗涤,静置分层,分出水层。再用饱和氯化钙溶液洗涤两次,弃去下层水相,酯层倒入干燥的锥形瓶中,用无水碳酸钾干燥10~ 20min。将干燥好的粗乙酸乙酯通过漏斗(滤纸过滤)滤入蒸馏瓶中,加入几粒沸石,加热进行蒸馏。收集73℃~80℃的乙酸乙酯馏分,记录精制乙酸乙酯的产量。根据称量产品的质量,计算产品的收率。
用阿贝折光仪测定所得乙酸乙酯的折光率,并换算到20℃时的折光率(文献值:)。折光率平行测定三次。不同温度下折光率的转换公式:

4.实验结果与讨论
(1)醇酸用量对产品收率及纯度的影响
当浓硫酸用量为7mL、无水乙醇用量为20mL,反应时间为80min时,改变冰醋酸的用量,结果表明冰醋酸用量为10mL时产品收率最高,纯度也很高。结果见表1。
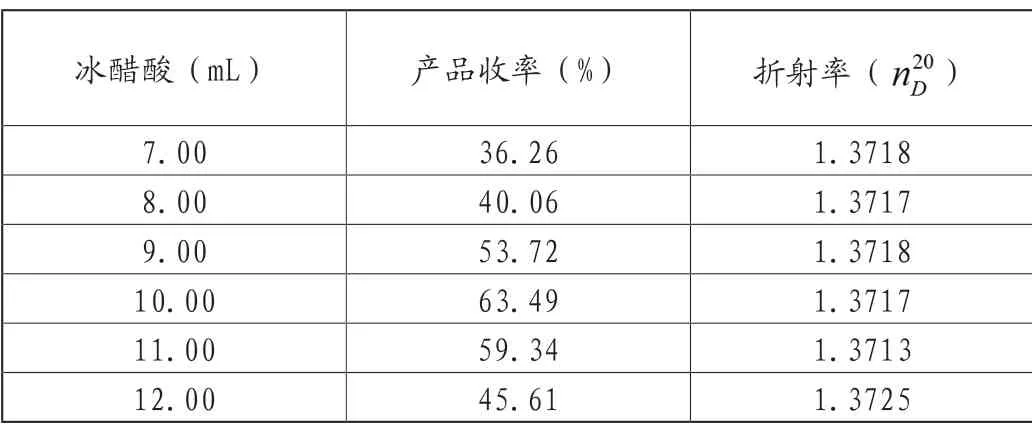
表1 醇酸用量对产品收率及纯度的影响
(2)不同催化剂对产率及纯度的影响
当无水乙醇用量为20mL、冰醋酸用量为10mL,反应时间为80min时,分别使用了浓硫酸、硫酸铁、氯化铁作为催化剂,结果表明使用浓硫酸时产品的收率最高,达到了63.49%,纯度也很高。结果见表2。
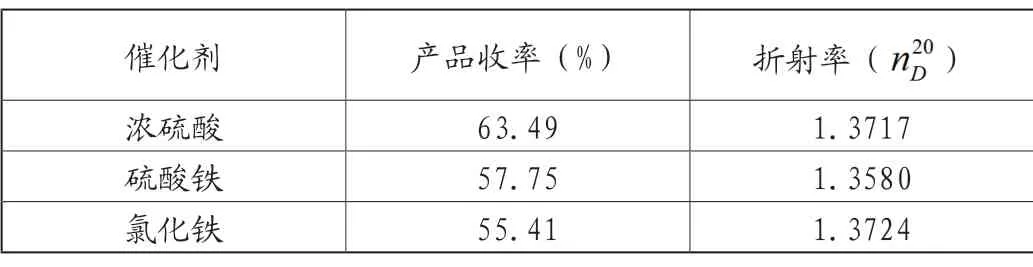
表2 不同催化剂对产品收率及纯度的影响
(3)催化剂用量对产率及纯度的影响
合成中发现,催化剂的用量太多或是太少都会使化学反应速率减慢而影响酯化率,用量太多时会发生碳化现象,产生很多的副产物而降低产率。固定反应物的用量,反应时间仍为80min,改变了浓硫酸的用量,对合成乙酸乙酯的产率及纯度进行试验,结果表明浓硫酸的用量为2.00mL时产品的收率和纯度最高。结果见表3。

表3 催化剂用量对产品收率及纯度的影响
(4)不同干燥剂对产率及纯度的影响
固定反应物的用量,使用2mL的浓硫酸作为催化剂,反应时间仍为80min,分别使用无水碳酸钾、无水硫酸镁、无水硫酸钠作为干燥剂,并改变它们的用量,对合成乙酸乙酯的产率及纯度进行试验,结果表明使用无水碳酸钾时产品的收率和纯度最高。结果见表4。

表4 不同干燥剂对产品收率及纯度的影响
(5)反应时间对产率及纯度的影响
固定反应物的用量,使用2mL的浓硫酸作为催化剂,选择无水碳酸钾作为干燥剂,合成过程中对反应时间进行了试验,结果表明反应时间为80min左右时产品的收率和纯度最高。结果见表5。

表5 反应时间对产品收率及纯度的影响
(6)反应温度对产率及纯度的影响
固定反应物的用量,使用2mL的浓硫酸作为催化剂,选择无水碳酸钾作为干燥剂,反应时间控制在80min左右,合成过程中对反应温度进行了试验,结果表明反应温度为90℃左右时产品的收率和纯度最高。结果见表6。

表6 反应温度对产品收率及纯度的影响
温度控制可以说是这个实验能否成功的关键,当温度达到170℃时,在浓硫酸催化作用下乙醇会生成乙烯,当温度达到140℃时,乙醇会产生乙醚。在不同温度下生成的副产物都不一样,所以在实验过程中一定要控制好实验反应的温度,以免产生很多的副产物而影响产品的产率及纯度。
(7)其他因素对产率及纯度的影响
①可选用硫酸氢钠代替浓硫酸从而减少对环境的污染,同时避免副产物的产生,符合绿色化学的理念。②通过向反应装置中加入干燥剂而使反应不断地向正反应方向进行,使得乙酸乙酯的产率升高。③饱和碳酸钠起到溶解乙醇、吸收乙酸、减小乙酸乙酯溶解度的作用。④加入药品时先加乙醇,再加浓硫酸,最后加冰醋酸。由于浓硫酸溶于乙醇或冰醋酸都会放出大量的热,使液体发生飞溅,所以不宜先加入浓硫酸再加其它物质。浓硫酸不宜最后滴加,以免在滴加浓硫酸的过程中乙酸与乙醇过早发生反应。
5.产品分析
乙酸乙酯为无色无味的、具有水果香味的易燃液体,沸点73℃~80℃(文献值77.06℃),折光率为(文献值为1.3720)。
6.结论
综上所述,大量实验结果显示乙酸乙酯合成反应的最佳条件为:无水乙醇20mL、冰乙酸10mL、浓硫酸2mL、反应时间为80min左右、反应温度控制在90℃左右、干燥剂选择无水碳酸钾时的产率和纯度是最高的。因为乙醇在市场上属于容易得到的原料,价格也比较便宜,故本次实验主要选择了无水乙醇过量的办法,而浓硫酸属于危险化学品,在实验中接触到是很危险的,且副产物多,所以我们将浓硫酸的用量降到了最小,不仅提高了产率,还节约了原料试剂,减少了污染也提高了产品质量。
