碱激发矿渣净浆对氯离子的固化作用
2021-11-08万小梅孙忠涛
万小梅,韩 笑,于 琦,王 腾,孙忠涛
(1.青岛理工大学 土木工程学院,山东 青岛 266033;2.青岛理工大学蓝色经济区工程建设与安全山东省协同创新中心,山东 青岛 266033)
土木工程领域中,氯盐侵入引起的钢筋锈蚀是导致混凝土结构耐久性劣化乃至失效的重要原因之一.引起钢筋锈蚀的并非只有进入混凝土内部的氯离子[1],还包括孔溶液中的自由氯离子.硬化浆体对氯离子的固化作用能够降低孔溶液中的自由氯离子浓度,对缓解钢筋锈蚀有一定作用.研究表明[2‑5],当氯离子侵入普通混凝土内部后,与单硫型水化硫铝酸钙(AFm)结合形成Friedel盐和Kuzel盐,并被水化硅酸钙(C‑S‑H)凝胶通过范德华力吸附到其表面.Diamond[6]认为C‑S‑H凝胶对氯离子的吸附能有效降低自由氯离子含量.Ramachandran[7]通过研究CaCl2与C3S水化物的作用机理,发现氯离子不仅存在于C‑S‑H凝胶的吸附层上,还可以渗透到C‑S‑H凝胶的层间孔隙,并被固化在C‑S‑H凝胶的微晶点阵中.
碱激发矿渣(AAS)是一种由碱性物质激发高炉矿渣而制成的绿色胶凝材料,其氯离子固化能力受到学者的关注.AAS主要水化产物为含铝相的C‑S‑H(C‑A‑S‑H),其次是微纳米级水滑石(也被称为Mg‑Al层状双氢氧化物)和AFm型相混合物[8‑10].AAS固化氯离子的性能受多因素影响,如矿渣化学矿物成分,激发剂种类、浓度,反应温度和碱度等[11].Ravikumar等[12]试验发现,碱矿渣水化产物的含量与矿渣含量成正比.除了C‑S‑H之外,作为碱矿渣最主要的水化产物之一,C‑A‑S‑H是由Al取代C‑S‑H桥接位上的Si所产生的铝硅酸盐空间结构产物.万小梅等[13]对合成的C‑A‑S‑H氯离子固化性能进行研究后发现,其所固化的氯离子量随着钙硅比的增大先增大后减小,对氯离子固化能力存在最优钙硅比.除了矿渣本身及其水化产物的影响,Dhir等[14]还在研究中发现,随着外界环境中氯离子浓度的增加,AAS中的固化氯离子和自由氯离子含量会显著提高.另外,浸泡液pH值也会影响AAS固化氯离子的性能,Tritthart[15]认为浸泡液的高pH值会抑制水泥基材 料固化氯离子的能力.
碱激发矿渣混凝土固化氯离子规律及其对氯离子传输性能影响效应的研究仍有较大空间.为此,本文研究了在不同激发剂种类和碱当量(质量分数,文中涉及的当量、含量等均为质量分数)、氯盐浸泡液pH值条件下AAS净浆氯离子固化能力的变化规律.通过X射线衍射(XRD)、热分析(TGA‑DSC)、扫描电镜(SEM),研究了氯盐浸泡前后AAS净浆的水化产物种类以及微观形貌,以期更深入地探究AAS净浆对氯离子的固化行为及其机理.
1 试验
1.1 原材料和试件制备
矿渣为青岛中矿宏远工贸有限公司提供的S95矿渣,颜色为灰白色;水泥为山东山铝水泥有限公司产P·I 42.5普通硅酸盐水泥;NaOH采用上海埃彼化学试剂有限公司产分析纯,含量≥96%,外观为白色结晶片状;水玻璃原液来自临沂绿森化工有限公司,外观为透明黏稠液体,模数3.2~3.4,制备试件时将水玻璃模数调配至1.8;用于配制氯盐浸泡液的NaCl来自上海埃彼化学试剂有限公司,分析纯,含量≥96%;试验用水均采用去离子水.胶凝材料的化学组成见表1.

表1 胶凝材料的化学组成Table 1 Chemical compositions of binding materials
考虑激发剂种类(NaOH和水玻璃)和碱当量的影响,共设计6种配合比的AAS净浆试件,另外还制备了1组普通硅酸盐水泥净浆试件,用于对比.各试件尺寸均为40 mm×40 mm×160 mm,其配合比见表2.

表2 试件配合比Table 2 Mix proportion of specimens
1.2 试验方法
试件脱模后,放入(20±1)℃的去离子水中养护28 d;取出破碎后,取样置于无水乙醇中浸泡3 d;之后放入干燥箱中以65℃真空烘干至恒重,终止试样水化并防止碳化发生;再将烘干好的样品在手套箱中磨粉过74μm筛,放入密封袋中干燥保存,分别用于氯盐溶液浸泡和微观测试.
采用平衡法原理试验评价试样的氯离子固化量.氯盐浸泡液选用浓度为1 mol/L的NaCl溶液.首先用NaOH将氯盐浸泡液的pH值分别调节为11.0、11.5、12.0、12.5、13.0和13.5,并用pH计测量确定;然后将3 g待测粉末样品置于40 mL的NaCl溶液中浸泡14 d;最后提取250μL上清液,稀释100倍后,采用ICS‑1500离子色谱仪测量其氯离子浓度,以确定试样对氯离子的固化量.每组数据为3个平行样结果的平均值.随后过滤粉末样品,真空烘干,密封保存以备微观测试.
将氯盐浸泡前后的AAS粉末在65℃下真空干燥48 h,采用XRD技术分析氯盐浸泡前后AAS的晶相变化.粉末样品在10°~70°内连续扫描,扫描步宽为0.02°,扫描速度为0.02(°)/s.
采用美国TA公司产SC‑TGA Q600同步热分析仪测试氯盐浸泡前后AAS粉末的TGA‑DSC曲线.取8 mg左右的粉末置于陶瓷坩埚中,进行热分析测试.升温区间为室温~800°C,加热速率为10°C/min,氮气作为保护气,其流量为20 mL/min.
采用日立S‑3500N型SEM,结合能谱仪研究氯盐浸泡对AAS形貌的影响.先将样品粉末用导电胶粘到铜片上,并用真空镀膜仪对其进行镀膜处理,使之具有导电性,然后开机观察.能谱分析(EDS)采用面扫描方式.
2 碱激发矿渣的氯离子固化能力
图1为AAS净浆氯离子固化量与氯盐浸泡液pH值之间的关系.由图1可见:(1)当氯盐浸泡液pH值为11.0~13.5时,AAS净浆的氯离子固化量随pH值增加呈线性减小趋势.(2)NaOH激发矿渣(NAS)净浆的氯离子固化量减少30%~71%,水玻璃激发矿渣(WAS)净浆的氯离子固化量减少21%~45%.(3)PC净浆的氯离子固化能力随氯盐浸泡液pH值的变化规律与AAS净浆一致,但总体低于AAS净浆.AAS固化氯离子的能力之所以会随着氯盐浸泡液pH值的增加而减弱,是由于游离氯离子能置换出水化产物内层的OH-[16],但如果溶液中pH值较高(即OH-浓度高),该离子置换作用将变得相对困难,所固化的氯离子量会减少.同样pH值下,WAS净浆的氯离子固化量高于NAS净浆是因为作为激发剂的水玻璃为矿渣提供了[SiO4]4-,使之水化生成更多的凝胶体用来吸附氯离子;另外,WAS聚合度较高[17],对氯离子的滞留能力更强.

图1 AAS净浆氯离子固化量与氯盐浸泡液pH值之间的关系Fig.1 Relationship between chloride binding amount of AAS pastes and pH value of chloride immersion solution
图2为AAS净浆及PC净浆氯离子固化量的比较.由图2可见:(1)当氯盐浸泡液pH值为11.0~13.5时,除碱当量最低的N1、W1之外,AAS净浆固化氯离子的能力普遍高于相同胶凝材料量的PC净浆.(2)相同碱当量条件下,WAS净浆的氯离子固化量普遍大于NAS净浆.(3)随着碱当量的提高,2类AAS净浆固化氯离子的能力均得以增强.但有研究表明[18],碱当量对AAS固化氯离子的能力还受到浸泡液氯离子浓度的影响,氯离子浓度过高(≥3.4 mol/L)或过低(≤0.36 mol/L)均不遵循此规律.
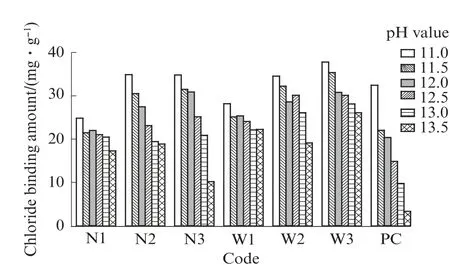
图2 各AAS净浆及PC净浆的氯离子固化量Fig.2 Chloride binding amount of AAS pastes and PC pastes
3 水化产物分析
3.1 XRD分析
图3为NAS、WAS和PC净浆经氯盐溶液浸泡14 d前后的XRD图谱.由图3可见:相比PC净浆,由于AAS净浆中没有Ca(OH)2,衍射峰明显较少,其主要水化产物C‑S‑H和C‑A‑S‑H的峰型主要为宽峰,且峰值较弱.虽然PC水化后XRD图谱中衍射峰数目较多,但其主要水化产物C‑S‑H凝胶在XRD图谱中难以体现,说明PC水化产物中除了C‑S‑H,其他水化产物结晶度相对较高.Ye等[19]研究发现,AAS的主要水化产物为C‑S‑H和水滑石.也有研究认为,AAS水化产物里存在非晶态的AFm相,且与C‑S‑H凝胶的峰存在重叠,因此无法通过XRD图谱区分出来[9].激发剂种类的不同导致体系中的阴离子不同,因而水化产物中水滑石相类的数量、原子结构和化学成分均会有所不同[19].XRD图谱中WAS净浆的峰型、峰数较少,反映出WAS净浆中含有较多的凝胶相,而NAS净浆中的水滑石相峰值高,反映其结晶度更高,因此可推断WAS净浆的物理吸附氯离子能力强于NAS净浆.

图3 NAS、WAS和PC净浆经氯盐溶液浸泡14 d前后的XRD图谱Fig.3 XRD patterns of NAS,WAS and PC pastes before and after 14 d of immersion in chloride solution
由图3还可见:(1)经氯盐溶液浸泡后的AAS和PC净浆衍射峰值显著增强,并且均出现了Friedel盐,但作用机理不同.研究表明[20‑22],在外渗氯离子的条件下,PC中由于未水化铝酸三钙(C3A)或者已水化的C3A相与氯离子发生化学结合生成了Friedel盐;而勾密峰等[16]认为AAS中的Friedel盐是由含铝相水化产物(C‑A‑H)与氯离子发生化学结合而生成的;Birnin‑yauri等[4]认为Friedel盐在AAS中的形成是现有AFm在氯化物暴露时相转变的结果.(2)NAS净浆在氯盐溶液浸泡后产生了Friedel盐,且峰值强度大于WAS净浆.其原因可能是WAS净浆的凝胶态水化产物比NAS净浆的水化产物更多,且大量包裹在其他水化产物的表面,聚合度更高,结构更致密,更易滞留氯离子.因此当氯离子进入矿渣中,首先就会接触到C‑(A)‑S‑H凝胶且被吸附,而来不及与其他物相反应生成Friedel盐.并且由于前述试验结果表明WAS净浆的氯离子固化量高于NAS净浆,由此推测WAS净浆固化氯离子的方式主要为物理吸附作用.结合XRD图谱与氯离子固化曲线可以发现,AAS碱当量提高后,Friedel盐的特征峰强度并没有明显变化规律.因此,推测碱当量变化主要影响的是AAS对氯离子的物理吸附作用,碱当量的提高促使AAS水化生成更多的凝胶产物C‑(A)‑S‑H去吸附氯离子.
3.2 TGA‑DSC分析
图4为AAS(N3、W3)和PC净浆经氯盐溶液浸泡14 d前 后 的TGA‑DSC曲 线.由 图4可 见:22~200℃的吸热峰主要由水化产物C‑S‑H和C‑A‑S‑H脱水产生,在此温度区间内NAS、WAS和PC净浆的质量损失率分别为7.35%、8.67%和7.79%,表明WAS净浆的凝胶水化产物多于NAS净浆.虽然PC净浆的质量损失率大于NAS净浆,但是PC水化产物复杂,该温度范围内吸热失重峰不仅包括C‑S‑H,还有钙矾石(AFt)等其他水化产物,但它们对氯离子结合的贡献微乎其微.史才军[23]认为水玻璃激发矿渣水泥砂浆表现出比硅酸盐水泥砂浆更低的孔隙率和更细小的孔结构,且白云志[24]研究发现碱激发矿渣比硅酸盐水泥更密实.因此,相比AAS净浆,孔隙较大的PC净浆对离子滞留作用较弱,不易结合氯离子.

图4 AAS(N3、W3)和PC净浆的TGA‑DSC曲线Fig.4 TGA‑DSC curves of AAS(N3,W3)and PC pastes
由图4还可知,各试样在230~410℃的质量损失主要为Friedel盐中主层水的质量损失[20].主层水质量损失率可通过TGA曲线中230~410℃暴露于氯盐溶液后的样品失重减去完整参考样品的失重计算得到.根据Friedel盐晶体结构,主层水为6个水分子.因 此,Friedel盐 的 质 量 分 数mFS(%)计 算式[25]为:
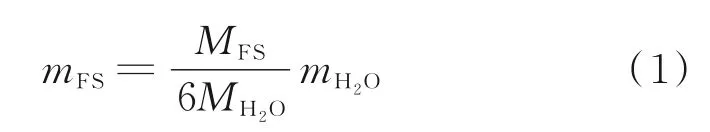
式中:mH2O为主层水在Friedel盐中的质量损失率,%;MFS和MH2O分别为Friedel盐和水的摩尔质量,本文分别取为561.30、18.02 g/mol.
由TGA测定的Friedel盐的质量分数mFS来计算化学结合氯离子量mg/g),其计算式为:

式中:MCl为氯的摩尔质量,本文取为35.45 g/mol;20为Friedel盐中氯的摩尔浓度(2 mol Cl/1 mol Frie‑del’s salt)、mFS与单位转换的影响因数.
C‑(A)‑S‑H凝 胶 物 理 吸 附 氯 离 子 量(mg/g)可通过从固化氯离子总量Cb减去化学结合氯离子量来计算:

图5为浸泡14 d时暴露于NaCl溶液中的NAS、WAS、PC物理吸附与化学结合氯离子量.养护28 d的NAS、WAS、PC对氯离子的固化作用中物理吸附作用均占50%以上,这可能是由于水化产物基本水化完毕,不易再与氯离子发生固化所致.水玻璃激发的矿渣物理吸附作用占比最大,这与水玻璃激发矿渣中存在大量凝胶性产物有关.
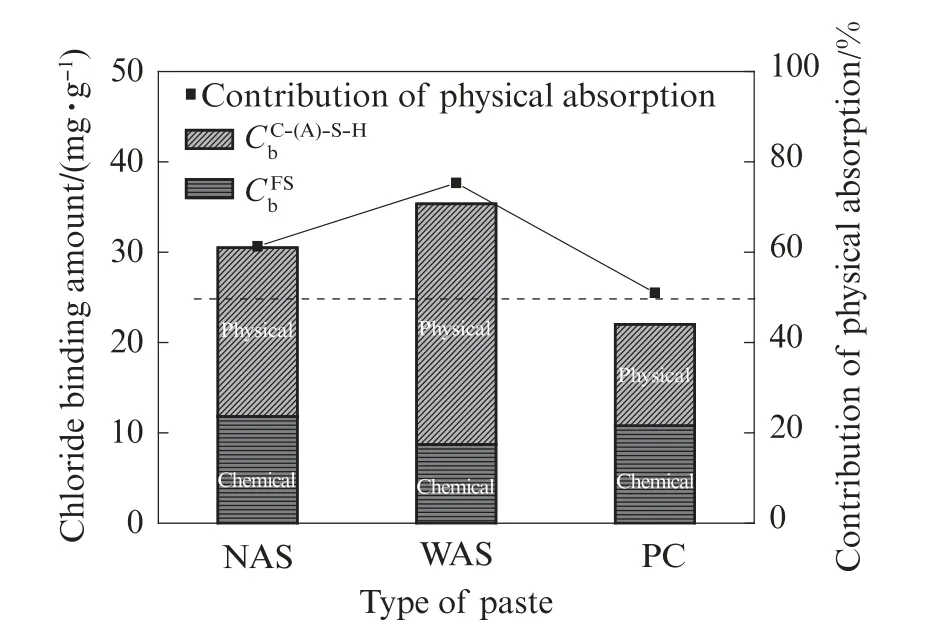
图5 NAS、WAS和PC净浆的物理吸附和化学结合氯离子量Fig.5 Physical adsorption and chemical binding chloride amount of NAS,WAS and PC pastes
3.3 SEM‑EDS分析
图6、7分别为NAS和WAS净浆在氯盐溶液中浸泡14 d前后的SEM‑EDS分析对比图.由图6可见:在300倍放大条件下,浸泡后NAS(N3‑2)由原来的有棱角颗粒变为较圆润颗粒;放大30 000倍后,NAS由浸泡前(N3‑1)的无数个堆簇而成的小圆球颗粒变为浸泡后的褶皱状形貌,且存在少量圆球颗粒状堆积.图7中的WAS在氯盐溶液浸泡前后也出现了与NAS相同的形貌变化.表3为EDS元素含量比例.表3显示:N3‑1的n(Si)/n(Ca)小于W3‑1,说明WAS的聚合度大于NAS.浸泡后WAS和PC的n(Si)/n(Ca)减小,说明氯盐溶液浸泡后凝胶体聚合程度变低.而浸泡后NAS的n(Si)/n(Ca)和n(Al)/n(Ca)普遍增大,可能是Ca2+从NAS中浸出到NaOH/NaCl溶液中导致的.

图6 NAS净浆在氯盐溶液中浸泡前后的SEM‑EDS分析Fig.6 SEM‑EDS analysis of NAS pastes before and after immersion in chloride solution

图7 WAS净浆在氯盐溶液中浸泡前后的SEM‑EDS分析Fig.7 SEM‑EDS analysis of WAS pastes before and after immersion in chloride solution

表3 EDS元素含量比例Table 3 Ratio of element content from EDS
由表3可以发现,氯盐溶液浸泡后的PC、NAS和WAS净浆的Cl/Al逐渐增大,说明氯离子固化能力PC<NAS<WAS.图8为经氯盐浸泡后AAS中Friedel盐的SEM照片.
图8为经氯盐溶液浸泡后AAS中Friedel盐的SEM照片.由图8可见:氯盐溶液中的AAS生成了六方片状结晶产物,但由于凝胶体的生成速率和数量要优于结晶体,因此其外表面被胶凝体包裹.结合XRD分析可知矿渣中没有Ca(OH)2晶体,且蔡跃波等[26]拍摄到的Friedel盐形貌为六方片状,因此推测图8中的六方片状晶体为Friedel盐.这也进一步证明了AAS对氯离子固化作用不仅包括物理吸附作用,还包括少量化学结合作用,并且产生了新物质Friedel盐.

图8 经氯盐溶液浸泡后AAS中Friedel盐的SEM照片Fig.8 SEM photos of Friedel’s salt in AAS after chloride solution immersion
4 结论
(1)在氯盐浸泡液pH值为11.0~13.5时,AAS净浆对氯离子的固化能力随着氯盐浸泡液pH值的增大而降低.AAS净浆所固化的氯离子量普遍高于PC净浆.其中WAS净浆固化氯离子的能力大于NAS.
(2)NAS、WAS和PC净浆对氯离子的固化作用中物理吸附作用均占50 %以上,其中,WAS的化学结合氯离子量最少,物理吸附氯离子量最多.
(3)经氯盐溶液浸泡后,AAS与氯离子反应生成一部分Friedel盐.AAS净浆对氯离子的固化作用不仅包括物理吸附作用,还包括少量化学结合作用.
