HPLC法测定蒲黄镇痛活性提取物的含量
2021-11-08唐倩男谢云秀王晋思胡圳春吴昭全
唐倩男,谢云秀,王晋思,胡圳春,吴昭全
(长沙医学院,湖南长沙 410219)
蒲黄为香蒲科植物水烛香蒲(Typha angustifoliaL.)、东方香蒲(Typha orientalisPresl)或同属植物的干燥花粉[1],具有促进体内循环和降低血脂进而阻止高脂血症所致的血管内皮损伤,防止动脉粥样硬化等作用[2-3]。《本草纲目》中记载,蒲黄有消瘀活血、止痛止血等功效,目前在蒲黄祛瘀止血方面有较多的
报道,对止痛效果研究较少。曾光尧等[4]研究证明,蒲黄95%乙醇提取物具有很强的镇痛活性,将蒲黄具有镇痛作用的成分先经大孔树脂再经聚酰胺柱分离纯化,发现香蒲新苷为其主要镇痛成分,但并未对其镇痛活性的质量进行评价。因此,本实验建立了HPLC法测定蒲黄中95%乙醇提取物中镇痛成分香蒲新苷的含量,并对其进行质量分析。
1 材料与方法
1.1 仪器
P1100型HPLC高效液相色谱仪,大连依利特分析仪器有限公司;D1100紫外-可见检测器,大连依利特分析仪器有限公司;YP6002B电子天平,上海力辰邦西仪器科技有限公司;KQ-300E型超声波清洗器,昆山市超声仪器有限公司;力辰牌C30型玻璃仪器气流烘干器,邦西仪器科技(上海)有限公司;AL204型电子天平,梅特勒-托利多仪器(上海)有限公司;YRE-52C旋转蒸发器,巩义予华仪器有限责任公司;DF-101S集热式恒温加热磁力搅拌器,巩义予华仪器有限责任公司;101-2BS型热风循环烘箱,邦西仪器科技(上海)有限公司;SHZ-D(Ⅲ)型循环水真空泵,邦西仪器科技(上海)有限公司。
1.2 试剂
香蒲新苷标准品,批号wkq19111107,四川省维克奇生物科技有限公司;蒲黄粉末,四川湘起之秀中药材有限公司;甲醇,色谱纯,天津欧博凯化工有限公司;乙腈,色谱纯,国药集团化学试剂有限公司;蒸馏水,广州屈臣氏食品有限公司;95%乙醇,分析纯,天津欧博凯化工有限公司;磷酸,分析纯,天津市恒兴化学试剂制造有限公司。
1.3 实验方法
1.3.1 蒲黄镇痛提取物
称取50.18 g蒲黄粉末,置于1 000 mL的圆底烧瓶中。分次加入400 mL的95%乙醇,超声回流提取3次,合并蒲黄提取液,浓缩烘干得到蒲黄提取物浸膏,重量为14.95 g。
1.3.2 溶液制备
(1)供试品溶液。精密称定蒲黄浸膏约0.5 g,置50 mL棕色容量瓶中,加入甲醇溶解,超声10 min,放冷,定容,摇匀,经0.45 μm微孔滤膜过滤后备用。
(2)对照品溶液。精密称取香蒲新苷对照品适量,置于100 mL容量瓶中,加入甲醇超声溶解,放冷,定容,摇匀,配制成100 μg/mL的香蒲新苷对照品溶液,经0.45 μm微孔滤膜过滤后备用。
1.3.3 色谱条件
取“1.3.2”项下供试品溶液和对照品溶液适量,分别采用HPLC-UVD法测定。色谱条件:色谱柱Amethyst C18-H(4.6 mm×250 mm,5 μm),流 动相为乙腈-0.05%磷酸(15∶85),UVD检测波长254 nm,流速 1.0 mL/min,柱温 25 ℃,进样量 20 μL。色谱图如图1所示。
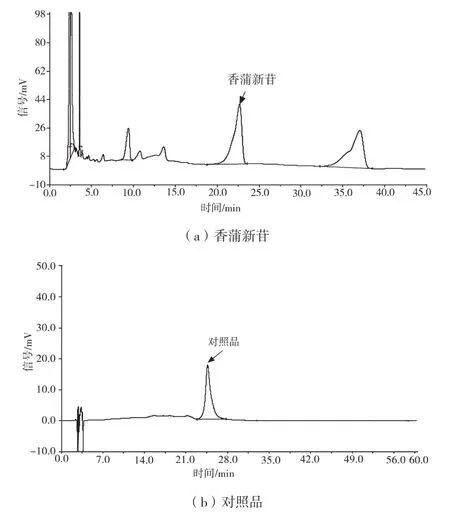
图1 蒲黄提取物中香蒲新苷的HPLC图
1.3.4 方法学考察
(1)线性关系的考察。取“1.3.2”项下制备的对照品溶液,精密吸取2 mL、4 mL、6 mL、8 mL和10 mL放置10 mL棕色容量瓶里,用甲醇定容,分别制成 20 μg/mL、40 μg/mL、60 μg/mL、80 μg/mL和100 μg/mL一系列梯度浓度的香蒲新苷对照品溶液。按照“1.3.3”项下色谱条件分别进样20 μL,记录相关峰面积。以浓度为横坐标(X),峰面积为纵坐标(Y),进行线性回归。
(2)稳定性考察。取“1.3.2”项下制备的供试品溶液适量,常温下放置,并且按照“1.3.3”项下色谱条件分别在0 h、2 h、4 h、6 h、8 h和12 h进样测定,记录色谱峰面积,考察溶液稳定性。
(3)精密度考察。取“1.3.2”项下香蒲新苷对照品溶液适量,按照“1.3.3”项下色谱条件连续进样6次,记录色谱峰面积。
(4)重复性考察。按照“1.3.2”项下方法平行制备供试品溶液6份,并按照“1.3.3”项下色谱条件分别进样测定,记录供试品中色谱峰面积。
(5)加标回收率考察。精密量取5 mL的供试品溶液6份置于10 mL的棕色容量瓶中,另精密量取2 mL含100 μg/mL的香蒲新苷对照品加入棕色容量瓶中,用甲醇定容,摇匀得6份样品,平行测定,记录色谱峰面积。
(6)样品含量测定。取3批样品,按“1.3.2”项下方法制备供试品溶液,再按“1.3.3”项下色谱条件进样,记录峰面积,计算3批样品中香蒲新苷的含量。
2 结果与分析
2.1 线性关系
HPLC检测蒲黄中香蒲新苷的线性关系如图2所示。结果表明,线性回归方程为y=11.362x-14.037,R2=0.997 2,香蒲新苷在20~100 μg/mL范围内线性关系良好。
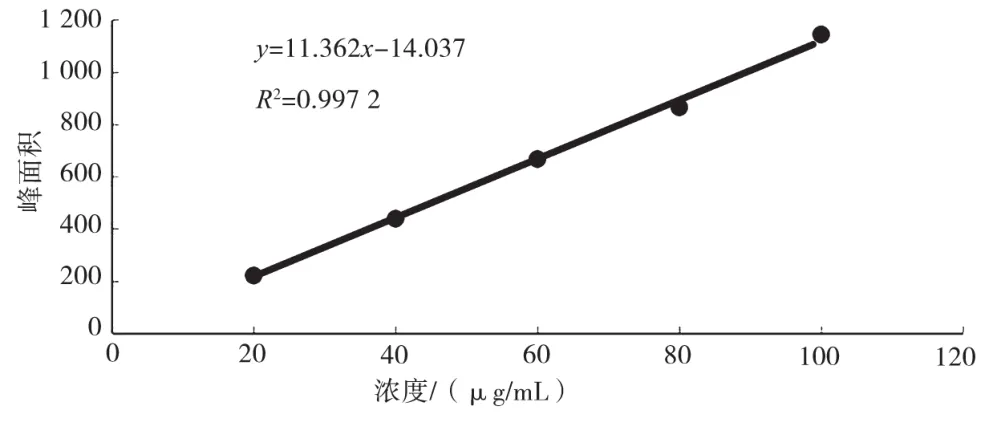
图2 香蒲新苷检测线性关系考察
2.2 稳定性
香蒲新苷检测稳定性实验结果见表2。如表2所示,计算得香蒲新苷峰面积的RSD值为2.27%(n=6),表示供试品溶液在12 h内稳定。

表2 香蒲新苷检测稳定性实验结果
2.3 精密度
香蒲新苷检测精密度实验结果见表3。如表3所示,计算得香蒲新苷峰面积的RSD值为2.55%(n=6),表明仪器精密度良好。

表3 香蒲新苷检测精密度实验结果
2.4 重复性
香蒲新苷检测重复性实验结果见表4。如表4所示,计算得香蒲新苷峰面积的RSD值为0.32%(n=6),表明该方法的重现性较好。
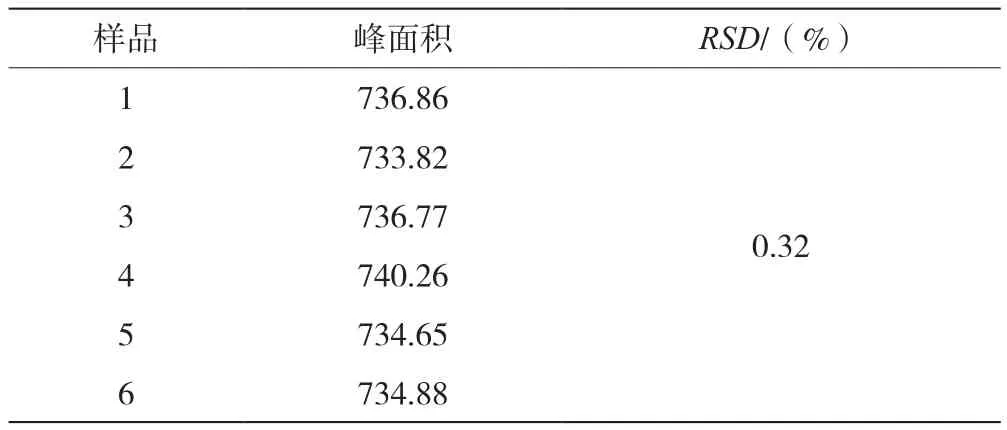
表4 香蒲新苷检测重复性实验结果
2.5 样品含量测定
3批样品中香蒲新苷含量检测结果见表5。如表5所示,3批样品中香蒲新苷的含量为0.63%~0.65%,香蒲新苷平均含量为0.64%。

表5 3批样品中香蒲新苷含量
2.6 加样回收率试验
香蒲新苷检测加样回收率实验结果见表6 。如表6所示,香蒲新苷的加样回收率RSD值为1.16%(n=6),则表明此方法的准确度较好。

表6 香蒲新苷检测加样回收率实验结果
3 结论
香蒲新苷是蒲黄的主成分之一[5],实验结果表明,本实验所建立的HPLC法测定蒲黄提取物中镇痛成分香蒲新苷的方法学考察符合要求,稳定性高,操作简单,重复性好,3批次样品中香蒲新苷的含量为0.64%,此方法为蒲黄镇痛成分的质量控制与评价奠定了基础。
