基于靶区与危及器官重叠度的自动治疗计划设计
2021-11-04潘兴晨汪冬胡丽琴
潘兴晨,汪冬,胡丽琴
1.中国科学院合肥物质科学研究院,安徽合肥230031;2.中国科学技术大学研究生院科学岛分院,安徽合肥230026
前言
癌症是全球范围内的主要公众卫生问题,已逐渐成为威胁人类生命的最大杀手。调强放疗(Intensity-Modulated Radiotherapy, IMRT)是国内外各放疗中心的标准治疗技术。IMRT 计划质量很大程度上依赖于物理师的经验和所花费的时间,严重影响患者的治疗效果,不同物理师制定的放疗计划有差异[1]。同时放疗技术发展是不均衡的,具体表现为国内外不均衡、城乡不均衡、基层与高级医院的不均衡[2-3]。放疗计划设计者常常根据临床协议的危及器官(Organs-at-Risk, OAR)剂量限值目标不断地尝试和修改获得较优计划[4-6]。使用放疗自动计划能让不发达地区或低水平医院制定高质量计划,降低高水平医院制定计划的时间,有效缓解放疗资源特别是人力资源的不平衡性。目前国内外有多家研究机构进行关于IMRT 自动计划的研究:Wu 等[7]引入重叠体积直方图(Overlap Volume Histogram, OVH)来描述靶区与OAR 的相对位置,通过比较新患者和数据库中患者的OVH来指导自动计划;Zhu等[8]利用主成分分析方法确定OAR 的剂量体积直方图(Dose-Volume Histogram, DVH)和OVH 的主成分,同时运用支持向量回归方法建立DVH 与OVH 主成分之间的数学模型来指导自动计划;Moore等[9]根据OAR的OVH 与其平均剂量之间关系的经验公式来引导计划的自动计划;Skarpman 等[10]利用DVH 的概率诠释,将DVH曲线上各个点的纵坐标定义为剂量高于某值的概率,通过预测剂量分布的概率密度来达到预测DVH 的目的,从而引导自动计划;Yuan 等[11]挑选了68 例头颈部肿瘤患者,其中35 例靶区与单侧腮腺有较大重叠,其余33例则没有重叠,对上述两种情形分别建立了腮腺剂量与解剖结构之间的数学模型(单侧腮腺和双侧腮腺模型),进而引导自动计划。基于放疗计划的现状和我国发展不均衡的问题,本研究提出基于靶区与OAR 重叠度的DVH 预测自动计划设计,以期望改善现状。对靶区与OAR 重叠度进行研究,建立基于靶区与OAR 重叠度的精确微分DVH预测模型,并发展脚本式自动计划流程,最后在前列腺癌症病例上进行测试与应用评估。通过精准预测OAR 的DVH 并自动设计计划来提高治疗计划的质量和效率。
1 材料和方法
1.1 前列腺癌放疗计划数据集
随机选取17 例前列腺恶性肿瘤患者,年龄为35~75 岁。放疗靶区PTV 分别在CTV 前后、左右、头尾方向各外放0.5~1.0 cm,以保护直肠;OAR 包括膀胱、直肠、股骨头等,靶区和OAR 均由放疗科经验丰富的主治医生勾画和并由一名医师进行审核。运用ADAC Pinnacle3计划系统进行5 野均分的IMRT 计划设计,采用直接机器参数优化,最小子野面积和最小机器单元分别为5 cm2和5 MU。
1.2 建立微分DVH的精确数学模型
1.2.1 OAR 分割成子块随机选择数据集中9 例作为训练集,其余作为测试集。以膀胱为例,将PTV 外扩到覆盖OAR 范围内,依次分割成层厚3 mm 的子块(Ai,i=0、1、2、3…,其中A0为PTV 与膀胱重叠部分),见图1;直肠等其它OAR 作同样处理。使用Pinnacle脚本[12]编码后导出各OAR所有子块Ai的微分DVH。

图1 膀胱的子块分割图Fig.1 Sub-block segmentation of the bladder
1.2.2 建立数学模型拟合子块Ai微分DVH由于每个Ai的微分DVH 均呈现偏正态分布[12-14],本研究拟用如下偏正态高斯函数拟合各Ai的Di(Di表示子块的微分DVH):

其中,D为Ai的剂量;p1为Di的中心剂量;p2为Di曲线半高宽;p3与Di曲线的尾部形状有关;a为拟合系数。以OAR 中膀胱为例,图2为膀胱和靶区的重叠度示意图。图3为使用该函数拟合9 例患者Ti(i=1、2、…8、9)膀胱子块Ai(i=1、2、3、4)的Di分布,其中黑色的点表示原始计划数据,蓝线表示拟合曲线。

图2 膀胱和靶区的重叠度Fig.2 Degree of overlap between the bladder and planning target volume(PTV)
1.2.3 OAR 与靶区的重叠度分析图3中的膀胱Ai的微分DVH拟合结果显示:随着离靶区越来越远,膀胱子块的微分DVH 的高度是逐渐降低的,与临床实践相符,即距离靶区越远的膀胱区域受到的辐照剂量越低。但是病人T6、T7、T8、T9结果异常。结合表1,从靶区与OAR 之间的重叠度来分析以上规律。T1的重叠度为0.36%,与其他病人相比,重叠度非常小,DVH的高度下降很明显;T2、T3、T4和T5的重叠度分别为3.66%、4.48%、6.55%和9.60%,此时由于靶区与膀胱重叠度较小,靶区的高剂量区对膀胱的剂量分布影响较小,规律正常;对于T6、T7、T8和T9的重叠度分别为11.10%、14.31%、20.00%和23.82%,此时靶区与膀胱重叠度较大,在维持靶区的高剂量的同时,高剂量区会对膀胱的剂量分布有较大影响。直肠等其他OAR也有类似情况。

表1 训练集中的膀胱与靶区的重叠度Tab.1 Degree of overlap between the bladder and PTV in training set

图3 9例病人膀胱子块Ai(i=1、2、3、4)拟合Fig.3 Fitting of bladder sub-blocks Ai(i=1,2,3,4)in 9 patients
1.3 基于微分DVH预测模型的自动计划设计
利用初步建立的每个OAR 所有Ai的微分DVH初始数学模型,应用式(1)得到预测训练集9 例病人OAR 各Ai的DVH,并将得到OAR 的DVH 与原临床计划病人OAR 的DVH 进行比较,若预测DVH 优于临床DVH,则采用预测子块DVH 指导重新设计治疗计划,通过分析相关参数,获得数学模型的自动计划设计[15-16]。
应用Pinnacle3上的脚本程序处理测试集中的8例病人影像,得到膀胱、直肠等OAR 各Ai的微分DVH。应用编写的Matlab 程序获取数据,结合各Ai微分DVH 精确模型预测膀胱、直肠等OAR 的子块DVH,并从中选取优于临床DVH 的处方剂量点作为OAR 逆向优化的目标函数[17],进而得到自动计划。本研究的自动计划流程见图4。

图4 基于OAR和靶区重叠度的自动治疗计划设计Fig.4 Automatic treatment planning based on the degree of overlap between organs-at-risk (OAR)and PTV
1.4 自动计划结果评估方案
1.4.1 评价标准选取比较分析两种治疗计划的差异[18-19],主要从几个方面考虑:适形度指数(CI)、均匀性指数(HI)、冷热剂量点、等剂量线、DVH曲线、临床上关注的剂量体积参数包括靶区PTV100%(100%剂量线包绕的靶区体积)以及膀胱等的V70、V60、V50、V40(其中V70代表70Gy 剂量线对应的膀胱体积,其余类似)。CI和HI的计算公式如下:

其中,VPTV,REF为处方剂量线所对应的靶区体积;VPTV为靶区体积;VREF为处方剂量线所对应的总体积;D2%是2%靶区体积受照的剂量;D50%为50%靶区体积受照的剂量;D98%是98%靶区体积受照的剂量。
1.4.2 统计学分析上述所用到的自动计划数据与原手工计划数据用均数±标准差表示,采用SPSS 25.0统计学分析软件对两组计划数据进行配对t检验,P<0.05 说明差异有统计学意义。对两组计划指标数据的差值与放疗计划的重叠度做相关性分析,两组数据均为连续变量,采用SPSS 25.0 统计学分析软件对两组数据进行Spearman 相关系数分析[20],P<0.05说明两者之间的相关关系有统计学意义。
2 结果与讨论
对测试集进行与训练集相同的前期处理操作,包括靶区外扩、获取OAR子块,然后通过脚本预测DVH,制定计划并根据子块DVH预测结果修改约束。测试集中的病例按照膀胱与靶区的重叠度大小排列如表2。

表2 测试集中膀胱与靶区的重叠度Tab.2 Degree of overlap between the bladder and PTV in test set
自动计划和原手工计划中的等剂量线均能包绕要求的靶区(图5);图6为自动计划与原手工计划的DVH。图5和图6是同一病例。与原手工计划的剂量分布图相比,自动计划的靶区剂量均匀性和适形度都能达到临床处方要求,并优于原手工计划。自动计划的HI稍优于原手工计划的HI,分别为0.11±0.03和0.12±0.03,两组间的差异具有统计学意义(t=-1.871,P=0.014);自动计划的CI也稍优于原手工计划的CI,分别为0.84±0.29 和0.83±0.27,两组间的差异具有统计学意义(t=3.742,P=0.007)。自动计划靶区的V100%稍差于原手工计划靶区的V100%,自动计划靶区的V95%稍优于原手工计划靶区的V95%,但是两个指标的组间差异无统计学意义(t=-0.539,0.289;P=0.606,0.781)。靶区V100%、V95%、HI和CI的统计学结果见表3。
表3 自动计划和原手工计划的靶区剂量学参数比较(±s)Tab.3 Dosimetric comparison of PTV between automatic plan and original plan(Mean±SD)

表3 自动计划和原手工计划的靶区剂量学参数比较(±s)Tab.3 Dosimetric comparison of PTV between automatic plan and original plan(Mean±SD)
参数自动计划原手工计划t值P值HI CI V100%/%V95%/%0.11±0.03 0.84±0.29 95.49±0.53 99.50±0.32 0.12±0.03 0.83±0.27 95.64±0.70 99.48±0.32-1.871 3.742-0.539 0.289 0.014 0.007 0.606 0.781

图5 两组计划的等剂量曲线Fig.5 Isodose curves between automatic plan and original plan

图6 自动计划(细实线)与原手工计划(细虚线)的DVHFig.6 Dose-volume histogram of automatic plan(thin solid line)and original plan(thin dotted line)
如表4所示,与原手工计划相比,自动计划的膀胱V70、V60、V50以及V40分别下降5.8%、4.1%、4.0%、6.9%,除膀胱V40比较无统计学意义外(t=-2.193;P=0.064),膀胱的其它指标V70、V60、V50的比较均具有统计学意义(t=-2.471、-3.439、-2.376;P=0.043、0.011、0.049)。自动计划的直肠V70、V60、V50以及V40分别下降11.0%、4.5%、2.5%、7.1%(t=-2.540、-3.416、-2.666、-2.777;P=0.039、0.011、0.032、0.027),差异具有统计学意义,其中直肠的V70较原手工计划相比明显下降。
表4 自动计划和原手工计划的OAR剂量学参数比较(%,±s)Tab.4 Dosimetric comparison of OAR between automatic plan and original plan(%,Mean±SD)

表4 自动计划和原手工计划的OAR剂量学参数比较(%,±s)Tab.4 Dosimetric comparison of OAR between automatic plan and original plan(%,Mean±SD)
OAR膀胱参数V70 V60 V50 V40直肠V70 V60 V50 V40自动计划9.51±4.49 25.81±9.25 38.52±11.20 51.63±16.34 2.19±2.46 24.92±6.11 41.82±10.00 61.62±15.31原手工计划10.10±4.29 26.90±8.96 40.13±11.19 55.45±17.70 2.46±2.66 26.10±5.72 42.88±9.50 66.33±15.47 t值-2.471-3.439-2.376-2.193-2.540-3.416-2.666-2.777 P值0.043 0.011 0.049 0.064 0.039 0.011 0.032 0.027
3 讨论
本研究利用基于重叠度的自动计划设计来实现前列腺肿瘤的自动计划,实验结果表明自动计划与原手工计划的等剂量曲线均能较好地包绕靶区,靶区剂量的均匀性和适形度均在临床接受范围内,OAR 的剂量也在临床接受的范围内。但是与原手工计划相比,对于膀胱的改善数值确是不一样,膀胱剂量参数差异具体见表5。
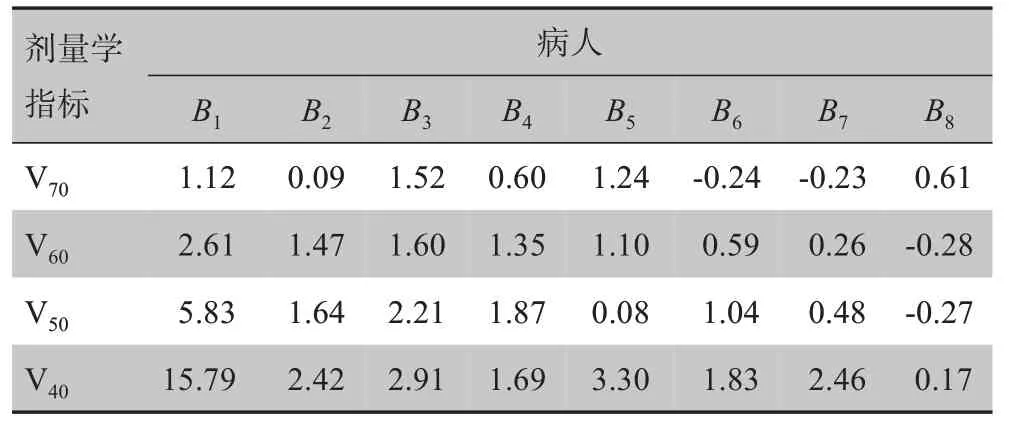
表5 自动计划和原手工计划的膀胱剂量差异(%)Tab.5 Differences in bladder dose between automatic plan and original plan(%)
根据Spearman 相关系数分析所示,自动计划和原手工计划的膀胱V70、V60和V50的差异值与重叠度呈负相关(相关系数=-0.357、-0.976、-0.857;P=0.385、0.000、0.007),除了V70的差异值与重叠度无统计学意义外,V60和V50的差异值与重叠度都有统计学意义,与重叠度呈强负相关关系。自动计划和原手工计划的膀胱V40的差异值与重叠度呈弱正相关(相关系数=0.381;P=0.352),无统计学意义。
对于有统计学意义的膀胱V60和V50来说,随着重叠度越来越大,在维持靶区的高剂量的同时,影响了OAR 的剂量分布,导致OAR 的剂量参数所能改善的剂量数值越来越小。所以,对于靶区与OAR 重叠区域较大时,计划优化参数的选取应当谨慎。直肠等OAR也有类似结论,在此不再讨论。
4 结论
在对前列腺癌症的病例研究中,靶区与OAR 的重叠度干扰了微分DVH 的变化规律。以微分DVH为基础,通过使用基于重叠度的自动计划设计,可以在满足靶区高剂量的同时,大幅度减少周围OAR(如膀胱和直肠)剂量区域中的照射剂量。由于患者靶区与OAR 的重叠度不同,导致最终对原手工计划所能改善的剂量数值是不一样的,靶区与OAR 重叠度越小,利用提出来的自动计划算法对原手工计划改善的剂量数值就越大。对于重叠度较小的病例,采用本文自动计划方法,可以得到较好计划结果,供用户参考。
本研究未考虑靶区体积、各OAR 之间的照射剂量相互影响等因素,在后续工作中会进一步分析不同病例、不同OAR、不同重叠度对结果的影响。
