储氢材料的研究进展
2021-11-03刘红梅徐向亚张蓝溪邬娇娇刘东兵
刘红梅,徐向亚,张蓝溪,邬娇娇,刘东兵
(中国石化 北京化工研究院,北京 100013)
氢是宇宙中分布最广泛的元素,氢能是兼具燃烧放热量高、来源丰富、绿色环保等诸多优点的二次能源[1]。目前,全球环境危机和能源危机日渐严重,很多发达国家正在积极部署氢能战略并大力发展氢能技术[2-3]。为了实现“碳达峰”和“碳中和”目标,我国的能源结构将发生重大变化,在能源产业布局大规模调整的历史背景下,氢能作为高效的清洁能源将占据更重要的地位[4-7]。氢能产业链主要包括氢气的制备、储存、运输和利用。处于产业链中段的氢气存储连接了氢气的生产和氢气的应用,是实现氢气大规模应用的关键技术和前提条件。目前较成熟的储氢方式主要有三种:高压气态储氢、低温液态储氢和以储氢材料为介质的固态储氢[8]。固态储氢方式的工作原理是利用某些特殊材料吸附氢气的能力实现对氢气的储存和运输。与其他两种储氢方式相比,固态储氢方式储氢密度更高、运输更方便、安全性更好,因此应用前景良好[9-11]。但这种储氢方式的发展和应用需要依赖储氢材料的开发和利用。根据吸氢机理的差异,储氢材料可以分为物理吸附储氢材料和化学储氢材料两大类。
本文综述了物理吸附类储氢材料和化学类储氢材料的研究进展,分析并对比了各类储氢材料的优缺点。
1 物理吸附储氢材料
物理储氢方式的主要工作原理是利用范德华力在比表面积较大的多孔材料上进行氢气的吸附。利用多孔材料进行物理储氢的优点是吸氢-放氢速率较快、物理吸附活化能较小、氢气吸附量仅受储氢材料物理结构的影响。物理吸附储氢材料主要包括:碳基储氢材料、无机多孔材料、金属有机骨架(MOF)材料、共价有机化合物(COF)材料。
1.1 碳基储氢材料
碳基储氢材料因种类繁多、结构多变、来源广泛较早受到关注[12]。鉴于碳基材料与氢气之间的相互作用较弱,材料储氢性能主要依靠适宜的微观形状和孔结构。因此,提高碳基材料的储氢性一般需要通过调节材料的比表面积、孔道尺寸和孔体积来实现。碳基储氢材料主要包括活性炭、碳纳米纤维和碳纳米管。
1.1.1 活性炭
活性炭又称碳分子筛,是一种石墨微晶堆积的无定形碳材料,具有独特的结构特征,如比表面积较大、孔道结构多样、孔径尺寸可以在较宽的范围内调节等。Fierro等[13]研究发现,在低温(77 K)常压条件下,活性炭的储氢能力与它的物理结构密切相关,即比表面积越大,储氢量越大,最高储氢量可以达到6.4%(w)。常压条件下,孔径在0.6~0.7 nm之间的孔道对活性炭吸附氢的贡献最大。但在6 MPa以上的高压条件下,只有孔径低于1.5 nm的孔道才有利于氢气的吸附[14]。
活性炭来源广泛,包括高分子聚合物、生物质材料(木材、农作物、果壳)和矿物质材料(煤、焦油)等。不同来源的活性炭材料,如果比表面积相似,在相同温度、压力条件下储氢量差异较小[15-18]。在77 K,0.1 MPa条件下,比表面积3 000 m2/g的活性炭储氢量大约为2.0%~3.0%(w)。升高压力可以有效提高活性炭储氢量。在77 K,1.0 MPa条件下,活性炭储氢量可达到5.0%左右(w);在77 K,2.0~4.0 MPa条件下,活性炭储氢量可以达到5.0%~7.0%(w)[19-20]。目前,超级活性炭在94 K,6.0 MPa条件下储氢量可以达到9.8%(w)。而室温下,即使压力达到20.0 MPa以上,活性炭的储氢量仍然仅有0.5%~2.0%(w)[21]。
1.1.2 碳纳米纤维
碳纳米纤维主要通过含碳化合物裂解的方法制备,比表面积较大,同时含有较多微孔。与传统的粒状活性炭相比,碳纳米纤维具有以下特点:1)纤维的直径更小,与氢分子的接触面积更大,吸附几率更高。2)与同质量的活性炭相比,碳纳米纤维的比表面积更大、微孔数目更多,所以氢气吸附量更大、吸附和脱附速率更快。3)碳纳米纤维的孔径分布范围很窄,而颗粒状的活性炭内部孔径分布却非常不规则。因此,碳纳米纤维材料的外形和孔道尺寸均会对它的储氢性能造成一定影响。在一定范围内,碳纳米纤维的储氢量与纤维直径呈反比,与重量呈正比。在常温、12 MPa条件下,碳纳米纤维的最大储氢量为6.5%(w),使用Li,K等碱金属对碳纳米纤维表面进行修饰[22],可以将同条件下的储氢量提高到10%(w)左右。改进碳纳米纤维的制备方法,在常温、11 MPa条件下,可以获得最高12%(w)的储氢量[23]。
1.1.3 碳纳米管
碳纳米管是一种由石墨烯片卷曲而成的径向尺寸纳米级、轴向尺寸微米级的一维材料,主要由呈六边形排列的碳原子构成。根据石墨烯片的层数不同,碳纳米管可以分为单壁和多壁两种。一般单壁碳纳米管具有较高的化学惰性,表面携带的官能团较少;多壁碳纳米管表面较为活泼,携带大量的表面基团。通过不同制备方法得到的碳纳米管表面结构有一定差别。由于碳纳米管具有中空的孔道结构,且表面结合了各种官能团,因而表现出了良好的储氢性能,储氢量与比表面积呈正比关系[24]。另外,通过控制碳纳米管的生长方式能够在一定程度上提高它的储氢性能[25]。目前,单壁碳纳米管在80 K,12 MPa条件下最高储氢量可以达到8.0%(w);而在室温、10 MPa条件下,最高储氢量可以达到4.2%(w)。多壁碳纳米管的最佳储氢能力在4 MPa时为1.97%(w),7 MPa时为3.7%(w),10 MPa时为4.0%(w),15 MPa时为6.3%(w)[26-27]。温度对多壁碳纳米管释放氢的能力影响很大,室温下氢的释放量不足0.3%(w),而77 K时氢气解吸量可以达到2.27%(w)。比较而言,单壁碳纳米管释放氢的能力较好,常温条件下即可释放吸附量80%的氢气。
1.2 无机多孔材料
无机多孔材料主要是具有微孔或介孔孔道结构的多孔材料,包括有序多孔材料(沸石分子筛或介孔分子筛)或具有无序多孔结构的天然矿石。沸石分子筛材料和介孔分子筛材料具有规整的孔道结构和固定的孔道尺寸,结构上的差异会影响到材料的比表面积和孔体积,进而影响到材料的储氢性能。
杜晓明等[28]研究了不同温度和压力条件下ZSM-5沸石分子筛的储氢性能。实验结果表明,ZSM-5分子筛在77 K,5 MPa条件下储氢量为1.97%(w);在195 K,7 MPa条件下的储氢量为0.65%(w);在293 K,7 MPa条件下的储氢量为0.4%(w)。具有不同结构的沸石分子筛储氢性能虽有差异,但储氢量普遍较低,一般不超过3.0%(w)。天然矿石中储氢性能较好的包括坡缕石、海泡石、埃洛石和凹凸棒石。其中,储氢量最大的是埃洛石,可达2.8%(w)。如果使用适当的金属对坡缕石进行修饰,可以将其298 K,0.7 MPa条件下的储氢量由1.1%(w)提高到2.35%(w)[29]。沸石分子筛的氢吸附等温线与脱附等温线基本重合,表明氢在沸石分子筛微孔中的吸附为物理吸附。因此,沸石分子筛吸附的氢可以全部释放,储氢材料可循环利用。
与沸石分子筛相比,介孔分子筛的孔道尺寸较大、比表面积和孔体积较大,更有利于氢气的吸附。因此从原理上说,介孔分子筛材料的储氢性能会稍优于沸石分子筛材料。张光旭等[30]研究发现,MCM-48介孔分子筛在248 K,0.2 MPa条件下的储氢量为0.7%(w);掺杂金属Ni以后在263 K,0.2 MPa条件下的储氢量达到0.8%(w)。
1.3 MOF材料
MOF材料是由金属氧化物与有机基团相互连接组成的一种规则多孔材料。因为MOF材料具有低密度、高比表面积、孔道结构多样等优点而受到了广泛关注。
2003年,Rosi等[31]报道了一种命名为MOF-5、结构为Zn4O(BDC)3的有机金属框架材料的储氢性能。该材料在77 K、中等压力条件下的储氢量为4.5%(w);但该材料在298 K,2 MPa条件下储氢量仅为1.0%(w)。通过对MOF-5材料中有机配体的调节,材料的储氢性能得到了显著提高[32]。MOF家族中储氢能力最强的是MOF-177,该材料在77 K,7 MPa条件下的储氢量可达7.5%(w),但常压储氢量仅为1.25%(w)[33]。改善MOF材料储氢性能的途径主要包括:1)调整骨架结构;2)掺杂低价态金属组分;3)掺杂贵金属;4)在有机骨架中引入特殊官能团[34-35]。经改性处理,MOF材料的储氢性能有所改善,但仍无法达到碳基储氢材料的水平。
1.4 COF材料
COF材料是在MOF材料基础上开发出来的一种新型多孔材料。由于COF材料的骨架全部由非金属的轻元素构成,COF材料的晶体密度较低,更有利于气体的吸附,因此COF材料的储氢性能引起了极大的关注[36-37]。COF材料的储氢性能与它的物理结构(包括孔体积、孔结构和晶体密度)有直接关系。在77 K,10 MPa条件下,COF-108的最大的储氢量为18.9%(w),而COF-102具有最大的体积吸附量,为40.4 g/L;在77K,0.01 MPa的条件下,具有最大储氢量和最大体积吸附量的材料是COF-1;在298 K,10 MPa的条件下,COF-105储氢量可达4.67%(w)[38]。
虽然与MOF材料相比,COF材料的储氢性能有所提高,但在常温条件下的储氢量还是不能令人满意。为改善COF材料的储氢能力,很多学者将碱金属离子引入COF材料骨架结构中,这大大提高了材料的储氢性能[39]。将锂醇基团引入COF-105的结构中,可使其室温储氢量提高到6.0%(w)[40]。
2 化学储氢材料
化学储氢材料的主要工作原理是氢以原子或离子形式与其他元素结合而实现储氢。基于化学机制的储氢材料主要包括:金属-合金储氢材料、氢化物储氢材料和液体有机氢化物。
2.1 金属-合金储氢材料
金属-合金储氢材料是研究较早的一类固体储氢材料,制备技术和制备工艺均已成熟。金属-合金类材料不仅具有超强的储氢性能,还同时具有操作安全、清洁无污染等优点。但金属或合金材料的氢化物通常过于稳定,与物理吸附类储氢材料相比,金属-合金储氢材料的储氢和放氢都只能在较高的温度条件下进行。金属-合金储氢材料可以分为镁系、钒系、稀土系、钛系、锆系、钙系等[41]。
金属镁的储氢性能早在20世纪六十年代就已经被研究人员发现了。理论上,镁的储氢量可以达到7.6%(w)。但鉴于吸氢过程中金属原子需要从颗粒表面向颗粒内部扩散,金属材料的吸氢速度不可避免地受到颗粒尺寸的限制,粒径越小,吸氢速率越快。在573 K,1.0 MPa条件下,金属镁颗粒大于1 μm时,2 h内几乎没有表现出储氢能力;粒径50 μm时,2 h内储氢量为5.8%(w);粒径减小到30 nm时,2 h内储氢量可以达到6.2%(w)[42]。由于单质镁吸放氢温度过高,镁系储氢材料多为含镁复合材料或镁系合金,其中,最有代表性的是Mg-Ni系列合金。Mg2Ni合金的理论储氢量为3.6%(w),吸氢温度473 K以上,放氢温度约573 K。在Mg-Ni合金中添加第三种元素,可以在一定程度上改善材料的储氢性能,但同时也会降低它的储氢容量[43]。
除Mg-Ni合金外,Mg-Pd合金、Mg-Co合金和Mg-Fe合金都表现出了良好的储氢性能。在上述工作基础上,研究人员又开发出了Mg-V-Al-Cr-Ni多元高熵合金储氢材料[44]。金属钒在常温常压条件下可以吸氢和放氢,理论最高储氢量为3.8%(w)。由于金属钒价格昂贵,目前还无法产业化应用。研究较多的钒基合金储氢材料包括V-Ti-Cr,V-Ti-Fe,V-Ti-Mn,V-Ti-Ni等。钒合金作为储氢材料的优点是吸放氢速率快、平衡压适中、储氢密度大,缺点是表面易生成氧化膜增加活化难度。
稀土系储氢材料以AB5型合金为代表。在1969年,荷兰的Philips实验室发现了LaNi5合金的储氢性能。该材料的理论储氢量为1.38%(w),用作镍氢电池的负极材料实现了商业化应用。LaNi5合金的优点是吸放氢条件温和、吸放氢速率快、对杂质不敏感、平衡压差小;缺点是储氢量小、吸氢后金属晶胞体积膨胀大、易粉化。为了提高LaNi5合金的储氢性能,研究人员开发出一种具有堆垛结构的超晶格La-Mg-Ni系合金。与LaNi5合金相比,这种新型合金具有更大的储氢量。但由于该材料中含有金属镁,在制备合成时存在一定的安全隐患,且结构组成难以控制[45]。为了解决上述问题,科学家研发出了高储氢量La-Y-Ni系合金材料[46-47]。除了开发三元合金以外,研究人员还使用其他稀土元素取代La来提升稀土合金的储氢性能。如MmNi5合金不仅能保持LaNi5合金的所有优点,还能够提高储氢量、降低生产成本,具有更好的应用前景。
钛系储氢材料多为合金,常见的有Ti-Fe,Ti-Zr,Ti-Cr,Ti-Mn等,其中,研究较多的是Ti-Fe合金(理论储氢量1.86%(w))。Ti-Fe合金资源丰富、制备简单、价格低廉、吸放氢条件温和,但该材料抗毒性能较差[48]。如果能够在Ti-Fe合金中添加少量Ni,即可显著提高吸放氢性能。另外,使用Co,Mn,Ni,Cr等金属替代Fe也可以有效改善Ti-Fe合金的储氢性能。与Ti-Fe合金相比,Ti-Co合金的活化性能和抗毒性能均有明显提高,Ti-Mn合金的储氢量更高,Ti-Cr合金吸放氢温度更低[49]。
锆系合金中只有C15立方Laves相和C14六方Laves相材料具有储氢能力,理论储氢量介于1.8%~2.4%(w)之间,常用材料包括Zr-V合金、Zr-Ni合金、Zr-Cr合金、Zr-Mn合金和Zr-Co合金。Zr-V合金吸放氢速率快,但制备困难;Zr-Ni合金储氢量大、结构稳定,但吸放氢可逆性差;Zr-Cr合金氢化物稳定、材料循环寿命高,但不易活化;Zr-Mn合金储氢量大、放电能力强,但成本较高[50];相对来说,综合性能较好的是Zr-Co合金[51]。
金属钙本身就是很好的储氢材料,理论储氢含量为4.8%(w)。在LaNi5合金基础上开发出来的CaNi5合金储氢量可达1.9%(w),明显优于LaNi5合金。近年来Ca-Ni-M系列合金材料中,比较突出的是Ca-Mg-Ni系储氢材料,该材料在吸放氢过程中动力学性能优异。图1对比了不同金属-合金储氢材料的最佳储氢性能。从图1可看出,储氢量最高的是镁系材料和钙系材料,而稀土类材料性能较差。

图1 不同金属-合金储氢材料的最高储氢量Fig.1 The maximum hydrogen storage capacities of different metal-alloy hydrogen storage materials.
2.2 氢化物储氢材料
氢化物储氢材料主要包括配位铝复合氢化物、金属氮氢化物、金属硼氢化物和氨硼烷化合物。
配位铝氢化物是一类非常重要的储氢材料,表达通式为M(AlH4)n,其中,M可以是碱金属或碱土金属。这类储氢材料中研究较多的是NaAlH4和Na3AlH6。NaAlH4的理论储氢量高达7.4%(w),但这种材料的吸放氢温度均较高。添加少量Ti元素以后,NaAlH4的吸放氢温度可降低[52]。配位金属氢化物在储氢领域的应用主要受限于氢化物的化学特点。这类材料吸氢后形成的产物化学性质过于稳定,放氢困难,导致吸放氢循环可逆性较差。改善配位铝氢化物储氢性能的方法是向材料中添加一定量的催化剂。常用催化剂有TiCl3,LaCl3,ScCl3,CeCl3,PrCl3。
金属氮氢化物是十几年前被发现的一种新型储氢材料,结构通式为M(NH2)n,其中,M以碱金属或碱土金属为主。最有代表性的金属氮氢化物储氢材料为LiNH2-LiH和Mg(NH2)2-LiH。LiNH2-LiH的吸放氢温度一般在423 K以上,理论储氢量11.4%(w);Mg(NH2)2-LiH体系的理论储氢量为9.1%(w),但吸放氢温度低于LiNH2-LiH材料,且可以通过调节Mg(NH2)2与LiH的比例来改善储氢性能。研究人员发现,用Mg部分取代Li制备得到的Mg(NH2)-2LiH材料在383 K条件下即可实现5%(w)左右的氢可逆充放[53]。Mg(NH2)-2LiH在0.1 MPa平衡氢压时的工作温度可以降低至363 K左右,完全可以满足美国能源部制定的质子交换膜燃料电池对车载氢源系统操作温度的要求。因此,这种新材料被寄予厚望,成为有希望实现应用的车载氢源材料[54]。
金属硼氢化物的结构通式为M(BH4)n,理论储氢量一般超过10%(w)。有代表性的金属硼氢化物储氢材料主为 LiBH4和 Mg(BH4)2。LiBH4的理论储氢量能够达到18.5%(w),但吸放氢温度高。Mg(BH4)2的热稳定性较好,理论储氢量为14.9%,在室温条件下即可满足质子交换膜燃料电池的使用要求[55]。
氨硼烷是一类结构独特的分子配合物,分子式为NH3BH3,分子中的氮原子与硼原子以配位键的形式相结合。氨硼烷的理论储氢量高达19.6%(w),且热稳定性好、放氢的温度较低,是一种非常有前途的新型储氢材料,近年来在学术界受到了广泛的关注。为提高氨硼烷的放氢速率,研究人员开发了包括硼烷氨锂(LiNH2BH3)在内的一系列的氨硼烷衍生物[56]。由于氨硼烷及其衍生物为储氢材料存在放氢过程中可控性不好、放氢温度偏高、产生挥发性的有毒气体等缺点,氨硼烷类储氢材料的再生是一个不可忽视的问题。可通过改变氨硼烷的脱氢环境、使用催化剂、添加促进剂等方法改善氨硼烷的释氢性能。目前,氨硼烷的合成工艺已经成熟,但再生技术却远远没有达到应用的需求,这将成为氨硼烷储氢材料未来发展的障碍。图2对比了不同种类氢化物储氢材料的最佳储氢性能。从图2可知,储氢量最高的是氨硼烷。
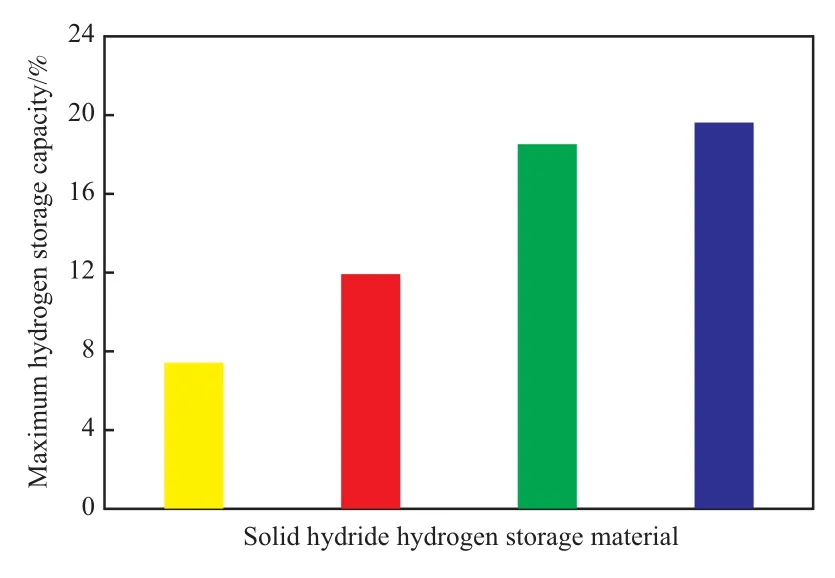
图2 不同固态氢化物储氢材料的最高储氢量Fig.2 The maximum hydrogen storage capacities of different solid hydride hydrogen storage materials.
2.3 液体有机氢化物储氢材料
不饱和液体有机物(包括烯烃、炔烃和芳烃)可以在加氢和脱氢的循环反应中实现吸氢和放氢。其中,储氢性能最好的是单环芳烃,苯和甲苯的理论储氢量都较大,是较有发展前景的储氢材料。研究人员发现,如果以氧化铝负载的金属镍为催化剂,可以将甲苯直接转化成环己烷[57]。与传统的固态储氢材料相比,液体有机氢化物储氢材料有以下优点:1)液体有机氢化物的储存和运输简单,是所有储氢材料中最稳定、最安全的;2)理论储氢量大,储氢密度也比较高;3)液体有机氢化物的加氢和脱氢反应可逆,储氢材料可反复循环使用[58]。
3 结语
随着全球能源供应逐渐紧张,各国的氢能安全问题都将提到日程上来。能否开发出性能优良的储氢材料是决定氢能能否大规模应用的关键问题。从应用的角度出发,目前各种储氢材料中最具优势的是金属-合金类储氢材料。其他化学储氢材料或物理储氢材料多因储氢量或储氢密度较低而难以达到应用要求。未来,储氢材料的研究开发工作应从以下几个方面着手:1)开发原料易得、价格低廉、能够实现工业化制备的储氢材料;2)向轻元素或混合轻元素方向努力,以进一步提高材料的储氢密度;3)重点关注储氢材料的可循环利用,将氢气的储存-释放体系作为一个整体,发展实用的储氢材料。
