结直肠癌肝转移患者TACE治疗后含表皮生长因子的纤维蛋白样细胞外基质2水平及意义
2021-10-28于清泳
于清泳,赵 辉
作者单位:226699 江苏南通 海安市中医院介入科(于清泳);南通大学附属医院介入科(赵 辉)
结直肠癌是常见的消化系统恶性肿瘤之一,易发生肝脏转移[1]。据调查60%~71%的结直肠癌发生了肝脏转移,其中仅有10%~20%结直肠癌肝转移患者可通过根治性手术切除进行治疗[2-3]。近年来,随着介入技术的发展,TACE 已被用于治疗结直肠癌肝转移,但整体治疗效果仍不理想,患者5年生存率仍较低[4]。探寻结直肠癌肝转移TACE 治疗预后的生物标志物,可了解患者生存预后情况,有利于治疗方案的制定。
含表皮生长因子的纤维蛋白样细胞外基质2(EGF containing fibulin-like extracellular matrix protein 2,EFEMP2)又名fibulin4,是fibulin 家族中一员,主要负责调控弹性纤维的合成与排列[5-6]。目前,EFEMP2 已被证实在结直肠癌中异常表达,并参与其进展[7]。有研究证实上调EFEMP2 可抑制肿瘤细胞的迁移、侵袭和上皮间质转化[8-10]。上皮间质转化与TACE 治疗疗效密切相关。本研究分析EFEMP2和结直肠癌肝转移TACE 治疗预后的关系。现报道如下。
1 材料与方法
1.1 临床资料
选择2015年3月至2017年7月在海安市中医院接受治疗的152 例结直肠癌肝转移患者作为研究对象。纳入标准:①经临床病理及影像学检查确诊为结直肠癌肝转移;②无法通过根治性手术切除或不接受根治性手术切除治疗;③接受TACE 治疗后未再次接受TACE 治疗;④临床治疗、检查及随访等资料完整。排除标准:①合并其他恶性肿瘤;②存在除肝脏以外其他脏器转移的肿瘤病灶;③心、肝、肾功能严重异常;④接受放疗、免疫治疗或靶向治疗等;⑤有自身免疫性疾病史或血液系统疾病;⑥临床资料不完整、不配合完成检查或随访失联等。152 例结直肠癌肝转移患者中男94 例,女58例,年龄52~70(61.6±4.3)岁;肿瘤单发52 例,肿瘤多发100(2~3 个)例,共268 个肿瘤病灶,肿瘤平均直径(3.28±0.44)cm。
收集所有受试者年龄、性别、原发病灶位置、转移灶个数、Child-Pugh 分级、肿瘤直径、AFP 和后续治疗方案等信息。采用电话、复诊等方式进行随访,了解预后情况。于患者出院后开始随访,每月随访1次,末次随访时间为2020年7月10日,随访终点为患者随访过程中死亡或至末次随访结束,中位随访时间为20(6~36)个月。
1.2 方法
1.2.1 TACE 治疗方法 采取仰卧位,消毒,铺巾,麻醉;血管造影下Seldinger 法置入导管鞘及导管,注入碘帕醇(上海博莱科信谊药业有限责任公司,国药准字:H20073014),观察肿瘤病灶位置、大小、数量和供血动脉等,灌注化疗药物并进行栓塞。化疗药物为奥沙利铂(江苏奥赛康药业股份有限公司,国药准字:H20064296)、雷替曲塞(南京正大天晴制药有限公司,国药准字:H20090325)和盐酸吡柔比星(深圳万乐药业有限公司,国药准字:H10930105),栓塞剂为碘化油(烟台鲁银药业有限公司,国药准字:H37022398)和明胶海绵颗粒[杭州艾力康医药科技有限公司,国食药监械(准)字2014 第3771056 号]。根据患者情况给予保肝、止吐等治疗。TACE 后定期复诊,行CT/MRI 检查观察肿瘤病灶碘油沉积及有无新发肿瘤病灶等情况[11]。
1.2.2 EFEMP2 水平检测 抽取所有受试者TACE前(T0)、术后3 d(T1)、7 d(T2)和14 d(T3)空腹外周静脉血10 mL,外周血中单个核细胞用Ficoll 密度梯度离心法分离[12]。用蛋白质印迹法检测单个核细胞中EFEMP2 水平[13]。用RIPA 裂解液裂解单个核细胞,分离出总蛋白,用BCA 法蛋白定量;10%SDS-PAGE 分离胶凝胶电泳至溴酚蓝跑出胶面,转膜,5%脱脂奶粉室温封闭2 h;分别滴加兔抗人EFEMP2 单克隆抗体(北京博奥森生物技术有限公司)和兔抗人β-actin 单克隆抗体(北京博奥森生物技术有限公司),4℃孵育过夜;滴加山羊抗兔二抗(上海信裕生物科技有限公司),室温下孵育2 h;ELC 发光液显影。用Image J 软件读取实验结果图像。
1.3 统计学方法
2 结果
2.1 两组EFEMP2 水平比较
根据结直肠癌肝转移患者3年生存预后将其分为两组:生存组(n=51)和死亡组(n=101)。两组EFEMP2 水平比较,差异有时间效应(F=1733.269,P<0.001)、组间效应(F=229.065,P<0.001)和交互效应(F=57.263,P<0.001)。两组EFEMP2 水平均随时间进展呈升高趋势。生存组T1、T2 和T3 时EFEMP2 水平均高于死亡组,差异均有统计学意义(P<0.05)。见表1、图1。

图1 两组EFEMP2 的蛋白质免疫印迹图
表1 两组EFEMP2 水平比较±s
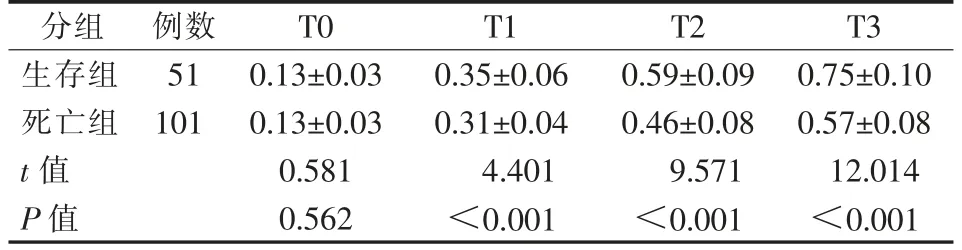
表1 两组EFEMP2 水平比较±s
分组例数T0T1T2T3生存组 51 0.13±0.030.35±0.060.59±0.09 0.75±0.10死亡组 101 0.13±0.030.31±0.040.46±0.08 0.57±0.08 t 值0.5814.4019.57112.014 P 值0.562<0.001<0.001<0.001
2.2 EFEMP2 诊断结直肠癌肝转移TACE 治疗预后的效能
T0-EFEMP2 诊断结直肠癌肝转移TACE 治疗预后的ROC 曲线下面积(AUC)、最佳截断点、灵敏度和特异度分别为0.524(95%CI:0.425~0.622)、0.08、99.01%和11.76%;T1-EFEMP2 诊断结直肠癌肝转移TACE 治疗预后的ROC AUC、最佳截断点、灵敏度和特异度分别为0.697(95%CI:0.601~0.793)、0.33、79.21%和54.90%;T2-EFEMP2 诊断结直肠癌肝转移TACE 治疗预后的ROC AUC、最佳截断点、灵敏度和特异度分别为0.876(95%CI:0.814~0.939)、0.51、78.22%和84.31%;T3-EFEMP2诊断结直肠癌肝转移TACE 治疗预后的ROC AUC、最佳截断点、灵敏度和特异度分别为0.922(95%CI:0.881~0.964)、0.60、72.30%和92.20%。T3-EFEMP2诊断结直肠癌肝转移TACE 治疗预后的效能高于T0-EFEMP2 和T1-EFEMP2,差异均有统计学意义(Z=7.549、4.187,P<0.001)。见图2。

图2 EFEMP2 诊断结直肠癌肝转移TACE 治疗预后的ROC 曲线
2.3 两组基线资料比较
以T3-EFEMP2 诊断结直肠癌肝转移TACE 治疗预后的最佳截断点将其分为两组:高EFEMP2 组(n=61)和低EFEMP2 组(n=91)。两组的年龄、性别、病灶位置、转移灶个数、Child-Pugh 分级、肿瘤直径、AFP 和靶向治疗方面比较,差异均无统计学意义(P>0.05)。见表2。

表2 两组基线资料比较
2.4 两组生存情况比较
高EFEMP2 组中位生存时间为36 个月,高于低EFEMP2 组(16 个月),差异有统计学意义(Log-Rank χ2=66.064,P<0.001)。见图3。

图3 两组生存曲线
2.5 结直肠癌肝转移预后的Cox 回归分析
将结直肠癌肝转移患者3年生存预后作为因变量,将年龄、性别、原发病灶位置、转移灶个数、Child-Pugh 分级、肿瘤直径、AFP、靶向治疗和T3-EFEMP2 作为自变量,分别纳入Cox 单因素分析,结果显示靶向治疗和T3-EFEMP2 与结直肠癌肝转移TACE 治疗3年生存预后有关(P<0.05)。将结直肠癌肝转移患者3年生存预后作为因变量,按P<0.1 的标准将Child-Pugh 分级、靶向治疗和T3-EFEMP2作为自变量,纳入Cox 多因素分析,结果显示靶向治疗和T3-EFEMP2 均是结直肠癌肝转移TACE 治疗3年生存预后的独立保护因素(P<0.05)。见表3。

表3 结直肠癌肝转移预后的Cox 回归分析
2.6 T3-EFEMP2 与结直肠癌肝转移TACE 治疗3年生存预后的关系
用限制性立方样条拟合Cox 回归分析T3-EFEMP2 与结直肠癌肝转移TACE 治疗3年生存预后的关系,当节点个数为4 时,AIC 值最小(AIC=854.907),此时结果显示T3-EFEMP2 与结直肠癌肝转移TACE 治疗3年生存预后有关(χ2=49.2,P<0.001),呈非线性关系(χ2=6.0,P=0.0499)。以T3-EFEMP2 诊断结直肠癌肝转移TACE 治疗预后的最佳截断点做为参考点,当T3-EFEMP2<0.60 时,结直肠癌肝转移TACE 治疗3年预后不良风险增加;当T3-EFEMP2>0.60 时,结直肠癌肝转移TACE 治疗3年预后不良风险降低。见图4。

图4 T3-EFEMP2 与结直肠癌肝转移TACE 治疗3年生存预后的限制性立方样条图
3 讨论
有极性的上皮细胞通过特定程序转化成有活动能力的间质细胞的过程即为上皮间质转化,进而促使细胞的迁移和侵袭,降低放、化疗疗效[14-15]。Kang 等[8]研究证实,EFEMP2 高表达可抑制乳腺癌细胞迁移、侵袭和上皮间质转化等。Zhou 等[9]研究证实EFEMP2 可调控膀胱癌细胞的上皮间质转化。Song 等[10]研究证实上调EFEMP2 水平可抑制肺癌细胞的侵袭、迁移和上皮间质转化。目前,陈勇[16]研究证实EFEMP2 在结直肠癌肝转移病灶中低表达,但关于其与TACE 治疗疗效的关系鲜见报道。
本研究结果显示生存组和死亡组EFEMP2 水平均随时间进展呈升高趋势,此外,生存组T1、T2和T3 时EFEMP2 水平均高于死亡组,上述结果表明EFEMP2 水平可能与结直肠癌肝转移TACE 治疗预后有关,其表达水平或可评价患者预后。遂构建了EFEMP2 诊断结直肠癌肝转移TACE 治疗预后的ROC 曲线,结果显示T3-EFEMP2 诊断结直肠癌肝转移TACE 治疗预后的ROCAUC、灵敏度和特异度分别为0.922、72.30%和92.20%,其诊断效能高于T0-EFEMP2 和T1-EFEMP2,上述结果表明T3-EFEMP2 评价结直肠癌肝转移TACE 治疗预后的效能高,但灵敏度偏低,可辅助评价结直肠癌肝转移TACE 治疗预后。
本研究进一步探究了EFEMP2 与结直肠癌肝转移TACE 治疗预后的关系,结果显示高EFEMP2组中位生存时间高于低EFEMP2 组,表明EFEMP2与结直肠癌肝转移TACE 治疗后的生存时间有关,可用于预后评估。叶涛等[17]研究证实结直肠癌肝转移的女性患者预后较男性患者好。鲁全芝[18]研究表明肝转移病灶数目是结直肠癌肝转移预后的独立危险因素。为避免混杂因素影响分析结果,本研究用Cox 回归分析影响结直肠癌肝转移TACE 治疗预后的因素,结果显示靶向治疗和T3-EFEMP2均是结直肠癌肝转移TACE 治疗3年生存预后的独立保护因素,而性别、肝转移病灶数目均与结直肠癌肝转移TACE 治疗3年生存预后无关,与上述研究结果存在出入,推测其差异可能与纳入研究样本量、随访时间及纳排标准等有关,后续还需开展大样本、多中心研究验证本研究结论。
人体EFEMP2 基因位于染色体11q13,该区域的易位、重排及扩增等均与恶性肿瘤发生、发展有关[19]。现有研究已表明EFEMP2 可调控Wnt/β-catenin 信号传导通路参与多数恶性肿瘤细胞的迁移、侵袭和上皮间质转化[8-9]。本研究推测EFEMP2 可能通过上述调节机制参与了结直肠癌肝转移细胞的上皮间质转化过程,进而影响了TACE 治疗疗效。受化疗药物影响,若癌细胞的上皮间质转化能力降低,EFEMP2 水平高;反之,EFEMP2 水平低。因此,检测其水平可反映结直肠癌肝转移TACE 治疗预后,是以T3-EFEMP2 与结直肠癌肝转移TACE 治疗3年生存预后有关,当T3-EFEMP2<0.60 时,结直肠癌肝转移TACE 治疗3年预后不良风险增加;当T3-EFEMP2>0.60 时,结直肠癌肝转移TACE 治疗3年预后不良风险降低。
综上所述,直肠癌肝转移患者外周血单个核细胞中EFEMP2 水平与TACE 治疗疗效有关,其水平低提示TACE 治疗临床获益较小。本研究样本量较小、随访时间偏短,且检测EFEMP2 水平的时点偏少,下一步将开展大样本、多中心研究,增加检测EFEMP2 的时点,完善本研究内容。
