磁响应氧化石墨烯纳米材料的合成与表征
2021-10-21张鑫韬王金玉
张鑫韬, 徐 瑾, 王金玉, 何 燕
(青岛科技大学 机电工程学院,山东 青岛 266061)
目前水处理方法有离子交换法、化学沉淀法、电解法和吸附法等,其中吸附法是公认最有效、经济和环保的水处理方法。传统的吸附剂吸附容量不高也不易分离,新型吸附材料受到广泛关注[1-2]。氧化石墨烯(GO)是以sp2杂化轨道形成的六边形呈蜂窝状周期排列的新型碳材料,表面的含氧基团赋予了其良好的亲水性和丰富的吸附位点,具有巨大的比表面积,高吸附量、物理化学性质稳定和原材料易获取等优势[3-5]。虽然氧化石墨烯在吸附方面优势明显,但由于其粒径小,不易过滤和沉淀,所以目前氧化石墨烯的分离回收是吸附的一大难题。迫切需要寻求一种简便易行的方法来实现氧化石墨烯的快速分离。
磁性纳米材料在外加磁场的情况下能够实现快速分离,石墨烯与金属及其氧化物的复合材料在吸附中的应用一般需结合金属及其氧化物[6-7]本身的特性,对环境友好的金属Mn[8]和Fe[9-10]及其氧化物常用于制备复合石墨烯材料。HE等[11]利用一种高效、绿色、可控制的方法,通过一步法制备出了附着有功能化四氧化三铁纳米粒子的石墨烯纳米片,其中四氧化三铁纳米粒子的直径为1.2~6.3 nm,覆盖密度为5.3%~57.9%。ZONG等[12]通过共沉淀法制备了还原型氧化石墨烯RGO@Fe3O4复合材料,并研究RGO@Fe3O4复合材料的微波吸收机理。氧化石墨烯和磁性纳米粒子通过化学键结合相比于静电作用有更强的相互作用力,在改性效果,使用重复率方面也具有更大优势。
本研究选用改进的Hummers法来制备氧化石墨烯,后利用超声共沉淀法制备出Fe3O4磁性纳米粒子并对其进行氨基改性,最后通过酰胺反应使Fe3O4纳米粒子通过化学键负载于氧化石墨烯片层上,得到磁性氧化石墨烯(MGO)。
1 实验部分
1.1 试剂及仪器
天然鳞片状石墨(3 000目(5 μm)),青岛腾盛达碳素机械有限公司;高锰酸钾、浓硫酸,烟台远东精细化工有限公司;氯化钡,北联精细化学品开发有限公司;氯化亚铁,天津市大茂化学试剂厂;3-氨丙基三乙氧基硅烷(APTES),上海博耀生物科技有限公司;碳化二亚胺(EDC),阿拉丁生化科技股份有限公司;N-羟基琥珀酰胺(NHS),上海麦克林生化科技有限公司;过氧化氢、硝酸钠、三氯化铁、氨水、正硅酸四乙酯和无水乙醇均采购于国药集团化学试剂有限公司。
高低温恒温水浴槽,DC0520-II型,上海平轩仪器有限公司;数控超声波清洗器,KQ-100DE型,昆山市超声仪器有限公司;离心机,YXJ-A型,江苏金坛市环宇科学仪器厂;真空冷冻干燥机,FD-1A-50型,北京博医康实验仪器有限公司;扫描电子显微镜,SU8010型,日本日立公司;透射电子显微镜,H-7650型,日本日立公司;红外光谱仪,NICOLET iS50型,赛默飞世尔科技有限公司;X射线衍射仪,UItima IV型,日本理学公司;共焦显微拉曼光谱仪,InVia Reflex型,雷尼绍公司。
1.2 氧化石墨烯的制备
采用改进的Hummers法制备:
1)低温反应。向三口烧瓶中加入110 mL浓H2SO4,当恒温水浴槽温度稳定至1 ℃时将烧瓶置于其中,然后在机械搅拌的条件下加入5 g天然鳞片状石墨和2.5 g NaNO3,最后将15 g KMnO4少量多次加入混合溶液中,搅拌反应90 min;
2)中温反应。将上述反应完成后的混合溶液置于35 ℃的恒温水槽中继续搅拌反应30 min;
3)高温反应。将三口烧瓶置于温度为98 ℃的油浴锅中,在搅拌条件下缓慢加入200 mL 3%的过氧化氢溶液,溶液稳定后,停止加热,将溶液在室温下静置;
4)洗涤。倒掉上清液,将底部沉淀用去离子水离心洗涤,直至用BaCl2溶液检测上层清液不出现大量白色沉淀;
5)剥离。将洗涤后的固体物质移入烧杯中,加入去离子水,在100 W超声功率条件下,搅拌超声处理8 h;
6)干燥。将黏稠的深棕色浆料充分冷冻,在真空条件下干燥12 h。在去离子水不产生影响的条件下,也可保存浆料使用,测定浆料固含量。
1.3 磁性纳米粒子的制备
1)将物质的量比为1∶2的FeCl2·4H2O和FeCl3·6H2O水溶液分别加入三口烧瓶中,通入N230 min排出内部空气。温度保持在30,50,70 ℃,加入25%(质量分数)浓氨水,超声并在N2保护条件下反应30 min。反应完成后依次用乙醇和去离子水清洗,通过真空冷冻干燥得到Fe3O4纳米粒子。
2)通过超声将Fe3O4纳米粒子分散至由80 mL乙醇,30 mL去离子水以及1 mL 25%氨水组成的溶液中,待均匀分散后将一定量的正硅酸四乙酯缓慢滴加入混合溶液中,在室温下超声搅拌反应5、6、7 h。反应结束后依次用乙醇和去离子水洗涤,通过真空冷冻干燥得到Fe3O4-OH纳米粒子。
3)将一定量的Fe3O4-OH纳米粒子超声分散到30 mL乙醇中,依次加入2 mL的氨水、2 mL去离子水,待溶液均匀后将一定量的ATPES缓慢加入,于80 ℃下搅拌反应6 h。反应完成后依次用乙醇和去离子水清洗,经真空冷冻干燥得到Fe3O4-NH2纳米粒子。
1.4 磁性氧化石墨烯的制备
取一定量的氧化石墨烯(GO)浆料均匀分散于去离子水中,后将一定量的Fe3O4-NH2纳米粒子加入上述溶液中并超声30 min,再加入一定量的EDC和NHS,80 ℃下搅拌反应1 h,反应后将固体样品用乙醇和去离子水清洗,通过真空冷冻干燥得到磁性氧化石墨烯(MGO)。
为了防止制备出的Fe3O4纳米粒子在空气中发生氧化和团聚,通过超声使正硅酸四乙酯在碱性条件下发生水解,产生SiO2并包覆在纳米粒子表面,羟基化改性使本身不具备官能团等结构的Fe3O4纳米粒子在其表面产生活性位点。通过磁场使磁性氧化石墨烯在基质中发生相对位移,需要磁性粒子与氧化石墨烯有较强的相互作用力,否则容易发生脱落和滞后,所以通过硅烷偶联剂在包覆有SiO2的Fe3O4纳米粒子表面带上氨基基团,再通过酰胺反应使磁性粒子上的氨基和氧化石墨烯上的羧基发生反应,从而使两者之间通过作用力较强的酰胺键连接起来,得到实验所需要的磁性氧化石墨烯。此过程如图1所示。

图1 氧化石墨烯的磁改性流程Fig.1 Magnetic modification process of graphene oxide
2 结果与讨论
2.1 氧化石墨烯的形貌与结构表征
图2为氧化石墨烯形貌图。

图2 氧化石墨烯形貌图Fig.2 SEM image of graphene oxide
由于粒径5 μm天然鳞片状石墨的堆积层数较少,平面尺寸较小,在氧化的过程中,氧化物更容易进入片层间,氧化均匀度好,充分度也更高。通过改进的Hummers法制备出的GO片层较薄且尺寸小于2 μm,具有较好的片层分布。通过低功率长时间的超声剥离,既不会导致超声频率过高破坏氧化石墨烯片层结构,也不会导致超声能量过低使剥离不充分。从图2中可以看到,氧化石墨烯片层表面存在大量褶皱,这是由于片层内存在大量官能团,原本完美的晶格结构遭到破坏而成为缺陷,片层有序度下降。


图3 氧化石墨烯的结构图Fig.3 Structure of grapheme oxide
Raman光谱图能够很好地表征纳米碳材料的有序程度,反言之为缺陷程度,GO在1 346 cm-1和1 604 cm-1出现拉曼散射峰,对应为D峰和G峰,其中D峰是由于环氧化物和羟基存在于碳基环上,从而产生的结构缺陷,和sp3杂化碳的含量有关。G峰是碳元素六边形上的碳原子发生面内平移,与sp2杂化碳的含量有关。本实验制备的GO的ID/IG值为1.007 6,说明石墨层氧化程度较高,GO片层缺陷度较高,石墨化程度下降明显,进一步解释了GO表面出现褶皱的原因,验证制备出结构特征明显的GO。
2.2 羟基化改性Fe3O4纳米粒子形貌与结构特征
为了探究Fe3O4纳米粒子在生长过程中,温度对其尺寸及尺寸分布的影响,分别在30、50、70 ℃下进行制备,利用透射电子显微镜对得到的样品进行观察,如图4所示。通过对比发现,随着反应温度的上升,制备出的Fe3O4纳米粒子具有更大的粒子平均尺寸,从10 nm增加至30 nm,并且随温度增加尺寸分布均一性下降,出现大小差别较大的不同粒子,同时类球形的纳米粒子形状逐渐变得不规则。分析出现上述现象原因是,在温度较低的条件下纳米粒子成核后,较少新核出现,大多数晶核同时生长且生长速率较为缓慢,故不存在晶体生长的不同步所引起的粒径分布不均,也不会因为生长速率过快引起尺寸变大。而在温度较高的条件下,晶体在生长的过程中受到周围环境的影响较大,成核速度加快从而出现形状变为不规则的现象。

图4 不同制备温度下Fe3O4的形貌图Fig.4 Morphology of Fe3O4 at different preparation temperatures
选取制备温度为30 ℃下的Fe3O4纳米粒子进行羟基化改性,使其产生能够发生反应的活性位点,从而继续进行功能化改性或者与其他物质进行化学反应。这一过程可以通过正硅酸乙酯在碱性条件下水解生成SiO2包覆在粒子表面来实现。其中水解时间这一因素尤为重要,为此设置反应时间分别为5、6、7 h,通过透射电子显微镜直接观察水解包覆情况结果见图5。从图5看出,当水解时间为5 h时,纳米粒子表面出现了少量固体物质但并没有被完全包覆,没有形成预期的核壳结构。而当水解6 h后表面形成了一层厚度为2~4 nm的包覆层且被完全包覆。随着水解时间的增加,产生的SiO2的量不断增加,全部沉积在纳米粒子表面,从图5(c)发现在纳米粒子周围出现大量的固体物质,将大多数纳米粒子包裹在一起,这会导致Fe3O4的磁感应性能下降。故选取6 h最为合适。

图5 不同羟基化改性时间下的Fe3O4-OH形貌图Fig.5 Morphology of Fe3O4-OH under different hydroxylation modification time
由图6可知,3 370 cm-1对应的是样品中结晶水的伸缩振动吸收峰,1 630 cm-1对应为样品中吸附水的弯曲振动吸收峰,583 cm-1对应于样品中Fe—O键的伸缩振动吸收峰。将Fe3O4纳米粒子的红外光谱图与羟基化改性后的纳米粒子进行对比发现,在1 060 cm-1处出现了吸收峰,其对应Si—O—Si键的反对称伸缩吸收峰。可以说明通过羟基化改性在Fe3O4纳米粒子上成功包覆了SiO2,即在纳米粒子上出现能够发生反应的羟基活性位点。由于粒子表面存在羟基,与水发生相互作用,故改性后的纳米粒子能够很好地分散在水中,放置较长时间也不会发生沉降。

图6 Fe3O4和Fe3O4-OH的红外光谱图Fig.6 The infrared spectrum of Fe3O4 and Fe3O4-OH
2.3 氨基化改性Fe3O4纳米粒子形貌与结构表征
ATPES可以用来合成有机硅中间体及高分子化合物,也可用作硅烷偶联剂,通过对其结构和性能分析可知,ATPES主要是由氨基和乙氧基组成,而乙氧基硅烷可以在碱性条件下发生水解,当乙氧链端水解接枝在物质表面时,另一端所携带的氨基也会存在于物质表面,从而使该物质也携带氨基。利用上述ATPES的上述特性,使其接枝在羟基改性后的纳米粒子表面,从而使纳米粒子拥有氨基官能团。氨基改性下的Fe3O4-NH2纳米粒子形貌图见图7。从图7发现,纳米粒子周围包覆有一层固体物质,与图5(b)对比发现,包裹的固体物质的厚度由2~4 nm增加至3~5 nm,并且粒子之间的间距也明显增大。这是由于ATPES在Fe3O4纳米粒子表面发生水解也会生成SiO2,从而使包覆层厚度增加。

图7 氨基改性下的Fe3O4-NH2纳米粒子形貌图Fig.7 Morphology of Fe3O4-NH2 nanoparticles under amino modification
对氨基改性后的样品进行红外光谱分析,结果见图8。如图8所示,3 440 cm-1对应羟基的伸缩振动吸收峰,1 629 cm-1对应为NH2的变角振动吸收峰,1 070 cm-1对应Si—O—Si键的反对称伸缩吸收峰,596 cm-1对应的是Fe—O键的伸缩振动吸收峰。氨基吸收峰的出现证明了Fe3O4纳米粒子表面出现了氨基基团,观察发现氨基改性后,纳米粒子在水中的分散性有所下降,长时间静置后会有少量沉淀,这是由于改性后在纳米粒子上接枝的氨基相较于羟基与水的相互作用弱。
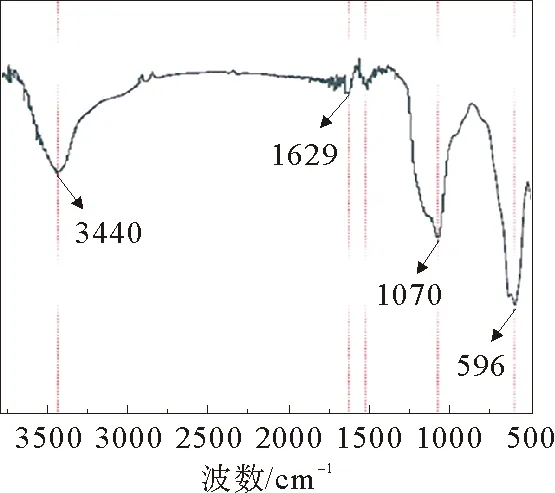
图8 氨基改性Fe3O4的红外光谱图Fig.8 Infrared spectrum of amino-modified Fe3O4
2.4 MGO的结构表征
将Fe3O4纳米粒子和GO枝接在一起,能够得到具有磁响应的氧化石墨烯(MGO)。多数研究将两者间仅仅通过静电相互作用连接在一起,虽然过程简单,但也存在响应性能不足,使用寿命短,回收利用率低等问题。化学键相较于静电吸引力能有效够防止Fe3O4从氧化石墨烯中脱落,也可避免局部Fe3O4纳米粒子过多而出现MGO性能不均一的情况。通过化学反应使两者以化学键结合在一起是一种很好的解决办法。通常条件下氨基和羧基无法自发进行酰胺反应,可以选用EDC和NHS来活化氧化石墨烯上的羧基和改性后Fe3O4上的氨基,提高两者的反应活性,从而进行酰胺反应。

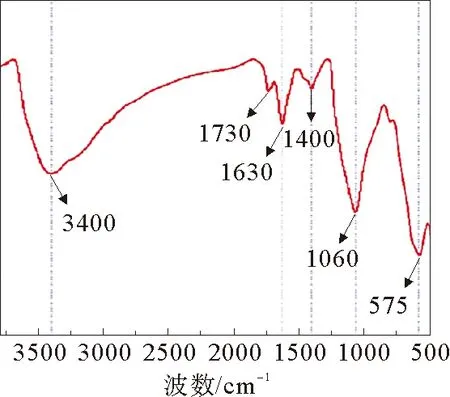
图9 MGO红外光谱图Fig.9 Infrared spectrum of MGO
GO、Fe3O4和MGO的拉曼光谱图见图10。从图10中可以看出,在MGO的拉曼图谱中存在对应于GO和Fe3O4的特征拉曼散射峰,由于散射峰的加和性,可以说明MGO是由GO和Fe3O4组成的,进一步证实了通过酰胺反应,将GO与Fe3O4结合起来制备出了MGO。

图10 GO、Fe3O4和MGO的拉曼光谱图Fig.10 Raman spectra of GO,Fe3O4 and MGO
2.5 MGO的磁响应表征
在样品管一侧放置磁铁,测试实验产物的磁性结果见图11。由图11看出,纳米四氧化三铁通过羟基和氨基改性后,由于纳米四氧化三铁在羟基化改性时表面包覆一层二氧化硅导致磁性有所下降,但在Fe3O4@SiO2-NH2混合溶液中和磁改性后的氧化石墨烯溶液中仍然出现改性粒子快速向磁铁聚集现象,表现出很好的顺磁性,可实现应用后的快速分离回收。

图11 氨基化改性Fe3O4纳米粒子和MGO的磁响应Fig.11 Magnetic response of amino modified Fe3O4 nanoparticles and MGO
3 结 论
通过改进Hummers法和超声共沉淀法分别制备了氧化石墨烯和Fe3O4纳米粒子,经过羟基化、氨基化对Fe3O4纳米粒子进行改性,最后通过酰胺反应使氧化石墨烯(GO)和Fe3O4纳米粒子发生反应得到磁性氧化石墨烯(MGO)纳米材料。采用形貌表征和测试分析等方法对GO、Fe3O4、Fe3O4-OH、Fe3O4-NH2、MGO进行形貌和结构表征,通过结果得出:
1)通过超声共沉淀法制备出的Fe3O4纳米粒子具有更小的尺寸和更好的尺寸分布,当反应温度为30 ℃时制备出的Fe3O4纳米粒子粒径较小,为7~13 nm,形状规则性更好;
2)对Fe3O4纳米粒子进行羟基化改性,成功在粒子表面包覆SiO2同时羟基化,当水解时间为6 h时有更好的包覆完整度及合适的包覆层厚度。也在羟基化改性后的Fe3O4纳米粒子上成功接枝了氨基;
3)在活化剂EDC和NHS存在的条件下,氧化石墨烯和改性后的Fe3O4纳米粒子发生酰胺反应,成功制备出MGO,并实现了较好的顺磁性,可实现MGO的快速分离回收。
