肺泡表面活性物质联合鼻塞持续气道正压通气对肺透明膜病早产儿血气指标的影响
2021-10-18莫志宇梁波卢兰花
莫志宇,梁波,卢兰花
(深圳市龙岗区第三人民医院,广东 深圳518000)
肺透明膜病(HMD)是新生儿常见疾病,多发于早产儿,主要为肺发育不成熟所致,肺泡表面难以顺利分泌活性物质,肺泡萎缩,具有进展迅速、死亡率高、预后效果差的特点[1]。治疗不及时易引发呼吸系统或神经系统后遗症,积极采取预防性措施是挽救HMD早产儿性命的关键。呼吸机支持是HMD的重要治疗手段,鼻塞持续气道正压通气(NCPAP)为首选方案。有研究[2]指出,HMD的发病原因与肺泡表面活性物质(PS)不足相关,PS可辅助提高呼吸机治疗效果,改善预后。本研究探讨PS+NCPAP治疗HMD早产儿的效果及对血气指标水平的影响。
1 资料与方法
1.1 一般资料选取2018年5月至2020年5月深圳市龙岗区第三人民医院诊治的72例HMD早产儿为对象,运用抽签法随机分组,每组36例。入选标准:符合HMD相关诊断标准[3];出生后24 h内症状明显;胎龄29~38周;出生体质量1.2~2.9 kg;家属知情本研究并签署同意书。排除标准:合并先天性疾病者;伴有其他呼吸系统疾病者;重要脏器功能严重障碍者;因吸入羊水/胎粪所致呼吸窘迫者;PS过敏者;有NCPAP禁忌证者。本研究符合《世界医学会赫尔辛基宣言》。对照组男女比例为21∶15,平均胎龄(32.53±5.16)周,平均出生体质量(1.76±0.32)kg。观察组男女比例为20∶16,平均胎龄(33.02±4.57)周,平均出生体质量 (1.72±0.35)kg。两组的一般资料比较,差异无统计学意义(P>0.05)。
1.2 治疗方法两组患儿均接受保暖、吸氧、静脉营养等常规治疗,同时给予患儿血氧监护和生命体征监测。对照组给予NCPAP治疗,设置呼吸机(型号:AirSense 10,瑞思迈)初始参数:吸入氧浓度(FiO2)30%~60%,流速5~8 L/min,呼吸末正压(PEEP)4~6 cmH2O。参数根据患儿血气检测情况适当调整。观察组在对照组基础上,于出生后12 h内给予PS治疗,气管插管后清除气道分泌物,于气管分叉部位注入猪肺磷脂注射液(规格:1.5 mL∶0.12 g/瓶;批准文号:注册证号H20181201;意大利凯西制药公司)100 mg/kg,后持续加压给氧10 min,SpO2>90%后拔出插管。
1.3 观察指标①血气指标:采用血气分析仪(型号:PL2200,南京普朗医疗设备有限公司)测定患儿治疗前及治疗24 h后的动脉血二氧化碳分压(PaCO2)、动脉血氧分压(PaO2)和pH值。②临床疗效[4]:根据症状改善情况,X线检查双肺阴影及血气指标结果,将疗效分为显效(症状完全消失,双肺阴影消失,30 mm Hg≤PaCO2≤50 mm Hg,PaO2>75 mm Hg,pH值范围7.25~7.45)、有效 (症状基本消失,双肺可见部分阴影,PaCO2<45 mm Hg,PaO2>45 mm Hg,pH值>7.25)和无效(症状加重或无改善,血气指标未达到有效和显效标准)。③并发症:包括肺炎、皮下气肿、腹胀、气漏、气胸等。
1.4 统计学分析应用SPSS 21.0统计软件分析数据。计量数据以±s表示,采用t检验;计数数据以率表示,采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 血气指标治疗24 h后,两组的PaCO2均下降,PaO2均升高(P<0.05);观察组的PaCO2显著低于对照组,PaO2显著高于对照组,差异有统计学意义(P<0.05)。见表1。
表1 两组治疗前后的血气指标比较(±s)
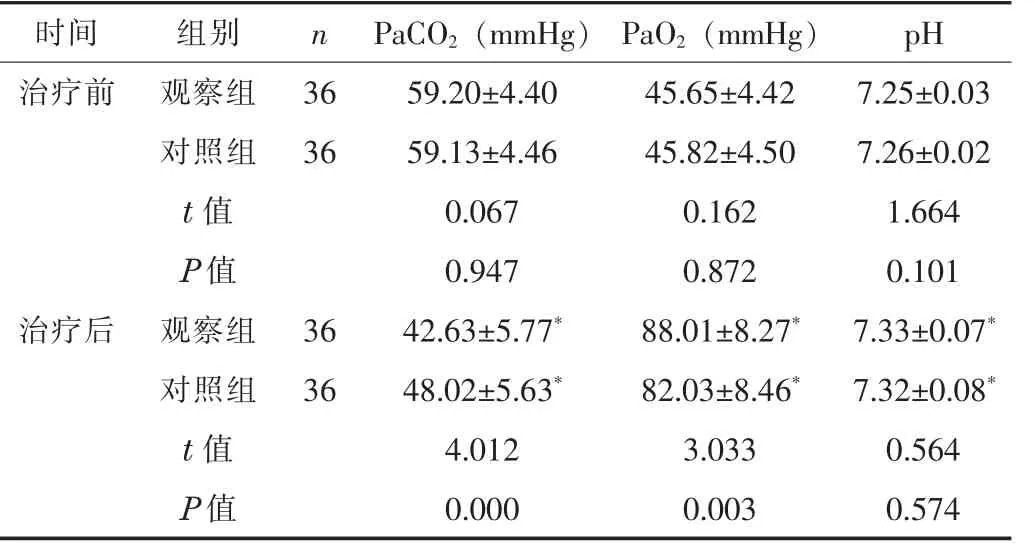
表1 两组治疗前后的血气指标比较(±s)
注:与本组治疗前比较,*P<0.05。
时间 组别 n PaCO2(mmHg)PaO2(mmHg) pH治疗前 观察组36 59.20±4.40 45.65±4.42 7.25±0.03对照组36 59.13±4.46 45.82±4.50 7.26±0.02 t值 0.067 0.162 1.664 P值 0.947 0.872 0.101治疗后 观察组36 42.63±5.77* 88.01±8.27* 7.33±0.07*对照组36 48.02±5.63* 82.03±8.46* 7.32±0.08*t值 4.012 3.033 0.564 P值 0.000 0.003 0.574
2.2 两组的疗效比较观察组的总有效率显著高于对照组,差异有统计学意义(P<0.05)。见表2。
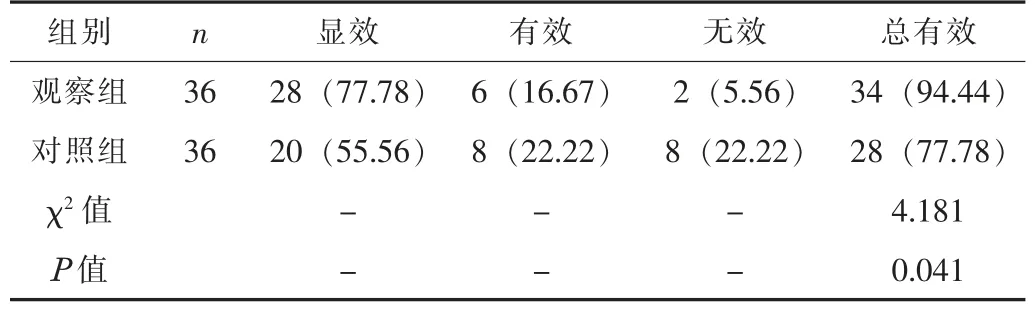
表2 两组的疗效比较[n(%)]
2.3 并发症观察组的并发症发生率为8.33%(腹胀、肺炎、气胸各1例),显著低于对照组的27.78%(肺炎1例,皮下气肿、腹胀、气漏各2例,气胸3例),差异有统计学意义(P<0.05)。
3 讨论
HMD的发病机制多为PS不足所致的进行性肺不张,是早产儿死亡的重要原因。研究[5]显示,胎龄越小,HMD发病率越高。早产儿出现HMD时,及时展开治疗,是减少并发症、改善预后的关键。临床治疗HMD的重点为呼吸支持,主要采取监测SpO2、清除呼吸道分泌物、吸氧、机械通气等综合治疗方案,其中重要措施为吸氧和机械通气,有助于改善肺顺应性和肺通气功能。NCPAP是无创通气疗法,可通过压力控制通气,维持患儿整个呼吸周期内正压,避免肺泡坍塌;自带加温湿化功能有助于呼吸道水分的维持,保证呼吸道完整性。但需维持SpO2和FiO2在安全范围,二者过高将分别导致视网膜病变和支气管肺发育不良。
在HMD的发病原因中,PS缺乏占主要地位,肺泡和空气的接触存在张力,肺泡表面缺乏充分的活性物质时,肺泡被压缩,引发肺不张,患儿呼吸困难,且有同时引发多种并发症的风险,导致早产儿死亡,因此需补充PS[6]。伴随PS替代疗法的成熟,PS逐渐成为临床治疗HMD的重要药物。临床较常用的外源性PS为猪肺磷脂注射液,主要成分为磷脂,具有多重生物活性和生理功能,可在扩张肺泡的同时,改善血气指标和呼吸机参数,从而有助于HMD患儿呼吸功能的恢复。但外源性PS不完全同于内源性PS,由于肺泡内多种物质的灭活作用,外源性PS随呼吸逐渐消耗后,为避免呼吸窘迫症状加重,需重复或大剂量给药。有研究[7]显示,NCPAP联合PS治疗HMD时具有协同作用,一方面可维持患儿肺泡表面积,发挥PS药效;另一方面,能有效抑制灭活作用,延长PS作用时间。
本研究结果显示,联合治疗的观察组总有效率较高,治疗24 h后的血气指标PaCO2和PaO2改善显著,即PS可有效改善换气,促进氧合。分析原因为,PS从病因入手,为患儿补充PS,改善肺泡和肺部功能;NCPAP着重于症状改善,作用于萎缩肺泡,改善通气效果。同时,联合PS治疗,缩短了呼吸机用时和氧暴露时间,在很大程度上有助于减少并发症。本研究中,联合治疗的患儿并发症发生率仅为8.33%,与相关研究[8]结果一致,提示NCPAP联合PS是治疗HMD安全高效的方案。
综上所述,NCPAP联合PS治疗早产儿HMD有助于提高疗效,改善血气指标,降低并发症发生率。
