补肾单味中药对绝经后骨质疏松症骨代谢信号通路调控机制的研究进展*
2021-10-13安方玉颜春鲁汪永锋贺娟娟吕学颖赵崇博蒋国凤
邓 婕,安方玉,颜春鲁,汪永锋,贺娟娟,吕学颖,赵崇博,蒋国凤
(1.甘肃中医药大学第一临床医学院,甘肃 兰州 730000; 2.甘肃中医药大学教学实验实训中心,甘肃 兰州 730000; 3.甘肃中医药大学中西医结合学院,甘肃 兰州 730000; 4.甘肃中医药大学基础医学院,甘肃 兰州 730000; 5.甘肃中医药大学中医临床学院,甘肃 兰州 730000)
世界卫生组织报道,骨质疏松症是一种以矿化骨组织减少、微结构骨组织恶化为特征的骨骼疾病,可导致骨质脆弱风险增加,骨折易感性增加[1]。骨质疏松症的发病率随着年龄的增长而增加,且最常发生于绝经后妇女,其主要病机可能是妇女绝经后,雌激素分泌缺乏而引发破骨细胞异常活跃,导致骨吸收障碍和整体骨丢失[2]。
对于绝经后骨质疏松症的治疗常采用激素替代疗法,但是长期的激素治疗会引发心脑血管疾病及各类癌症的发生,极大地影响了其临床疗效的发挥。因此,开发高效、安全、低毒、能有效预防过度骨丢失的新型药物迫在眉睫。如何降低绝经后骨质疏松症的发病率、提高临床治疗效果成为研究者关注的焦点。中医学将骨质疏松症归为 “骨枯”“骨痹”范畴,主要采用中药、针灸、推拿等治疗手段,取得了一定的临床疗效。治疗绝经后骨质疏松症时,根据中医学“肾主骨”理论,多选择补肾中药;但目前其治疗机制尚无详细总结,尤其是针对单味补肾中药的治疗机制总结更少。为此,本文通过总结近年来单味补肾中药对绝经后骨质疏松症骨代谢信号通路的调控机制,为补肾中药的临床应用提供理论依据。
1 绝经后骨质疏松症的治疗现状
绝经后骨质疏松症有多种治疗手段,包括标准治疗和其他疗法。标准治疗常用膳食钙和维生素D,其他疗法主要采用双磷酸盐、选择性雌激素受体调节剂(selective estrogen receptor modulators,SERM)、雌激素和甲状旁腺激素类似物。这些疗法虽然能显著降低骨折发生率,但对非脊椎骨折的疗效有限,且不良事件的发生限制了其应用[3]。使用中草药治疗绝经后骨质疏松症疗效良好,成本更低,副作用少。近年来,临床大力提倡中医诊治及中西医联合治疗,以减少单纯西药治疗的不良反应。以“肾藏精”“肾主骨”为理论支撑,补肾壮骨法成为治疗绝经后骨质疏松症的有效方法,得到了许多学者的认可。
2 绝经后骨质疏松症骨代谢相关信号通路
2.1 Wnt 基因(Wnt)/β连环蛋白(β-catenin)信号通路
Wnt信号通路通过促进骨形成、抑制骨吸收从而重建骨平衡,对骨骼发育和骨形成有着至关重要的作用,与骨质疏松的发生与发展密切相关。Wnt信号通路分为经典和非经典两大类,参与骨质疏松发生、发展的主要是经典的Wnt 信号通路。
经典的Wnt 信号通路由Wnt配体、Wnt受体、卷曲蛋白Frizzled 家族跨膜受体蛋白(frizzled,Frz)和低密度脂蛋白受体相关蛋白5/6(low density lipoprotein receptor related protein 5/6,LRP 5/6)共同组成[4]。β-连环蛋白(β-catenin)作为Wnt 信号通路的开关控制器,通过调节Wnt 信号通路的β-catenin进一步控制相关基因的转录。Wnt与Frz结合形成的复合物促进了LRP的磷酸化,磷酸化的LRP促使糖原合成激酶3β(Glycogen synthesis kinase-3β,GSK-3β)的解体,从而促进了β-catenin的稳定和积累。积聚在细胞质中的β-catenin会向细胞核中移动并在细胞核中与淋巴增强因子/T细胞因子(lymphatic enhancement factor/T-cell factor,Lef/Tcf)相互作用,最终Lef/Tcf转录因子激活使成骨细胞特异性基因得以表达[5]。此外,Wnt 信号通路的胞外调制器主要包括两种类型的天然抑制剂,一种是Wnt抑制因子1(Wnt inhibitory factor 1,WIF1),能够结合并中和Wnt蛋白,溶解Frz受体,阻止Wnt与其受体结合;另一种为拮抗蛋白Dickkopf(DKK)和硬化蛋白(recombinant sclerostin,SOST),能与Wnt配体竞争性的结合Wnt受体,从而阻断该通路。其中,SOST几乎只能表达于骨细胞中,不仅抑制成骨细胞的形成还具有破坏骨的作用;但其明确的作用机制尚未阐明,有待于进一步的研究[6]。相关研究发现,骨质疏松组中骨组织的Wnt-3a的表达明显降低[7],去势骨质疏松大鼠骨组织中拮抗蛋白Dickkopf相关蛋白1(Dickkopf related protein 1,DKK1)基因表达的减少,可减轻骨量和相关生物力学的损失[8]。樊萍通过研究发现,DKK1可抑制Wnt/β-catenin信号通路,并与β-连环蛋白的表达呈负相关,这为早期临床通过针对DKK1的靶向治疗预防绝经后骨质疏松提供了一定的理论支撑[9]。最新研究[10]发现:成骨细胞中长链非编码RNA Crnde的过表达促进了成骨细胞的增殖;反之,Crnde的低或不表达抑制了成骨细胞的增殖。Crnde的这一调节作用可以通过Wnt/β-catenin信号通路来实现,并同时调节骨形成。这表明Crnde是骨质疏松症的一种新的骨代谢调节因子。因此,笔者推测,可以通过促进Crnde的表达来治疗骨退行性疾病。此为临床治疗提供了一定的思路。此外,有学者研究发现,富含亮氨酸的重复序列包含G蛋白偶联受体6(leucine-rich repeat-containing G-protein coupled receptor 6,LGR6)高度表达于成骨细胞的祖细胞,促进骨生成,并且能够增强β-catenin的稳定性,从而加强Wnt信号通路[11]。由此,通过调控Wnt信号通路中的相关蛋白Wnt、DKK-1、β-catenin、SOST、Crnde和LGR6的表达可达到预防与治疗骨质疏松的目的,尤其是最新发现的Crnde可能是未来补肾中药筛选的有效靶点。
2.2 骨保护素/核因子κB受体激动子/核因子κB受体激动子配体信号通路
中医学多从脾肾两方面对骨调节机制进行研究,骨保护素(osteoprotegerin,OPG)/核因子κB受体激动子(receptor activator of nuclear factor κB,RANK)/核因子κB受体激动子配体(receptor activator of nuclear factor κB ligand,RANKL)信号通路的发现开创了中医研究骨质疏松的新纪元[12]。该通路主要是由OPG、RANK和RANKL组成,RANKL与其破骨细胞前体上的受体RANK结合,招募肿瘤坏死因子(TNF)受体相关因子,而这些因子是衔接蛋白和泛素连接酶,调节NF-κB、JNK、c-Fos、NFATc1-ERK、p38、NFATc1和AKT信号,从而控制正常和病理性骨吸收中破骨细胞的形成和活性[13]。 RANK与RANKL结合能够加速骨吸收,RANK是破骨细胞表达的天然受体;OPG作为诱饵受体能够阻断RANK和RANKL的结合,致破骨细胞的增殖、活性等均有所下降,进一步促进其凋亡[14]。
在人体内,成骨细胞和破骨细胞在多种作用因子的耦连作用下使人体维持骨平衡。破骨细胞的生长需要核受体激活剂NF-κB受体活化因子和成骨细胞分泌蛋白。除此之外,成骨细胞能够分泌破骨细胞生成抑制因子或诱饵受体[15]。有学者[17]对补肾OPG/RANKL/RANK信号通路干预激素性股骨头坏死进行了实验研究,结果发现激素性股骨头坏死模型小鼠RANK和RANKL表达均上调,OPG表达下调,从而有效地缓解绝经后骨质疏松症的症状。另有学者也发现,骨质疏松模型鼠RANK和RANKL表达的上调和OPG表达的下调[17]。可见,通过调节RANKL诱导的信号通路来抑制破骨细胞的形成是治疗绝经后骨质疏松症等与破骨细胞相关疾病的一种可行的治疗策略。
3 补肾单味中药治疗绝经后骨质疏松症骨代谢信号通路的调控机制
3.1 单味中药淫羊藿和杜仲对骨代谢Wnt/β-catenin信号通路的调控机制研究
淫羊藿最早收载于《神农本草经》,历史悠久,成分复杂,有效成分主要为淫羊藿苷、朝藿定 A、朝藿定 B、 朝藿定 C、淫羊藿次苷Ⅰ、宝藿苷Ⅰ和宝藿苷Ⅱ等黄酮类成分[18],以骨保护作用为主的活性成分主要是淫羊藿苷。周先进等[19]研究发现,淫羊藿苷主要通过上调成骨细胞β-catenin 及Runx2 等成骨基因的表达来促进成骨细胞的增殖与分化,进一步促进骨的生长。涂艳等[20]研究发现,淫羊藿苷也可提高骨髓间充质干细胞(bone marrow mesenchymal stem cells,BMSC)GSK-3、LEF-1的水平,通过进一步激活Wnt/β-catenin信号通路来促进BMSC的成骨分化。Wei等[21]研究指出,0.1 μmol/L淫羊藿苷能显著提高碱性磷酸酶(alkaline phosphatase,ALP)的活性,同时还可以显著上调成骨基因(Runx2、osteopotin、DLX5、骨钙素、Ⅰ型胶原和ERα)和Wnt信号分子(β-catenin、Lef1、TCF7、c-jun、c-myc和cyclin D)的表达。淫羊藿苷也可以通过刺激β-catenin的活化来促进β-catenin的核移位。尹素娟[22]研究发现,淫羊藿可通过上调Wnt/β-catenin信号通路中Lrp6受体mRNA的表达,增加GSK-3β mRNA的磷酸化,使得更多的β-catenin在细胞核中积累,从而激活Wnt/β-catenin信号通路,刺激Wnt/β-catenin信号通路下游靶基因Runx2 mRNA表达。据此推测,淫羊藿对成骨细胞增殖和分化的调控主要是通过激活Wnt/β-catenin信号通路的成骨细胞调控基因Runx2、osteopotin、DLX5、骨钙素、Ⅰ型胶原、β-catenin、Lef1、TCF7、c-jun、c-myc和cyclin D等实现的。
杜仲有补肝肾、强筋骨之功效,性微甘,味辛温,是我国名贵的滋补药材[23]。现代研究表明,杜仲可改善骨微观结构,增加骨密度,促进骨形成[24]。李三华等[25]通过实验研究了杜仲总黄酮对去卵巢大鼠骨代谢的影响,结果表明,雌激素缺乏的大鼠骨形成的能力低于骨吸收,杜仲总黄酮有抑制骨吸收、促进骨形成的作用。赵亮等[26]通过研究盐炙杜仲对去卵巢骨质疏松大鼠骨代谢生化指标的影响发现,高剂量杜仲可提高绝经后骨质疏松大鼠血清中碱性磷酸酶(alkaline phosphatase,ALP)和成骨细胞中酸性蛋白的表达,降低血清抗酒石酸酸性磷酸酶(tartrate resistant acid phosphatase,TRACP)的表达,发挥加速骨形成的作用,对绝经后骨质疏松具有一定的治疗作用。同时,骆瑶等[27]的研究表明,杜仲提取物可显著升高血清中雌二醇的表达,从而有效改善骨密度和骨小梁微结构,发挥对绝经后骨质疏松大鼠的骨保护作用。此外,杜仲还可与熟地黄、枸杞子等中药联合使用,在绝经后骨质疏松的治疗中共同发挥补益肝肾的效用。因此,杜仲对骨形成的调控作用可能是激活Wnt/β-catenin 信号通路中促成骨形成因子Wnt-3a、β-catenin及ALP、雌二醇、酸性蛋白、TRACP的表达来发挥作用。
综上所述,淫羊藿和杜仲都是通过激活Wnt/β-catenin信号通路的促成骨形成因子的表达从而加速了骨形成,显著改善了绝经后骨质疏松骨微结构的破坏,促进了绝经后骨质疏松的骨重建而发挥治疗作用。
3.2 单味中药蛇床子、淫羊藿、巴戟天对骨代谢OPG/RANK/ RANKL信号通路的调控机制研究
中药蛇床子性苦而温,《本草从新》载其有 “强阳益阴,补肾祛寒,祛风燥湿”的功效,可防治骨质疏松。沃小敏等[28]报道,蛇床子可以通过促进OPG的基因表达和抑制RANKL的基因表达来提高OPG/RANKL的比值,从而抑制破骨细胞的分化、增殖,减少骨吸收,进一步降低骨质疏松症的发生,并在一定程度上延缓了骨质疏松的发展。赵永见等[29]通过观察不同剂量蛇床子素对 OPG 基因敲除小鼠骨代谢的影响发现,不同剂量蛇床子素可以提高OPG 基因敲除小鼠的BMD,并增加骨小梁的厚度、降低骨小梁的分离度,以中剂量最为显著。研究表明,佛手苷内酯来源于蛇床子属植物,是一种香豆素衍生物,通过减少RANKL诱导的破骨细胞生成和骨吸收来抑制绝经后骨质疏松,而没有任何细胞毒性。这些抗吸收作用和抗破骨细胞的特性表明,佛手苷内酯是预防或治疗绝经后骨质疏松症的一个有效的候选药物[30]。因此,蛇床子的治疗机制主要是通过提高OPG,降低RANKL的表达来增加骨密度,调节骨代谢,从而治疗骨质疏松症及疼痛等并发症。
淫羊藿性温味苦,归肝肾经,具有补肾阳、强筋骨、祛风湿之效。研究表明,淫羊藿黄铜提取物具有类雌激素作用,可用于有效治疗绝经后骨质疏松[31]。淫羊藿苷是淫羊藿的主要活性成分,淫羊藿苷可抑制脂多糖(lipopolysaccharide,LPS)诱导的骨吸收和白细胞介素-6及肿瘤坏死因子-α的表达,同时可上调OPG基因表达和下调RANKL的基因表达,还可抑制LPS介导的破骨细胞p38丝裂原活化蛋白激酶(p38 mitogen-activated protein kinase,p38 MAPK)和c-Jun氨基末端激酶(c-Jun N-terminal kinase,JNK)的激活,降低LPS诱导的成骨细胞细胞外调节蛋白激酶(extracellular regulated protein kinases1/2,ERK1/2)和核因子κB的抑制蛋白α(inhibitor α of NF-κB,I-κB α)的激活,从而被称为天然抗骨质疏松的药物[32]。此外,淫羊藿中两种同分异构体黄酮CIT和IT对骨质疏松大鼠有治疗作用。其中,CIT主要作用是上调OPG,下调RANKL,降低血清AKP和TRACP水平,异构化黄酮(CIT/IT)与OPG/RANKL靶点的联合作用减弱了OPG或RANKL对RANKL的激发作用。由于CIT与RANKL的结合比IT更牢固,所以CIT通过抑制骨吸收而具有更强的抗骨质疏松作用[33]。吴峻[34]采用淫羊藿苷对去卵巢大鼠进行干预,结果发现,淫羊藿苷不仅可以增加骨密度和骨矿含量,还可以显著上调骨组织中OPG mRNA的表达并下调RANKL mRNA、RANK mRNA的表达,从而调节成骨与破骨的骨平衡,在一定程度上缓解了绝经后骨质疏松症的疼痛,有一定的治疗作用。研究表明,淫羊藿苷可以抑制RANKL诱导的破骨细胞转录因子c-Fos和活化T细胞核因子1(nuclear factor-activated T cell 1,NFATc1)的表达,抑制下游破骨细胞特异性标记物[35]。 综上所述,淫羊藿苷通过抑制NF-κB和MAPK活化来实现对RANKL诱导的破骨细胞的形成和功能的抑制。这些发现表明其有效成分淫羊藿苷有望成为未来治疗骨质疏松症的有效药物。
《神农本草经》记载,巴戟天“主大风邪气,阳痿不起,强筋骨,安五脏,补中益气”,具有补肾壮阳、强筋健骨、祛除风湿等功效[36]。林华芳等[37]发现,巴戟天可以通过抑制去势大鼠骨组织中 RANK、活化 T 细胞核因子信号通路2(NFAT2)和空泡型 V-ATP酶(V-ATP)mRNA的表达从而抑制破骨细胞的增殖,减少去势大鼠的骨丢失。胡英勇等[38]通过观察巴戟天提取物对去势大鼠骨质疏松症的防治作用发现,巴戟天可提高去势骨质疏松症大鼠骨密度、骨钙含量及血清中雌二醇的表达,推测其可通过调节激素水平从而改善骨质疏松。郑德开等[39]发现,巴戟天对骨质疏松的治疗通过调控OPG/RANK/RANKL信号通路中OPG水平的升高、RANKL水平的降低来发挥促进成骨抑制破骨的作用。杨博辰等[40]通过研究巴戟天与雌激素对骨质疏松大鼠破骨细胞 RANK 和 碳酸酐酶Ⅱ(carbonic anhydrase Ⅱ,CAⅡ)的表达,发现巴戟天与雌激素对CAII、RANK mRNA的表达具有显著的抑制作用,使破骨细胞水平降低,有效减少骨吸收。Bao等[41]通过研究巴戟天蒽醌类化合物体外抑制破骨细胞骨吸收发现,巴戟天有效成分蒽醌对RANKL诱导的NF-κB和JNK的磷酸化有明显的抑制作用,从而降低RANKL的表达,提高OPG/RANKL的相对比值,有效缓解绝经后骨质疏松症。因此,笔者推测,巴戟天对于绝经后骨质疏松的防治作用主要是通过激活OPG/RANK/RANKL通路中促成骨因子OPG的表达、抑制RANKL、CAII的表达来有效缓解绝经后骨质疏松引起的骨丢失。
综上所述,蛇床子、淫羊藿、巴戟天等补肾单味中药抗绝经后骨质疏松的共同机制是通过激活OPG/RANK/RANKL信号通路中OPG的表达,抑制其通路中RANKL的表达,最终使OPG/RANKL比值降低,进而抑制破骨细胞的增殖和促进成骨细胞的分化,从而促进骨质疏松的骨形成和抑制其骨破坏。
4 小 结
近年来,随着绝经后骨质疏松发病机制研究的不断深入,国内外对信号通路机制的研究也逐步引起重视,以信号通路为靶点的补肾中药疗效筛选将是今后研究的重点。本综述发现,影响绝经后骨质疏松骨代谢的信号通路主要是Wnt/ β-catenin信号通路和OPG/RANK/RANKL信号通路。通过激活或抑制上述信号通路中的关键蛋白,可有效防治绝经后骨质疏松症。此外,本综述也发现,补肾单味中药在治疗绝经后骨质疏松中也可通过调控Wnt/β-catenin信号通路的关键蛋白Wnt、DKK、β-catenin、SOST、Crnde、Runx2、LGR6的表达,OPG/RANK/RANKL信号通路的关键蛋白OPG、RANK、RANKL的表达,从而促进成骨细胞形成、增殖和分化,达到防治绝经后骨质疏松症的目的(见图1)。但是鉴于中药作用方式的多样性、多器官性及多靶点性等特点,上述补肾单味中药对信号通路的调控究竟以哪条为主、哪条为辅,以及这些信号通路之间是否存在交互作用,这也将成为未来研究的方向。
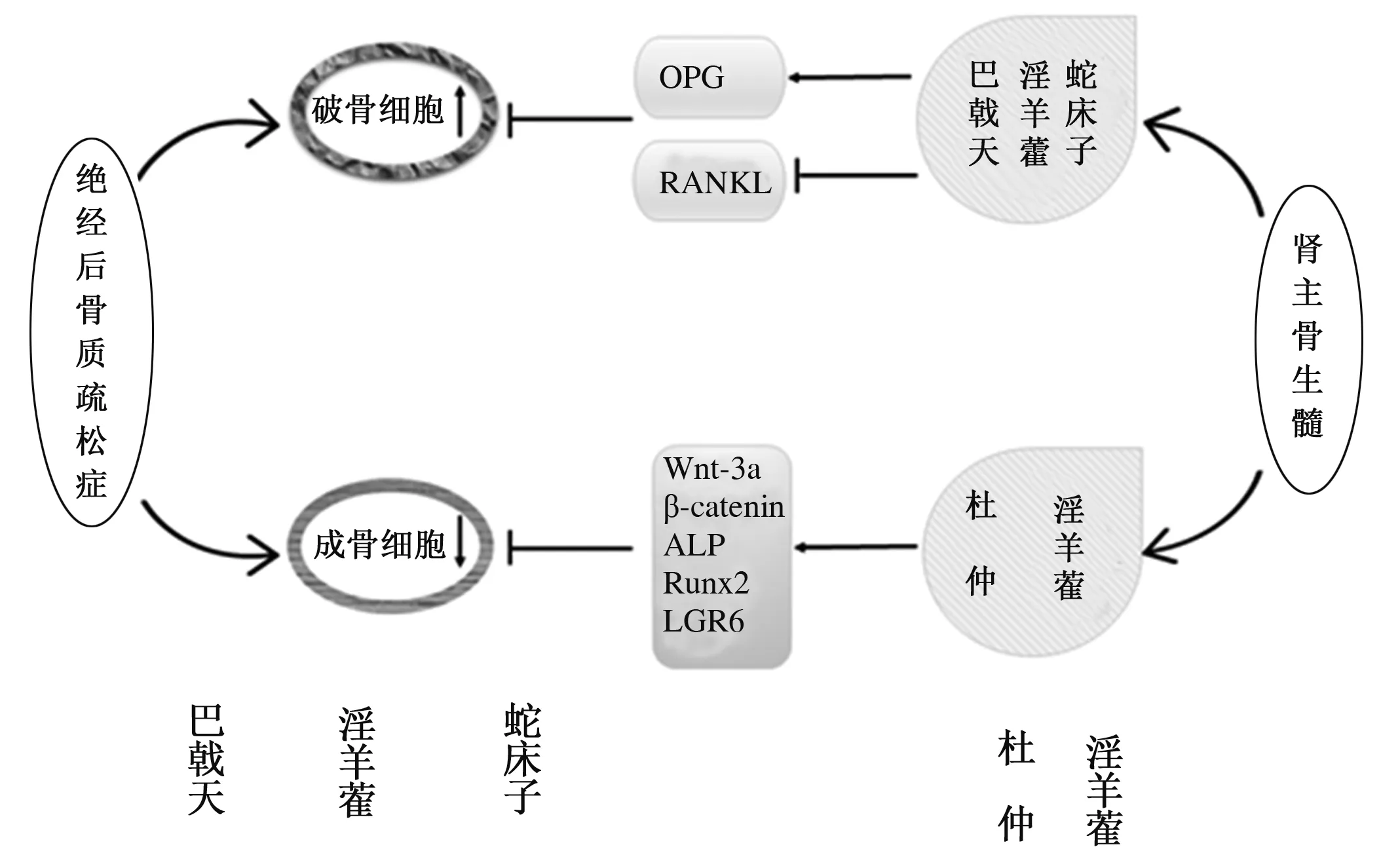
图1 补肾单味中药抗绝经后骨质疏松的作用机制
