示踪用盐酸米托蒽醌注射液用于甲状腺癌前哨淋巴结示踪的临床疗效、安全性及药代动力学Ⅰ期试验
2021-10-12陈少博刘玮楠张圣洁王淑君
陈少博,刘玮楠,张圣洁,孙 健,杨 瑞,王淑君,陈 革
中国医学科学院 北京协和医学院 北京协和医院 1外科 2基本外科 3手术室 4病理科,北京 100730沈阳药科大学 5中药学院 6药学院, 沈阳 110000
甲状腺癌是内分泌系统和头颈部肿瘤中最常见的恶性肿瘤[1]。2015年甲状腺癌发病数为20.1万,发病率为14.6/10万,中标率为12.05/10万,城市人群的发病率高于农村人群(19.59/10万比8.24/10万),女性高于男性(29.29/10万比9.80/10万)[2]。目前,甲状腺癌最主要的治疗手段为手术切除,基本原则为整块切除肿瘤组织和/或联合中央区淋巴结清扫[3]。前哨淋巴结(sentinel lymph node, SLN)是原发肿瘤淋巴途径转移经过的第一站淋巴结[4],将其切除后活检,以此判断区域淋巴结是否存在转移的诊断技术即为前哨淋巴结活检(sentinel lymph node biopsy, SLNB)。理论上,若SLN阴性,其他淋巴结亦应为阴性;若SLN阳性,第2站及更远的淋巴结亦存在肿瘤转移的可能性。由于淋巴结通常隐匿于脂肪组织,与大血管伴行,术中视野受到影响,彻底清除引流的淋巴结十分困难[5]。
淋巴示踪剂可在注射人体后聚集于淋巴组织内,对淋巴组织具有标记及定位作用[6- 7]。术中使用淋巴示踪剂将活体淋巴结染色进行示踪、标记,有助于彻底摘除淋巴结,提高恶性肿瘤治疗效果。目前,淋巴示踪方法主要包括蓝染法、黑染法、放射性核素示踪法、联合法以及荧光显像技术。蓝染法使用的染料主要为亚甲蓝,其可对甲状旁腺进行染色、造成误切,不推荐亚甲蓝用于甲状腺手术[8]。黑染法使用的主要染料为纳米活性炭[9],其对甲状旁腺具有保护作用,但注射剂量难以把握,剂量过多或过少均达不到示踪目的[10]。放射性核素示踪法因其设备贵、耗时长、操作过程复杂,且核素物质具有放射性而难以推广应用。荧光探测法设备较昂贵、操作过程相对复杂,亦难以普遍推广。另一方面,上述所有淋巴示踪方法均未获得监管机构批准的甲状腺领域应用适应证[4]。因此,亟需寻找一种具有甲状腺领域适应证且患者可及性强、使用方便的淋巴示踪剂。
示踪用盐酸米托蒽醌注射液具有高度淋巴结靶向性,其经腺体给药后,通过组织间隙渗透进入毛细淋巴管并富集于区域淋巴结,将淋巴结染成蓝色,以达到淋巴结示踪目的[11]。本研究旨在评价示踪用盐酸米托蒽醌注射液用于甲状腺癌根治术中对淋巴结的染色、示踪效果,并探究其安全性和耐受性。
1 对象与方法
1.1 研究对象及分组
1.1.1 研究对象
本研究釆用单中心、开放、空白对照试验设计,按剂量递增原则,逐剂量组进行人体耐受性试验和药代动力学试验。前瞻性纳入2016年12月至2017年3月北京协和医院拟行甲状腺癌根治术的患者为受试者。
纳入标准:(1)用药前临床诊断为甲状腺癌;(2)根据术中探查,手术方式为甲状腺叶全切除+中央区淋巴结清扫术;(3)年龄18~65岁,性别不限,但单性别例数不得少于受试者总数的1/3;(4)体质量指数≤28 kg/m2;(5)无手术禁忌证;(6)了解本研究内容,且签署知情同意书。
排除标准:(1)妊娠或哺乳期女性;(2)有严重药物过敏史或对本研究药物过敏者;(3)合并有心血管、肝脏、肾脏及血液系统严重原发疾病者;(4)合并精神疾病者;(5)酒精、镇静药物依赖或有本类药物使用史者;(6)给药前3个月内参与其他临床试验者;(7)存在其他特殊情况,研究者认为不适合进行试验者。
退出标准:(1)受试者自愿退出;(2)不遵守本试验安排;(3)术中发现疾病与用药前判断不符者;(4)发生严重药物过敏反应者;(5)医师认为受试者需退出试验者。
1.1.2 分组
将受试者分为空白对照组和试验组(受试者按照入组顺序依次进入各剂量组)。空白对照组进行常规手术,不注射示踪剂;试验组由低至高依次进行5个剂量组的爬坡试验,拟分别注射0.2 mL、0.4 mL、0.6 mL、0.8 mL、1.2 mL示踪用盐酸米托蒽醌注射液(沈阳鑫泰格尔医药科技开发有限公司,规格2 mL∶10 mg,批号:151001)。
本研究已在临床试验登记与信息公示平台登记(登记号:CTR20160376),已通过北京协和医院药物临床试验伦理审查委员会审批(审批号:HS2016131)。
1.2 研究方法
1.2.1 耐受性试验
试验组注射示踪用盐酸米托蒽醌注射液,起始剂量定为0.2 mL,最大剂量为1.2 mL。注射方法:暴露术野后,取本药物用皮试针头在甲状腺腺体上分2~6处注射,每处注射0.1~0.2 mL,缓慢注射(约3 min完成)。给药后(14±3)d内完成安全性评价,确定安全后方可进行下一个剂量组试验。每位受试者仅接受1个剂量组的试验,不得同时进行2个及以上剂量组的试验。出现较重不良反应(Ⅲ级不良反应,影响日常生活,需停用试验药物)或半数受试者岀现轻度不良反应(Ⅰ级不良反应,无需处理)或受试者注射部位对药物注射剂量承载达饱和,即使未达最大剂量组,均需终止试验。
1.2.2 药代动力学试验
在给药前及给药后10 min、20 min、30 min、60 min、90 min、120 min,分别采集受试者静脉血4 mL,测定其血药浓度,计算药代动力学参数。
1.3 临床疗效评定
(1)主要观察指标为淋巴结示踪率和淋巴结染色率。淋巴结示踪率=(染色的淋巴结总数/染色的组织块总数)×100%,其中染色的组织块包括染色的淋巴结及染色的非淋巴组织(注射部位除外)。淋巴结染色率=(染色的淋巴结总数/清除的淋巴结总数)×100%。
(2)次要观察指标为淋巴结染色程度评分和示踪持续成功率。淋巴结染色程度评分标准:① 0分:淋巴结颜色无改变;② 0.5分:可见淋巴结或边缘窦轻度或部分蓝染;③ 1分:可见整个淋巴结深度蓝染,呈深蓝色甚至黑色。示踪持续成功率为注射示踪剂后染色至手术结束时尚未褪色的淋巴结占染色淋巴结总数的百分比。
1.4 安全性、耐受性评价
观察受试者注射药物后生命体征、临床症状、实验室检查指标等变化以及有无不良事件发生,确定最大耐受剂量及安全剂量范围。
1.5 统计学处理
釆用SAS 9.13软件进行统计学分析。由于样本量较小,淋巴结示踪率、染色率以均数表示,组间比较采用单因素方差分析或t检验;药代动力学参数以均数±标准差表示。计数资料以百分数表示,组间比较采用卡方检验或秩和检验。双侧检验,以P<0.05差异有统计学意义。
2 结果
2.1 一般资料
共纳入27例甲状腺癌受试者,其中空白对照组3例;试验组0.2 mL、0.4 mL、0.6 mL、0.8 mL、1.2 mL 5个剂量组分别为3例、3例、6例、6例、6例。当试验进行至第3个剂量组(0.6 mL)时,受试者注射部位对药物注射剂量承载达饱和,根据试验方案,需终止试验,故实际共15例受试者完成试验。其中空白对照组男性1例,女性2例;年龄(46.33±9.02)岁;体质量指数(25.17±1.63)kg/m2。试验组男性7例,女性5例;年龄(41.23±7.84)岁;体质量指数(24.48±3.03)kg/m2。
2.2 临床疗效
空白对照组均未出现淋巴结染色。试验组中,12例受试者中央区淋巴结全部染色,部分侧颈部淋巴结也出现染色(颈部2、3、4区淋巴结),甲状旁腺不被染色、呈负显影(图1)。0.2 mL、0.4 mL、0.6 mL剂量组分别为2、4、6处注射(每处注射0.1 mL),给药前后淋巴结染色程度评分率(给药前淋巴结染色程度评分为0)有显著差异(P<0.05)(表1)。平均淋巴结染色率分别为90.47%、91.67%、91.36%,平均淋巴结示踪率分别为79.17%、100%、98.67%,3个剂量组之间平均淋巴结染色率、平均淋巴结示踪率均无显著性差异(P均>0.05)。对淋巴结直径进行分级后,0.2 mL、0.4 mL、0.6 mL剂量组对不同直径的平均淋巴结染色率均无显著差异(P均>0.05)(表2),提示0.2~0.6 mL的示踪剂对癌灶引流淋巴结均具有良好的染色和示踪作用。
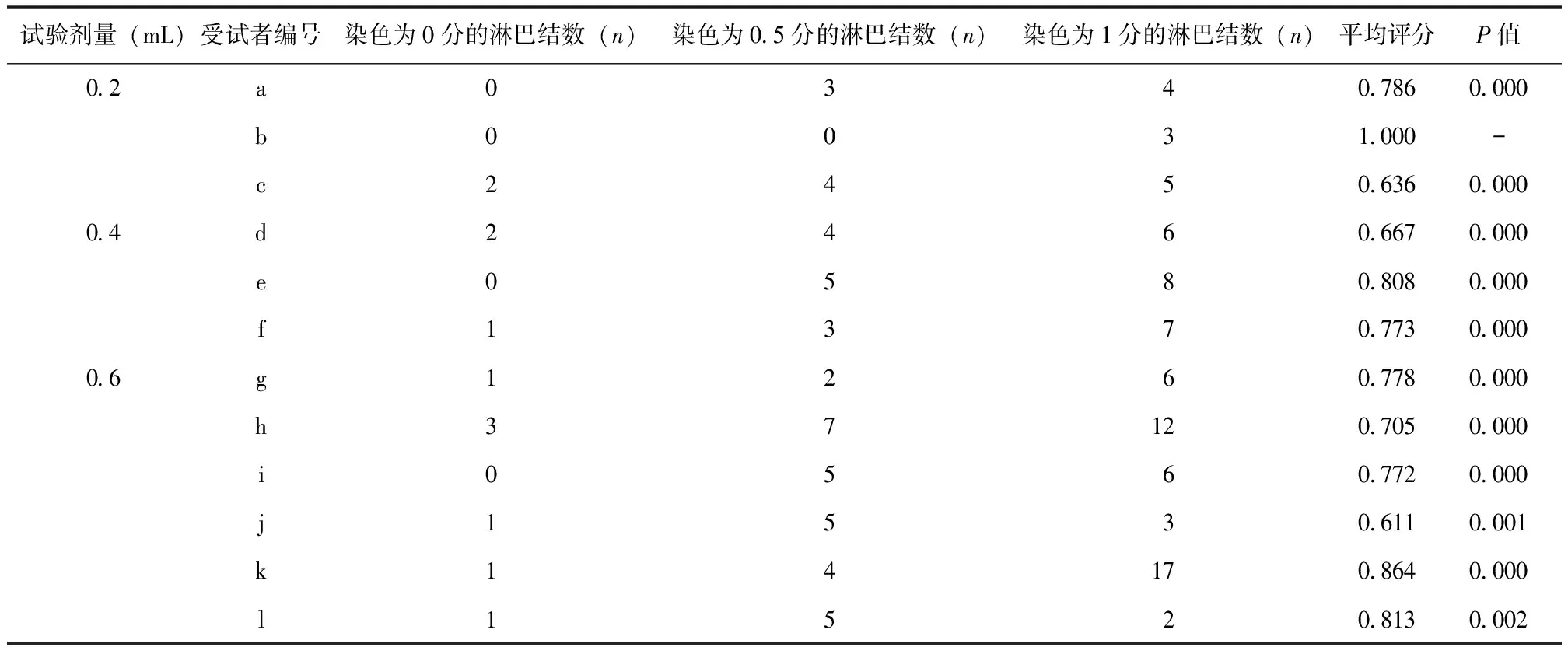
表1 不同剂量试验组淋巴结染色程度评分#

表2 不同剂量试验组不同直径淋巴结染色率(%)
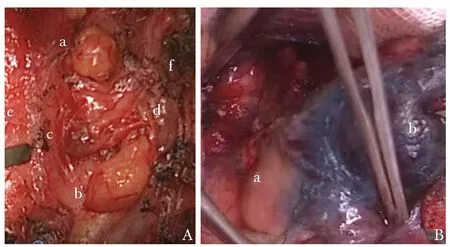
图1 示踪用盐酸米托蒽醌注射液辅助甲状腺切除手术示意图A.甲状腺切除后进行中央区淋巴结清扫时(e为颈总动脉,f为气管),可清楚区分未染色的甲状旁腺(a、b)以及染色的淋巴结(c、d); B.术中可清晰区分未染色的甲状旁腺(a)及染色的甲状腺(b)
试验组中,12例受试者的淋巴结清扫持续时间为5~20 min,注射示踪剂至淋巴结清扫结束,均未出现染色淋巴结褪色,示踪持续成功率为100%。
2.3 安全性评价
15例受试者,共4例出现不良事件,其中试验组3例、对照组1例;主要表现为麻木、大汗、实验室数据异常(如低血钙、感染等),两组均未出现严重不良事件,且不良反应发生原因与该示踪剂肯定无关。试验组不良事件发生率与对照组无显著性差异(25.0%比33.3%,P=0.770)。提示甲状腺癌根治术中使用0.2~0.6 mL示踪用盐酸米托蒽醌注射液安全性、耐受性好。由于0.6 mL剂量药物已达到饱和,无法计算最大耐受剂量。
2.4 药代动力学参数
给药后血药浓度总体呈剂量依赖性关系。0.2 mL剂量组受试者不同时间点的血药浓度均低于定量下限(5 μg/L),无法进行药代动力学参数的计算。0.4 mL 剂量组与0.6 mL剂量组釆用DAS 2.1.1软件计算药代动力学参数,但由于各受试者血药浓度高于定量下限的时间点太少(2~3个时间点),无法进行拟合计算,故釆用梯形法估算不同受试者给药后的药时曲线下面积AUC0-120。另外,由于受试者血药浓度高于定量下限的时间点太少,无法采用房室模型拟合,并计算其他药代动力学参数。
0.4 mL、0.6 mL剂量组不同受试者的药物作用峰值时间Tmax(实测值)分别为(13±6)min、(10±0)min,药物的峰值浓度Cmax(实测值)分别为(9.95±2.62)μg/L、(9.72±3.07)μg/L,AUC0-120分别为(152±47)μg·min/L、(177±62)μg·min/L。本示踪剂经腺体注射给药后快速吸收,注射后10 min血液浓度达峰值并迅速消除,给药30 min后血浆中几乎完全消除,最高血药浓度为13.1 μg/L(图2)。
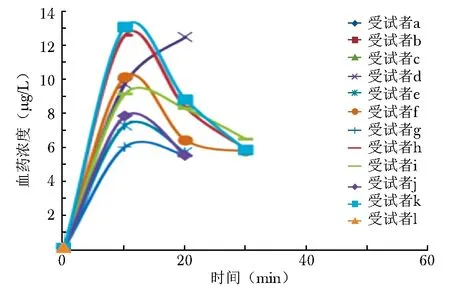
图2 示踪用盐酸米托蒽醌注射液经腺体注射给药后不同受试者药-时曲线
3 讨论
本研究结果显示,0.2 mL、0.4 mL、0.6 mL剂量组的平均淋巴结染色率分别为90.47%、91.67%、91.36%,平均淋巴结示踪率分别为79.17%、100%、98.67%。淋巴结清扫持续时间为5~20 min,3个剂量试验组的示踪持续成功率均为100%。安全性评价中,空白对照组和试验组均未发生严重不良事件,且不良事件发生原因与该示踪剂肯定无关。药代动力学试验显示,示踪剂经腺体注射给药后快速吸收,注射后10 min血液浓度达峰值(最高血药浓度为13.1 μg/L),并迅速消除。
甲状腺癌易发生淋巴结转移,特别是颈部淋巴结转移,甲状腺根治术中常需对局部淋巴结进行清扫,但由于淋巴结位置隐匿、显露困难,从而难以彻底摘除。目前常用的淋巴结示踪剂存在易误染甲状旁腺、剂量难以掌握或具有辐射、设备昂贵等局限性,临床应用受限。盐酸米托蒽醌为抗肿瘤药,主要用于恶性淋巴瘤、乳腺癌和急性白血病的治疗。示踪用盐酸米托蒽醌注射液为米托蒽醌与盐酸复合后形成均匀的酸性溶液,将复合液注射于组织间隙后,局部pH发生改变可使其逐渐析出纳米结晶,并难以通过毛细血管壁进入血液循环,可通过内皮细胞间隙和内皮细胞的胞饮及吞噬作用进入毛细淋巴管,然后通过淋巴引流作用富集于区域淋巴结,并暂时滞留在淋巴结中,最终将淋巴结染成蓝色,发挥淋巴结示踪作用。纳米结晶可阻止其通过毛细血管进入血液循环,从而仅靶向淋巴组织,因此减少了全身毒副反应。示踪用盐酸米托蒽醌处方中对药物渗透压进行了调节,使药物由组织间隙向淋巴管渗透得更快,不仅增强淋巴结染色效果,且安全性更高。
本研究为首次探讨示踪用盐酸米托蒽醌注射液在甲状腺癌根治术中对淋巴结的示踪作用及其安全性。结果显示,空白对照组均未出现淋巴结染色。试验组12例受试者中央区淋巴结均出现蓝染,甲状旁腺不被染色、呈负显影;给药后不同剂量试验组淋巴结染色程度评分均高于给药前,证实本品对区域淋巴结有显著的染色效果。3个剂量组的主要疗效指标平均淋巴结示踪率分别为79.17%、100%、98.67%,提示其示踪效果良好,对淋巴结具有较好的选择性,有助于术中探寻更多淋巴结,并摘除转移的淋巴结。3个剂量组平均淋巴结染色率均在90%以上,提示该示踪剂具有较好的淋巴结染色效果。本研究对淋巴结直径分级后发现,3个剂量组对不同直径淋巴结的染色率均无显著差异,进一步说明0.2~0.6 mL的示踪剂对癌灶引流淋巴结均具有良好的染色和示踪作用。
本研究淋巴结清扫持续时间为5~20 min,至手术结束,所有染色的淋巴结均未发生褪色,示踪持续成功率达100%,提示本示踪剂可满足淋巴清扫时长为20 min内的手术需求。甲状腺癌切除术中,淋巴结清扫所需时间一般较短,但对于不同经验水平的术者或不同病情的患者,淋巴结清扫时间存在差异,该示踪剂是否可满足在更长时长手术中的应用,有待在后期研究中进一步验证。
本示踪剂局部注射后,需在人体内环境中进行纳米晶体自主装,粒径逐渐变大,在此过程中有微量进入血液循环,组装完成后由于粒径变大,将不再进入血液循环。本试验检测的示踪剂最高血药浓度仅为13.1 μg/L,与Larson等[12]报道的急性白血病患者静脉滴注米托蒽醌10~12 mg/(m2·d)的达峰浓度(510±206)μg/L相比,本品Cmax显著偏小(仅为此文献报道的2.6%)。Stiff等[13]应用高剂量米托蒽醌对卵巢癌患者进行化疗,米托蒽醌静脉滴注给药最大耐受总剂量为75 mg/m2,该剂量下的AUC0-72 h为560~1700 μg·h/L,为本试验的135.5~411.3倍。本研究空白对照组和试验组均未发生严重不良事件,且不良事件发生原因与该示踪剂肯定无关,提示0.2~0.6 mL该示踪剂安全性较高,一般不会引起全身毒副作用。
本研究局限性:(1)未收集到试验组与空白对照组甲状旁腺损伤情况;(2)每个剂量组的样本数较少,确切结论需增大样本量进一步验证。
综上,0.2~0.6 mL示踪用盐酸米托蒽醌注射液在甲状腺癌根治术中具有良好的淋巴结染色性能,可准确对淋巴结进行示踪,而甲状旁腺不被染色,大幅度提高术者对甲状旁腺的有效辨识度,对甲状旁腺具有较好的保护作用。本品极微量入血,不产生全身毒副作用,具有良好的耐受性和安全性。
作者贡献:陈革、陈少博、刘玮楠、张圣洁、孙健负责撰写临床试验方案、受试者管理、给药、临床监护、采集生物样本、撰写总结报告等;陈少博负责撰写、修订论文;陈革负责研究设计;杨瑞负责药代动力学试验检测;王淑君负责示踪用盐酸米托蒽醌注射液药学研究。
利益冲突:无
