恶性血液病患者接受CAR-T细胞治疗后相关并发症的诊断及治疗研究进展
2021-10-08陈丹综述苏毅姚浩审校
陈丹 综述 苏毅,姚浩 审校
中国人民解放军西部战区总医院血液科,四川 成都 610083
嵌合抗原T (chimeric antigen T cell,CAR-T)细胞疗法常用于恶性血液病的治疗,作为新的治疗方式,其相关并发症的临床管理也面临着新的挑战[1]。CAR-T 细胞治疗的副作用包括细胞因子释放综合征(cytokine release syndrome,CRS)、神经毒性、肿瘤释放综合征和移植物抗宿主病(graft-versus-host disease,GVHD),以上症状均需住院治疗[2]。其中,CRS可分为中度至重度,中度患者在门急诊即可处理,而伴随多器官衰竭的重度副反应患者则需要转至重症监护室(ICU)进行治疗[2]。护理人员作为临床一线工作者,是较早发现和鉴别以上症状和患者状态急性改变的人员。因此,深入理解和认识该病的副作用及其临床表现和对应的处理策略,将会大大提高接受CAR-T细胞治疗患者临床治疗效果的安全性和有效性。本文对接受CAR-T 细胞治疗后发生中度至重度副作用的恶性血液病患者的临床管理进行了总结。
1 CRS
CRS是指外源输注的T细胞在体内开始扩增时被激活并释放大量细胞因子引发全身炎症反应后表现出的一系列症状,是导致接受CAR-T治疗患者需要住院治疗的主要因素[2]。根据症状严重程度不同,CRS可分为Ⅰ~Ⅴ级(表1),当患者发生CRS 时,体内白介素-6 (IL-6)会明显升高,同时会伴随IL-10 等其他细胞因子的表达量增高[3]。CRS的其他指标包括乳酸脱氢酶、C 反应蛋白(CRP)以及铁蛋白的升高,这些指标预示着炎症进展,而铁蛋白的升高则比较缓慢[2-3]。尽管这些指标不绝对反映CRS的严重程度,但可提示患者炎症反应的持续时间。CRS 的恶性程度与患者接受CAR-T治疗前的肿瘤负荷密切相关,越高的肿瘤负荷,其发生CRS的可能性越高。

表1 CRS分级标准
1.1 诊断发生CRS患者常常表现为高热,体温在38℃~40℃之间,可持续数天至数周。对乙酰氨基酚并不能缓解高热症状,高热患者常伴随心动过速和寒战等症状[4]。患者会表现出食欲减退、恶心和呕吐等症状,这些症状在其他CRS症状减轻的情况下还会持续数周,部分患者会出现肌肉疼痛和头痛症状[4-5]。以上症状一般在细胞输注的第二天开始出现,持续时间可从数天至数周(表1)。严重的CRS 症状包括血管渗漏综合征和低血压,常出现在细胞输注后第4~7天[2]。随着CRS 造成的炎症反应,毛细血管的高渗透性造成液体从血管渗至肺脏和间质组织中,从而造成血管内耗竭,最终会导致或加重已存在的低血压状况,以此往复的恶性循环会造成肺水肿,患者需要从鼻部插管提供呼吸支持[6]。CRS也可导致凝血酶原时间(PT)、部分凝血酶原时间(PTT)延长和纤维蛋白原水平降低等严重的凝血障碍[7]。也有患者会因凝血异常造成的严重出血等不常见情况。CRS 造成的炎症反应会引起血流动力学的改变,从而引起肾血流量减少、肾小球滤过率降低,最终会引起肾脏的急性损伤和肾衰[8]。肾衰可从中度(如肌酐轻度升高,引起药物清除困难)至重度(需要透析),而细胞因子产物的增多也会对肾小球造成直接损伤[6,8]。部分发生重度CRS反应的患者会出现巨噬细胞活化综合征或嗜血细胞淋巴细胞增多症的状况,患者表现出持续稳定高热、肝脾肿大、重度凝血障碍、铁蛋白、甘油三酯和转氨酶的升高等症状[4,9]。
1.2 治疗CRS 是由CAR-T 细胞在体内增殖和破坏CD19 阳性的恶性肿瘤细胞时产生的炎症反应[3-4,10]。CRS是可逆性的炎症反应过程,针对其治疗的主要原则是在控制相关症状的基础上对T细胞的活性和效率不造成影响,这就需要在对症治疗和保持CAR-T细胞功能之间找到合适的平衡点[11]。抗炎的同时会破坏T细胞对恶性肿瘤细胞的杀伤能力,但不处理又可能会导致多器官衰竭甚至死亡[2,5]。一线治疗方式常为对症治疗,如采用营养剂和止吐药来止吐,疼痛严重者需静脉输注阿片类药物止痛。患者出现血压降低时,在静脉补液后应尽快利用血管升压素进行治疗,从而最小化发生大面积肺水肿的风险。炎症反应会引起D-二聚体增加,在区别弥散性血管内出血后,可通过输注冷凝蛋白来维持纤维蛋白原水平在150 mg/dL以上,新鲜冷冻血浆可用来处理PT/PTT延长造成的凝血问题[5,7]。部分患者会需要输血来维持血小板的量在20×109以上,当合并出血时,该阈值要相应提高[2,4,7],当患者出现多器官衰竭时再采用其他治疗手段(表2)。
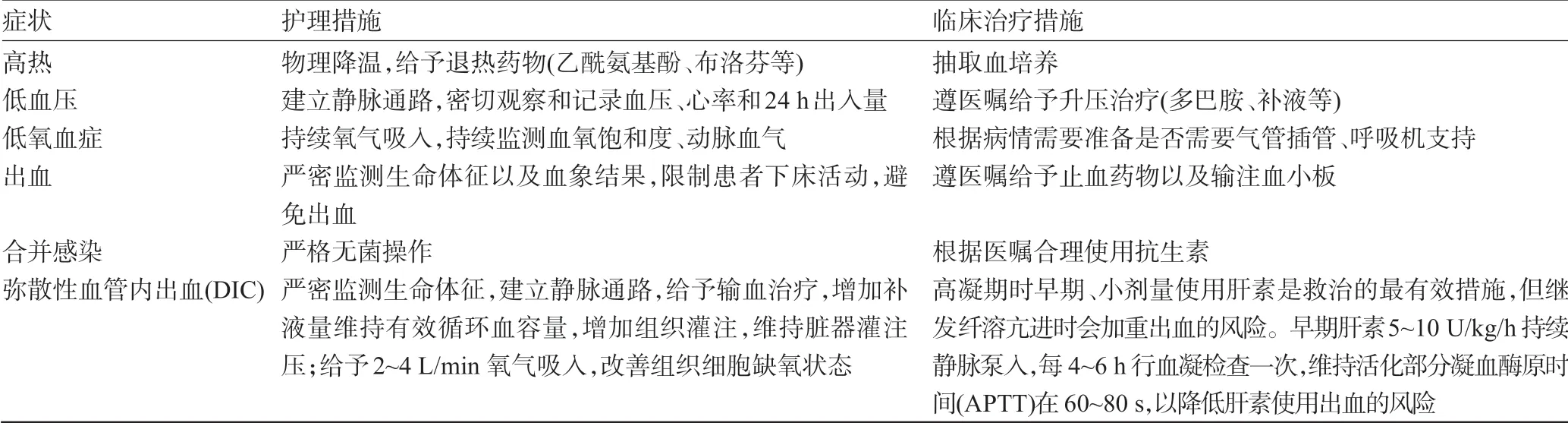
表2 CRS症状及临床管理措施
1.2.1 托珠单抗托珠单抗是靶向IL-6 受体的人源化单克隆抗体,当其与受体结合后,可阻止IL-6 与靶细胞的结合和炎症反应的产生,由于其不是直接作用于T 细胞,因此被认为对T 细胞功能无长期影响[12]。托珠单抗虽然具有很好的耐受性,但在部分极端病例中可导致肝脏转氨酶升高以及中性粒细胞减少症,因此在输注前可预防性给予患者对乙酰氨基酚和苯海拉明[2,5]。托珠单抗可迅速解决不适症状,用药后24~48 h可退热,之后很短的时间内血氧和血压即可恢复至正常水平[6]。托珠单抗的临床用药指征包括低血压以及心率加快、呼吸功能障碍和缺氧等呼吸状况恶化需要气管插管时[12]。
1.2.2 甲强龙甲强龙可直接抑制T细胞的活化从而减少炎症反应,由于其是直接作用于T细胞,因此使用后可能会影响CAR-T细胞的功能。因此,甲强龙只适用于针对托珠单抗等药物无效时才采用[5,11-12]。
2 神经系统症状
2.1 诊断CAR-T 细胞输注后会出现特殊性神经系统(central newous system,CNS)症状。无论患者是否出现神经系统症状,在患者脑脊液中均可检测到CAR-T 细胞,部分患者会出现独特的脑部疾病,如出现幻觉、意识混乱和谵妄等症状,发病虽然迅速,但持续时间较短,极个别患者会出现表现性失语,个别重度病例中患者由于重度CNS 反应会造成丧失意识数天[13](表3)。
2.2 治疗目前尚无逆转该神经系统症状的方法,只能对症治疗,所有患者均能得到缓解并且无长期影响。对第一批出现CNS反应的患者进行CT和核磁扫描以及腰椎穿刺检测,结果均未见异常,部分患者之前有出现过癫痫,后续可能会再次出现[10]。因此,本中心会评估有较高概率出现癫痫的患者在出现CNS时即预防性给予左乙拉西坦直至CNS症状得到缓解。另外,本中心有患者在治疗后第8天出现意识混乱和失语症状,具体表现为时间和地点的间歇性意识混乱。其症状包括表现性失语和表达含糊不清,具体监测时可以经常性检查神经系统检查及对时间及空间认知的恢复,以上症状持续至移植后16 d才完全恢复正常。
3 B细胞发育不良的诊断及治疗
靶向CD19 的CAR-T 主要针对表达CD19 的细胞,其中也包括正常的B细胞,因此,接受CART-19治疗的患者会出现B 细胞发育不良的症状[9]。B 细胞发育不良会由于B细胞产生免疫球蛋白的数量减少而导致低丙种球蛋白血症[14]。免疫球蛋白会识别异源蛋白,并启动免疫系统来清除它们。免疫球蛋白G (IgG)含有75%~80%的免疫球蛋白,患者可每个月静脉输注免疫球蛋白来维持IgG 水平在500 mg/dL,从而预防IgG 缺乏引起的感染风险[6,9](表3)。当患者出现B 细胞发育异常时,需要进行静脉输注免疫球蛋白来维持体内的免疫球蛋白水平。
4 肿瘤裂解综合征的诊断和治疗
肿瘤细胞的快速死亡会导致以高尿酸血症、高钾血症、高磷血症和低钙血症为表现的肿瘤溶解综合征,如果不及时处理,会引发急性肾功能衰竭[15]。对于肿瘤负荷较高的患者在进行CAR-T 细胞治疗前一定要特别重视,可给予别嘌呤醇,在治疗的同时需每天监测患者尿酸和电解质变化[5,15](表3)。

表3 CAR-T治疗不同副作用的临床管理
5 移植物抗宿主病的诊断和治疗
当移植的(供者)淋巴细胞识别受者为异源细胞时会导致免疫反应,即移植物抗宿主病(GVHD),其最主要的靶器官为皮肤(皮疹)、胃肠道系统(腹泻)和肝脏(高胆红素血症)[16]。对于异基因造血干细胞移植患者,特别是在接受CAR-T 细胞治疗前已经接受过造血干细胞移植的患者,要特别注意GVHD 的发生[16](表3)。患者的细胞常收集自供者,对于活化的T细胞,如CAR-T细胞可导致GVHD,当然,接受干细胞移植的患者可能已经经历过GVHD。但需要注意的是,治疗GVHD 的主要药物是甲强龙,而甲强龙对T细胞的增殖又有很大的影响[5,16]。目前,在本中心接受CAR-T细胞治疗的患者均未发生GVHD。
6 总结
CAR-T患者的出院标准包括24 h体温正常,输血时间在两周以上,或者频率更低,以及维持足够的水合能力[5,17]。在出院前,医务工作者需对重症CRS 患者进行全面评估以保证患者能够安全出院,对于病情比较复杂的患者,可能需要继续留院治疗。对于粒细胞缺乏的患者,需在出院时带药,如左氧氟沙星,进行预防感染。考虑到患者护理等问题,特别是需要治疗的长途患者,应在出院前就考虑路途和居家治疗时所需的药物等物品的准备,如准备6 周左右的左氧氟沙星和抗真菌药物等[18]。因为大多数患者在出院时会伴随粒细胞缺乏,因此患者家属应学会识别感染的预防以及何种情况需要用到药物处理。患者需每两周到门诊进行随访直至其达到回家恢复的标准。
患者及其家属的心理护理有着十分重要的作用[17],本中心的患者会有专门的医生指导患者如何应对治疗中可能会出现的各种情况以及对新环境的适应,从而保持与护理计划的一致性,也可增加患者与医生及护理之间的信任。对于难以配合医生工作的患者,也可以通过多学科团队(MDT)来提供更加全面的心理咨询[19],从而能够让患者及其护理者更愿意尝试CAR-T细胞这种新的治疗方式。
对于CAR-T 细胞治疗的患者一定要告知该治疗方式的副作用(如CRS)和治疗效果之间的平衡。虽然CRS程度直接受到输注前患者疾病状态的影响,但其不会对CAR-T 细胞的抗肿瘤效果产生影响[20]。医护团队需明确告知患者,该治疗方式可能不会出现严重的CRS,即便出现也不会对治疗效果产生影响。但部分常规护理政策(如中心导管的插管和取用)会因医院而异,除了白血病多次复发带来的压力之外,患者及家属还要对各种处置措施的改变进行适应。医护人员自身对处置方式和流程的熟练程度将给患者的治疗安全和压力带来直接影响。为了解决这些压力,本中心对中心导管和鼻饲护理等常规操作流程提供了纸质版材料,从而让家属和患者对治疗和护理方式的改变进行学习。
CAR-T 细胞治疗是针对多种肿瘤的一种新型免疫治疗方式,随着该治疗方式的普及,医护团队需要学习与之相关的各种副反应和毒性的临床管理知识。利用循证医学知识来指导这些并发症的评估、鉴定和管理,可为肿瘤患者提供更为安全有效的临床管理。了解CAR-T 细胞治疗的作用原理,就会对CRS、神经毒性、GVHD、肿瘤裂解综合征和B细胞发育等不良出现的起因、症状和治疗措施有更加深刻的理解,也可以提高对该病的临床管理知识。最终,类似CAR-T细胞治疗这种新的免疫治疗方式,可产生一系列独特的临床特征,也最终会形成相应的解决办法。而治疗期间和治疗后的整体管理,以及门诊、住院和家庭环境的多方位护理协调可大大提高患者的生活质量以及针对该病的管理经验。
