除草剂安全剂的开发与应用研究现状
2021-10-06陈仙艳余世贤曾东强
陈仙艳,余世贤,曾东强
(广西大学农学院 南宁市 530000)
农田除草剂的发现,在很大程度上促进了农业的发展。除草剂的使用在我国已经有近一百年的历史,对我们国家的农业发展产生了深远的影响,不仅有效地保证了农作物的高产与稳定,而且减少了劳动力投入以及促进栽培技术的创新。但随着除草剂的大量以及高剂量使用,其对环境以及农作物造成的危害也愈加严重,逐渐引起了人们的重视。为解决除草剂的使用引起的农作物药害问题,人们发现了除草剂安全剂(Safener),且随着除草剂的使用得到快速发展。除草剂安全剂是一类重要的药剂,保护农作物免受除草剂的药害,它对于除草剂的安全应用起着重要作用。
1 除草剂安全剂的发现及研究历史
1.1 除草剂安全剂的发现
除草剂安全剂最初是由霍夫曼(Hoffman)在1947年意外地发现的。Hoffman在实验中发现,用2,4-二氯苯氧乙酸药剂处理西红柿后,即使后期西红柿用2,4-二氯苯氧乙酸药剂处理,也再不会产生药害现象[1]。为探究出现这种现象的原因,Hoffman用燕麦灵(Barban)处理小麦后,用2,4-二氯苯氧乙酸对小麦进行茎叶喷施,观察到小麦并没有受到燕麦灵的药害;但在后面的实验中,将处理材料由小麦换成种子,给予同样的处理后,却发现小麦会遭到除草剂的药害,而且叶面喷施处理方式不利于小麦田杂草的清除,因而Hoffman认为以上出现的现象是不能够被开发利用的。但Hoffman仍坚信出现这种现象肯定存在着某种机理,于是在经过多年的研究后,成功研制出世界上第一个安全剂——1,8-萘二甲酸酐(1,8-Naphthalic–anhydride;NA),主要用来保护玉米、高粱等农作物,防止灭草喹、硫代氨基甲酸酯类以及氯代乙酰胺类除草剂对作物产生的毒性[2]。
1.2 除草剂安全剂的发展历程
安全剂NA在1972年被Gulfoil公司开发进入市场而被广泛应用。NA既能作为种子处理剂,又可以用于土壤处理,减轻不同种类的除草剂对农作物产生的药害[3]。在之后的15 a里,部分安全剂不断被开发进入市场,比较具有代表性的是由美国史托福石化公司开发的二氯丙烯胺(Dichlormid,R-25788),能够保护玉米、高粱等农作物不被丙草丹(EPTC)、乙草胺等药剂危害。自1,8-萘二甲酸酐和二氯丙烯胺被人们发现之后,很多化学公司发现了安全剂的商业前景并对其进行探索研究。早期安全剂的活性主要集中于谷类作物上,例如水稻、玉米、高粱和其他作物,其作用机制范围较窄,例如氯乙酰苯胺和硫代氨基甲酸酯类除草剂仅在发芽前使用才有效[4]。目前,随着除草剂在出芽后处理中的应用不断发展,用于治疗越冬后出芽谷物的安全剂正在逐渐商业化[5]。
1.3 除草剂安全剂的开发应用现状
随着除草剂的大规模使用,其引起的植物毒性问题也变得更加严重。除草剂安全剂的研究逐渐引起人们的关注,新的一些安全剂也被陆续开发出来。目前除草剂安全剂的开发研究及应用现状如表1所示,主要列出了目前几大类除草剂安全剂的主要代表商品、适用的除草剂及可作用的农作物。

表1 除草剂安全剂的开发研究及应用概况[6-7]
2 除草剂安全剂种类及作用机制
2.1 除草剂安全剂的类型
按照化合物以及作用方式进行分类,除草剂安全剂常见的类型包括2种:(1)按化合物分类:二氯乙酰胺类、磺酰脲类、肟醚类、三嗪类、三唑类、萘酸酐、羧酸衍生物、杂环类等;(2)按作用方式分类:分解型、补偿型、混合型以及拮抗型。
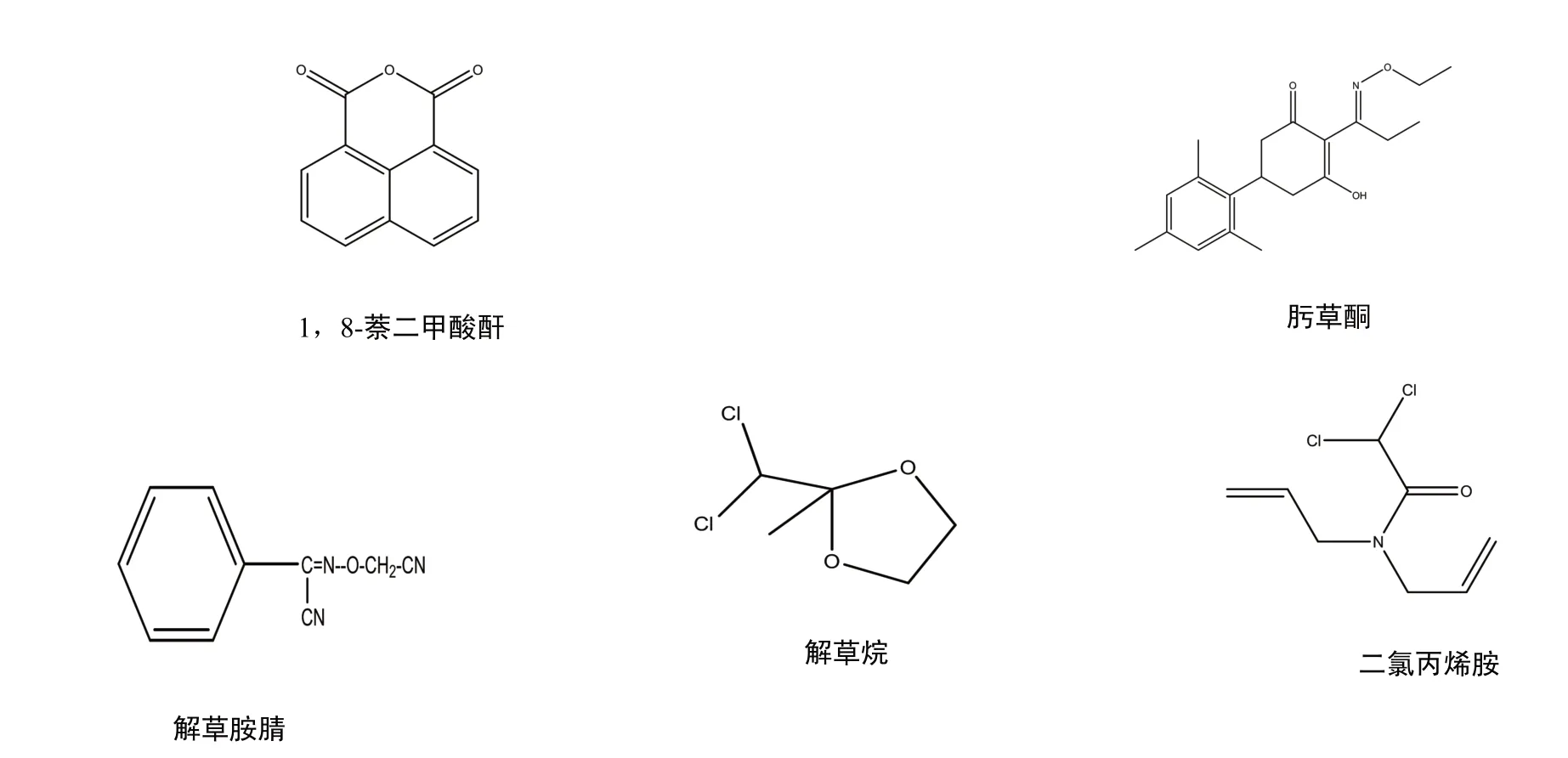
图1 常见的几种除草剂安全剂结构
2.2 除草剂安全剂的作用机制
除草剂-植物-安全剂三者之间的相互作用极其复杂,目前对于除草剂安全剂的作用机制仍没有明确的定论。但人们有提出几种普遍认可的假说[8]:①结构相似的安全剂与除草剂通过竞争受体及结合位点,减少除草剂对作物造成的药害(结构活性理论)[9];②安全剂通过阻碍农作物中除草剂的吸收和转运,提高农作物的安全性[10];③安全剂通过诱导作物体内谷胱甘肽-S-转移酶(GSTs)、细胞色素P450(P450s)、糖基转移酶(UGTs)等代谢酶的活性,提高除草剂的代谢速率;④促进除草剂在农作物中的降解[11]。关于除草剂安全剂的假说主要包括以上4种,目前对于除草剂安全剂的作用理论主要包括有结构活性理论、谷胱甘肽轭合理论以及由细胞色素P450催化的羟基化理论[12]。
(1)结构活性理论(QSAR)
Stephenson等[13]为验证以上猜想,通过测量大量的酰胺类衍生物对除草剂丙草丹(EPTC)的解毒作用后,提出了类似结构活性理论。他们观察到与除草剂EPTC结构相似的化合物,例如N,N-二取代基的2,2-二氯乙酰胺,酰胺类的衍生物对于EPTC能够表现出很高的活性,而且二氯的酰胺类衍生物要远大于一氯以及三氯的安全活性。但当酰胺类衍生物化学结构中的-NR1烃基R1或RCO-烃基R被另一些结构相差很大的基团所取代时,安全活性发生很大的变化,有可能会迅速下降。大量的研究表明,除草剂安全剂的安全活性与自身的化学结构联系密切,只有安全剂与除草剂的结构相差不大时,其安全活性才会更高[14]。另外,Yenne等[15]通过运用计算机辅助分子模型设计(CAMM)发现,在除草剂安全剂的解毒现象中,其分子结构的特征官能团起到非常重要的作用,如果这些分子结构发生某些变化的话,将有可能会直接影响到安全剂的解毒活性,甚至有可能会丧失。Yenne等人的发现,在很大程度上支持了Stephenson的类似结构活性理论。

图2 结构活性理论(QSAR)机制注释图
(2)谷胱甘肽轭合理论
谷胱甘肽-S-转移酶(GSTs)以及谷胱甘肽(GSH)是除草剂安全剂发挥解毒效应过程中不可缺少的物质[16-17]。Shimabukuro等[18]在1970年首次发现除草剂莠去津与谷胱甘肽之间能发生轭合作用,即在GSTs的催化作用下,莠去津能与谷胱甘肽轭合,从而生成无毒性的化合物。随后lay和kasida[19]研究了硫代氨基甲酸酯类除草剂和二氯乙酰胺解毒剂的作用机理,在前人的基础上做了大量的实验研究,提出了谷胱甘肽轭合机理的理论。如图3所示,表明硫代氨基甲酸酯类除草剂在作物体内,首先会生成有毒性的亚砜代谢产物,安全剂通过提高GSTs的活性以及增加GSH的含量,加速作物体内亚砜代谢产物与GSH发生轭合,从而将有毒性的代谢产物转化为无毒性或者低毒的化合物[20]。Ekler等[21]研究也发现,安全剂BAS-145138、苯叉酰胺、Dichlormid、MG-191以及解草烯能够加快除草剂乙草胺在玉米体内的降解,主要原因是安全剂作用于玉米体内后GSTs的活性得到了提高。近年来,毕红梅等[22]采用室内生物测定法,发现安全剂ND2144在保护玉米免受除草剂乙草胺的药害时,可以使GSH含量达到对照的108.1%,ALS活性达到对照的142.9%。上述研究表明,安全剂可以通过增加GSH的含量以及提高GSTs的活性,从而缓解作物体内除草剂造成的药害。
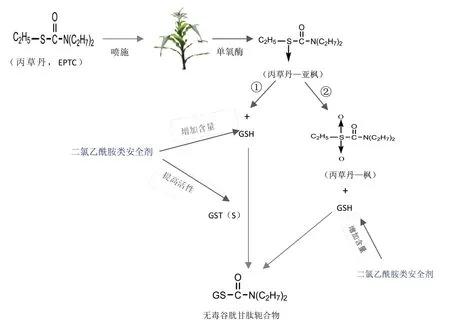
图3 谷胱甘肽轭合机制论注释图[23-26]
(3)植物细胞色素P450催化的羟基化理论
在植物体内,微粒体P450单氧酶广泛存在,是作物体内除草剂代谢功能最广泛的一类酶,能催化各种氧化反应[27]。经研究发现,除草剂安全剂可以诱导植物细胞色素P450的活性,如安全剂NA通过诱导P450的活性发挥解毒效应。Robert等[28]在研究安全剂烯丙酰草胺在保护玉米不被除草剂EPTC药害时,发现玉米体内除草剂代谢过程中包含有氧化和磺化作用,从而首次提出了安全剂解毒效应中存在氧化反应。其他研究者在比较了除草剂及其代谢产物后,也得到了类似的结论。例如,除草剂氟嘧磺隆在细胞色素P450的诱导下,在玉米中能产生羟基化反应[29];Cole和Thalacke等[30-31]经研究表明,P450s可促进作物体内磺酰脲类除草剂和醚苯磺隆发生羟基化反应。上述研究结果表明细胞色素P450的活性能被除草剂安全剂所诱导,P450s对于农作物体内除草剂的代谢具有重要作用。
除了以上涉及到的GSH、GSTs、P450s等物质之外,在安全剂缓解作物体内除草剂药害的过程中,乙酰乙酸合成酶(ALS)、糖基转移酶(UGTs)、ABC转运体、谷胱甘肽转运体、液泡酶等物质也起着非常重要的作用。除草剂安全剂的解毒效果是多种物质结合起来发挥作用的,其作用机制尤其复杂,并非只限于某一物质。目前,对于除草剂-植物-安全剂三者之间的相互关系,研究者们已经做了大量的研究,但具体的作用机制还不明确,仍需要进一步探究阐明。
3 除草剂安全剂的发展前景
在除草剂大量以及高剂量使用的今天,其带来的环境问题不容小觑,尤其是除草剂的长期使用对农作物以及环境产生的影响,有可能会直接威胁到社会的发展[32-34]。现阶段,针对除草剂安全剂作用机理研究中的不足,笔者认为应从以下几个方面展开研究:1)利用分子生物学手段,鉴定出细胞色素P450基因的功能,明确P450基因所调控的分子机制;2)运用基因转录学、蛋白质组学等分子技术,确定除草剂安全剂保护农作物过程中所涉及的物质及相关酶系;3)结合生理生化研究除草剂和安全剂对作物的影响[35]。最后,笔者认为除草剂安全剂商业化制剂的研究应向新型、高效、低毒、残留期短的方向发展,在保证除草剂靶标活性的前提下,研制出有效保护农作物安全的制剂。
