JAK抑制剂治疗炎症性肠病有效性及安全性的Meta分析
2021-09-29张玉梅黄丹阳
张玉梅,冯 新,黄丹阳,姜 政
重庆医科大学附属第一医院消化内科,重庆 400016
炎症性肠病(inflammatory bowel disease,IBD)主要包括溃疡性结肠炎(UC)和克罗恩病(CD),是一种主要累及胃肠道的慢性、非特异性、缓解与复发性交替发生的炎症性疾病。研究[1]发现,IBD与高脂肪、高蛋白、高糖饮食等生活方式密切相关,多见于西欧和北美地区,但近20年来随着人们饮食结构的西方化、生活方式及环境的明显变化,我国IBD的发病率快速增长。目前包括抗肿瘤坏死因子、整合素拮抗剂等生物制剂的应用,使IBD的治疗发生了革命性的变化,但产生免疫原性是所有生物制剂面临的普遍问题[2]。与生物制剂相比,无免疫原性是小分子药物的优点,此外,小分子药物半衰期更短,并且价格低廉,更加经济,可及性高。目前,Janus激酶(JAK)-转录激活因子(STAT)通路是IBD小分子药物研发中的一个比较热门的靶点,针对这个靶点研发的药物主要是JAK抑制剂。
JAK是一种存在于胞内非受体酪氨酸激酶,在许多细胞因子的信号通路中扮演了重要角色[3],JAK—STAT信号通路在IBD的发病机制中起着关键作用,JAK抑制剂对IBD具有潜在的治疗价值[4]。目前已有多项JAK抑制剂治疗IBD的前瞻性随机双盲临床研究完成,证实JAK抑制剂对IBD有确切的疗效[5]。JAK有JAK1、JAK2、JAK3和TYK2四种异构体[4],Tofacitinib是一代JAK抑制剂,作为一种泛JAK抑制剂主要抑制JAK1和JAK3,并且在较小程度上也抑制JAK2[6],最近被批准用于治疗中-重度UC,但由于多种细胞因子的作用被Tofacitinib阻断,感染等药物不良反应成为一个值得关注的问题[7]。为了提高这一类药物的效益风险比,一些第二代亚型选择性JAK抑制剂正在开发中。然而,选择性抑制JAK亚型能否提高临床疗效、获得更好的安全性仍存在争议。目前,国内外尚缺乏泛JAK亚型抑制剂与JAK亚型选择性抑制剂直接对比的相关研究,本研究通过间接比较Meta分析,对2种治疗方法进行间接比较,为临床治疗提供证据。目前对Tofacitinib的最佳剂量仍无明确的标准,由于大部分相关文献使用的剂量为5 mg bid、10 mg bid、15 mg bid,本研究收集近年来使用5 mg bid、10 mg bid、15 mg bid剂量的Tofacitinib治疗IBD的文献进行Meta分析,为明确Tofacitinib治疗IBD的合适剂量提供参考依据。
1 资料与方法
1.1 文献检索由2名研究者独立检索计算机数据库PubMed、The Cochrane Library、Web of Science、EmBase、中国知网(CNKI)、VIP、万方数据库、CBM、临床试验注册数据库,搜索JAK抑制剂治疗IBD的随机对照试验(RCTs),检索时限均为建库至2020年10月。检索方式采用主题词和自由词相结合的方式,并追溯纳入文章的参考文献,以补充获取相关文献。检索词包括:中文检索词:“炎症性肠病”、“克罗恩病”、“溃疡性结肠炎”、“JAK抑制剂”、“托法替布”、“非哥替尼”、“乌帕替尼”。英文检索词包括:Tofacitinib、Filgotinib、Upadacitinib、Peficitinib、TD-1473、JAKi、JAK inhibitor、Inflammatory bowel disease、Crohn’s disease、Ulcerative colitis。
1.2 文献纳入及排除标准纳入标准:(1)研究类型:RCT研究,无论是否采用盲法。文种限制为中、英文;(2)研究对象:纳入CD或UC的成年患者,CD及UC诊断标准符合IBD诊断治疗规范第6次共识意见[8];(3)干预措施:试验组:给予JAK抑制剂(Tofacitinib、Filgotinib、Upadacitinib、Peficitinib、TD-1473)辅助治疗;对照组:给予安慰剂辅助治疗(安慰剂的使用必须在知情同意的前提下并符合药物使用临床规范);(4)结局指标:有效性指标:主要用临床反应率及临床缓解率评估治疗效果。CD使用克罗恩病活动指数(CDAI)[9-13]评估临床结果,UC使用改良Mayo评分[14](MCS)评估临床结果,该评分由排便次数、直肠出血(RBS)、医师整体评估(physician global assessment)和内镜(MCSe)4个亚评分组成的综合指标。临床反应:CD:CDAI与基线相比下降100分。UC:MCS与基线相比下降30%及得分≥3分,且RBS减少≥1分或RBS=0分或1分。临床缓解:CD:CDAI<150分。UC:MCS≤2分且无亚评分>1分且RBS=0分。不良反应的指标:不良反应率;(6)可阅读全文。排除标准:(1)综述、个案报道、指南、述评、信函、动物实验、与JAK抑制剂和IBD无关的研究;(2)重复发表的文献;(3)无法获得全文的文献;(4)无法获得数据或数据不全的文献。
1.3 文献筛选与数据提取由2位研究者独立筛选文献,提取资料并交叉核对,如遇分歧,则讨论解决或交由第三位研究者协助判断。对缺乏资料的文献,尽量与原作者取得联系予以补充。提取资料包括:(1)纳入研究的基本信息,包括作者姓名、发表年份、国家;(2)研究对象的基本特征,包括样本量、年龄、病程、抗肿瘤坏死因子使用率、激素使用率、CDAI分值基线、Mayo分值基线;(3)干预措施的具体细节及疗程;(4)偏倚风险评价的关键要素;(5)所关注的结局指标的主要数据。
1.4 纳入研究的偏倚风险评价纳入研究的偏倚风险评价采用Cochrane手册5.1.0版推荐的针对RCT的偏倚风险评价工具进行评价;(1)随机方法是否正确;(2)分配是否隐藏;(3)对受试者和研究者是否采用盲法;(4)结果数据的完整性;(5)是否有选择性报告研究结果;(6)其他偏倚来源。由2位研究员独立进行偏倚风险评价,并交叉核对结果,如遇分歧,讨论解决。
1.5 统计学分析采用RevMan 5.3及ITC统计软件进行Meta分析,因结局指标均为二分类变量,故采用相对危险度(relative risk,RR)为效应指标,各效应量均给出点估计值及95%CI,P<0.05为差异有统计学意义。对纳入研究的异质性采用χ2检验进行评价(检验水准为α=0.1),并结合I2<50%,则采用固定效应模型进行Meta分析;若异质性检验结果I2≥50%,表示研究间异质性较大,合并效应量采用随机效应模型生成或终止合并。漏斗图法检测发表偏倚。
2 结果
2.1 纳入文献基本情况通过文献检索,查找到1 011篇相关文献,均为中英文文献。去除重复文献396篇,阅读题目及摘要排除584篇,剩余31篇。阅读全文后有22篇不满足全部纳入标准,最终纳入9篇文献[15-23],共包括12项(5项CD,7项UC)RCTs,试验药物有对JAK亚型有广泛抑制作用的Tofacitinib、Peficitinib和TD-1473、对JAK1有高度选择性抑制的Filgotinib、Upadacitinib。共计活动性IBD患者3 450例,包括试验组2 606例,安慰剂组844例,具体筛选流程如图1所示。纳入研究的基本信息如表1所示,各类JAK抑制剂的作用机制如表2所示。
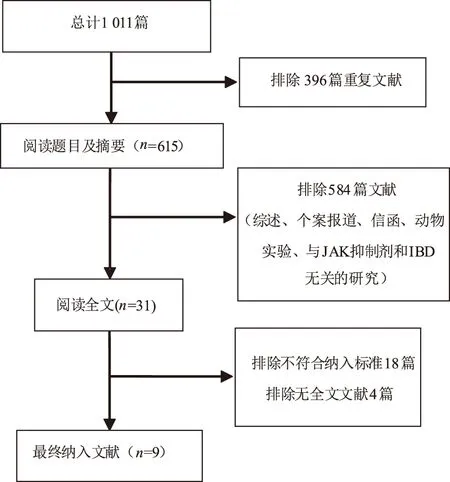
图1 文献筛选流程图Fig 1 Literature selection flow chart
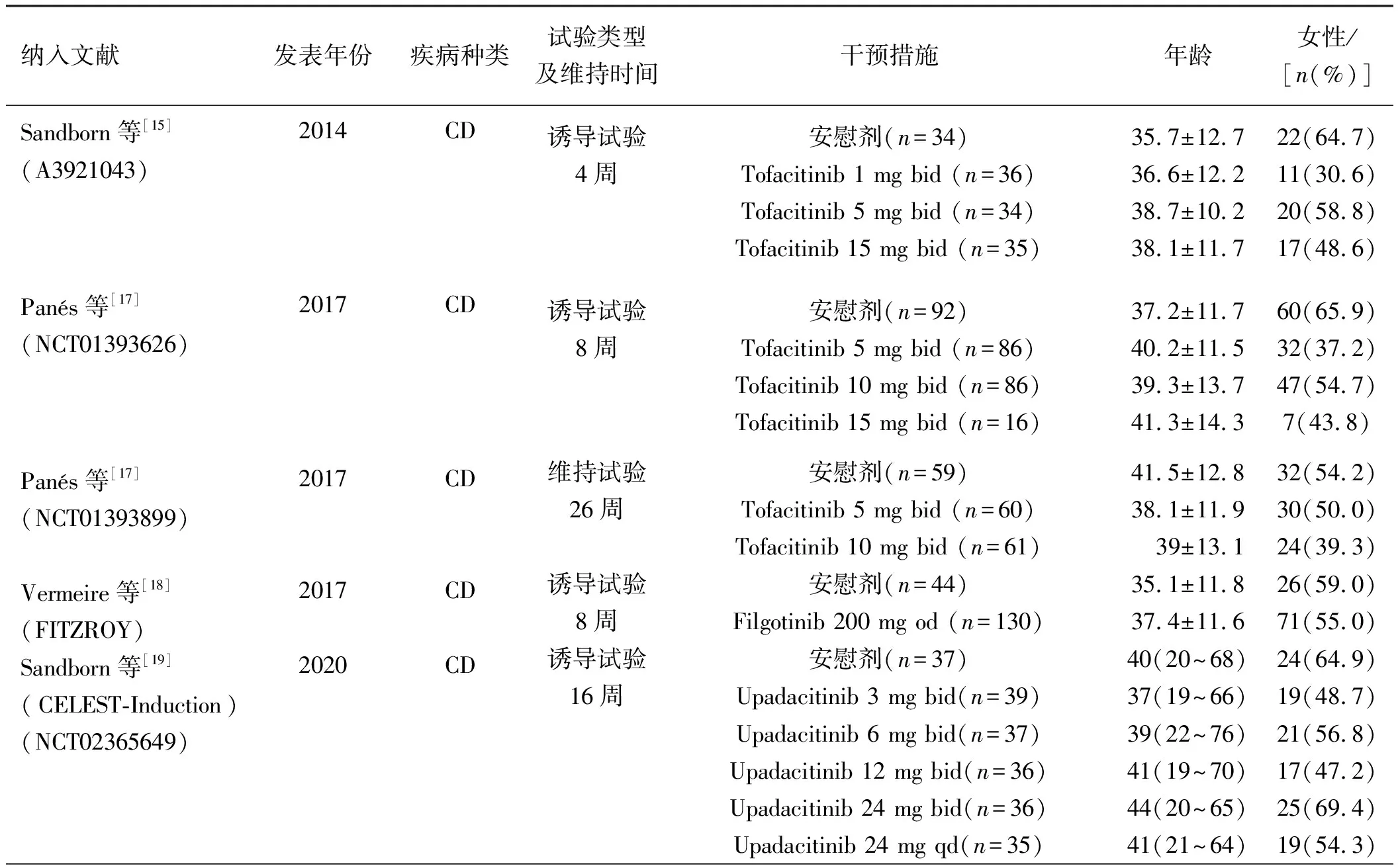
表1 纳入文献的基本特征Tab 1 Basic characteristics of included literature
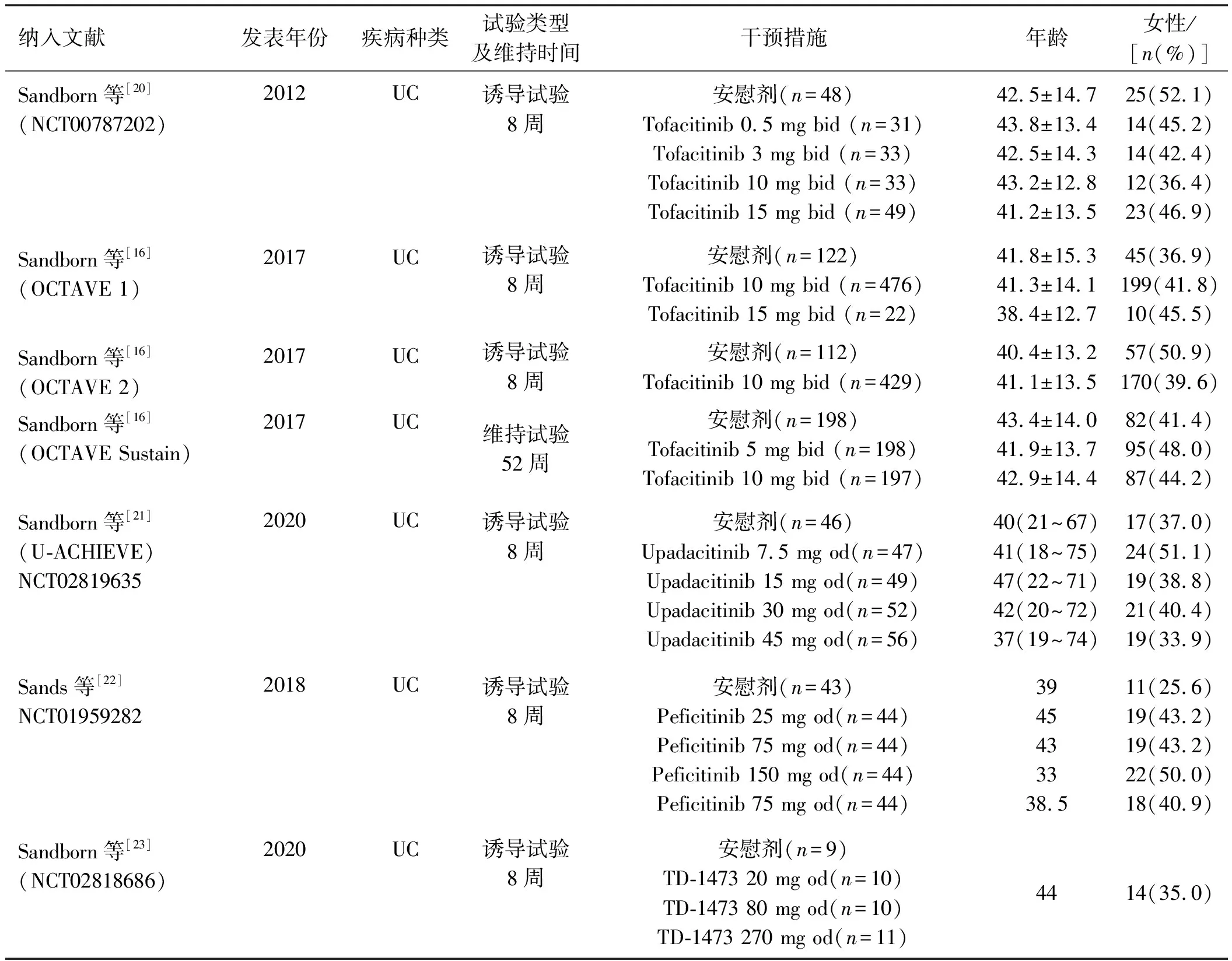
续表1

表2 各类JAK抑制剂的作用机制Tab 2 Action mechanism of various JAK inhibitors
2.2 纳入研究的方法学质量评价纳入的12项研究均为RCTs,每项研究均提到了随机,8项研究对随机序列的产生方式进行了详细说明,仅2项研究明确说明了对分配进行隐藏,所有研究均列出了本次Meta分析的主要研究指标,均无选择性报告研究结果。纳入研究的质量评价如图2所示。
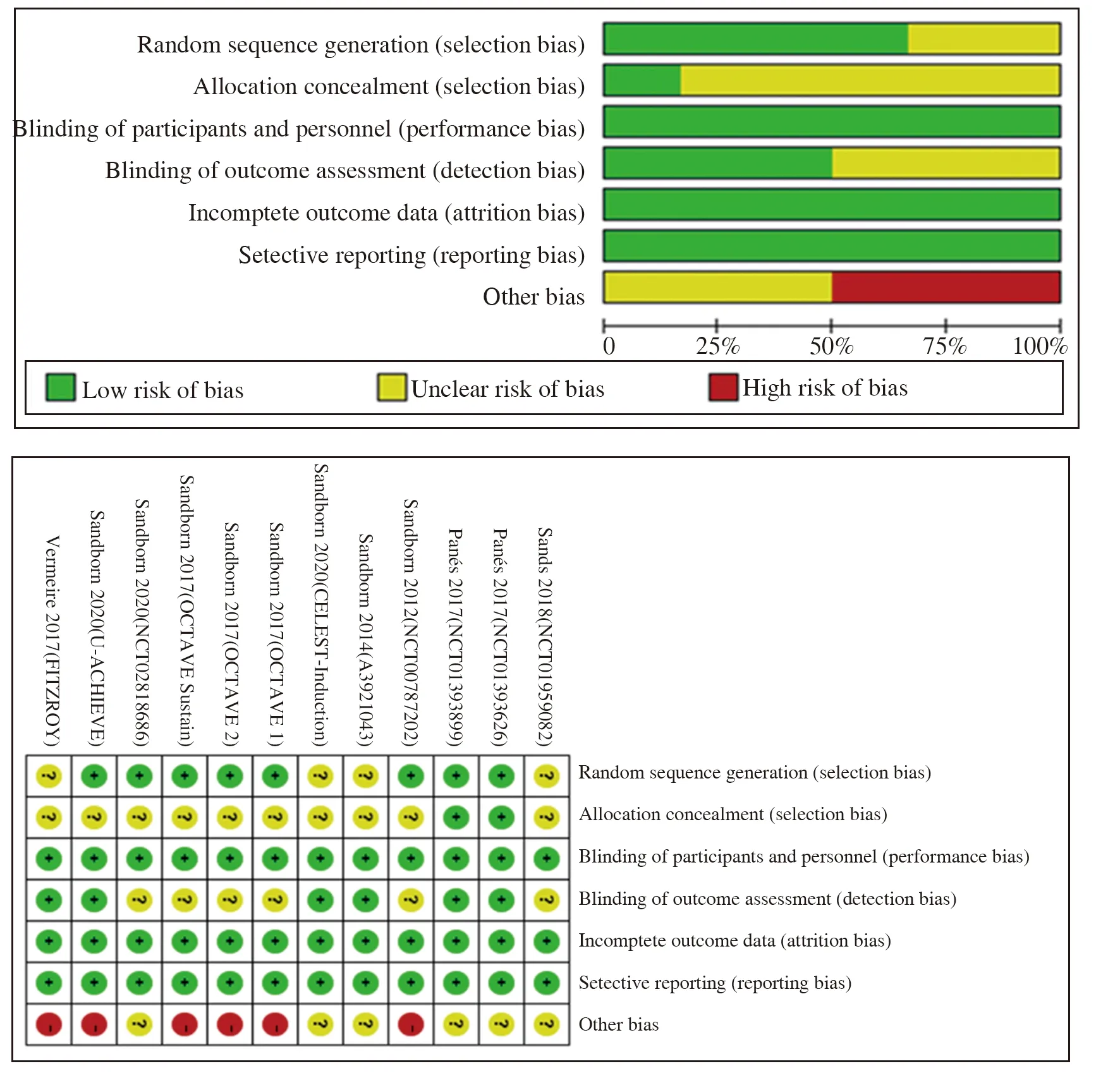
图2 纳入研究的质量评价Fig 2 Quality evaluation of included studies
2.3 泛JAK抑制剂与JAK1选择性抑制剂治疗IBD的有效性及安全性对比结果
2.3.1 泛JAK抑制剂与安慰剂有效性及安全性的比较:所有纳入研究的结局指标结果如表3所示。有9项研究比较了泛JAK抑制剂与安慰剂的临床反应率,有8项研究[15-17,20,22-23]比较了泛JAK抑制剂与安慰剂的临床缓解率及不良反应发生率,各研究进行异质性检验,在进行临床反应率比较时提示异质性较大(P=0.0007,I2=70%),使用随机效应模型进行Meta分析,结果显示,泛JAK抑制剂较安慰剂治疗IBD临床反应率高,差异有统计学意义(RR=1.61,95%CI:1.29~2.01,Z=4.20,P<0.0001)(见图3)。在进行临床缓解率比较时提示异质性较大(P=0.0003,I2=75%),使用随机效应模型进行Meta分析,结果显示,泛JAK抑制剂比较安慰剂治疗IBD临床缓解率升高,差异有统计学意义(RR=2.11,95%CI:1.38~3.24,Z=3.43,P=0.0006)(见图4)。在进行不良反应率比较时提示异质性较小(P=0.84,I2=0),使用固定效应模型进行Meta分析,结果显示,泛JAK抑制剂比较安慰剂治疗IBD不良反应发生率差异无统计学意义(RR=1.01,95%CI:0.94~1.07,Z=0.16,P=0.87)(见图5)。
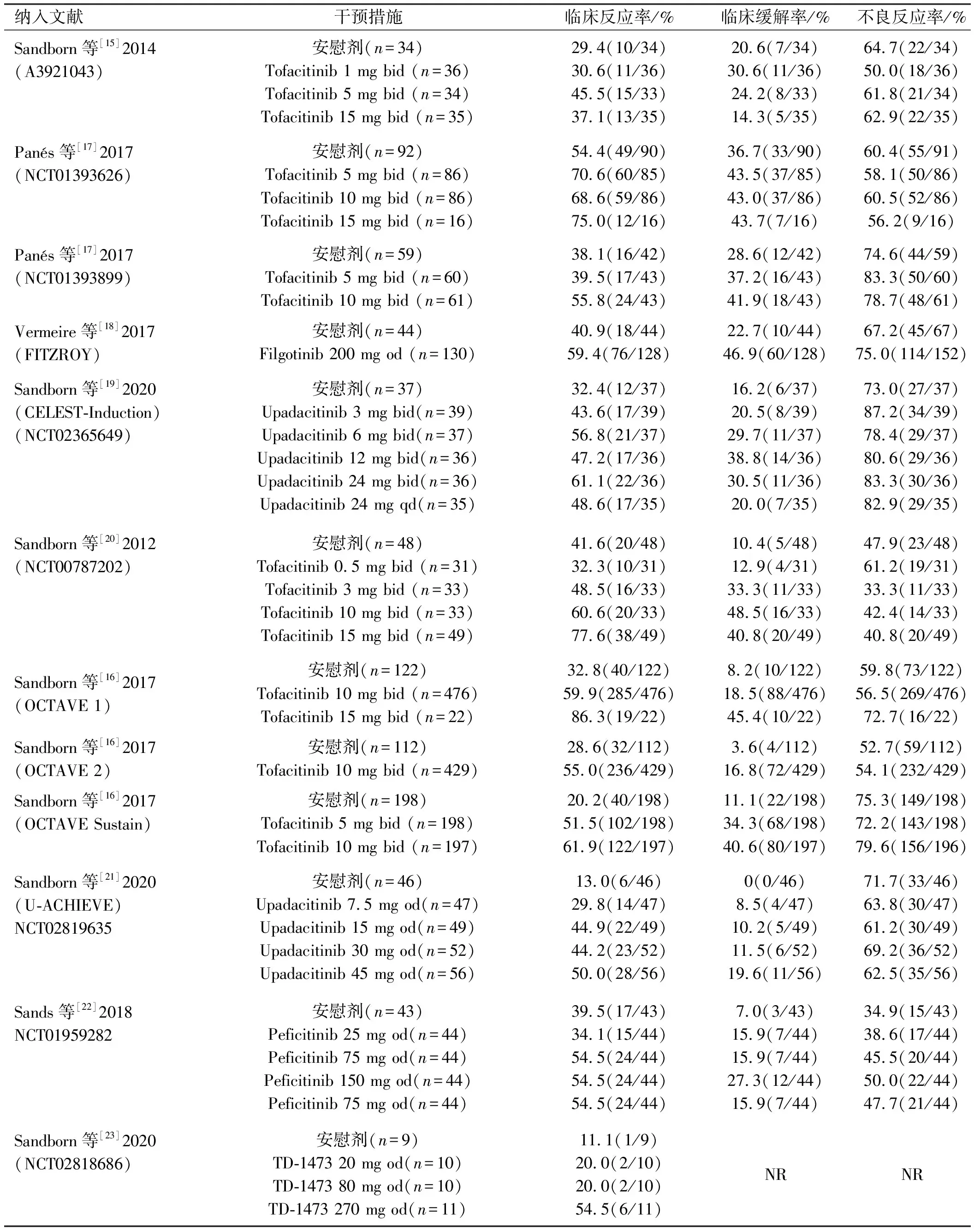
表3 纳入研究的结局指标结果Tab 3 The outcome indicators results of the included studies
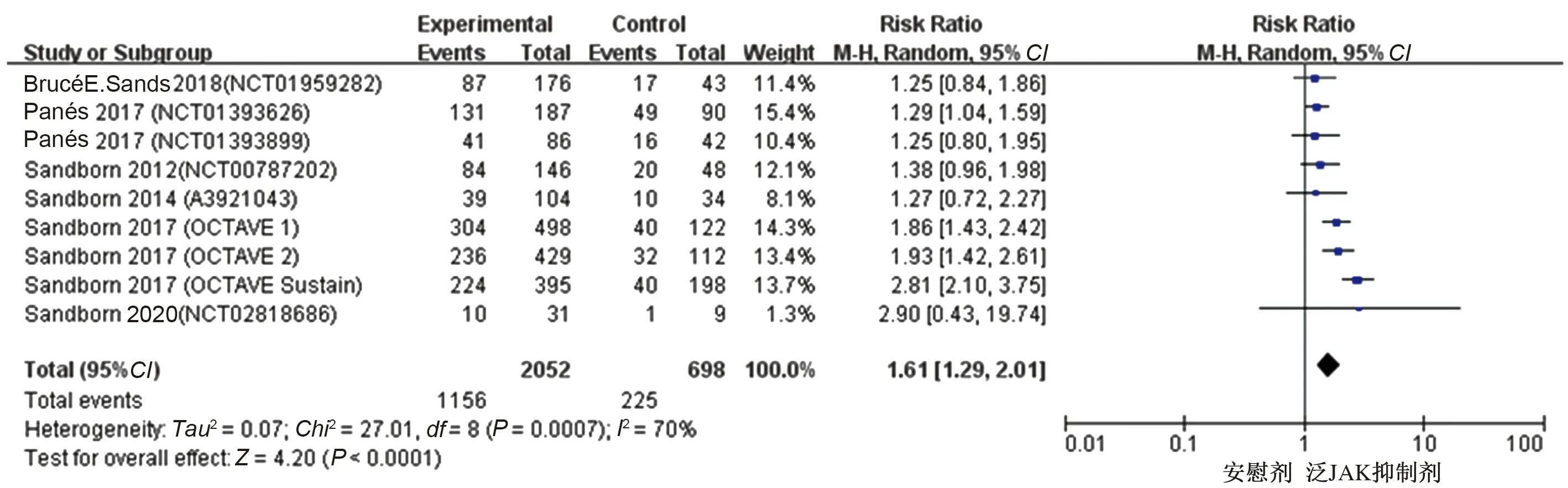
图3 泛JAK抑制剂治疗IBD的临床反应率森林图Fig 3 Forest plot of clinical reaction rate of Pan JAK inhibitors treat IBD
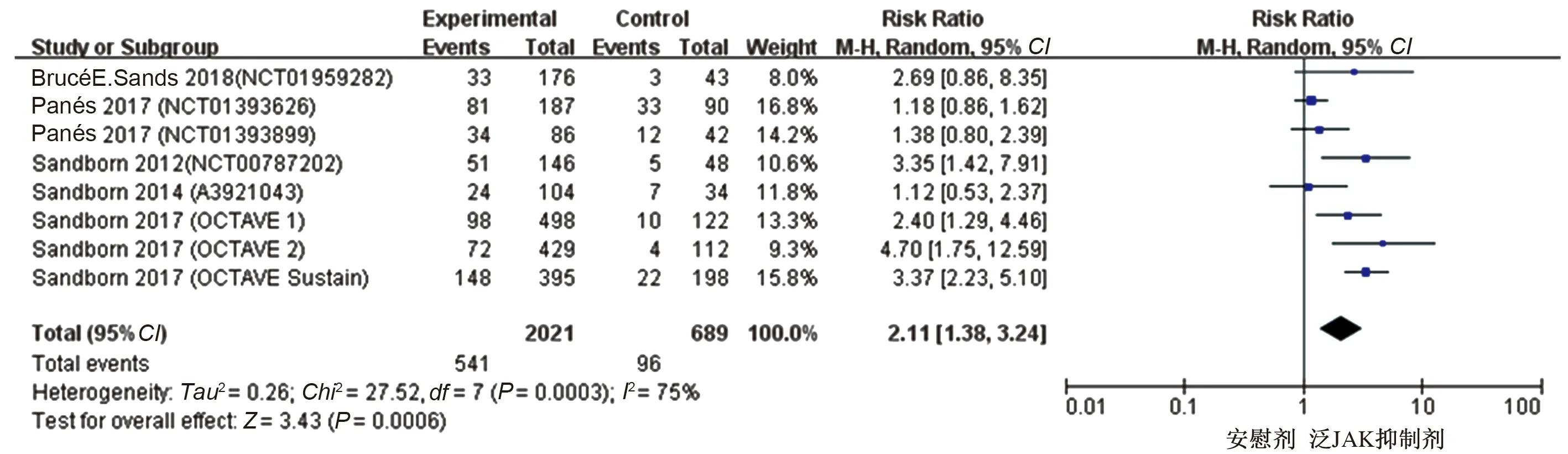
图4 泛JAK抑制剂治疗IBD的临床缓解率森林图Fig 4 Forest plot of clinical remission rate of Pan JAK inhibitors treat IBD
图5 泛JAK抑制剂治疗IBD的不良反应发生率森林图Fig 5 Forest plot of adverse reaction rate of Pan JAK inhibitors treat IBD
2.3.2 JAK1选择性抑制剂与安慰剂有效性及安全性的比较:有3项研究[18-19,21]比较了JAK1选择性抑制剂与安慰剂的临床缓解率及不良反应率,各研究进行异质性检验,在进行临床反应率比较时提示异质性较小(P=0.14,I2=49%),使用固定效应模型进行Meta分析,结果显示,JAK1选择性抑制剂较安慰剂治疗IBD临床反应率高,差异有统计学意义(RR=1.81,95%CI:1.36~2.42,Z=4.03,P<0.0001)(见图6)。在进行临床缓解率比较时提示异质性较小(P=0.37,I2=0),使用固定效应模型进行Meta分析,结果显示,JAK1选择性抑制剂比较安慰剂治疗IBD临床缓解率升高,差异有统计学意义(RR=2.25,95%CI:1.42~3.56,Z=3.45,P=0.0006)(见图7)。在进行不良反应率比较时提示异质性较小(P=0.21,I2=36%),使用固定效应模型进行Meta分析,结果显示,JAK1选择性抑制剂比较安慰剂治疗IBD不良反应率差异无统计学意义(RR=1.05,95%CI:0.93~1.18,Z=0.77,P=0.44)(见图8)。

图6 JAK1选择性抑制剂治疗IBD的临床反应率森林图Fig 6 Forest plot of clinical reaction rate of JAK1 selective inhibitors treat IBD
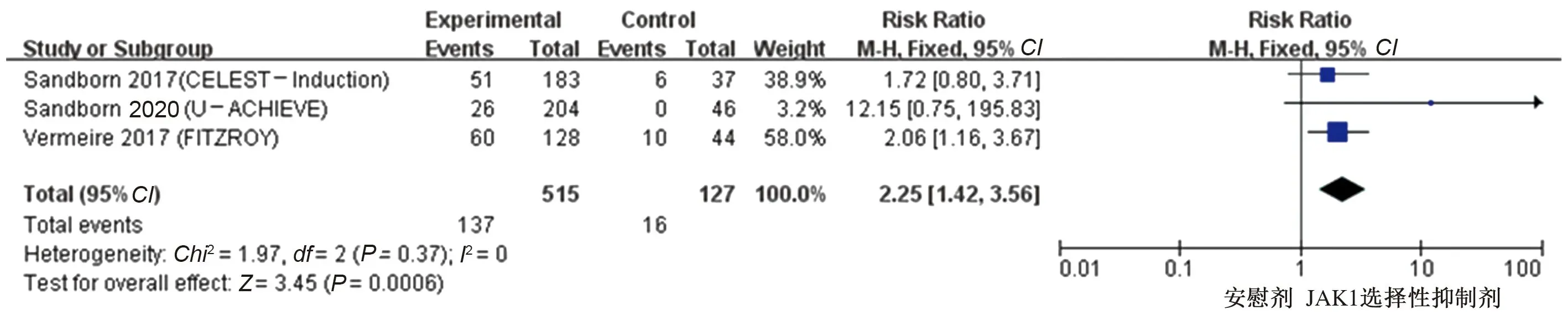
图7 JAK1选择性抑制剂治疗IBD的临床缓解率森林图Fig 7 Forest plot of clinical remission rate of JAK1 selective inhibitors treat IBD
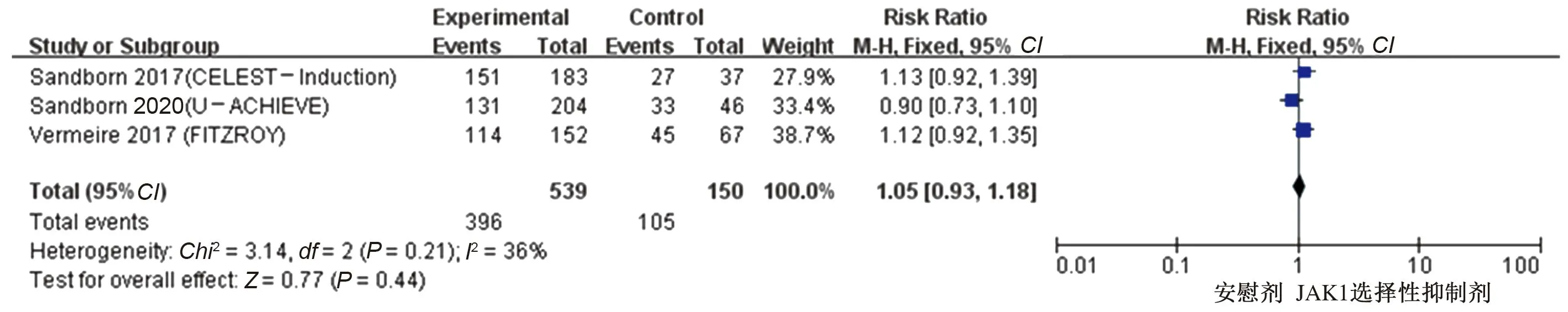
图8 JAK1选择性抑制剂治疗IBD的不良反应率森林图Fig 8 Forest plot of adverse reaction rate of JAK1 selective inhibitors treat IBD
2.3.3 泛JAK抑制剂与JAK1选择性抑制剂有效性及安全性的间接比较:通过ITC软件对泛JAK抑制剂与JAK1选择性抑制剂的有效率及不良反应发生率进行间接比较,结果显示,泛JAK抑制剂与JAK1选择性抑制剂治疗IBD的疗效及安全性比较,差异均无统计学意义(P>0.05,见表4)。
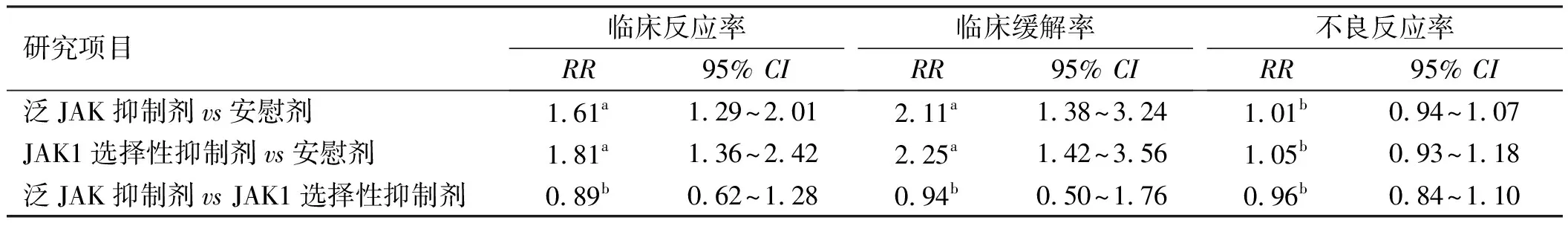
表4 泛JAK抑制剂与JAK1选择性抑制剂的有效率及不良反应率的间接比较Tab 4 Indirect comparison of efficacy and rate of adverse reactions between Pan JAK1 inhibitors and JAK1 selective inhibitors
2.4 不同剂量组Tofacitinib的有效性及安全性评估的对比
2.4.1 5 mg Tofacitinib与安慰剂有效性及安全性的比较:有4项研究[15-17]比较了5 mg Tofacitinib与安慰剂的临床反应率、临床缓解率及不良反应率,各研究进行异质性检验,在进行临床反应率比较时提示异质性较大(P=0.001,I2=81%),使用随机效应模型进行Meta分析,结果显示,5 mg Tofacitinib与安慰剂治疗IBD临床反应率比较,差异无统计学意义(RR=1.55,95%CI:1.00~2.40,Z=1.95,P=0.05)(见图9)。在进行临床缓解率比较时提示异质性较大(P=0.005,I2=76%),使用随机效应模型进行Meta分析,结果显示,5 mg Tofacitinib与安慰剂治疗IBD临床缓解率比较,差异无统计学意义(RR=1.59,95%CI:0.92~2.74,Z=1.65,P=0.10)(见图10)。在进行不良反应率比较时提示异质性较小(P=0.57,I2=0),使用固定效应模型进行Meta分析,结果显示,5 mg Tofacitinib与安慰剂治疗IBD临床不良反应发生率比较,差异无统计学意义(RR=0.99,95%CI:0.90~1.08,Z=0.31,P=0.76)(见图11)。

图9 5 mg Tofacitinib治疗IBD的临床反应率森林图Fig 9 Forest plot of clinical reaction rate of 5 mg Tofacitinib treat IBD
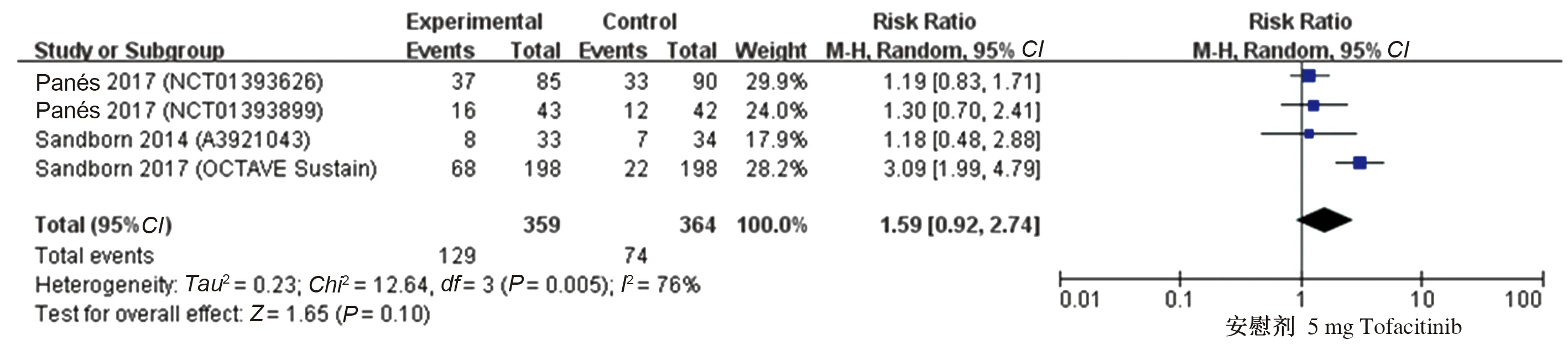
图10 5 mg Tofacitinib治疗IBD的临床缓解率森林图Fig 10 Forest plot of clinical remission rate of 5 mg Tofacitinib treat IBD

图11 5 mg Tofacitinib治疗IBD的不良反应率森林图Fig 11 Forest plot of adverse reaction rate of 5 mg Tofacitinib treat IBD
2.4.2 10 mg Tofacitinib与安慰剂有效性及安全性的比较:有6项研究[16-17,20]比较了10 mg Tofacitinib与安慰剂的临床反应率、临床缓解率及不良反应率,各研究进行异质性检验,在进行临床反应率比较时提示异质性较大(P=0.0002,I2=79%),使用随机效应模型进行Meta分析,结果显示,10 mg Tofacitinib较安慰剂治疗IBD临床反应率高,差异有统计学意义(RR=1.77,95%CI:1.33~2.35,Z=3.93,P<0.0001)(见图12)。在进行临床缓解率比较时提示异质性较大(P=0.0001,I2=80%),使用随机效应模型进行Meta分析,结果显示,10 mg Tofacitinib较安慰剂治疗IBD临床缓解率升高,差异有统计学意义(RR=2.44,95%CI:1.43~4.15,Z=3.29,P=0.001)(见图13)。在进行不良反应率比较时提示异质性较小(P=0.87,I2=0),使用固定效应模型进行Meta分析,结果显示,10 mg Tofacitinib与安慰剂治疗IBD不良反应发生率比较,差异无统计学意义(RR=1.01,95%CI:0.94~1.09,Z=0.27,P=0.79)(见图14)。

图12 10 mg Tofacitinib治疗IBD的临床反应率森林图Fig 12 Forest plot of clinical reaction rate of 10 mg Tofacitinib treat IBD
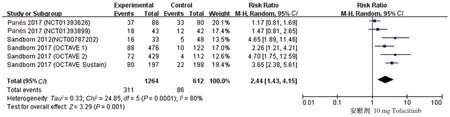
图13 10 mg Tofacitinib治疗IBD的临床缓解率森林图Fig 13 Forest plot of clinical remission rate of 10 mg Tofacitinib treat IBD
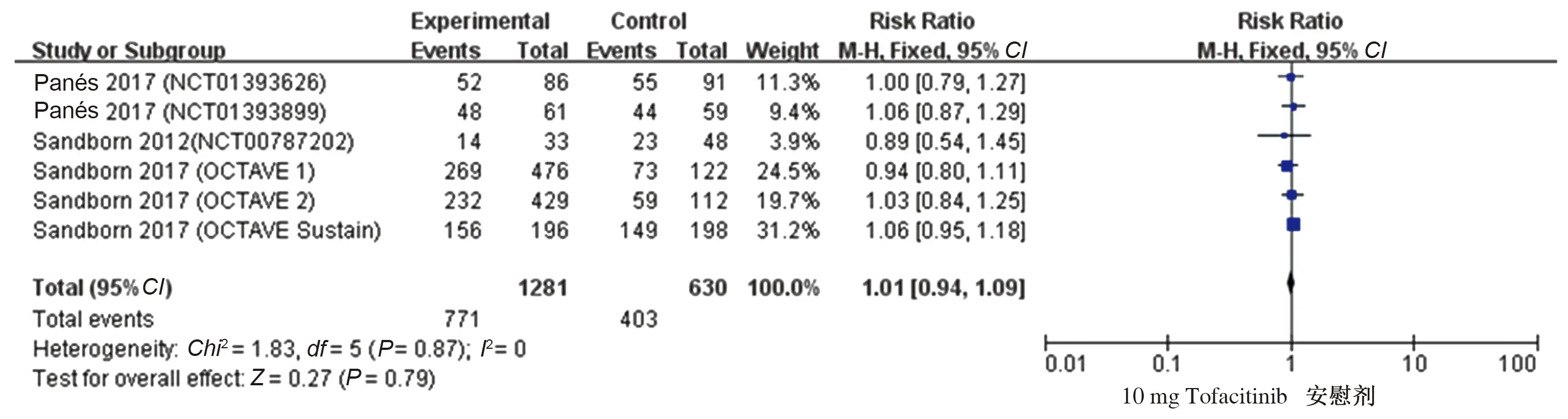
图14 10 mg Tofacitinib治疗IBD的不良反应率森林图Fig 14 Forest plot of adverse reaction rate of 10 mg Tofacitinib treat IBD
2.4.3 15 mg Tofacitinib与安慰剂有效性及安全性的比较:有4项研究[15-17,20]比较了15 mg Tofacitinib与安慰剂的临床反应率、临床缓解率及不良反应率,各研究进行异质性检验,在进行临床反应率比较时提示异质性较大(P=0.02,I2=69%),使用随机效应模型进行Meta分析,结果显示,15 mg Tofacitinib较安慰剂治疗IBD临床反应率高,差异有统计学意义(RR=1.78,95%CI:1.26~2.53,Z=3.25,P=0.001)(见图15)。在进行临床缓解率比较时提示异质性较大(P=0.001,I2=81%),使用随机效应模型进行Meta分析,结果显示,15 mg Tofacitinib与安慰剂治疗IBD临床缓解率比较,差异无统计学意义(RR=2.10,95%CI:0.83~5.31,Z=1.57,P=0.12)(见图16)。在进行不良反应率比较时提示异质性较小(P=0.51,I2=0),使用固定效应模型进行Meta分析,结果显示,15 mg Tofacitinib与安慰剂治疗IBD不良反应发生率比较,差异无统计学意义(RR=1.00,95%CI:0.82~1.21,Z=0.05,P=0.96)(见图17)。
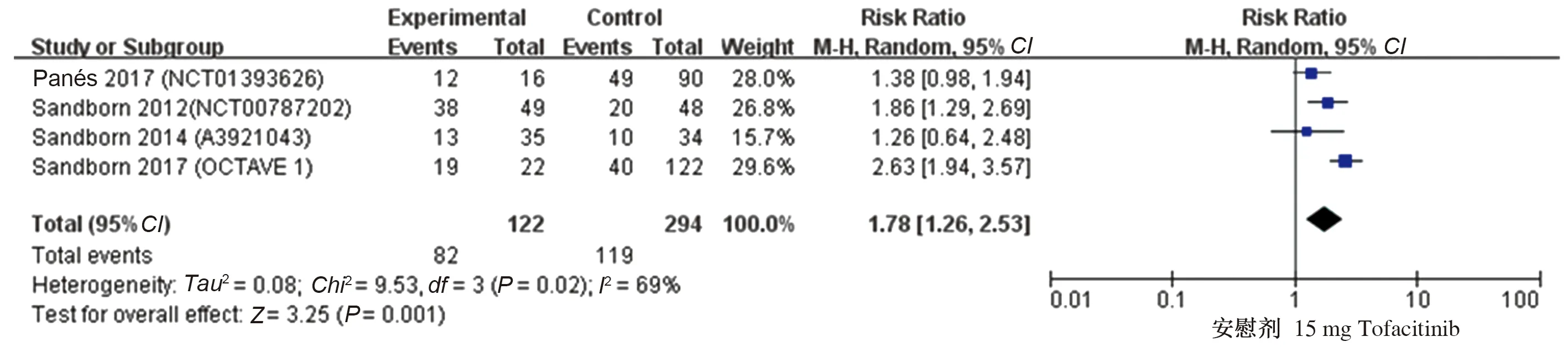
图15 15 mg Tofacitinib治疗IBD的临床反应率森林图Fig 15 Forest plot of clinical reaction rate of 15 mg Tofacitinib treat IBD
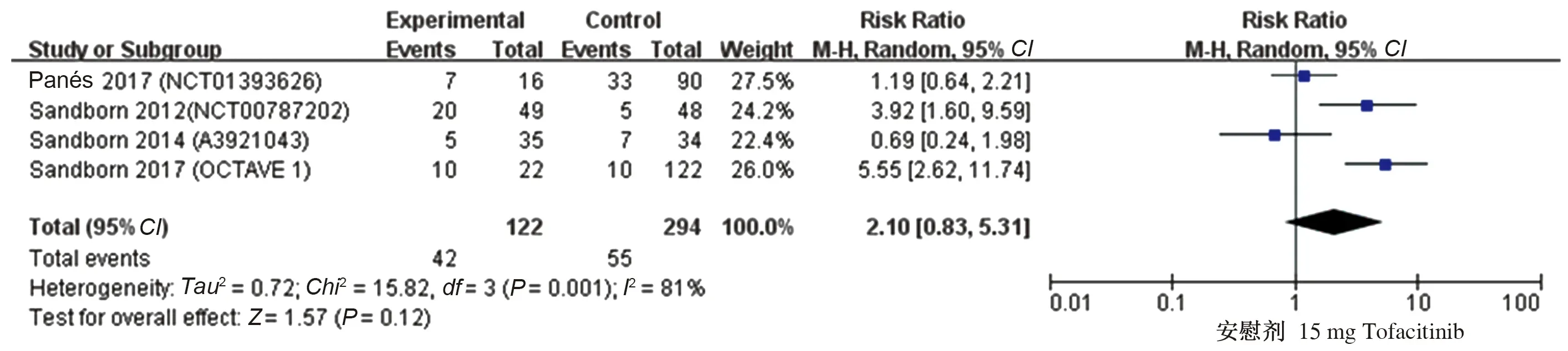
图16 15 mg Tofacitinib治疗IBD的临床缓解率森林图Fig 16 Forest plot of clinical remission rate of 15 mg Tofacitinib treat IBD
2.4.4 5 mg Tofacitinib、10 mg Tofacitinib与15 mg Tofacitinib有效性及安全性的比较:有3项研究[16-17]比较了5 mg Tofacitinib与10 mg Tofacitinib的临床反应率、临床缓解率及不良反应率,各研究进行异质性检验,在进行临床反应率比较时提示异质性较小(P=0.15,I2=46%),使用固定效应模型进行Meta分析,结果显示,10 mg Tofacitinib较5 mg Tofacitinib治疗IBD临床反应率高,差异有统计学意义(RR=1.14,95%CI:1.01~1.30,Z=2.07,P=0.004)(见图18)。在进行临床缓解率比较时提示异质性较小(P=0.71,I2=0),使用固定效应模型进行Meta分析,结果显示,10 mg Tofacitinib与5 mg Tofacitinib治疗IBD临床缓解率比较,差异无统计学意义(RR=1.12,95%CI:0.92~1.35,Z=1.12,P=0.26)(见图19)。在进行不良反应率比较时提示异质性较小(P=0.34,I2=9%),使用固定效应模型进行Meta分析,结果显示,10 mg Tofacitinib与5 mg Tofacitinib治疗IBD不良反应发生率比较,差异无统计学意义(RR=1.06,95%CI:0.97~1.16,Z=1.19,P=0.23)(见图20)。
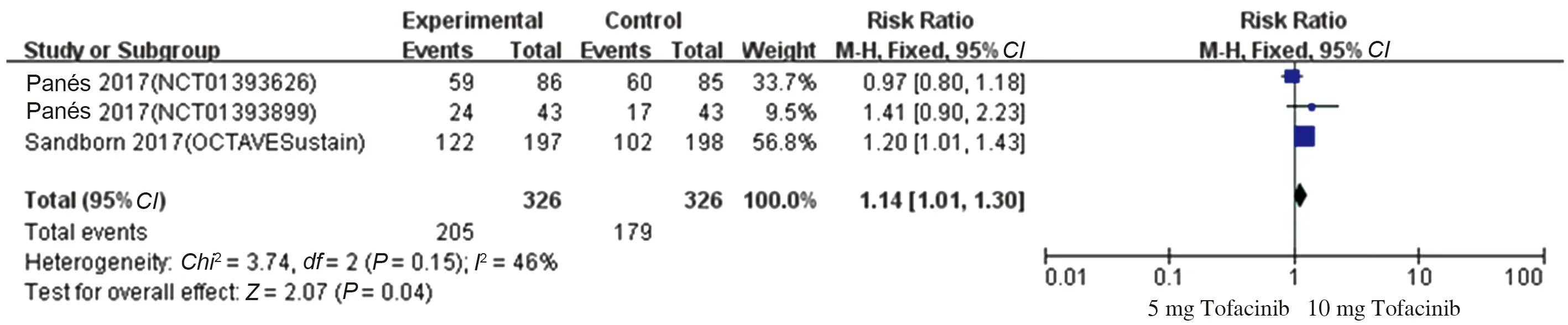
图18 5 mg Tofacitinib vs 10 mg Tofacitinib治疗IBD的临床反应率森林图Fig 18 Forest plot of clinical reaction rate of Tofacitinib treat IBD (5 mg vs 10 mg)
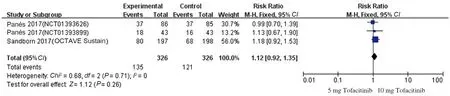
图19 5 mg Tofacitinib vs 10 mg Tofacitinib治疗IBD的临床缓解率森林图Fig 19 Forest plot of clinical remission rate of Tofacitinib treat IBD (5 mg vs 10 mg)

图20 5 mg Tofacitinib vs 10 mg Tofacitinib治疗IBD的不良反应率森林图Fig 20 Forest plot of adverse reaction rate of Tofacitinib treat IBD (5 mg vs 10 mg)
有2项研究[15,17]比较了5 mg Tofacitinib与15 mg Tofacitinib的临床反应率、临床缓解率及不良反应率,各研究进行异质性检验,在进行临床反应率比较时提示异质性较小(P=0.34,I2=0),使用固定效应模型进行Meta分析,结果显示,15 mg Tofacitinib与5 mg Tofacitinib治疗IBD临床反应率比较,差异无统计学意义(RR=0.97,95%CI:0.72~1.31,Z=0.21,P=0.83)(见图21)。在进行临床缓解率比较时提示异质性较小(P=0.37,I2=0),使用固定效应模型进行Meta分析,结果显示,15 mg Tofacitinib与5 mg Tofacitinib治疗IBD临床缓解率比较,差异无统计学意义(RR=0.83,95%CI:0.49~1.41,Z=0.68,P=0.50)(见图22)。在进行不良反应率比较时提示异质性较小(P=0.87,I2=0),使用固定效应模型进行Meta分析,结果显示,15 mg Tofacitinib与5 mg Tofacitinib治疗IBD不良反应发生率比较,差异无统计学意义(RR=1.00,95%CI:0.75~1.33,Z=0.02,P=0.98)(见图23)。
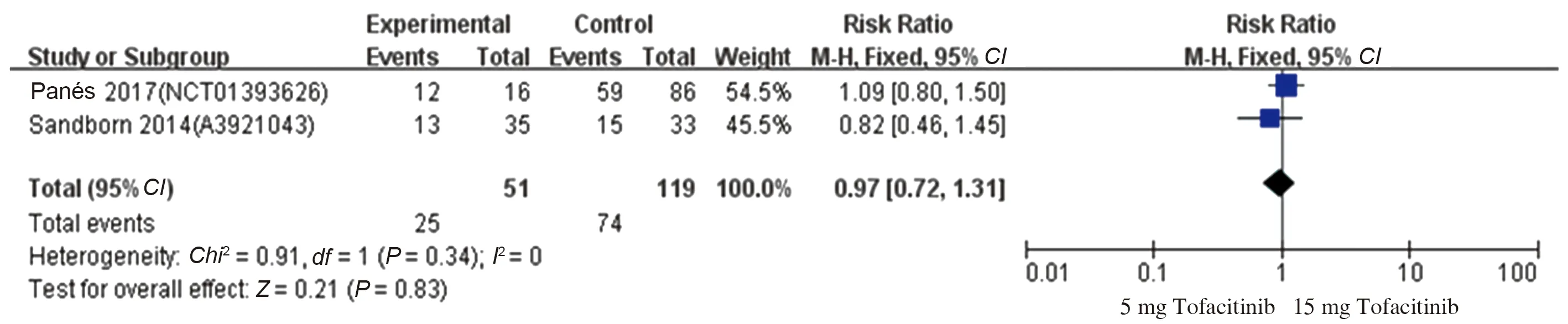
图21 5 mg Tofacitinib vs 15 mg Tofacitinib治疗IBD的临床反应率森林图Fig 21 Forest plot of clinical reaction rate of Tofacitinib treat IBD (5 mg vs 15 mg)
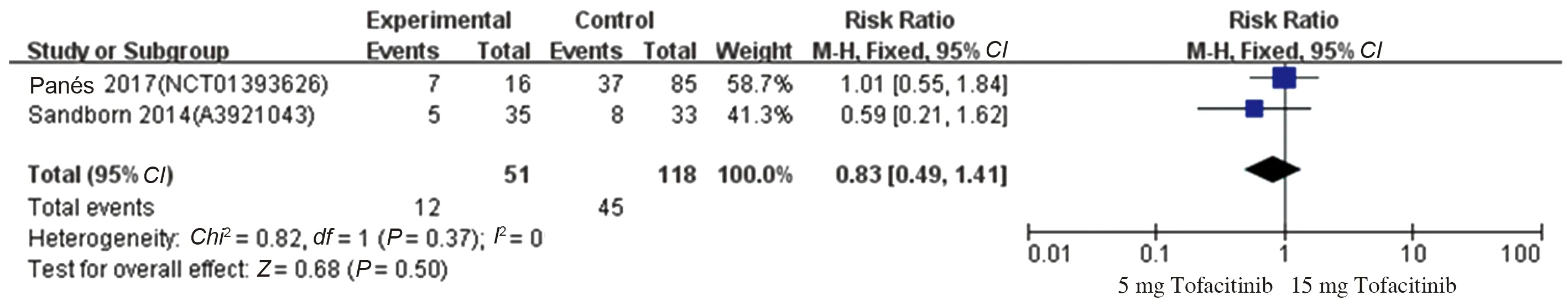
图22 5mg Tofacitinib vs 15 mg Tofacitinib治疗IBD的临床缓解率森林图Fig 22 Forest plot of clinical remission rate of Tofacitinib treat IBD (5 mg vs 15 mg)
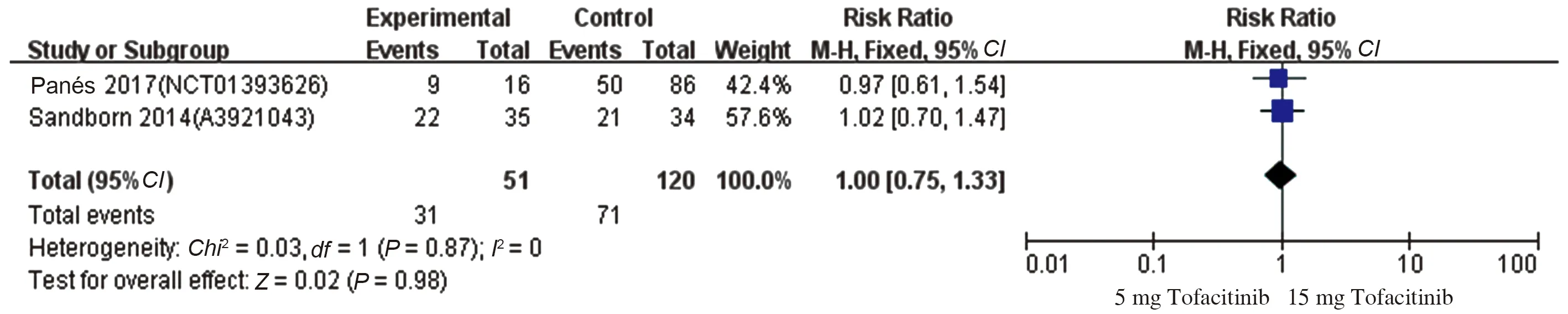
图23 5 mg Tofacitinib vs 15 mg Tofacitinib治疗IBD的不良反应率森林图Fig 23 Forest plot of adverse reaction rate of Tofacitinib treat IBD (5 mg vs 15 mg)
有3项研究[16-17,20]比较了10 mg Tofacitinib与15 mg Tofacitinib的临床反应率、临床缓解率及不良反应率,各研究进行异质性检验,在进行临床反应率比较时提示异质性较小(P=0.28,I2=20%),使用固定效应模型进行Meta分析,结果显示,15 mg Tofacitinib较10 mg Tofacitinib治疗IBD临床反应率高,差异有统计学意义(RR=1.29,95%CI:1.11~1.50,Z=3.23,P=0.001)(见图24)。在进行临床缓解率比较时提示异质性较大(P=0.006,I2=81%),使用随机效应模型进行Meta分析,结果显示,15 mg Tofacitinib与10 mg Tofacitinib治疗IBD临床缓解率比较,差异无统计学意义(RR=1.29,95%CI:0.65~2.57,Z=0.72,P=0.47)(见图25)。在进行不良反应率比较时提示异质性较小(P=0.34,I2=7%),使用固定效应模型进行Meta分析,结果显示,15 mg Tofacitinib与10 mg Tofacitinib治疗IBD不良反应发生率比较,差异无统计学意义(RR=1.09,95%CI:0.87~1.36,Z=0.74,P=0.46)(见图26)。
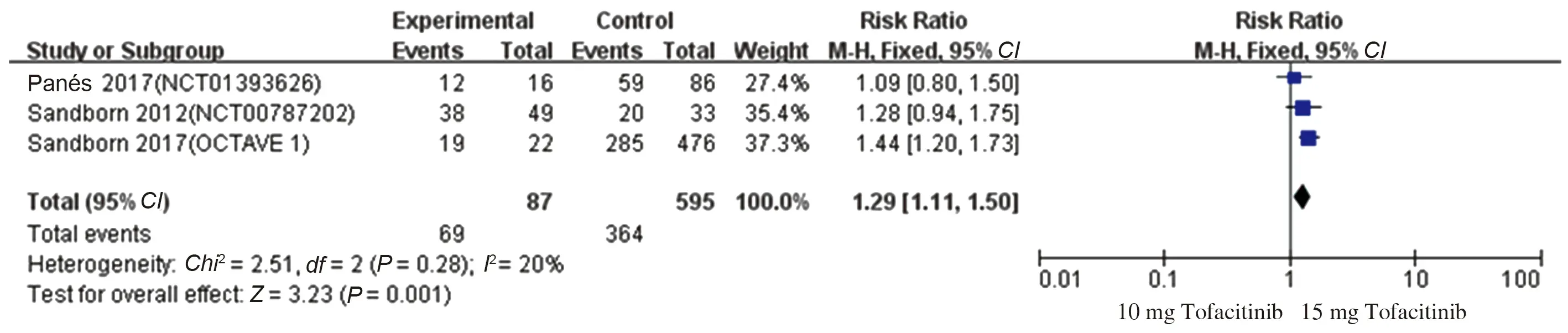
图24 10 mg Tofacitinib vs 15 mg Tofacitinib治疗IBD的临床反应率森林图Fig 24 Forest plot of clinical reaction rate of Tofacitinib treat IBD (10 mg vs 15 mg)
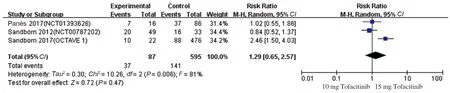
图25 10 mg Tofacitinib vs 15 mg Tofacitinib治疗IBD的临床缓解率森林图Fig 25 Forest plot of clinical remission rate of Tofacitinib treat IBD (10 mg vs 15 mg)
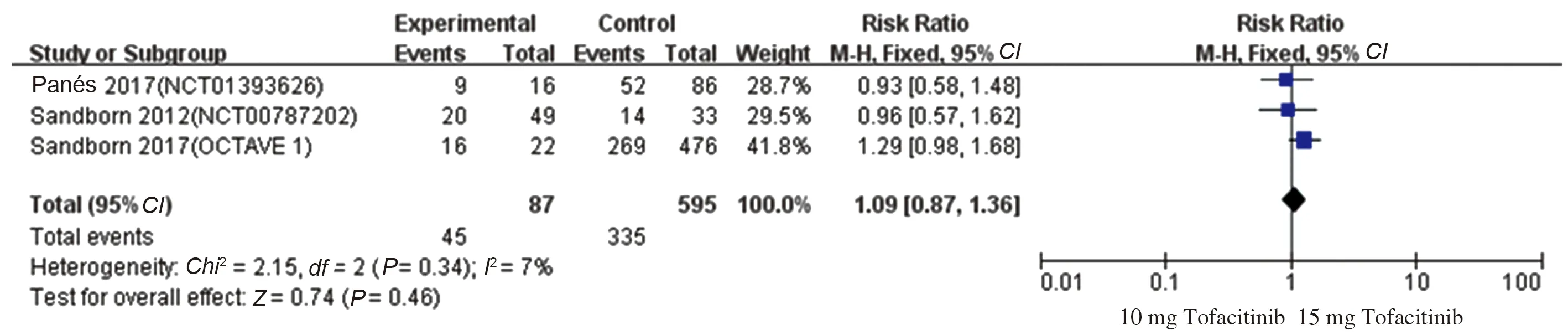
图26 10 mg Tofacitinib vs 15 mg Tofacitinib治疗IBD的不良反应率森林图Fig 26 Forest plot of adverse reaction rate of Tofacitinib treat IBD (10 mg vs 15 mg)
不同剂量Tofacitinib治疗IBD的有效性与不良反应率的直接比较总结如下,结果显示5 mg Tofacitinib、10 mg Tofacitinib与15 mg Tofacitinib临床缓解率率及不良反应发生率比较,差异均无统计学意义(P>0.05),10 mg Tofacitinib与5 mg Tofacitinib及15 mg Tofacitinib与10 mg Tofacitinib比较临床反应率均升高,差异有统计学意义(P<0.05)(见表5)。
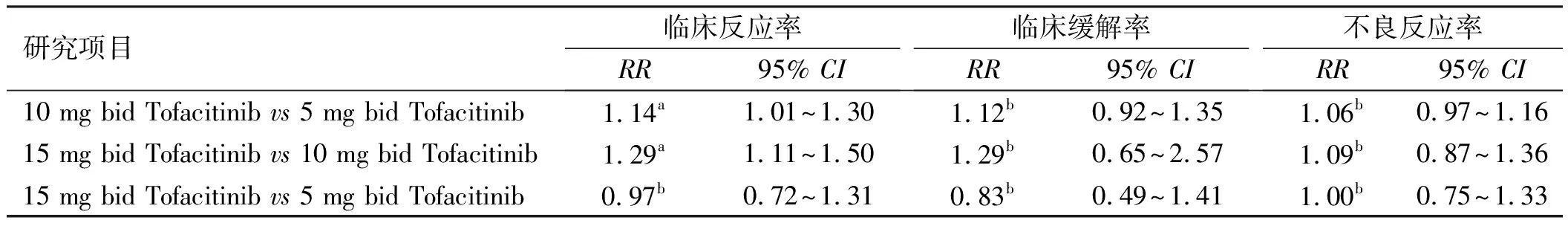
表5 不同剂量Tofacitinib的有效率及不良反应发生率的直接比较Tab 5 Direct comparison of the effective rate and adverse reaction rate of different doses of Tofacitinib
2.5 敏感性分析在对泛JAK抑制剂治疗IBD临床缓解率比较时进行Meta分析时,发现其异质性较高(P=0.0003,I2=75%),对纳入的8项研究[15-17,20,22]进行敏感性分析,逐一剔除1项研究后观察异质性改变,结果显示,剔除Panes等的诱导试验(nduction)(NCT01393626)后各研究间异质性明显下降(见图27)。分析原因可能与试验药物的种类、剂量等有关。
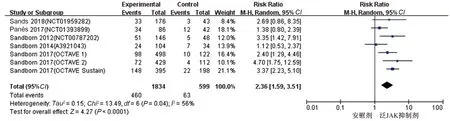
图27 敏感性分析森林图Fig 27 Forest plot of sensitivity analysis
2.6 发表偏倚针对总有临床反应率、临床缓解率、不良反应率三个结局指标绘制漏斗图进行发表偏倚检验,结果显示以总临床反应率为指标的漏斗图各研究点左右并不对称(见图28A),提示存在一定的发表偏倚;以临床缓解率、不良反应率为指标的漏斗图各研究点左右基本对称分布(见图28B~28C),但个别研究离群,提示可能存在的发表偏倚较小。
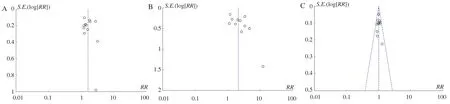
注:A:总临床反应率;B:总临床缓解率;C:总临床不良反应率。
3 讨论
近几十年IBD在激素、5-氨基水杨酸、免疫抑制剂的使用下得到了良好的控制,尤其对肿瘤坏死因子有拮抗作用的生物制剂的使用使IBD的治疗发生了革命性的变化,但高发的原发性无应答和继发性失应答限制了生物制剂的使用[24],随着对IBD发病机制的认识逐渐加深,生物制剂的使用使治疗手段更加丰富。半衰期短、口服给药途径、产生免疫原性的风险低,使小分子药物成为IBD治疗的新热点。托法替布已被美国FDA和欧洲EMA批准用于对传统治疗及生物制剂无应答或不耐受的UC患者,但严重感染、带状疱疹感染及再激活、恶性肿瘤、血栓形成、粒细胞减少等不良反应也限制了其在临床上的应用[25]。JAK抑制剂对于IBD目前仍处于初始阶段相关研究较少,目前缺乏泛JAK抑制剂和JAK1选择性抑制剂治疗IBD直接比较的临床研究,目前也缺少专门对两者疗效进行的Meta分析。JAK抑制最早用于类风湿关节炎的治疗,对于JAK1选择性抑制能否在类风湿性关节炎中有更好的临床获益虽缺乏直接比较的临床研究,但有大量Meta分析能够有一定的提示意义,Lee等[26]基于RCT的贝叶斯网状Meta分析提示Tofacitinib、Filgotinib两种药物严重不良反应发生率差异无统计学意义。Lee等[27]的另一项基于RCT的贝叶斯网状Meta分析提示,Upadacitinib的疗效优于Tofacitinib,但Sung等[28]的基于RCT的网状Meta分析提示,达到ACR50和ACR70应答率的概率排序提示Tofacitinib优于Upadacitinib和Filgotinib。结论存在一定的矛盾,故有必要对此问题进行进一步研究。在基础研究领域中,目前国外有研究表明JAK1是IBD的一个重要治疗靶点,JAK1的激活参与了IL-6、IFN和包括IL-2和IL-15在内含γ链的细胞因子信号传导,JAK1的抑制可有效阻断炎症瀑布的发生[29]。目前JAK2是否是IBD的关键靶点尚不清楚,促炎细胞因子GM-CSF信号传导要通过JAK2,同时抑制JAK1和JAK2可产生更大的抗炎作用。但JAK2的抑制可能与造血系统相关不良反应有关,它能够抑制促红细胞生成素、IL-3、IL-5、催乳素、生长激素的生成。长期的JAK2抑制试验临床尚未开展,但已有体外实验表明JAK2参与血小板的活化,长期抑制JAK2可增加血小板计数甚至导致深静脉血栓形成和发生肺栓塞[30]。选择性三环JAK3抑制剂已经被体外培养。能够不可逆地抑制JAK3酶活性(IC50<100 nmol/L),且具有高选择性。进一步的研究正在进行中,以评估选择性JAK3抑制剂治疗患者的潜在疗效[31]。目前选择性JAK抑制剂正在进入一个研究热潮,目前有大量有关JAK选择性抑制剂的二期、三期临床研究正在快速推进,但在临床上JAK抑制剂的应用是否能获得更好的有效性及安全性仍存在疑问,且缺乏直接比较的临床研究,本文为首次对此问题进行专门的研究。
本研究全面检索了中外文献数据库关于JAK抑制剂治疗IBD的研究,最终筛选出9项泛JAK抑制剂治疗IBD,3项JAK1选择性抑制剂治疗活动性IBD的RCTs,通过对上述文献进行Meta分析得到,两种药物对比安慰剂均能有效提高活动性IBD的临床缓解率及临床反应率,差异有统计学意义,另外与安慰剂相比未明显增加不良反应的发生率。两种药物间接比较的Meta分析显示,JAK1的选择性抑制不能明显提高活动性IBD的临床缓解率及临床反应率,也不能降低不良反应的发生风险,差异均无统计学意义。关于托法替布治疗IBD的研究中剂量多为5 mg bid、10 mg bid和15 mg bid,通过对不同剂量组进行Meta分析显示,Tofacitinib 5 mg bid治疗活动性IBD患者与安慰剂组相比不能明显提高患者的临床缓解率及临床反应率,不良反应率组间差异无统计学意义,Tofacitinib 10 mg bid组与15 mg bid组较安慰剂组均能明显提高活动性IBD的临床缓解率及临床反应率,不良反应率组间差异无统计学意义。Tofacitinib 15 mg bid组与10 mg bid组相比能提高活动性IBD患者的临床反应率,但对于临床缓解率无明显提高,不良反应率在组间差异无统计学意义。
本研究存在以下几个方面局限性。第一,虽制定严格的检索策略,但仍可能有部分文献未能被检出,且本研究纳入文献均为已发表文献。第二,试验药物的种类、剂量、疗程等不统一,患者同时使用免疫调节剂、激素等药物的种类、剂量未能完全统一。第三,关于JAK1选择性抑制剂治疗IBD的随机试验较少,样本量较小。第四,关于不同剂量Tofacitinib治疗IBD之间的随机试验较少,样本量较小。这些局限性可能对结果的可靠性有一定影响。
总之,本研究表明,泛JAK抑制剂与JAK1选择性抑制剂治疗IBD的疗效及安全性相当;Tofacitinib 15 mg bid临床反应率优于Tofacitinib 10 mg bid,Tofacitinib 10 mg bid临床反应率优于Tofacitinib 5 mg bid,临床缓解率及不良反应率在不同剂量组之间相当。这对新一代JAK抑制剂的研究方向具有一定的指导意义,目前包括选择性JAK1抑制剂及选择性JAK3抑制剂正在研究中,对于JAK亚型选择性抑制能否提高临床疗效,获得更好的安全性,就目前有限的研究证据显示,两者之间的疗效及安全性相当,但目前选择性JAK抑制治疗活动性IBD的临床研究较少,因此未来采用更多的多中心、大样本量,更长疗程的双盲、临床RCT以验证上述结果是非常有必要的。针对Tofacitinib剂量选择问题,就当前有限的证据显示,以Tofacitinib治疗活动性IBD患者,5 mg bid的疗效不理想,当剂量增至10 mg bid时才开始对活动性IBD有明显的治疗效果,若10 mg bid治疗不理想时可增量至15 mg bid可改善疗效。受纳入研究数量和质量的限制,上述结论仍有待更多高质量的研究加以验证。
