A型禽流感病毒H7N9株NS1基因的克隆和真核表达
2021-09-29黄海岩刘新宇蔡葵蒸
黄海岩,刘新宇,蔡葵蒸
(西北民族大学 生命科学与工程学院,甘肃 兰州 730030)
禽流感(Avian Influenza,AI)是一种由禽流感病毒(Avian Influenza Virus,AIV)引起的易感染禽类(鸡、鸭、鹅)以及哺乳动物和人的人畜共患病。该病主要以呼吸道飞沫传播为主,因而传播速度快,严重危害着养禽业的发展。人的感染主要是接触患病的禽类及其排泄物,粪口传播亦能引起感染,虽未见人和人的传播,但对公共卫生及人类健康造成的威胁不可小觑。国际兽疫局将禽流感定为A类传染病,我国也将其列为一类动物传染病。禽流感病毒在分类上属于正黏病毒科,根据病毒的核蛋白和膜蛋白等特性的差异,又分为A、B、C三型[1],A型最易引起传染,宿主多样,能够感染禽、猪、马和人类,每次流行时感染范围大,常导致世界性的大流行[2]。
流感病毒有2种表面抗原,分别为血凝素(HA)和神经氨酸酶(NA),依次将该病毒分为若干亚型。根据报道,已知有H亚型16个(H1~H16),N亚型10个(N1~N10)[3]。据研究,世界各地的海鸟和水禽都是流感的天然贮存宿主[4,5]。
由于流感病毒的变异,人感染流感是由于禽类贮存宿主流感病毒的遗传物质重现所引起[6]。AIV最早感染人的亚型是H7N7,是从人的眼分泌物中分离得到,1997年我国香港发生H5N1型AIV感染人并导致死亡的病例,突破了只有H1、H2、H3亚型AIV感染人及哺乳动物的界限[7]。本研究中涉及H7N9亚型AIV,曾经有一段时间认为并不感染人,但自从2013年首次发现人类感染以来,病例不断增多且有蔓延趋势,至2017年累计感染人1 344例,其中511人死亡,致死率高达38%[8],应引起公共卫生界的高度关注。
AIV基因组是由8条单股的RNA片段构成,这些片段编码10种病毒蛋白,其中2个较小的RNA片段编码了2种非结构蛋白(Nonstructural proteins,NS)[9],分别为NS1和NS2,它们由2个读码框翻译,NS1蛋白分子量为22~28 KD,是一个易活性的转录活性剂[10]。NS2的阅读框不连续分子量为12 KD。NS1蛋白是唯一的转录后调控子,具有N端RNA结合R和C端效应区两个功能域[11]。NS1蛋白是一个参与禽流感病毒致病力的主要蛋白质,在感染早期与宿主蛋白发生相互作用后就大量表达,主要聚集于宿主细胞核内,能诱导宿主产生早期感染的抗体。据此可以区分野毒感染和人工免疫抗体,作为禽流感早期诊断指标[12],NS1还可抑制宿主蛋白的表达与转运[13],可能扮演着损害被病毒感染宿主细胞的重要角色,在病毒致病性中发挥着重要作用。因此,NS1在禽流感免疫学研究及病毒早期诊断中有较大的应用价值。
王晶钰等[14]对H9N2亚型禽流感病毒NS1基因进行了原核表达和真核表达研究。本研究的目的是扩增H7N9亚型禽流感病毒分离株NS1基因,构建真核表达载体,同时利用293T细胞进行表达,为日后进一步研究NS1蛋白的功能及H7N9亚型禽流感的诊断提供参考。
1 材料与方法
1.1 材料
1.1.1 病毒株 H7N9亚型禽流感病毒株系中国农业科学院兰州兽医研究所提供和保存。病毒接种于10日龄SPF鸡胚尿囊腔,无菌收集死亡后鸡胚的尿囊液,置-20℃冰箱保存备用。
1.1.2 细胞系和菌株 DH5a感受态细胞及293T细胞,保存于中国农业科学院兰州兽医研究所畜禽疾病重点实验室。
1.1.3 主要试剂设备 本研究中主要试剂及仪器见黄海岩等[15]关于A型禽流感病毒H7N9株M1基因的克隆和表达。
1.2 方法
1.2.1 PCR引物 用引物设计软件(Primer 5.0)设计特异性引物,其序列如下:5’-GATGTCG ACCATGGATTCCAATACTGTGTC-3’为上游引物,5’-CTGGCGGCCGCCTACTTTGTAGAGAG TGG-3’为下游引物,引物由华大基因公司合成,扩增产物大小预期为654 bp。
1.2.2 总RNA提取和PCR扩增 按照试剂盒的操作说明书,直接从鸡胚尿囊液中抽提所需试验病毒株的基因组RNA,根据反转录试剂盒的接种说明书合成cDNA。扩增目的基因的PCR体系为50 μl;模板cDNA 0.05 μl(50 mg),NS1上下引物各2.5 μl,5*PCR buffer 10 μl,dNTP 1 μl,DNA聚合酶1 μl,补去离子水至50 μl,按照黄海岩等[15]报道的方法设计PCR扩增反应参数,获得PCR扩增产物后于4℃保存。
1.2.3 NS1基因真核表达载体的构建 参照王晶钰等[14]的方法,将上述PCR产物与真核表达载体PRK-FLAG双酶切后,在T4连接酶的作用下链接,获得真核表达质粒PRK-FLAG-NS1,连接产物转化至DH5a感受态细胞,再经Sa1 I和Not I内切酶,PCR鉴定,菌液送华大基因公司测序鉴定。
1.2.4 重组NS1基因在293T细胞中的表达 取培养在10%胎牛血清中的传三代293T细胞,参照杜江龙等和王晶钰等的方法,重组NS1质粒转染于293T细胞,在37℃、5% CO2条件下,培养转染细胞。
1.2.5 表达产物的Western blot分析 参照王晶钰等[14]的方法收集培养48 h后的细胞,用0.5%胰酶消化细胞,离心等处理后作为蛋白电泳的样品。部分样品进行SDS-PAGE电泳分析,考马斯亮蓝染色;部分样品置于转膜中进行Western blot分析。
2 结果
2.1 NS1基因RT-PCR扩增
以A型流感病毒H7N9株的总RNA为模板完成RT-PCR扩增后,产物经琼脂糖凝胶电泳,得大小约650 bp左右条带(见图1)。查阅相关资料,与预期和NS1基因实际大小相符合。
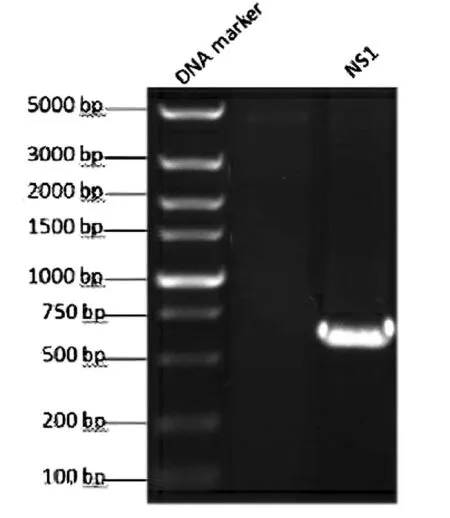
图1 A型流感病毒H7N9株NS1基因RTPCR产物凝胶结果
2.2 NS1基因的酶切鉴定
经双酶切获得NS1基因条带,NS1基因大小为654 bp(见图2),证明NS1基因真核重组质粒构建成功。由图2可知,左侧和右侧分别为15 000 bp、2 000 bp 的marker,NS1基因的条带位于500~750 bp。

图2 A型流感病毒H7N9株NS1基因的重组质粒酶切鉴定
2.3 Western Blot蛋白鉴定
转染pRK-FLAG-NS1后的293T细胞表达的重组蛋白可以被FLAG抗体识别,且重组蛋白实际大小与预期大小相同,空载体没有阳性结果,说明NS1基因在293T细胞中成功表达(见图3)。此外,蛋白印记表明,H7N9-NS1的蛋白大小为23.9 KD,与基因大小相符。
图3 A型流感病毒H7N9株FLAG-NS1的蛋白印记表达
3 讨论
本研究利用RT-PCR克隆出禽流感H7N9亚型分离株NS1基因,基因大小与引物设计片段一致,经阴性克隆、酶切鉴定,构建了NS1基因真核重现质粒,瞬时转染293T细胞,通过转染的培养细胞裂解后进行Western Blot分析,获及的蛋白大小为23.9 KD,与预期结果相符,从而在转染细胞中成功表达了NS1蛋白。
目前世界上高度重视有关禽流感的研究。流感病毒的传统检测方法包括血清学试验和免疫荧光技术等,鸡卵培养多是诊断流感不同亚型的确切依据,但病毒培养由于耗时费力、工作量大,难以在实际生产中实施。分子生物学诊断技术发展迅猛,如RT-PCR(逆转录-聚合酶链反应)、RRT-PCR(实时RT-PCR)、RT-LAMP(逆转录-环介导等温扩增技术)和基因芯片技术,这些技术检测禽流感需要的样品量少,具有特异性好、敏感性强、最为有效等特点。
研究表明,NS1蛋白作为ELISA检测抗体,能成功区分野毒感染马和人工免疫马[16]。Tumpey等研究证明[17],NS1蛋白作为检测抗体可以区分野毒感染鸡群和灭活疫苗接种鸡群[18],显示出其未来在疫苗免疫和野毒感染的鉴别诊断方向有着广阔的应用前景。
