感染后继发性机化性肺炎1例的报道
2021-09-28梁培干黄淑贤罗秋平邱峻詹淑娜谭少兴
梁培干,黄淑贤,罗秋平,邱峻,詹淑娜,谭少兴
(1.广州中西医结合医院 呼吸科,广东 广州 510800;2.炭步镇中心卫生院,广东 广州 510820)
0 引言
机化性肺炎(Organizing Pneumonia, OP)指发生于肺部的炎症,由于各种原因治疗不彻底导致炎症病变不吸收或吸收延迟,肺组织损伤后的一种炎性反应、机化,临床表现缺乏特征性,与其他呼吸系统疾病并无太大区别,极易误诊为肺炎、肺结核及肺真菌感染、肿瘤等,其按病因可分为特发性的隐源性机化性肺炎(COP)和发生于多种病因的继发性机化性肺炎(SOP)。近些年来,COP已逐渐为业界所认识,将之归入特发性间质性肺炎的范畴[1],但是对SOP的研究较少,未得到足够的重视,现对我院明确诊断和治疗的感染后导致的继发性机化性肺炎1例进行报道和讨论。
1 病例资料
患者男性,52岁,务农。因“发热伴咳嗽3天”于2020年3月23日入住我院呼吸科。患者入院前3天无明显诱因下出现发热,体温最高达39 ℃,咳嗽,少痰,胸闷,无呼吸困难,无咯血。至门诊查胸部CT提示右肺多发斑片状增密影,考虑感染性病变(病原体待查),见图1,拟“肺炎”收入院。既往10余年前外院诊断“结核性胸膜炎”,经治疗后痊愈,余无特殊。入院查体:体温(T):38.5 ℃,精神稍差,右肺呼吸音稍减弱,可闻及少量湿性啰音,余未见明显异常。入院后辅助检查:血常规:WBC 7.23×109/L,N 76.2%,Hb104 g/L,PLT 251×109/L;CRP 98.3 mg/L,PCT 0.23 ng/mL,肝肾功能、电解质、肺肿瘤五项未见明显异常,风湿免疫11项:RF 49.3 IU/mL,抗SSB(+),抗SSA(+-),抗Ro-52(+);CD4/CD8/CD3细胞免疫检验:CD4220;CD8152;CD3400;CD4/CD81.45。血清G、GM试验、HIV抗体、呼吸道病毒七项、肺炎支原体IgM、抗核抗体、抗双链DNA、抗SM抗体、TB-DNA、T-SPOT:均阴性,肺泡灌洗液Xpert MTB:阴性;痰涂片及培养未见真菌、细菌及抗酸杆菌,3月27日血培养为金黄色葡萄球菌,对苯唑西林、青霉素耐药,肺泡灌洗液病原体宏基因组检测报告(NGS):检出屎肠球菌特异性序列数73条,以及常见的呼吸道菌群。考虑CAP、败血症,入院先后予哌拉西林钠舒巴坦钠、左氧氟沙星、万古霉素、利奈唑胺,抗感染治疗3周,患者仍有发热,逐渐出现呼吸困难,复查胸部CT显示肺部病灶明显进展,见图2。遂行右下肺经皮肺穿刺活检,病理提示:(右肺下叶肺组织)局灶肺泡上皮增生,肺泡腔内可见少许纤维素渗出,有机化灶形成,间质淋巴细胞浸润,组织改变为肺机化性肺炎,见图3。最终诊断:肺炎伴继发性机化性肺炎,于4月16日给予甲泼尼龙琥珀酸钠(40 mg VD QD)抗炎治疗,患者体温用药后第2天即恢复正常,呼吸困难亦明显缓解,于4月22日出院,出院当天复查胸部CT病灶大部分吸收,见图4。出院后继续口服甲泼尼龙片(40 mg PO QD)并逐渐减量,总疗程6个月,患者未再出现发热症状,电话随访至今病情无复发[2]。

图1 3月22日胸部CT病灶图像

图2 4月5日胸部CT病灶图像

图3 右下肺穿刺活检病理
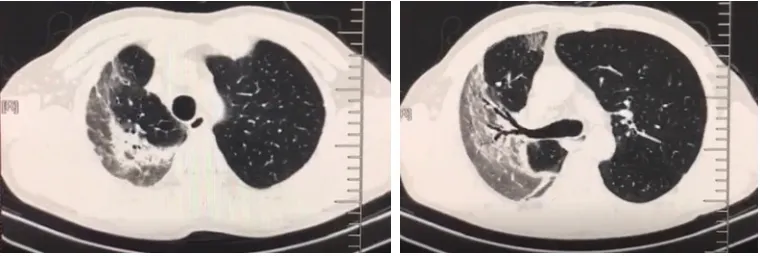
图4 4月21日胸部CT病灶图像
2 讨论
SOP病因多样,包括感染(各种病原体)、药物(胺碘酮、金制剂等)、吸入、可卡因中毒、放射性损伤、免疫相关性疾病(红斑狼疮、类风湿关、肌炎和皮肌炎等)、器官/骨髓移植、炎症性肠病、肝硬化等[3]。机体受病原微生物感染后,虽经抗感染治疗,病原体得到部分或全部清除,但肺泡及末梢细支气管炎症吸收不完全,且持续的炎症反应导致了肺泡腔内纤维蛋白渗出,从而导致感染后SOP的发生。检索近年国内外文献,已知可引起SOP的包括病毒、细菌、真菌、寄生虫,如甲型流感病毒、副流感嗜血菌、金黄色葡萄球菌、铜绿假单胞菌、大肠埃希菌、烟曲霉、黄曲霉、白色念珠菌等[4]。其中细菌感染后继发的OP,临床实践中很容易被误诊为单纯的细菌感染,往往给予大量抗菌药物抗感染仍效果甚微,延误病情并导致医疗资源浪费。
本例最初由于存在呼吸道感染症状,查体时发现湿啰音,化验示外周血中性粒百分比及CRP升高,胸部CT示肺渗出、实变影,后先后查出金黄色葡萄球菌、屎肠球菌等菌种,细菌感染明确,于我院门诊及入院后一直按CAP、败血症治疗,先后给予针对性的强有力之抗菌药物达3周未取得显著疗效仍未及时更改诊治方案,后行肺穿刺活检才得以明确病因,因此如何早期识别感染后SOP对于临床的诊治有重大的意义。
感染后SOP的诊断主要依靠相关临床表现(发热、干咳、呼吸困难等)、明确的病原学、影像学典型表现、规范足疗程抗感染治疗无效并排除其他已知原因(如结缔组织疾病、肿瘤化疗、服用药物、器官移植等),且典型病理提示由疏松肉芽结缔组织充填于肺泡和终末气道内。李惠萍等[5]研究提示COP影像学表现为多发性、多形态、多变性、多复发性、多双肺受累但蜂窝肺少见,总结为“五多一少”,最典型的表现为双肺多发的斑片状实变影,可伴见网格状、结节状,反晕征、空洞、胸腔积液则相对少见。相关研究者发现大体而言SOP和COP在影像学的表现方面差别并不明显,而相关学者的研究则发现SOP患者似乎更倾向出现胸腔积液,国内报道有表现为片状实变影,可见支气管充气征,但未见病灶的游走性及多变性的,有表现为孤立的局灶型肺部阴影,有支气管充气征,常位于上肺,与局灶性机化性肺炎类似的。SOP和COP影像学上是否有区别、区别大小还有待于进一步大样本的病例研究。
本病例依据临床及病理确诊为SOP应无异议,考虑感染所致可能性大,但临床尚存在一些疑点,患者风湿免疫11项提示RF偏高,抗SSB、抗Ro-52抗体为弱阳性(+),抗SSA抗体为可疑阳性,而CD4/CD8/CD3细胞免疫检验亦示患者CD4及CD8计数值偏低,提示免疫功能下降。综上,提示患者存在免疫缺陷状态,是患者本身存在风湿免疫疾病如类风湿性关节炎因而导致患者感染后出现了继发性机化性肺炎,抑或是感染性机化性肺炎本身导致的免疫低下。由于患者病愈后拒绝进一步的检查,因而对于本例无法得出最终的结论,但此问题值得我们在今后的临床工作当中加以留意。
糖皮质激素是目前治疗机化性肺炎的主要方法,SOP除了使用糖皮质激素治疗外,同时还要针对病因治疗,对于感染后SOP尽量明确病原体并进行规范的抗感染治疗。大部分感染后SOP患者接受糖皮质激素及规范足疗程抗感染治疗后临床症状和影像学变化可大部分甚至全部消失[6],预后较好,但激素减量过快或过早停药病情可能复发。糖皮质激素的用量、疗程尚未统一,本例患者起始予甲泼尼龙40 mg/d,后根据病情逐渐减量,总疗程6个月,随访病情未复发。
综上所述,对于存在明确感染,临床表现为发热、咳嗽、咳痰、痰中带血、胸闷痛伴逐渐加重的呼吸困难,血氧分压下降,胸部影像学主要表现为双肺多发斑片状渗出、实变,经规范的抗感染治疗无明显效果的患者,需注意感染后SOP的可能,有条件及时获取组织病理学加以诊断,治疗应及时给予糖皮质激素。
