荞麦蜜对酒精诱导的小鼠肝损伤和肠道菌群失调的改善效果
2021-09-27朱静宇王峻金秀娥陈向丹刘睿鲁群
朱静宇,王峻,金秀娥,陈向丹,刘睿,3,4,鲁群,3
1.华中农业大学食品科学技术学院/环境食品学教育部重点实验室,武汉 430070; 2.湖北省农产品质量安全检测中心,武汉 430070; 3.武汉市蜂产品质量控制工程技术研究中心,武汉 430070;4.农业农村部都市农业重点实验室,武汉 430070
饮酒与健康是全世界人们广泛关注的热点问题,长期或过量的饮酒对身体是有害的。肝脏是酒精代谢的主要场所,长期或过量饮酒容易引起酒精性肝病(alcoholic liver disease,ALD),其发展进程依次为:酒精性脂肪肝(脂肪变性)、脂肪性肝炎、酒精性肝纤维化、肝硬化、肝细胞癌[1]。90%~ 95%大量饮酒的人会发生脂肪变性,10%~ 40%最终会发展为肝纤维化[2]。最近研究表明“肠-肝”轴参与了ALD的发展,酒精滥用会导致肠道菌群失调,肠道通透性升高,细菌及其产物进入门静脉系统和肝,引起肝细胞损伤,从而导致酒精性肝病[3-4]。因此,通过膳食或者药物调节肠道菌群可能减缓ALD的发展。
蜂蜜是蜜蜂采集植物的花蜜、分泌物或蜜露,与自身分泌物结合后,经充分酿造而成的天然甜物质,具有多种生物活性[5],是我国药食同源目录中的物质。已有文献[6-7]报道部分蜂蜜可以改善酒精引起的肝损伤,但少见关于蜂蜜干预酒精诱导的肠道微生物失衡延缓ALD的研究报道。荞麦蜜,蜜源植物为荞麦,主要产自我国东北三省和内蒙古、宁夏、甘肃等地,是一种深琥珀色、具有强烈刺激性气味的蜂蜜。与其他品种蜂蜜相比,荞麦蜜具有较高含量的酚类化合物、矿物质、蛋白质和维生素,从而具有更高的营养价值和抗氧化、抗菌等生物活性[8-9]。但由于荞麦蜜自身的刺激性气味和色泽,导致其食用和药用价值未被合理开发利用[10]。因此,本研究通过建立小鼠酒精性肝损伤模型,探讨荞麦蜜对酒精性肝损伤的保护作用以及对酒精引起的肠道菌群失衡的调节作用,以期进一步挖掘荞麦蜜护肝功能特性,提高荞麦蜜的接受度和商业价值。
1 材料与方法
1.1 材料、试剂与实验动物
荞麦蜜,产地为阿尔泰,由武汉乐神三宝蜂业有限公司提供;Lieber-Decarli酒精液体鼠粮和Lieber-Decarli对照液体鼠粮购买于戴茨生物科技(无锡)有限公司;谷草转氨酶(AST)、谷丙转氨酶(ALT)、丙二醛(MDA)、超氧化物歧化酶(SOD)试剂盒,南京建成生物工程研究所;总胆固醇(total cholesterol,TC)、甘油三酯(TG)试剂盒,浙江东瓯诊断产品有限公司;肝脏病理学切片,武汉市皮诺飞生物科技有限公司;其他试剂均为分析纯或色谱纯。
SPF级雄性C57BL/6小鼠,体质量(18±2) g,许可证号:SCXK(鄂)2017-0012。
1.2 仪器与设备
HI96785蜂蜜色度测定仪,哈纳水环境工程(上海)有限公司;配有示差折光检测器的高效液相色谱仪,岛津20AD,日本岛津公司;Agilent 7800 ICP-MS,美国Agilent公司;全波长酶标仪,美国Thermo Fisher公司;F6/10手持式高速匀浆机,上海净信实业发展有限公司;低温高速冷冻离心机,德国Ependoff公司;倒置荧光显微镜,日本尼康公司。
1.3 荞麦蜜主要理化性质与成分测定
色度的测定采用SN/T 0852-2012《中华人民共和国出入境检验检疫行业标准 进出口蜂蜜检验规程》 中专用的卜方特比色计比色法。用蒸馏水进行调零,将不含气泡的试样倒入卜方特(Pfund)比色槽内,以卜方特比色计进行比色读取色值后确定色泽,色值单位为mm。
总酚含量的测定参照Folin-Ciocalteu比色法[11]。
糖含量的测定参考文献[8]中的方法,并略有改动。采用40%乙腈溶液配制成0.04 g/mL样品溶液,采用高效液相色谱仪进行分析,色谱柱为NH2氨基柱(4.6 mm × 150 mm,5.0 μm),柱温35 ℃。流动相为乙腈∶水= 8∶2(V/V),流速1 mL/min,进样量20 μL。
矿物质元素的测定参考国家标准GB 5009.268-2016 《食品安全国家标准 食品中多元素的测定》。
1.4 动物实验方案
动物模型参照Bertola等[12]报道的小鼠实验模型。雄性SPF级C57 BL/6小鼠在12 h的光/暗循环中饲养,环境温度控制在18~26 ℃,相对湿度为40%~70%。将小鼠分为空白对照组(C)、酒精模型组(M)、荞麦蜜干预组(B),每组10只,用Lieber-Decarli对照液体鼠粮适应性喂养5 d后,第6天开始样品组以10 g/kg的剂量灌胃荞麦蜜,同时空白对照组和酒精模型组给予7.8 g/kg剂量的麦芽糊精灌胃,除空白对照组用Lieber-Decarli对照液体鼠粮进行喂养外,其他各组小鼠用Lieber-Decarli酒精液体鼠粮进行喂养,连续10 d,并在第15天收集粪便。在第16天,除空白对照组给予麦芽糊精溶液外,其他组均给予31.5%乙醇按小鼠体质量的2%灌胃。9 h后,取血和肝脏。血液于4 ℃、5 000 r/min离心15 min后分离血清,待测。肝脏取部分加入组织固定液固定用于组织病理学观察,其余冰浴制成10%匀浆液,于4 ℃、3 500 r/min离心10 min后分离上清于-80 ℃保存,待测。
1.5 小鼠体质量变化和肝脏指数测定
肝脏是酒精代谢的主要场所,过量饮酒会导致热量增加、摄食减少、代谢异常等情况,使得营养物质缺乏,加剧对肝脏的损伤,体质量和肝脏指数的变化在一定程度上可以反映肝脏的损伤程度。建立模型期间,每天记录小鼠体质量,计算各组小鼠体质量的变化量。解剖取出肝脏后,用预先冷却的生理盐水洗去血液,用滤纸吸干并称质量。肝脏指数按照公式(1)计算:
肝脏指数= 肝脏质量/小鼠体质量×100%
(1)
1.6 生化指标测定
ALT升高反映了肝细胞膜的损伤,AST升高表明肝细胞损伤到了细胞器,AST和ALT是反映肝损害和样品是否有保护肝损伤效果的最直接和最重要的指标。酒精性肝损伤的初期表现为酒精性脂肪肝,而TC和TG是评估脂肪肝发生风险和病情分度的重要指标,其中TG的关联度更高。活性氧自由基引发的氧化应激是多种肝损伤发生的共同病理生理基础,MDA、SOD指标可以反映机体脂质过氧化和氧化应激程度。血清AST、ALT活力、肝脏TC、TG含量、血清MDA含量、肝脏SOD活力等指标的测定参照试剂盒说明书进行。
1.7 肝脏组织病理学观察
肝脏组织固定后,经过梯度乙醇脱水和石蜡包埋后用病理切片机进行切片,将切片再次经过梯度乙醇脱水、脱蜡后用苏木精-伊红染色,在光学显微镜下观察切片病理学形态。
1.8 小鼠粪便微生物分析
肠道菌群与肝脏疾病的发生、发展有着紧密的联系。评估肠道菌群稳态通常分析其物种多样性和丰富度的变化、物种组成差异等。其中,α多样性反映了样本微生物群落的丰富度和多样性,包括Simpson指数、Shannon指数、Chao指数、Good’s coverage指数等。Shannon指数包含着物种数和各种间个体分配的均匀性两个部分。样品多样性越高,个体分配越均匀,Shannon指数值就越大。Simpson指数是随机抽取的2个个体属于不同种的概率。Simpson指数越高,表明群落多样性越高。Chao指数反映群落丰富度,即群落中所含物种种类的多少。Good’s coverage指数反映测序深度,指数越接近于1,说明测序深度已经基本覆盖到样品中所有的物种。PCA图可以直观反映样本微生物群落差异,样本组成越相似,反映在PCA图中的距离越近。取小鼠粪便,提取其中的DNA,并对16S rDNA进行扩增,送往上海欧易生物医学科技有限公司进行高通量测序。对测序结果优化处理后进行OUT聚类,对物种进行注解,然后进行α多样性分析、物种组成分析等。
1.9 数据分析
本研究数据采用SPSS软件进行统计学显著性分析,多组间比较采用单因素方差分析(ANOVA),采用Duncan’s多重比较法检验数据的差异显著性。
2 结果与分析
2.1 荞麦蜜的主要理化性质与成分
蜂蜜的抗氧化活性与其组成成分相关,尤其是酚类化合物、矿物质等,因此对荞麦蜜中的主要相关成分进行了测定。荞麦蜜的色度值为150 mm,为深色蜜。果糖和葡萄糖的含量为43.03和35.19 g/100 g,二者总和超过60 g/100 g,蔗糖未检测出,符合GB 14963-2011对蜂蜜糖含量的规定。重要的是荞麦蜜的总酚含量高达(145.81±3.93) mg/100 g,明显高于其他品种的蜂蜜[13]。而且荞麦蜜中矿物质元素种类丰富,钾是主要的矿物质元素(221.22 mg/kg),其次是钙、镁、锰、铁、钠、铝、铜、锌等(分别为27.94、11.87、5.48、4.84、3.27、2.11、0.56、0.46 mg/kg),这些矿物质均可以影响蜂蜜的价值。此外,蜂蜜中的铅、镉、汞等重金属含量符合GB 2762-2017中规定的限量值。
2.2 荞麦蜜对酒精引起的肝损伤小鼠体质量和肝脏指数的影响
小鼠体质量和肝脏指数的变化结果见图1。如图1A所示,与空白对照组相比,酒精的摄入使小鼠体质量显著减轻(P<0.05);而相对于酒精模型组,荞麦蜜的摄入明显减缓了小鼠体质量的下降(P=0.075),说明荞麦蜜可以减缓饮酒导致的体质量降低。由图1B可知,与空白对照组相比,酒精模型组的肝脏指数明显升高(P<0.05);而荞麦蜜干预组的肝脏指数与酒精模型组相比出现一定程度的降低(P=0.087)。
2.3 荞麦蜜对酒精引起的肝损伤小鼠血清ALT和AST的影响
小鼠血清中ALT和AST活力测定结果如图2所示。酒精模型组的ALT和AST活性明显高于空白对照组(P<0.05),说明肝细胞受到严重损伤;但是给予荞麦蜜干预后,与酒精模型组相比,样品干预组的ALT和AST显著降低(P<0.05),尤其是血清中AST活性几乎恢复到空白对照组水平(P>0.05)。说明荞麦蜜对酒精诱导的小鼠肝脏细胞膜和肝内细胞器的损伤具有较好的修复效果,肝脏功能明显改善。

C.空白对照组;M.酒精模型组;B.荞麦蜜干预组。下同。*表示与空白组相比有显著性差异(P<0.05)。C.Control group; M.Model group; B.Buckwheat honey group. The same as below. *indicates significant difference compared with the control group(P<0.05 ).
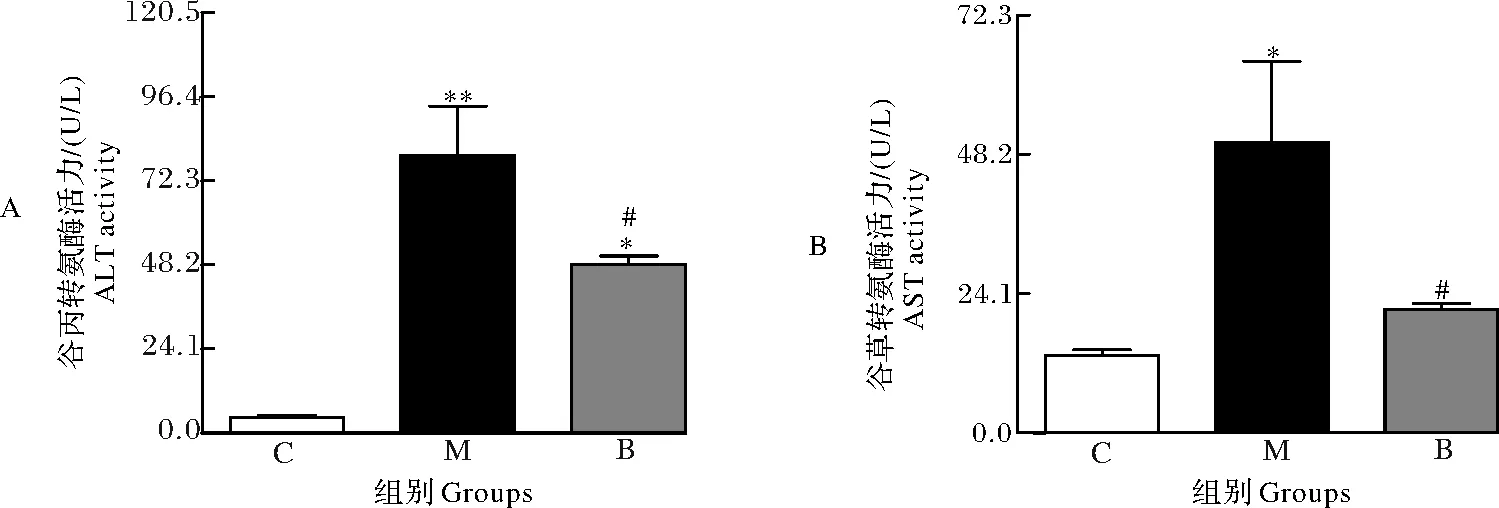
*表示与空白对照组相比,在α=0.05水平上有显著性差异;#表示与酒精模型组相比,在α=0.05水平上有显著性差异;下同。* indicates significant difference compared with the control group(P<0.05). “#” indicates significant difference compared with alcohol model group(P<0.05).The same as below.
2.4 荞麦蜜对酒精引起的肝损伤小鼠肝脏TC和TG的影响
对肝脏中的TC和TG含量进行测定。由图3可知,持续的酒精饲喂导致小鼠肝脏中TC和TG水平显著升高(P<0.05),诱导脂肪肝的形成。通过摄入荞麦蜜进行干预,略降低了小鼠肝脏中TG含量(P>0.05),但对TC改善效果不明显。
2.5 荞麦蜜对酒精引起的肝损伤小鼠MDA和SOD的影响
MDA、SOD反映机体脂质过氧化和氧化应激程度,结果如图4所示。与空白对照组相比,酒精模型组的MDA值显著升高(P<0.05),SOD活性显著降低(P<0.05),说明酒精的摄入使肝脏的氧化应激水平升高,抗氧化能力降低。荞麦蜜的摄入能显著降低MDA含量(P<0.05),且与空白对照组无显著性差异(P>0.05),同时提高了SOD活性(P=0.098)。该结果表明荞麦蜜能抑制酒精引起的小鼠肝脏脂质过氧化损伤程度,提高小鼠机体内的抗氧化能力。

图3 荞麦蜜对小鼠肝脏TC(A)和TG(B)的影响Fig.3 Effects of buckwheat honey on liver TC(A) and TG(B) of mice
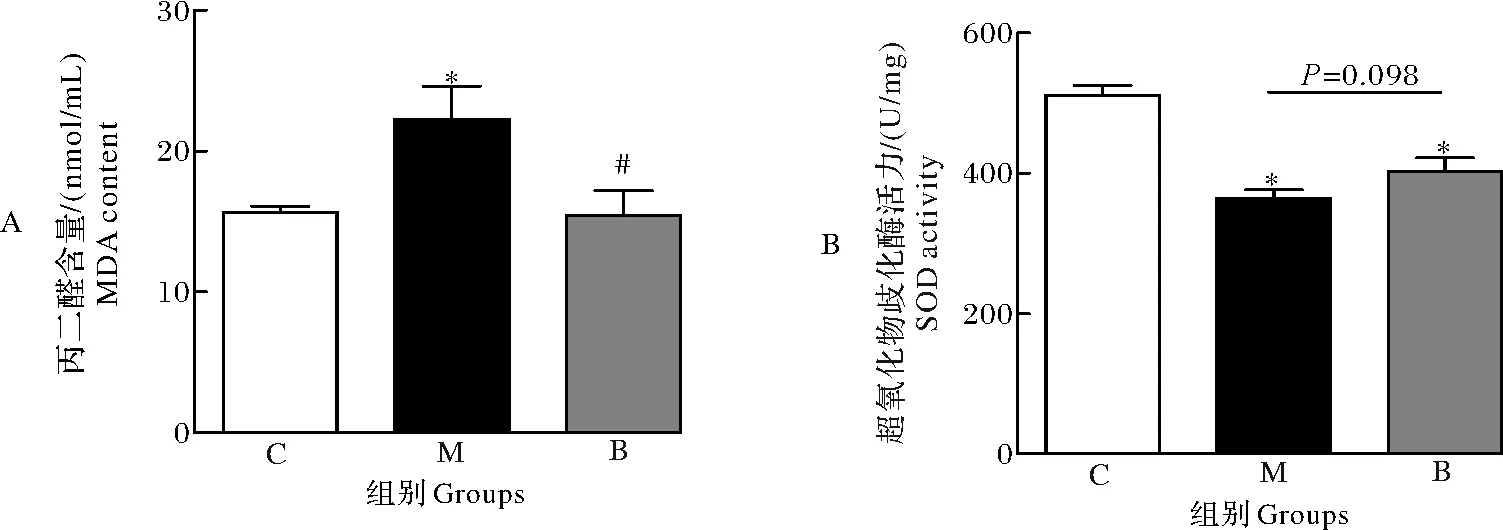
图4 荞麦蜜对小鼠MDA(A)和SOD(B)的影响Fig.4 Effects of buckwheat honey on MDA(A) and SOD(B) of mice
2.6 肝脏病理学切片结果
各处理组肝脏病理学切片结果见图5,直观反映了各组小鼠肝脏损伤的情况。空白对照组(C)肝细胞结构完整,排列整齐,胞浆内无脂滴分布,无气球样变性和炎性浸润现象,肝组织无异常改变。在酒精模型组(M)很明显可以看出,胞浆内有大量脂滴分布,结构紊乱,表明酒精模型组肝脏脂肪变性严重。在使用荞麦蜜干预(B)后,可以观察到胞浆内脂滴明显减少,肝细胞较完整且肝细胞排列趋于正常,肝脏脂肪变性明显减轻,这表明荞麦蜜对酒精引起的肝脏脂肪变性有明显的改善作用,肝脏受到很好的保护。
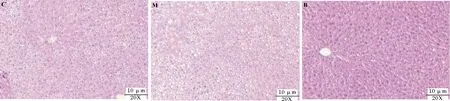
图5 小鼠肝脏组织病理学变化Fig.5 Histopathological changes of mice liver
2.7 小鼠肠道菌群的α多样性分析
如图6所示,各组的测序深度均接近于1,且无显著性差异(P>0.05)。与空白对照组相比,酒精模型组的Simpson指数、Shannon指数均下降,Chao指数升高但无显著性差异。而荞麦蜜的摄入使Simpson指数、Shannon指数、Chao指数均有所提升。

图6 α多样性分析Fig.6 α diversity analysis
2.8 小鼠肠道菌群群落组成
如图7所示,3组样本聚为3类,空白对照组与酒精模型组完全分开,而同样给予酒精的样品干预组也与空白对照组分开,与酒精模型组也几乎分开,说明了空白对照组与酒精模型组和样品干预组的肠道菌群组成存在差异,而且酒精模型组与样品干预组的肠道菌群组成也存在差异。因此,酒精和荞麦蜜的摄入使小鼠肠道菌群的组成发生了改变。
肠道菌群的各菌种间形成一种互相制约、互相依存的平衡关系,多种因素可导致其失调。通过对小鼠粪便肠道菌群进行不同水平上的物种组成分析,比较不同组之间的物种组成差异,门水平结果如图8和9所示。由图8可知,拟杆菌门(Bacteroidetes)和厚壁菌门(Firmicutes)在门水平上主导肠道菌群的组成,占比90%左右,其次还包括Proteobacteria、Epsilonbacteraeota、Deferribacteres、Actinobacteria、Fusobacteria、Tenericutes、Spirochaetes等。由图9A~D可知:与空白对照组相比,酒精的摄入使厚壁菌门相对丰度增加了24.56%,拟杆菌门相对丰度下降了4.4%,Proteobacteria相对丰度下降了21.6%,厚壁菌门/拟杆菌门(F/B)的比例升高了30.30%;而荞麦蜜的干预逆转了这一现象,与酒精模型组相比,荞麦蜜干预组厚壁菌门降低15.59%,拟杆菌门升高7.18%,二者的比值下降21.25%,并基本恢复到与空白对照组一致的水平。
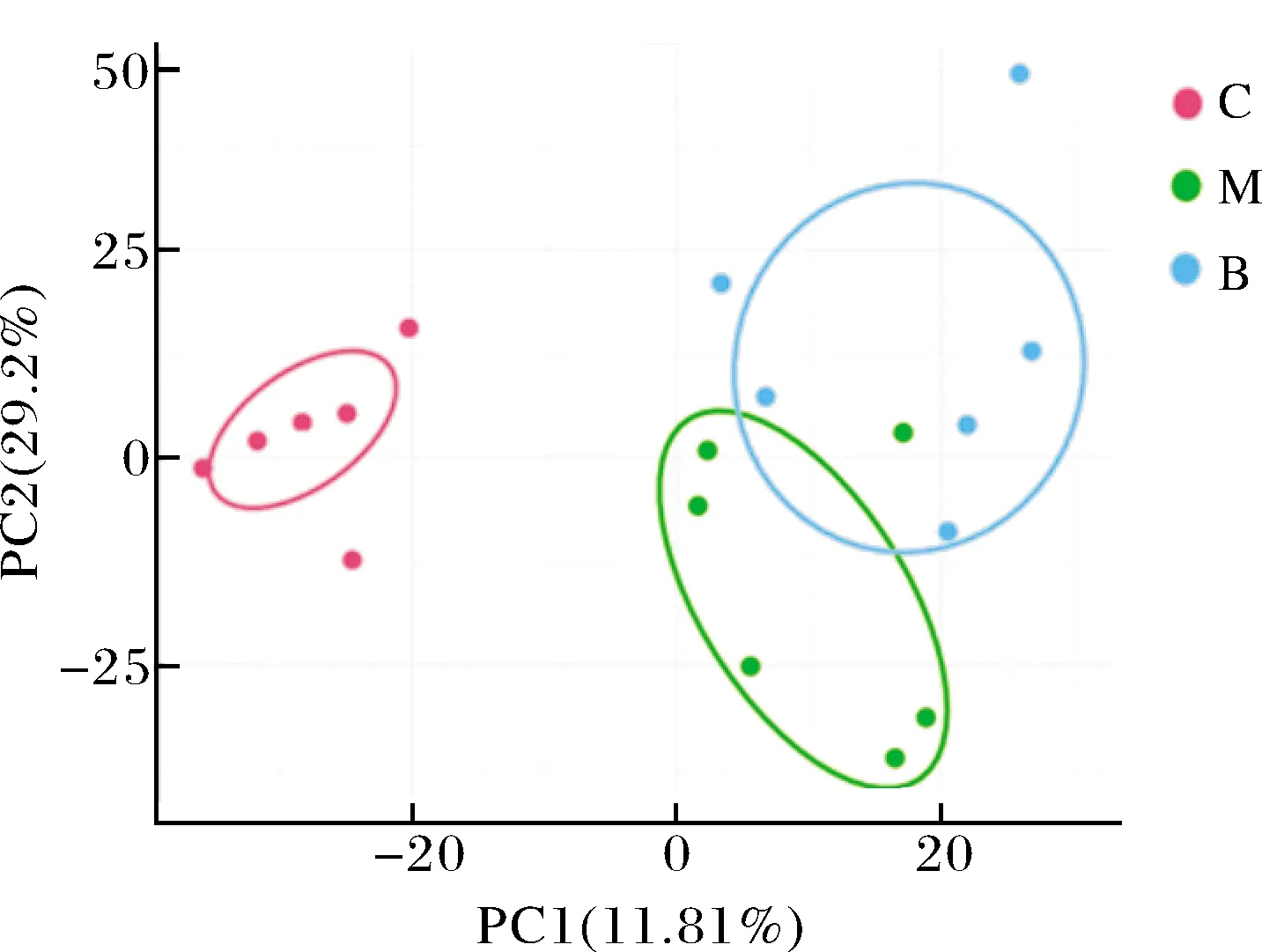
图7 PCA分析图Fig.7 PCA analysis diagram
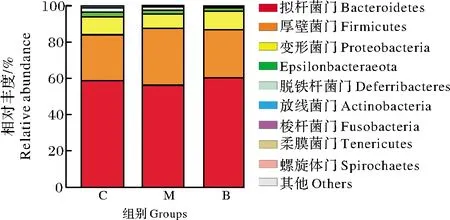
图8 门水平肠道菌群物种分析Fig.8 Species analysis of gut microbiotaat phylum level
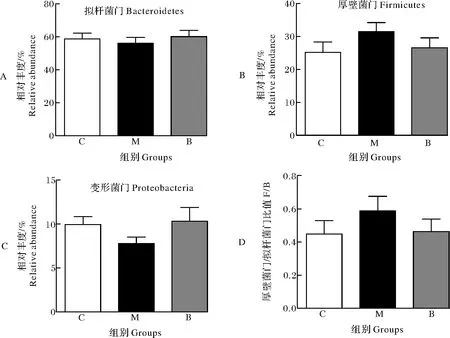
图9 拟杆菌门(A)、厚壁菌门(B)、变形菌门(C)的相对丰度以及厚壁菌门/拟杆菌门比值(D)Fig.9 Relative abundance of Bacteroidetes(A),Firmicutes(B),Proteobacteria(C) and F/B(D)
为进一步说明荞麦蜜的摄入是否对酒精引起的肠道菌群变化有改善作用,对属水平相对丰度排前36的菌属进行了差异分析(图10)。由图10可知,各组间微生物相对丰度存在差异。图11A~C中,各组中Ruminococcaceae_UCG-013、Lachnospiraceae_NK4A136_group、Helicobacter、Alistipes、Parasutterella、Faecalibaculum、Lachnoclostridium等菌属基本无变化;与空白对照组相比,酒精的摄入使uncultured_bacterium、Bacteroides、Alloprevotella、Mucispirillum、Dubosiella、Ambiguous_taxa、Ruminiclostridium、Rikenellaceae_RC9_gut_group、[Eubacterium]_coprostanoligenes_group、Coriobacteriaceae_UCG-002、Muribaculum、Pseudomonas等菌属丰度减少,而Parabacteroides、Blautia、Butyricimonas、Intestinimonas、Lachnoclostridium、Ruminococcaceae_UCG-003、Harryflintia、Roseburia、Escherichia-Shigella、Romboutsia、Oscillibacter、Anaerotruncus、Prevotella_9、Ruminiclostridium_9、Tyzzerella、Desulfovibrio等菌属丰度增加。在给予荞麦蜜进行干预后,uncultured_bacterium、Bacteroides、Rikenellaceae_RC9_gut_group、Alloprevotella、Muribaculum、[Eubacterium]_coprostanoligenes_group等菌属丰度升高,同时Parabacteroides、Intestinimonas、Lachnoclostridium、Harryflintia、Roseburia、Romboutsia、Oscillibacter、Anaerotruncus、Prevotella_9、Tyzzerella等菌属丰度降低。
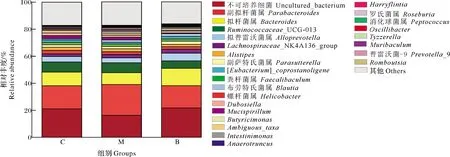
图10 属水平物种分析图Fig.10 Species analysis of gut microbiota at genus level
3 讨 论
3.1 荞麦蜜对酒精引起的小鼠体质量、肝脏指数和组织病理学的影响
脂肪变性、体质量减轻是酒精性肝损伤发生的症状,在酒精肝损伤早期往往伴随着肝脏的肿大,从而使肝脏指数升高[14]。本研究所用动物模型是长期适量酒精诱导加单次过量酒精饲喂协同诱导肝损伤,结果表明,酒精的摄入使小鼠的体质量显著下降,肝脏指数升高,导致肝脏发生损伤,肝组织病理学特征异常改变,发生严重的脂肪变性,预示着实验模型的成功。由于液体饲料中添加了酒精,造模前期小鼠不适应导致食欲减退,进食量变少,后期酒精的毒性会使胃肠道消化及吸收发生障碍,从而使小鼠体质量下降。而荞麦蜜的干预使这一结果得到改善,说明荞麦蜜可以在一定程度上减轻饮酒所致的肝脏损伤。
3.2 荞麦蜜对酒精引起的肝脏损伤小鼠ALT、AST、TC、TG、MDA和SOD的影响
血清中ALT和AST的升高是酒精性肝损伤的重要标志[14]。正常情况下,ALT和AST是存在于肝细胞内的指示肝功能的重要酶,当肝脏受损时,血清中的ALT和AST活性会升高。饮酒会导致脂代谢紊乱,肝脏脂质积累[15]。氧化应激是导致酒精性肝损伤发生的主要机制之一。MDA是脂质过氧化代谢的产物,常用于反映机体内脂质过氧化的程度;肝脏SOD活性的高低能够反映肝脏清除氧自由基的能力,进而反映肝脏抗氧化能力[16]。本研究结果表明,与空白对照组相比,酒精模型组小鼠血清ALT和AST活性显著升高,肝脏脂质过氧化物含量升高,抗氧化能力降低,肝脏的氧化应激水平升高;与酒精模型组相比,荞麦蜜的干预使血清中的转氨酶活性、MDA含量显著降低,SOD活性有所提高,这一结果与Cheng等[6]以及黄颖等[7]的结果相似。荞麦蜜中酚类化合物含量很高,而酚类化合物又是公认的抗氧化剂,表明荞麦蜜具有良好的抗氧化活性,可以抑制酒精引起的小鼠肝脏脂质过氧化物损伤程度和提高小鼠机体内的抗氧化能力。
3.3 荞麦蜜对酒精引起的小鼠肠道菌群的影响
肠道菌群的组成和多样性在体内平衡中扮演着重要角色。多种因素如饮食、疾病、生活方式或抗生素的使用等都可能导致肠道菌群失调和多样性的改变[17]。本研究中,酒精的摄入降低了肠道菌群群落的α多样性,此结果与Fan等[18]的研究结果相似。而饲喂荞麦蜜可以改善酒精引起的小鼠肠道菌群的多样性和丰富度的变化,改善小鼠肠道的内部环境。厚壁菌门和拟杆菌门是肠道菌群中的优势菌门[19],酒精及其代谢产物的毒性会使肠道菌群失调。研究表明,饮酒人群中拟杆菌门的相对含量低于健康人群[20]。在ALD小鼠模型中,肠道菌群的变化与肠道拟杆菌门水平的降低和厚壁菌门水平的升高有关[20]。本研究结果表明,酒精的摄入确实改变了肠道菌群的组成,给予酒精后的小鼠肠道中肠道菌群在门水平上主要引起了Bacteroidetes、Firmicutes等菌门的变化;在属水平上,酒精使多种菌属发生了改变,其中相对丰度较高的Parabacteroides菌属发生显著性升高,Alloprevotella相对丰度降低。而在给予荞麦蜜干预后,小鼠肠道菌群发生变化,厚壁菌门相对丰度降低、拟杆菌门相对丰度增加,属水平上16种菌属的相对丰度发生改变,其中Parabacteroides菌属发生显著下降,Alloprevotella相对丰度上升。Alloprevotella可以产生短链脂肪酸,有助于肠道紧密连接蛋白的保持,有助于肠黏液的产生来改善肠道屏障,减少有害物质易位[21]。这表明荞麦蜜可以改善酒精引起的小鼠肠道菌群的失调。此外,过量的酒精摄入造成的肠道菌群失调会进一步导致微生态失衡,进而引起肠道屏障功能发生改变,紧密连接蛋白被破坏,肠道通透性增加,细菌易位,大量的有害物质通过“肠-肝”轴转运进入门静脉系统和肝脏刺激促炎介质的释放,如活性氧、白三烯、趋化因子和细胞因子,引发炎症造成肝脏和其他器官的炎症浸润和纤维化[22-23]。
荞麦蜜作为深色蜜,含有丰富的果糖、酚类物质和矿物质,这些成分与体内的抗氧化反应的发挥以及肠道菌群的调节密切相关[24]。本研究中,酒精性肝损伤小鼠给予荞麦蜜干预可以改善肝脏病理切片中脂滴现象,提高了机体的抗氧化水平,对酒精引起的肝损伤有一定的保护作用。更重要的是,荞麦蜜的干预对酒精引起的小鼠肠道菌群结构异常变化起到改善作用,提高了肠道菌群的丰富度和多样性。预示荞麦蜜具有开发为护肝功能性食品的潜力。此外,本研究肠道菌群分析结果还可通过相关基因和相关信号通路的表达进一步探讨荞麦蜜改善肠道健康的作用机制。
