霍奇金淋巴瘤患者化疗后并发耶氏肺孢子菌肺炎1例报告及文献复习
2021-09-25李婷婷赵永娟
李婷婷,赵永娟,路 玲,王 静
(吉林大学中日联谊医院 呼吸内科,吉林 长春130033)
耶氏肺孢子菌肺炎(PCP)是由耶氏肺孢子菌引起的一种机会性、致病性真菌感染,通常发生在免疫系统受损的疾病中,最常见于人类免疫缺陷病毒(HIV)感染的患者。近年来,随着化学预防和高效抗逆转录病毒疗法的引入,PCP在HIV患者中的发病率大大降低[1]。随着接受抗肿瘤化疗剂、免疫抑制剂和器官移植的患者数量的增加,HIV阴性的PCP患者数量也在增加,最常见的潜在疾病是血液系统恶性肿瘤(29.1%),其次是自身免疫性疾病(20.1%)、器官或骨髓移植(14.0%)和实体瘤(6.0%)[2]。与HIV阳性的PCP患者相比,HIV阴性的PCP患者的特点是疾病进展较快,呼吸衰竭发生率高,死亡率高[3],且容易误诊。本文报道1例霍奇金淋巴瘤化疗后并发PCP的患者,并结合相关文献进行复习,以提高对非HIV感染的PCP患者的诊治水平及防治意识。
1 临床资料
某患者,女,37岁,因“间断咳嗽伴呼吸困难5天,发热3天”于2021年3月16日入院。入院5天前无明显诱因出现咳嗽、呼吸困难,吸气时加重,端坐位时稍缓解,伴乏力,无咳痰,无胸闷、胸痛,无头晕、头痛,3天前出现发热,体温最高39℃,伴盗汗,发热门诊行肺CT示肺炎,给予抗感染治疗(具体不详),症状较前改善,仍有间断发热,现为进一步系统诊治,再次来医院就诊。病程中精神可,饮食睡眠一般,二便如常,体重近半年内下降5 kg。查体:双肺呼吸音尚清晰,吸气末闻及少量湿性啰音,无胸膜摩擦音。该患于半年前因出现颈部无痛性淋巴结肿大就诊于本院血液肿瘤科,行颈部淋巴结穿刺活检病理示:霍奇金淋巴瘤,结节硬化型。已行多比柔星、博来霉素、长春新碱、达卡巴嗪(ABVD)方案化疗四周期。14日胸部CT平扫:双肺可见斑片状、索条状高密度影,边界不清,纵隔窗部分显示不清,部分范围缩小,呈软组织密度影;右肺上叶前段(5-120)、后段(5-164)、中叶(5-292)、下叶背段(5-190)、外基底段(5-271、403)及左肺下叶后基底段胸膜下(5-342)可见结节样高密度影,边界清晰,较大者直径约0.4 cm。纵隔内可见多发淋巴结影,较大者短径约0.7 cm。右侧叶间胸膜及双侧胸膜增厚(图1)。入院时动脉血气分析(未吸氧):pH:7.48,PO2:91 mmHg,PCO2:35 mmHg。全血细胞计数:白细胞计数 6.68×109/L,中性粒细胞68.9%,淋巴细胞13%。中性粒细胞载脂蛋白228.61 ng/ml。Th1/Th2/Th17细胞因子(CBA):IL-6 58.91 pg/ml。C-反应蛋白 24.52 mg/L。肺炎支原体、衣原体抗体检测:肺炎支原体IgG>300.00AU/ml。淋巴细胞免疫分析:CD3+ 83.8%,CD3+CD4+ 53.4%,CD3-CD19+1.1%,CD3+CD4+/CD3+CD8+比值2.02,提示存在免疫异常。降钙素原、结核感染T细胞、G试验、GM试验、呼吸道病原体谱抗体IgM检测、EB病毒定量PCR检测、巨细胞病毒定量PCR检测、免疫球蛋白+补体、类风湿因子、抗中性粒细胞胞浆抗体系列、抗核抗体系列(ANA)、抗环瓜氨酸肽(CCP)抗体测定、抗心磷脂抗体测定未见异常。结合患者发病特点及相关辅助检查,给予莫西沙星氯化钠注射液0.4 g静脉滴注 1/日,联合喷昔洛韦 0.25 g静脉滴注 2/日,抗感染治疗5天。由于患者为血液系统恶性肿瘤化疗后免疫缺陷人群,此次合并有肺部炎症考虑不除外特殊菌感染,故行气管镜取肺泡灌洗液标本(3月17日)进行细菌培养以及送华大基因公司行高通量基因测序检测。3月19日检测报告回复:耶氏肺孢子菌(序列数为46),耶氏肺孢子菌肺炎诊断明确,故将抗感染方案调整为复方磺胺甲噁唑片3片,每6 h一次口服,联合莫西沙星氯化钠注射液0.4 g,静脉滴注 1/日,治疗4天。于3月22日复查胸部CT与14日比较:肺内炎症基本消失;纵隔内淋巴结较前增大;余未见明显变化(图2)。复查全血细胞计数:中性粒细胞56.0%,淋巴细胞21.9%。C-反应蛋白 2.27 mg/L。中性粒细胞载脂蛋白181.23 ng/ml。Th1/Th2/Th17细胞因子(CBA):IL-6 4.37 pg/ml。患者已无发热,咳嗽,呼吸困难症状明显好转,因患者为血液肿瘤化疗患者,基础免疫较差,故嘱患者院外继续用药至少两周,定期复查肺CT。
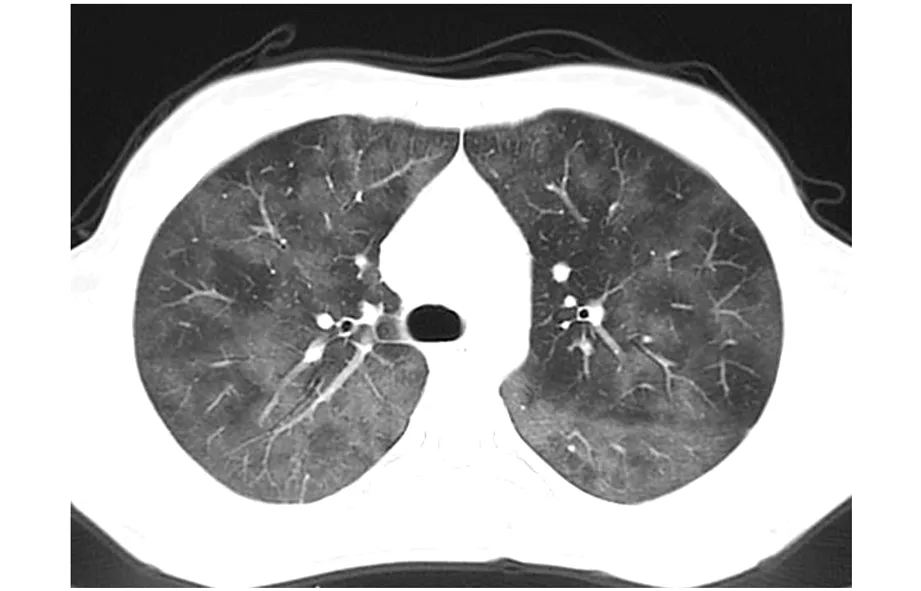
图1 胸部CT:双肺可见斑片状、索条状高密度影,边界不清
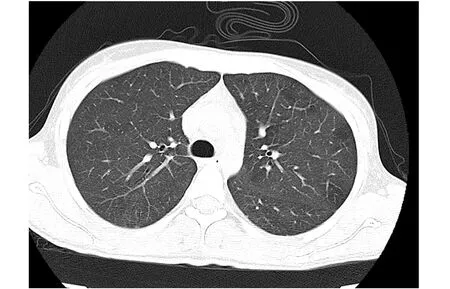
图2 胸部CT:肺内炎症基本消失
2 讨论
血液系统恶性肿瘤是HIV阴性的PCP患者中最常见的基础疾病[4],长期使用化疗药物是HIV阴性患者感染PCP的高危因素,此类药物破坏了外周血中淋巴细胞的免疫功能,损伤了患者的免疫系统,使患者处于易感状态。HIV阳性的PCP患者发病多为亚急性,常于数周后确诊,起病较平缓,最初的非特异性症状包括食欲差、腹泻、低热、干咳和气短,可伴有呼吸急促、紫绀等,单纯吸氧不易缓解。而在HIV阴性的PCP患者中,症状的出现多呈急剧、爆发性,且更常与糖皮质激素类药物(GCS)治疗相关,前期表现多为急性的反复发热,多为稽留热,体温可达39℃-40℃,伴频繁的刺激性干咳,后迅速出现胸骨后憋气和呼吸急促等[5],随着感染的进展,呼吸窘迫和缺氧逐渐加剧,最终会出现呼吸衰竭,病情进展快。肺部查体阳性体征不明显,听诊多为正常呼吸音,早期易误诊为急性上呼吸道感染,体征与症状的严重程度不相符是PCP的一个典型特点。在HIV阴性的PCP患者中,有些患者可无明显临床症状,这在临床诊断中常常会出现漏诊、误诊的情形。
在实验室相关检查中,PCP感染的风险与CD4+T细胞计数的下降密切相关,大多数血液肿瘤患者的CD4+T淋巴细胞计数是降低的,当CD4+T淋巴细胞计数<200/μl时,PCP的风险常呈指数级增加,因此当CD4+T淋巴细胞<200/μl时应对PCP患者使用甲氧苄啶/磺胺甲噁唑(TMP/SMX)进行预防治疗[6]。但仍有一部分合并PCP感染的血液病患者的CD4+T淋巴细胞处于正常值。乳酸脱氢酶(LDH)在PCP感染中具有高度敏感性,多表现为升高,且常与患者的预后相关,该指标缺乏特异性,它可能是潜在的肺部及肺外疾病炎症和损伤的反映,而不是该疾病的特定标志[7],若LDH持续升高,则提示预后不良。真菌感染是血液恶性肿瘤危及生命的严重并发症,而(1-3)-β-D-葡聚糖(BG)是肺孢子菌及大多数真菌细胞壁的组成成分[8],一项回顾性研究显示:在合并有PCP的血液恶性肿瘤患者中,(1-3)-β-D-葡聚糖的灵敏度为100%,特异性为96.4%[9]。虽然当合并有其他真菌感染(如念珠菌、曲霉菌)时(1-3)-β-D-葡聚糖也会有不同程度的升高,但当发现该指标异常时应考虑到PCP的感染进而早期行相关病原学诊断。PCP患者的CT表现无特异性,且有多种表现,主要表现为双肺以肺门为中心向外扩散的弥漫性磨玻璃影,正常组织与病变组织呈地图样分布,逐渐进展为间质浸润、结节影、纵隔及肺门淋巴结肿大,PCP的CT改变多由下肺逐渐向上肺蔓延,部分病例会因间质水肿或细胞渗出而并发小叶间隔增厚。在HIV阳性的患者中还可并发肺气肿及气胸[10]。本例患者因患霍奇金淋巴瘤已行四周期的化疗,于第四周期后出现发热、咳嗽、呼吸困难等临床症状,体温最高达到39℃,且肺CT提示有“双肺可见斑片状、索条状高密度影”,经验性抗感染治疗后效果不佳,应高度警惕合并有PCP感染的可能性,尽早行气管镜检查以明确诊断。
由于症状与体征缺乏特异性,且很难在体外培养出肺孢子菌,PCP诊断的金标准是在呼吸道样本中查见病原体[11],最常用的方法是从支气管肺泡灌洗液(BALF)或诱导痰中获得标本,但呼吸道没有标准化的取样方法,且样本的类型、质量以及不同的检测中心对检测结果均有影响。近年来高通量测序技术(NGS)在短时间内便能检测出细菌、真菌、病毒及寄生虫等多种病原体[12]。本例患者行纤维支气管镜提取肺泡灌洗液行高通量基因检测,结果回报为“耶氏肺孢子菌(序列数 46)”,明确诊断。
延迟治疗将会增加对机械通气的需求和死亡率。血液恶性肿瘤的患者若在临床出现了与PCP相似的肺部感染症状,应高度警惕该病,提前采取相应的诊断程序及预防性治疗。2016年欧洲白血病抗感染指南(ECIL-6)[13]指出:在患有PCP的非HIV感染患者中,持续2周以上的高剂量TMP/SMZ仍然是推荐的一线治疗方法,治疗剂量可按患者的体重计算,甲氧苄啶 15-20 mg/kg/d,磺胺甲噁唑 75-100 mg/kg/d,对于非常肥胖的患者,没有具体的剂量限制。对于非HIV感染患者,疗程≥3周,轻者至少≥2周,若超过1周未见好转迹象,应考虑是否合并有其他感染。目前我国临床常用的制剂为复方新诺明,每片含TMP 80 mg和 SMZ 400 mg。为防止不良反应,上述药物应避免与甲氨蝶呤合用。对TMP/SMZ有禁忌症的患者可选择二线药物如伯氨喹联合克林霉素(30 mg/d+600 mg/d,每8 h一次)、静脉注射喷他脒(4 mg/kg/d)、阿托伐醌(750 mg/d,每8 h或者12 h一次)。对于肠内吸收不受影响且依从性较好的轻度PCP患者可采取口服给药,对于中度至重度PCP患者,应采用静脉给药。在HIV阳性的PCP患者中,有证据表明GCS辅助治疗可提高患者的生存率,但在HIV阴性的患者中使用GCS是否有益于患者仍缺乏相关证据,且长期使用GCS为肺孢子菌的易感因素,ECIL表明在非HIV感染的患者中不推荐使用GCS作为常规辅助用药。卡泊芬净是一类棘白菌素类抗真菌药物,能抑制(1-3)-β-D-葡聚糖的合成,阻碍真菌细胞壁形成[14],临床中对TMP/SMZ耐药的患者也可使用卡泊芬净。卡泊芬净治疗PCP 的临床效果确切,而卡泊芬净联合TMP/SMZ能够提高治疗效果,同时降低单独用药的不良反应,为该疾病提供一个新的治疗选择。
综上所述,血液恶性肿瘤是PCP感染的高危因素,且进展较快,死亡率高,但该病临床表现及辅助检查缺乏特异性,易误诊,因此患有肺部感染的免疫功能低下的HIV阴性患者都应仔细评估PCP,尽早行病原学检查,高危患者应行TMP/SMX预防性治疗。血液疾病患者及时明确PCP的诊断是提高生存率以及改善预后的关键。
