基于肌肉细胞水凝胶纤维的光固化生物打印系统设计
2021-09-24胥国勇陆志威
胥国勇,赵 钢,陆志威,关 冠
(中国科学技术大学 精密机械与精密仪器系,合肥230026)
生物打印技术是指使用计算机控制3D 打印设备,将细胞和生物材料精确地沉积成指定几何形状的一种技术。这些设备能够打印细胞聚集物、含有细胞的水凝胶以及高分子聚合物[1]。生物混合驱动是指以可移动的微生物、可收缩的细胞或者组织作为动力来源的驱动方式,例如骨骼肌组织和心肌细胞已被用作生物致动器[2-3]。其中,骨骼肌是常见的纤维状组织,对基于骨骼肌的致动器的应用具有重要意义,因此有必要在体外复制出其纤维状结构。
生物打印机因其良好的生物兼容性和可操作性可以精确制备含有细胞的水凝胶纤维[4]。目前制备水凝胶纤维的生物打印系统主流的方法是“微挤出法”,根据其动力来源,可以分为气动压力驱动和机械 位 移驱动[5]。美 国的Tyler K Merceron 等[6]在2015年利用气动压力法打印出了肌肉纤维,并用该纤维制造了肌肉肌腱单元结构。2016年,韩国浦项科技大学的Yeong-Jin Choi 等[7]也利用气动压力法制备了功能性骨骼肌结构纤维。虽然气动驱动法可以使用气压挤出高粘度的纤维,具有较大的可打印性范围,但是其响应时间长,存在控制迟滞的问题。机械驱动系统可以对水凝胶的流动提供更稳定、精确的控制[8-9]。
水凝胶从液态到形成最终的纤维的过程,目前主流是采用化学试剂和光固化两种方法。2011年,荷兰乌得勒支大学医学中心骨科的Natalja E.Fedorovich 等[10]利用化学的方法,将水凝胶和CaCl2水溶液进行交联得到了纤维,但是该过程劳动强度大且对细胞伤害大,细胞存活率不高。光固化是一种非接触式的纤维固化方法,经过紫外光(UV 光)照射后的水凝胶发生交联,形成稳定的结构。因此设计一种结合机械驱动和光固化的生物打印系统具有十分重要的研究价值。
本文设计开发了一种基于机械驱动的光固化生物打印系统,以GelMA 水凝胶和C2C12 细胞的混合液作为打印材料,制备了含有肌肉细胞的水凝胶纤维。基于机械位移的驱动方式使水凝胶的流动更加稳定、精确。实验分析了不同紫外光强和水凝胶流量对纤维平均线宽和均匀性的影响。结果表明,在光强为20 mW/cm2和流量为120 μL/min 时,纤维的效果最佳,同时细胞保持94.15%的存活率。该研究对生物致动器的研究具有重要意义。
1 生物打印系统组成
系统总体结构如图1所示,该系统主要由注射泵、UV 光源、单片机、上位机、喷头、和移动台6 个部件组成。注射泵以机械驱动的方法挤压水凝胶到喷头中,水凝胶在UV 光源照射下固化,移动台配合移动形成水凝胶纤维结构。注射泵、UV 光源和移动台都是由单片机控制,同时我们为上位机开发了图形用户界面,实现了整个过程的全自动化。
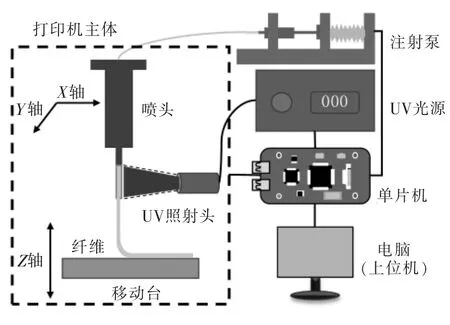
图1 系统总体结构示意图Fig.1 Diagram of the overall structure of the system
2 系统硬件设计
生物打印系统由上位机、Arduino Mega 2560控制器、温度控制模块、驱动控制模块、UV 光固化控制模块组成,系统的硬件结构如图2所示。上位机设置不同的打印参数,将数据发给Arduino Mega 2560 控制器,控制器控制温度控制模块、驱动控制模块、UV 光固化控制模块协同工作。温度控制模块控制水凝胶保持在指定的温度,驱动控制模块控制电机移动和注射泵推进,UV 光固化控制模块控制合适的紫外光强,从而打印出水凝胶纤维。
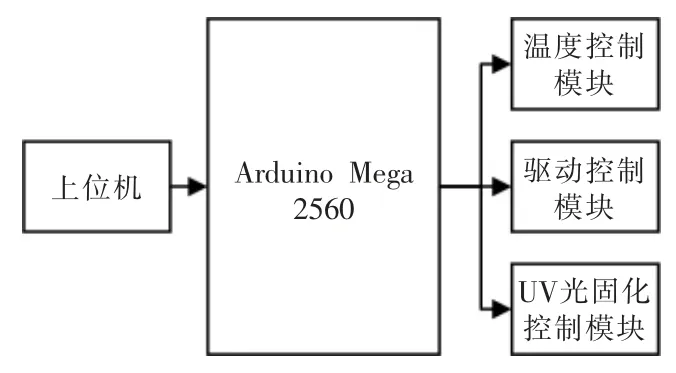
图2 系统硬件结构框图Fig.2 Hardware structure diagram of the system
2.1 Arduino Mega2560 控制器
本系统采用Arduino Mega 2560(MEGA2560 R3,中国)芯片作为MCU。控制板是采用USB 接口的核心电路板,处理器核心是ATMega 2560,同时具有54 路数字IO 口,16 路模拟输入,4 路UART接口,一个16 MHz 晶振,已广泛应用于开源3D 打印机中[11]。这些丰富的接口和资源,可以方便地进行各种外设的开发。
2.2 温度控制模块组成
由于GelMA 水凝胶的温度敏感性使其在温度高于37 ℃时是液态,但温度太高会使细胞逐渐凋亡,酶一般最适温度是37 ℃,因此需要将GelMA 水凝胶打印过程中的温度范围控制在36 ℃~38 ℃,维持液态的同时保持细胞活力。本系统温度控制模块是由温度传感器、加热棒和控制板组成。温度传感器选择的是热敏电阻,型号是单端玻封的NTC100K 3950,具有灵敏度高、反应迅速、结构小巧、使用温区宽、稳定性好、可靠性高、互换性强和精度高的特点。加热棒是单头电热管加热棒,规格是12 V/40 W,具有耐高温且升温快的特点。
2.3 驱动控制模块
驱动控制包含方向驱动控制和进料驱动控制两部分。方向驱动主要由3 个42 步进电机构成。其中,XY 方向采用42 步进电机和同步带(2GT-550-6 mm,中国)控制,Z 方向采用42 步进电机和滚珠丝杠(SFU1204,中国)控制。42 步进电机是通过电流脉冲来精确控制转动量的电机,电机的每一个脉冲都是一个固定的长度,将每1 mm 的进给量转化为电机的脉冲数。电机的控制是由脉冲宽度调制(PWM)信号控制,电机每个脉冲转1.8°。进料驱动是采用挤压的方式,由注射泵(SPLab02,中国)提供动力。注射泵可以灵活调节流量,对水凝胶的流量提供直接的控制。
2.4 UV 光固化控制模块
本系统UV 光源采用365 nm 紫外光UVLED 点光源照射机(DSX-UVP60,中国),照射头的光斑直径是12 mm,紫外光能量密度最大是800 mW/cm2,在0~100%可调。在光引发剂的作用下,曝光于UV光下的GelMA 水凝胶可以交联形成固化的水凝胶结构。如图3所示,GelMA 在熔化前为泡沫状的固体,加上PBS 溶液和光引发剂,熔化后溶液为液态,经过UV 曝光后变为固态,且该固化过程不可逆。图4展示了GelMA 水凝胶纤维的生成过程,在UV 光的照射下,水凝胶溶液交联后形成长条形纤维从喷头中流出,从而完成了肌肉细胞水凝胶纤维的制备。

图3 GelMA 光固化特性图Fig.3 Photocuring properties of GelMA

图4 水凝胶纤维打印图Fig.4 Print of hydrogel fiber
3 系统软件设计
3.1 上位机软件设计
本系统上位机软件是基于Repetier-Host 软件进行二次开发的,利用其插件框架进行扩展应用。因为未进行扩展的上位机软件可以完成对生物打印机的运动控制、GelMA 水凝胶的温度控制,还需要在系统中加入UV 光控制模块和注射泵驱动控制模块,原本的Repetier-Host 软件不足以满足使用要求,因此在Repetier-Host 软件基础上,采用C# 语言开发相应的插件。经过二次开发的上位机在打印过程中可以实时对温度等不同参数进行记录和调节。
3.2 控制设计
控制器的固件是基于Marlin 固件开发的,该固件采用C++语言,具有高效、稳定、可移植性强的特点[12]。打印系统的操作基于G 代码,G 代码是在3D 打印系统市场占有率最高的语言。在固件中修改了机械挤出的E 代码和用于UV 光固化的M代码。
系统打印纤维时会首先初始化各个部件,然后将温度和UV 紫外光调节到设定的目标数值,纤维打印的过程是一边曝光,一边打印,打印完成后,更换参数,继续打印,将所有需要的纤维都打印完成后,系统各部件归位,恢复到原始位置,完成实验,控制流程如图5所示。
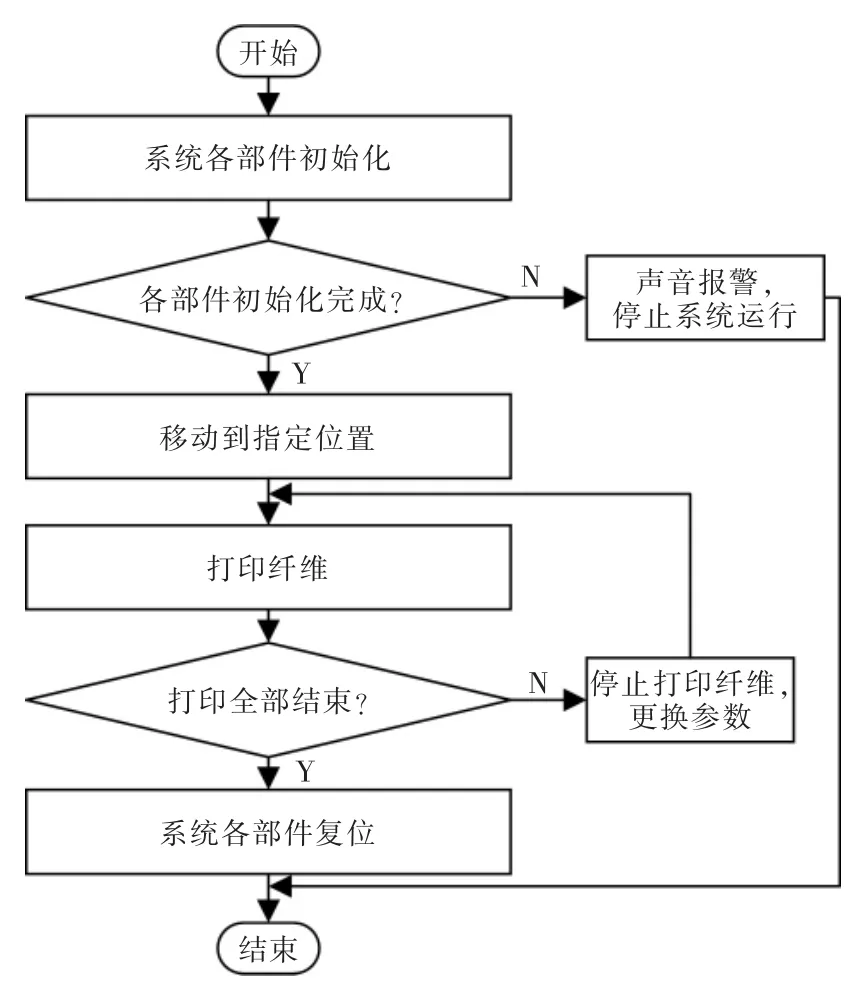
图5 控制流程Fig.5 Control flow chart
4 系统实验结果表征
本文中的系统是用于打印含有C2C12 肌肉细胞的GelMA 水凝胶的,衡量的指标主要是不同光强和流量下的可打印性范围、纤维平均线宽和均匀性以及细胞存活率。
实验中采用的打印材料为可光交联的甲基丙烯酸化水凝胶(GelMA),喷头管道的直径为0.5 mm。参照现有GelMA 合成工艺[13],通过交联反应、过滤、透析和冻干,得到GelMA 白色泡沫,1HNMR 光谱检测表明所合成的GelMA 取代率为93.75%。接下来,将GelMA 水凝胶、光引发剂与PBS 缓冲液按0.1∶0.005∶1 的比例进行混合,同时加入小鼠成肌细胞细胞(C2C12,中科院上海细胞库)得到混合溶液。GelMA 水凝胶具有可光交联的性质,经过UV 光照射后会固化,形成的结构对细胞的兼容性好。
4.1 水凝胶纤维的可打印性范围
为了得到稳定的生物致动器纤维结构,需要对水凝胶纤维进行缠绕拉伸,并固定成型。为此设计了柱-孔阵列的水凝胶纤维缠绕装置[14],尺寸如图6所示,该装置的长、宽、高分别为35 mm,10 mm 和2 mm,装置有1 个样品观察窗和2 列用于支柱固定的孔,微柱间的可调节距离为20 mm~32 mm。得到的纤维需要被缠绕在2 个微柱上,为了能够使纤维稳定地缠绕在微柱上,实验中将能够打印长度大于等于50 mm 的纤维的参数定义为可打印的,反之就是不可打印的。图7展示了打印过程中经过UV 光照射后得到的纤维实物图。图8表明了流量和光强对可打印性范围的影响,当UV 光强从10 mW/cm2增加到30 mW/cm2时,纤维的可打印性范围从30 μL/min~60 μL/min 变为60 μL/min~210 μL/min,范围区间明显增大,由此可以看出随着UV 光强的增加,纤维可打印性范围也会增加。
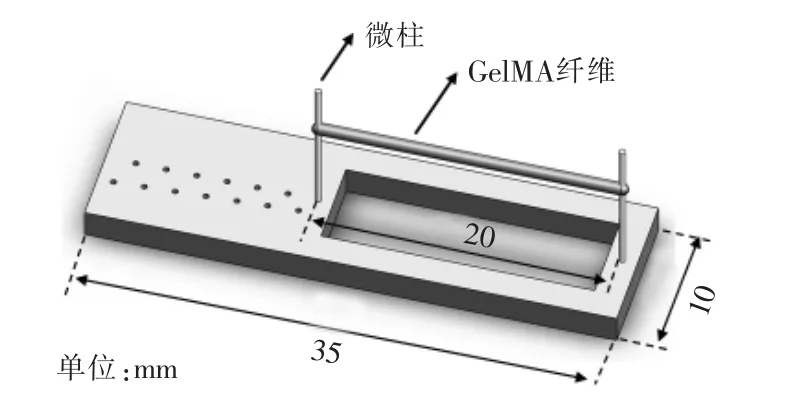
图6 柱-孔阵列的实验装置示意图Fig.6 Schematic diagram of experimental device based on column-hole array

图7 UV 光固化后的纤维实物图Fig.7 Physical picture of the fiber after UV light curing
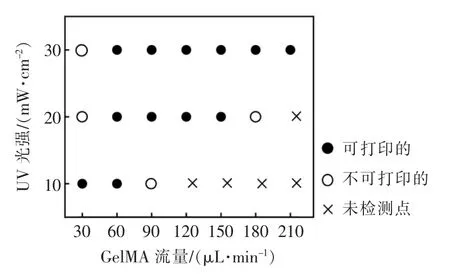
图8 水凝胶纤维可打印性图Fig.8 Printability diagram of hydrogel fibers
4.2 水凝胶纤维的线宽和均匀性
为了探究喷头打印出的纤维在不同UV 光强下,纤维平均线宽和均匀性与流量的关系,实验对纤维进行了进一步研究。从图9的结果中可看出,在UV 光强一定时,随着GelMA 流量的增加,纤维的平均线宽先增加后减小,线宽的均匀性越来越差。如UV 光强在20 mW/cm2时,GelMA 流量从60 μL/min 增加到180 μL/min 时,纤维的平均线宽从534.79 μm 增加到747.21 μm,再降到701.46 μm,而平均线宽的误差值从7.20 μm 一直增加到26.58 μm,即均匀性越来越差。这是因为流量增加使得UV 光照射时间减小,导致GelMA 固化的效果变差了,当流量达到某一值后,纤维不能完全固化,线宽又变小,同时纤维固化效果变差会导致平均线宽值波动较大,故均匀性一直在变差。图10展示了UV光在20 mW/cm2时,GelMA 流量分别为90 μL/min,120 μL/min 和150 μL/min 时的纤维实物图。
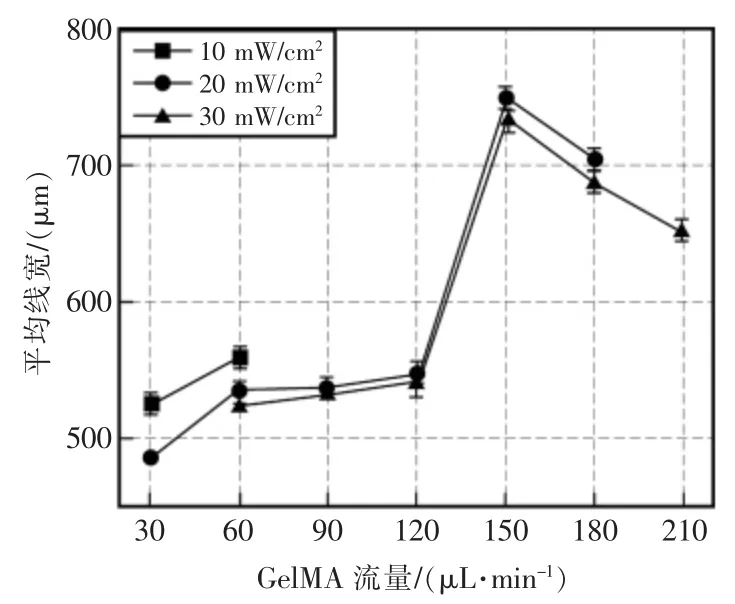
图9 不同UV 曝光强度下的纤维平均线宽Fig.9 Average linewidths of fibers under different UV exposure intensities

图10 UV 光20 mW/cm2 时不同流量下纤维实物图(标尺=200 μm)Fig.10 Physical images of fibers at different flow rates under UV light of 20 mW/cm2(scale bar=200 μm)
4.3 水凝胶纤维中C2C12 细胞存活率
高强度的UV 辐射会对细胞产生伤害[15-16],因此需要研究不同UV 光强下的C2C12 细胞的存活率。实验中采用活-死细胞生存能力试剂盒(Live/Dead Viability Kit,Invitrogen,美国)对纤维内细胞的存活率进行评估。染色后,在倒置荧光显微镜(Leica DMI 3000b,德国)下进行观察,活细胞呈现绿色,死细胞为红色,最终的荧光图像如图11所示。图片使用Fiji/ImageJ 软件进行数据处理,得到的结果如图12所示。可以看出在UV 光强一定时,GelMA 的流量越大,C2C12 细胞的存活率越高。如UV 光强在20 mW/cm2时,GelMA 流量从60 μL/min 增加到180 μL/min 时,细胞存活率从93.12%增加到95.28%。这是因为流量增大导致C2C12 细胞被UV 光照射的时间减小,使得细胞受到UV 辐射变少,细胞存活率就增大了。
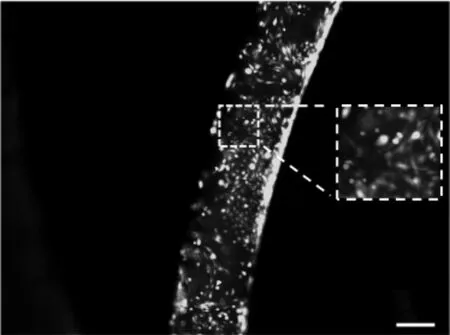
图11 水凝胶中C2C12 细胞的活/死染色的荧光图像(标尺=200 μm)Fig.11 Fluorescence images of live/dead staining of C2C12 cells in hydrogel(scale bar=200 μm)
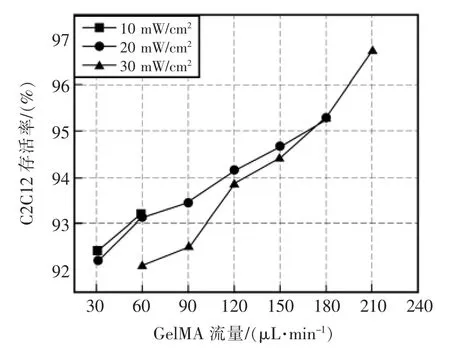
图12 不同UV 曝光强度下的水凝胶纤维中C2C12 细胞存活率Fig.12 Survival rate of C2C12 cells in hydrogel fibers under different UV exposure intensity
4.4 水凝胶纤维最优参数表征
最后对纤维平均线宽和细胞存活率与GelMA流量变化关系进行了综合研究。实验时,UV 光强选的是20 mW/cm2。实验结果如图13所示,当流量分别为90 μL/min,120 μL/min 和150 μL/min 时,纤维平均线宽分别为535.46 μm,545.94 μm 和747.21 μm,C2C12 细胞存活率分别为93.45%,94.15%和94.67%。当流量从90 μL/min 增加到120 μL/min 时,纤维平均线宽和细胞存活率增加值分别是10.48 μm和0.7%;当流量从120 μL/min 增加到150 μL/min时,纤维平均线宽增加值为201.27 μm,细胞存活率增加值为0.52%。GelMA 流量在150 μL/min 时的线宽增加值比流量为120 μL/min 时的线宽增加值增大了18.2 倍,平均线宽显著增加,但是存活率增加值变化不明显。同时,从前文可知,随着流量增加,线宽的均匀性也会变得越来越差的。因此在保持细胞高存活率的前提下,UV 光强为20 mW/cm2时的GelMA 流量最优是120 μL/min。
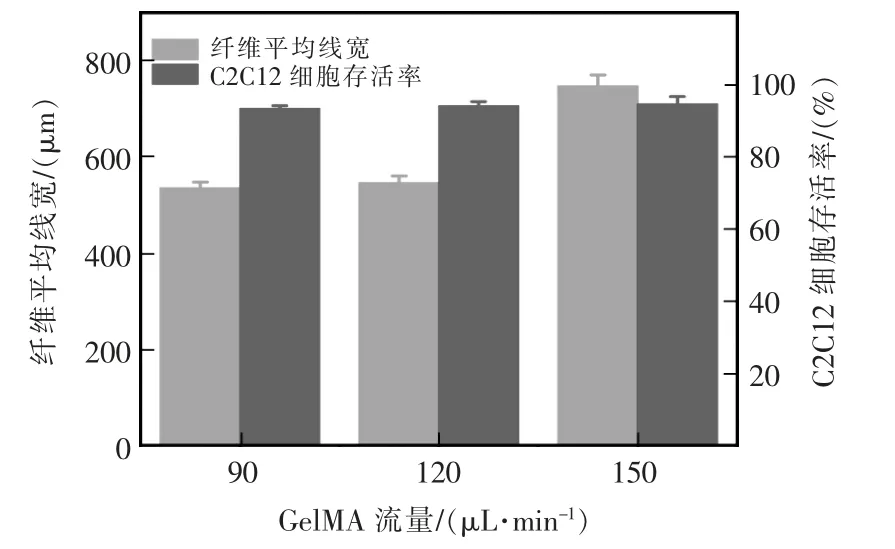
图13 纤维平均线宽和细胞存活率与GelMA 流量变化关系图Fig.13 Relationship between average fiber line width,cell survival rate and GelMA flow rate
5 结语
本文设计开发了一种基于机械挤压的光固化生物打印系统,以GelMA 水凝胶和C2C12 细胞的混合液作为打印材料,得到了肌肉细胞水凝胶纤维,并对其进行了实验表征。分析了水凝胶纤维的可打印范围,并研究了不同紫外光强和水凝胶流量下的纤维平均线宽和均匀性。实验结果表明UV 光强越大,纤维的可打印性范围区间越大。在UV 光强一定时,流量增大会导致纤维的平均线宽先增大后减小,均匀性一直在变差,C2C12 细胞的存活率在缓慢增加。当UV 光强为20 mW/cm2,GelMA 流量为120 μL/min 时,纤维线宽较小,同时细胞保持很高的存活率。该研究结果对于光固化生物打印系统的设计和生物致动器的研究具有重大意义。
