磷酸锌改性提高正极材料LiNi0.8Co0.1Mn0.1O2的电化学性能
2021-09-18王祯涛
王祯涛,顾 虹,王 娟
(西安建筑科技大学 西安市清洁能源重点实验室,陕西 西安 710016)
1 前 言
富镍层状氧化物LiNixCoyMnzO2(NCM,x>0.6,x+y+z=1)由于其成本低、放电比容量大等优势吸引了材料科学家们的广泛关注,被认为在商业化应用上具有较大的潜力[1, 2]。然而,富镍三元正极材料循环性能及结构稳定性随镍含量的提高而显著下降[3-5]。高镍正极材料具有差的界面稳定性,结构持续衰退,阻碍了其进一步的商业化应用[6-8]。随着电化学循环的进行,电解液中分解的氟化氢(HF)与电极表面发生副反应,引起“表面重构”,恶化电极-电解液界面[9-11]。另外,随着循环的进行,部分Ni2+占据在锂层,导致界面阻抗的增加和结构的衰退[12, 13]。
在充放电过程中,Ni2+占据晶格中Li+的位置,导致表面晶格的变化和“表面重构”[14, 15],材料的空间群结构由R-3m(层状结构)变为Fm-3m(立方岩盐相)[16, 17],不利于Li+迁移,减少了Li+嵌入/脱出位置,正极材料电化学性能恶化。随着结构的变化和Ni3+的还原,富镍正极材料由于电荷平衡释放出氧,从而氧化电解质并导致严重的电解质分解[18-20]。此外,当电极处于高倍率充放电状态时,电极材料变得不稳定,并可能通过相变分解[21, 22]。带电正极材料的分解会导致含氧物质的释放,而这些物质具有很高的反应活性,最终严重影响正极材料的安全性[23-25]。此外,在充放电过程中,LiNi0.8Co0.1Mn0.1O2(NCM811)材料的二次颗粒会产生9%~10%的体积变化,产生细小的裂纹[26, 27]。正极材料在循环过程中,由于一次颗粒之间各向异性变化导致二次颗粒之间微裂纹的产生,电解液与一次颗粒之间接触面积增大,一次颗粒表面形成新的固体电解质界面层(solid electrolyte interface, SEI),二次颗粒提供容量减少,最终材料结构稳定性和电化学反应能力降低[28-30]。
为了稳定界面结构和抑制整体结构衰退,表面包覆和掺杂等方法被广泛采用[31-36]。由于包覆层抑制了电解液中HF对电极表面的腐蚀和表面结构的变化,可有效提高界面结构稳定性[37, 38]。磷酸锌(Zn3(PO4)2)具有较好的热力学稳定性,能够在循环过程中抑制电解液的腐蚀,并抑制表面结构由层状向尖晶石相的转变[39, 40]。聚乙烯吡咯烷酮(polyvinylpyrrolidone, PVP)可以将羰基氧中的一对电子传递给金属阳离子,因此,在包覆过程中借助PVP链的桥联作用可使Zn3(PO4)2颗粒均匀分散在正极材料颗粒表面[41]。本文采用PVP辅助Zn3-(PO4)2包覆改性NCM811材料,并通过XRD、X射线光电子能谱(X-ray photoelectron spectroscopy, XPS)、扫描电镜(scanning electron microscope, SEM)及能谱(energy dispersive spectrometer, EDS)等表征测试,讨论了Zn3(PO4)2表面包覆对NCM811正极材料表面结构和形貌的影响,测试分析了包覆改性后正极材料的电化学性能和提升机理。
2 实 验
2.1 材料合成
本实验中富镍正极材料NCM811的制备方法为共沉淀法。将摩尔比为8∶1∶1的NiSO4·6H2O、CoSO4·6H2O和MnSO4·H2O溶解在蒸馏水中,金属离子总浓度为1.5 mol·L-1,在氮气气氛下连续搅拌并缓慢添加到反应釜中。同时,向反应釜中以一定速率滴加螯合剂NH3·H2O和沉淀剂NaOH,反应温度维持在55 ℃,反应16 h得到墨绿色粉末,将粉末进行洗涤、过滤并在120 ℃下干燥获得前驱体。将所得前驱体粉末与LiOH·H2O混合,在马弗炉中550 ℃下预热4 h,然后在800 ℃下、氧气气氛烧结12 h,得到NCM811正极材料粉末。
包覆改性过程如下:首先将1 g NCM811粉末溶于10 mL去离子水,搅拌30 min。随后,将0.05 g PVP粉末与磷酸氢二铵粉末添加到上述溶液中并搅拌均匀。取3份溶液,分别添加1%、3%、5%质量分数的氧化锌(ZnO)粉末并搅拌均匀。其中,磷酸氢二铵与氧化锌的摩尔比为1∶1.5。然后将上述混合溶液加热至50 ℃,直至溶液蒸发,将所得的粉末进行研磨并在120 ℃下干燥。随后,将所得的粉末在氧气气氛下550 ℃热处理5 h,最终得到Zn3(PO4)2改性的NCM811正极材料,上述不同ZnO添加量的改性样品分别标记为NCM1、NCM2、NCM3。
2.2 电池组装与电化学性能测试
电池组装流程如下:①干燥:将导电炭黑、正极材料等原材料放置于干燥箱中以去除水分。②混料:以N-甲基吡咯烷酮(NMP)作为有机溶剂,利用其油溶性将正极材料粉末、导电剂以及聚偏氟乙烯(poly(vinylidene fluoride),PVDF)充分溶解便于混合,上述物料的质量比为8∶1∶1,搅拌均匀形成黑色浆料。③涂布: 将准备好的平整的铝箔放于涂布机,将黑色浆料均匀倒入形成均匀的电极。④烘干: 将上述步骤制备的浆料在干燥箱中去除多余溶剂,温度维持在60 ℃,时间保持12 h以上。⑤裁片: 将干燥好的浆料在室温下用裁片机裁成直径为10 mm的圆片。⑥称重: 将切好的圆片放置于电子天平,记录准确值。⑦烘干: 将称量好的电极片继续干燥去除空气中残留的水气等,温度维持在60 ℃,时间保持12 h。⑧组装电池: 在手套箱中依次放置CR2032负极壳、电极片、电解液、隔膜、锂片、集流体、弹片、CR2032正极壳等材料和辅助用品(如手套与卫生纸等用品);组装过程严格控制水与氧气含量,保证组装过程不影响电解液的分解与电极片的氧化等;并按照材料摆放顺序依次组装;最后用封口机以800 MPa压力压实,完成组装。
对组装的CR2032扣式电池的循环性能及倍率性能等,采用新威NEWARE电池测试系统进行测试。测试的电压范围设置为2.8~4.3 V。循环性能测试中,充放电电流密度为0.1C。在倍率性能测试中,所用电流密度顺序分别为0.1C、0.5C、1C、2C、5C,最后恢复到0.1C。对于富镍正极材料NCM811,1C=280 mA·g-1。使用普林斯顿2270系列电化学工作站测试电池循环伏安(cyclic voltammetry, CV)特性,其中扫速为0.1 mV·s-1。进行交流阻抗谱(electrochemical impedance spectroscopy, EIS)测试时,频率范围设置为0.01 Hz~100 kHz,振幅范围为5 mV。
2.3 材料分析与表征
采用X射线衍射(XRD)表征材料的晶体结构。X射线衍射仪由日本Rigaku公司生产,辐射源为Cu靶,扫描角度为10°~80°,工作电压为40 kV。为了表征材料的形貌与成分,采用日立公司的场发射扫描电镜,电镜的工作电压为10 kV,可以调节电镜的放大倍数范围在50~20 000倍。采用能谱(energy dispersive spectrometer, EDS)分析对材料表面化学元素进行表征。同时采用X射线光电子能谱(X-ray photoelectron spectroscopy, XPS)表征材料表面元素价态。
3 结果与讨论
3.1 结构和成分分析
图1为不同Zn3(PO4)2添加量改性NCM811材料与NCM811纯样的XRD图谱对比。由图1a可以观察到,所有样品都具有纯相的α-NaFeO2层状结构,属于R-3m空间群。所有样品的衍射峰尖锐,没有杂峰,表明结晶度较好。图中没有观察到Zn3(PO4)2的衍射峰,可能Zn3(PO4)2量过少而没有被检测到。Zn3(PO4)2改性的NCM811样品(006)/(102)和(108)/(110)峰的分裂表明材料的层状结构不受Zn3(PO4)2改性的影响。计算的晶格参数列于表1中,I(003)/I(104)比值和c/a值被广泛用于判断层状结构中的阳离子混排程度[42]。NCM2样品的I(003)/I(104)比值最大;随着Zn3(PO4)2含量的逐渐增大,改性样品的c/a值先增加后减少,NCM2样品c/a值大于纯样,表明NCM2样品相比纯样NCM811具有更低的Li+/Ni+混排。同时,由于改性过程中的离子相互作用,部分Zn2+可能进入颗粒表面晶格。如图1b和图1c所示,NCM2样品(003)和(102)峰峰位比标准卡片峰位向右偏移,根据布拉格方程可知Zn2+进入表面晶格,占据了Li+的3b位[42]。同时Zn2+半径大于Li+,导致晶面间距的扩大,(003)平面内原子散射能力提升。
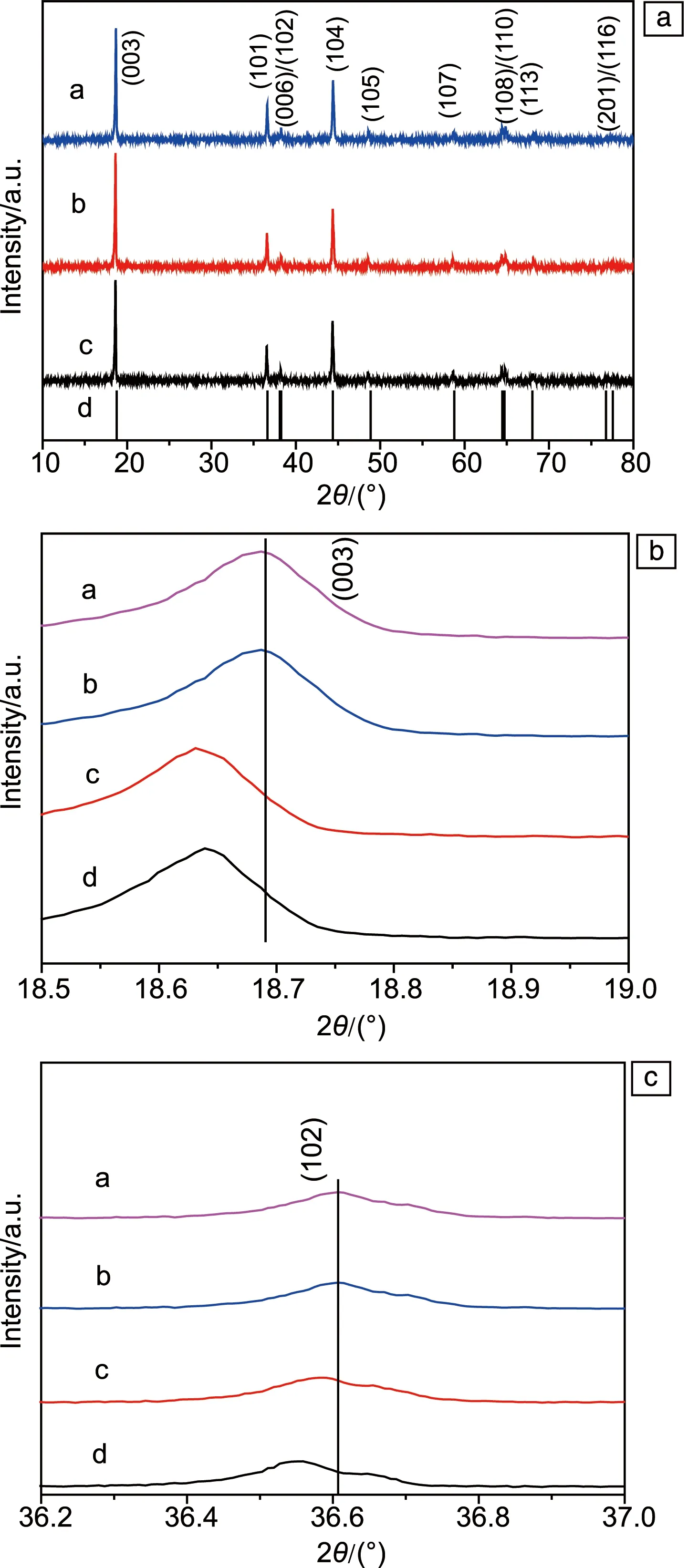
图1 NCM811纯样与不同Zn3(PO4)2添加量改性的NCM811的XRD图谱(a),(003)与(102)峰局部放大图(b,c),图中曲线a,b,c,d分别代表样品NCM1、NCM2、NCM3、NCM811Fig.1 XRD patterns of pure sample of NCM811 and zinc phosphate modified NCM811 with different Zn proportions (a),enlarged regions for the (003)and(102)peaks of samples(b,c), the curves a, b, c and d in the figure represent NCM1, NCM2, NCM3 and NCM811, respectively
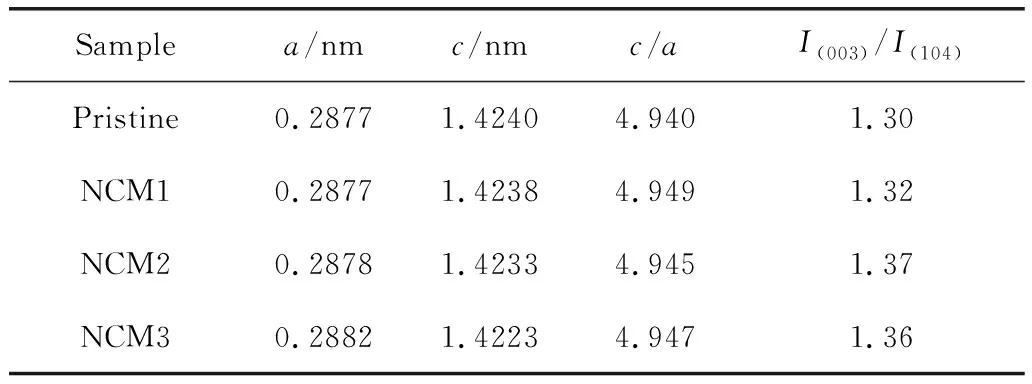
表1 NCM811纯样与Zn3(PO4)2包覆改性样品的晶胞参数
图2为不同Zn3(PO4)2添加量改性的NCM811正极材料的SEM照片。可以清晰地看到,未改性样品的二次颗粒边缘清晰,形状较规则,一次颗粒之间连接紧密。如图2b所示,NCM1样品形貌相比纯样变化最小,二次颗粒存在一定的粘连。如图2c和2d所示,NCM2样品颗粒表面有一些小粒子;在高倍率的SEM照片下,可以清晰地观察到一次颗粒表面存在一些粉状颗粒。如图2e所示,随着Zn3(PO4)2添加量的增大,NCM3样品颗粒边缘存在较多的粒子。这可能是由于Zn3(PO4)2含量较大,伴随着热处理过程,一部分Zn3(PO4)2颗粒便沉积在颗粒周围,形成大量的小颗粒。
图2g~2l给出了NCM2样品的各元素分布EDS面扫描结果,图中的彩色点对应于材料表面的不同元素。该图显示了镍、钴、锰、氧、磷和锌等元素的存在,表明Zn3(PO4)2分布在原始样品上。文章采用的是PVP辅助包覆Zn3(PO4)2对纯样NCM811材料进行改性,PVP包覆的优势在于,其羰基氧中的一对电子与金属阳离子形成复杂的键。在包覆过程中,PVP与包覆物的复合物均匀沉积在颗粒表面,热处理后Zn3(PO4)2比较均匀地包覆在颗粒表面。由于在包覆过程中无法保证复合物的均匀分散,所以存在一定的包覆不均匀问题,导致元素非均匀分布等现象。
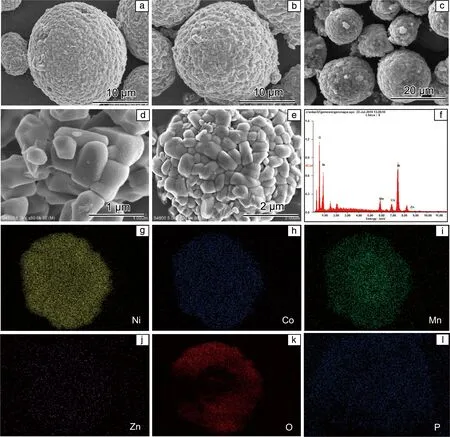
图2 NCM811纯样的SEM照片(a), NCM1样品的SEM照片(b),NCM2样品的SEM照片(c,d),NCM3样品的SEM照片(e),NCM2样品的能谱(energy dispersive spectrometer, EDS)分析(f)及Ni, Co, Mn, Zn, O和P元素面扫描结果(g~l)Fig.2 SEM images of the pristine NCM (a), NCM1 sample (b), NCM2 sample (c, d) and NCM3 sample (e); EDS analysis of NCM2 sample (f); EDS mappings of Ni, Co, Mn, Zn, O and P (g~l)
为进一步研究改性前后正极材料的元素组成和化学态等,采用XPS对样品进行测试。图3为NCM811和NCM2样品各元素按C 1s峰标定后的XPS图谱。由图3a可知,在NCM811和NCM2样品中,Ni 2p3/2峰对应的结合能位于854.2 eV附近,表明均存在Ni2+(853.7 eV)与Ni3+(854.7 eV) ;Zn3(PO4)2包覆后,NCM2材料的Ni 2p3/2峰逐渐向低能量方向偏移,从NCM811的853.7 eV左移至853.3 eV,Ni的氧化态的降低说明Zn3(PO4)2包覆导致部分Zn2+掺杂进NCM811材料的表层[17]。Co 2p、Mn 2p和O 1s XPS图谱的峰对应结合能(图3b~3d)分别为776.9, 640.7,528.2 eV,分别对应Co3+、Mn4+、O2-;改性后,NCM2样品这3个元素的峰都不如NCM811样品的峰尖锐,峰强度有所降低,主要是因为改性后材料表面Co,Mn和O的含量相对原始材料较少。在NCM2 样品中检测到Zn(图3e),相应的结合能为1017.5 和1042.5 eV,与Zn2+的结合能接近。在NCM2 样品中检测到P(图3f),相应的结合能为131.2 eV,与P5+的结合能接近。XPS 分析结果表明,Zn3(PO4)2包覆到了NCM811材料表面,并有部分Zn2+掺杂进NCM811材料的表层[15, 18]。
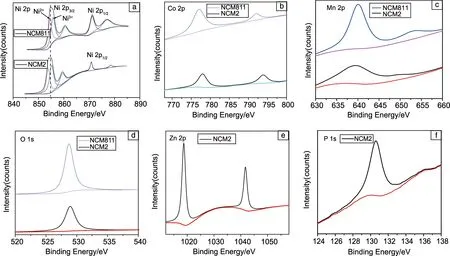
图3 NCM811纯样和NCM2材料元素的X射线光电子能谱(X-ray photoelectron spectroscopy, XPS)分析:Ni 2p (a), Co 2p (b), Mn 2p (c), O 1s (d), Zn 2p (e), P 1s (f)Fig.3 XPS analysis of Ni 2p (a), Co 2p (b), Mn 2p (c), O 1s (d), Zn 2p (e), P 1s (f) of pure NCM811 and NCM2 samples
3.2 电化学性能及分析
不同Zn3(PO4)2添加量改性的NCM811正极材料和NCM811纯样的首次充放电曲线如图4a所示。所有改性材料在2.8~4.3 V的电压范围内具有相同的容量变化趋势,这间接地证明Zn3(PO4)2改性不会改变原始的电化学反应过程。纯样NCM正极材料的初始放电容量为204.5 mAh·g-1。由于电极表面SEI膜的形成,导致材料在首次循环过程中存在不可逆容量损失,以及由于过渡金属离子的溶解而导致的活性物质损失[28, 29]。NCM2样品的首次放电容量为206.8 mAh·g-1,在所有4个样品中最高,这可能是由于在其表面上形成了一部分LiZnPO4,从而抑制了SEI膜的形成并为Li+的传输提供丰富的通道,进一步提高放电容量[30, 31]。NCM1和NCM3样品的首次放电容量分别为202.4和200.2 mAh·g-1,随着Zn3(PO4)2含量的进一步增加,非活性材料占比更大,所以放电容量较低。
图4b为不同Zn3(PO4)2添加量改性的NCM811正极材料和纯样NCM811的循环性能曲线。NCM2样品在0.1C电流密度下循环100周后放电比容量为191.1 mAh·g-1,容量保持率为92%,相比未改性样品的87%,提升较大。NCM1和NCM3样品在循环100周后放电比容量分别为177.3和181 mAh·g-1。NCM2样品循环性能提升的原因是,Zn3(PO4)2包覆层阻止了颗粒表面与电解液的副反应,从而提升了颗粒表面的结构稳定性。在改性过程中,表面结构与离子的静电力作用导致一部分Zn2+进入到晶格中,Zn2+半径(0.074 nm)大于过渡金属离子及Li+半径,使晶面间距扩大,Li+传输过程中进入被扩大的晶格相对容易,因此,颗粒表面离子与电解液接触范围增大,过渡金属离子电化学反应更为活泼,容量得到部分提升[26, 27]。由于Zn3(PO4)2改性NCM811材料晶格参数中c/a值相比NCM811纯样增大,晶面间距增大,“锂镍混排”程度降低,所以循环过程中材料结构稳定性提高,循环性能增强,容量保持率高。随着Zn3(PO4)2含量的增大,活性物质的量减小,NCM3样品在100次循环后容量保持率较低,为90.2%。3个改性样品中,NCM2样品相比纯样循环性能提升效果最为理想。
图4c为不同Zn3(PO4)2添加量改性的NCM811正极材料与NCM811纯样的倍率循环曲线。由图可以清晰地看出,在大倍率充放电过程中,未改性NCM811和Zn3(PO4)2改性NCM811样品的放电比容量相较于小倍率下的放电比容量下降较大,主要原因是大电流密度下电解液中Li+无法与电极材料颗粒进行充分接触,材料内部无法充分参与电化学反应,颗粒内部Li+电化学反应速率小于外部反应速率,放电比容量呈下降趋势[33, 34]。相同电流密度下,3种改性样品中NCM2样品相比纯样的倍率性能提升最大,NCM2样品在电流密度5C下循环10圈后放电比容量为115 mAh·g-1,最后仍以0.1C循环10圈后放电比容量为174 mAh·g-1。未改性的NCM811材料在电流密度5C下循环10圈后放电比容量为80 mAh·g-1,最后仍以0.1C循环10圈后放电比容量为161 mAh·g-1。NCM2改性样品相比未改性材料NCM811在5C下的放电比容量提升了43%。当放电倍率由5C恢复到0.1C时,NCM2样品的容量恢复率为87%,高于未改性样品NCM811的70%。NCM2样品具有比较好的容量恢复特性的原因是,Zn3(PO4)2涂层显著抑制了“表面重构”,提高了大倍率放电时材料的结构稳定性,最终材料的倍率性能得到提升。图4d为NCM2样品不同倍率下的首次放电曲线,可以看到,在5C下样品的放电电压下降到3.9 V,相比于0.1C时的放电电压,其下降了0.4 V,表明电化学过程中样品结构稳定。
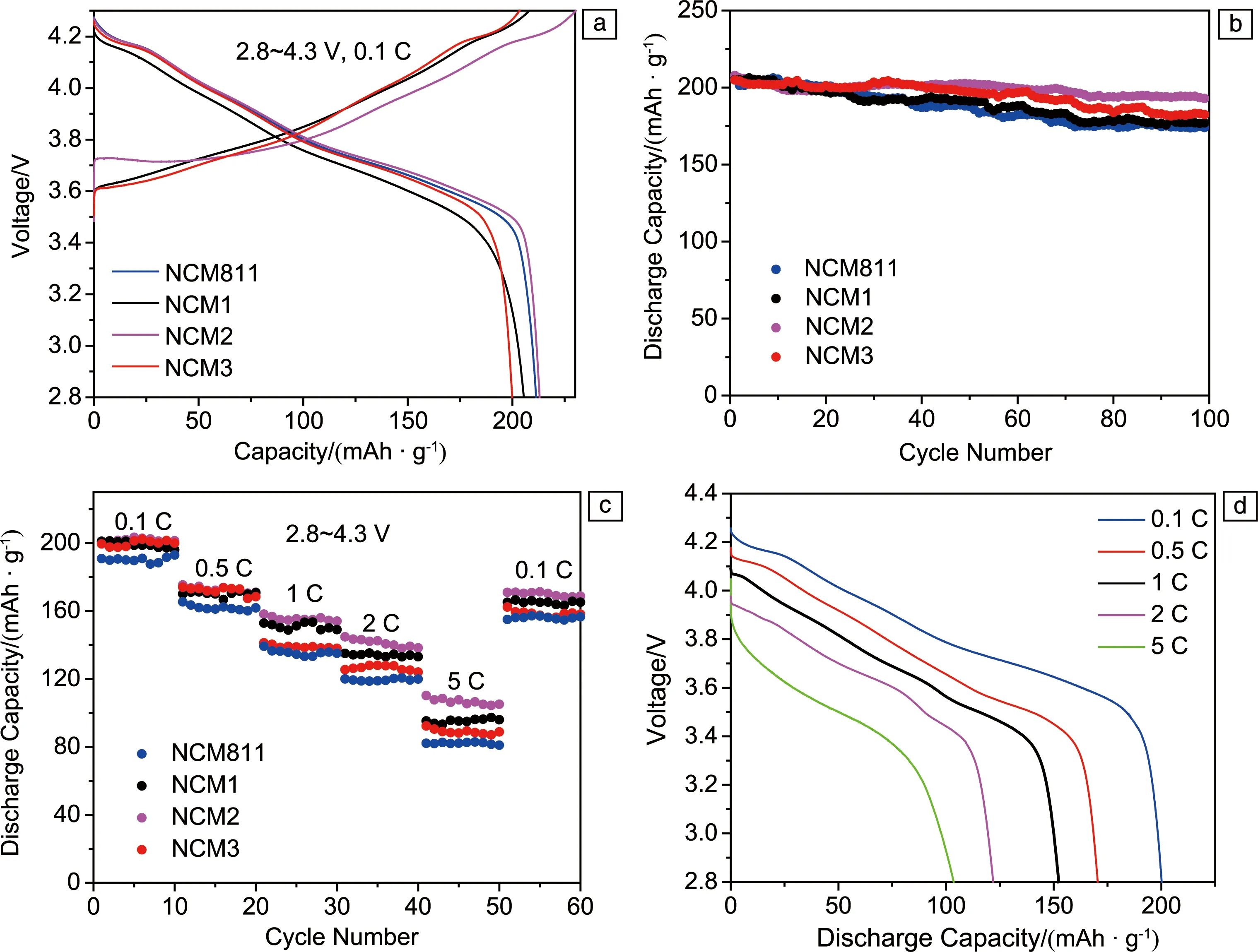
图4 NCM811纯样和Zn3(PO4)2包覆改性样品的首次充放电曲线(a),循环曲线(b),倍率循环曲线(c);NCM2不同倍率下的首次放电曲线(d)Fig.4 Initial charge-discharge profiles(a), cycling performance(b),rate cycling performance(c)of pure NCM811 and Zn3(PO4)2 modified NCM811 samples; First discharge curves of NCM2 under different rates (d)
图5a给出了NCM811纯样与包覆改性样品在循环100周后的EIS图谱。锂离子电池内部Li+的放电动力学过程如下:首先Li+在浓度梯度等驱动下进行迁移,到达电极材料表面,成为吸附态的Li+,然后Li+进入电极表面晶体的晶格[44, 45]。EIS的Nyquist图中高频区域出现的半圆弧代表电池中SEI膜的电阻,标记为RSEI。溶液电阻标记为Rs,NCM811、NCM1、NCM2、NCM3样品的阻抗谱拟合参数如表2所示。Rs随着Zn3(PO4)2添加量增加先降低后增加,NCM2样品具有最小的Rs。NCM2样品的RSEI值最低,原因是Zn3(PO4)2改性层有效抑制了SEI膜的形成,样品电极界面处的极化反应最小。低频区出现的阻抗弧则代表Li+穿越电极/电解液界面的电荷传输阻抗Rct[46, 47]。由表2可知,改性样品相比于未改性NCM811显示较小的Rct阻抗,这可能是Zn3(PO4)2改性层抑制了界面副反应和颗粒表面的恶化,抑制了充电过程中Ni4+到Ni2+的转变。
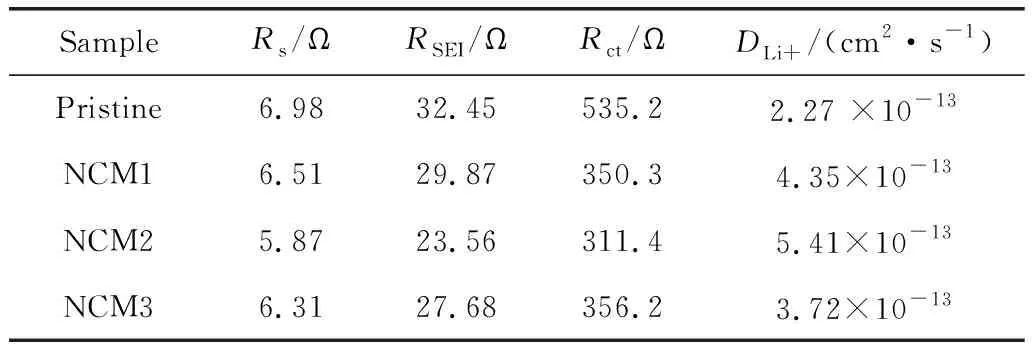
表2 NCM811纯样和包覆改性样品的阻抗拟合参数
图5b为纯样NCM811和包覆改性样品NCM2循环100周后的首周CV曲线。CV曲线位于3.97 V处的氧化峰对应Ni2+向Ni4+的氧化过程,位于3.58 V处的还原峰则是上述过程的逆过程。包覆改性样品NCM2的氧化峰与还原峰峰位差值较小,为0.31 V。改性样品相比NCM811纯样的电化学反应活性得到一定的增强。由于Zn3(PO4)2具有一定的电导率,在一定程度上提高了电子和离子的传输速率,降低了极化,最终改性后的材料氧化还原可逆性提高[42, 43]。
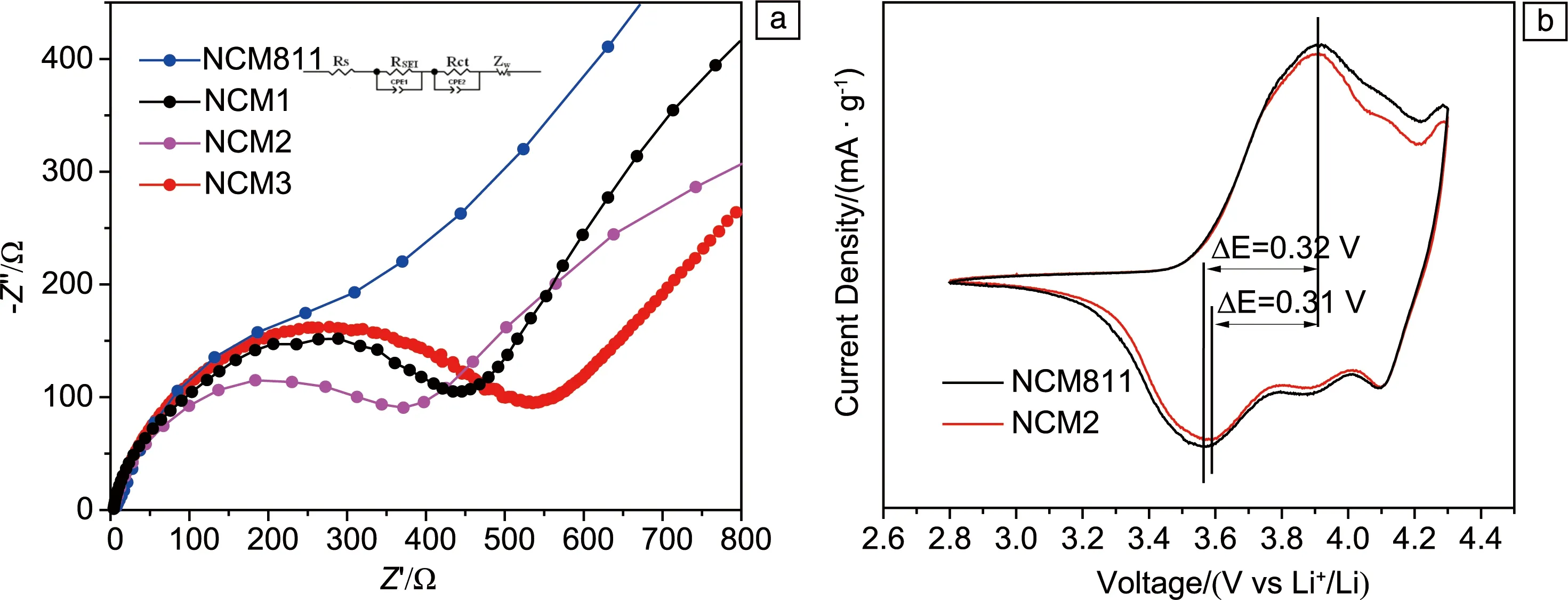
图5 NCM811纯样和NCM2样品循环100次后的电化学阻抗(electrochemical impedance spectroscopy, EIS)分析(a)与循环伏安(CV)曲线(b)Fig.5 EIS analysis(a)and the CV curves(b)of pure NCM811 and NCM2 samples after 100 times charge-discharge
4 结 论
制备了不同Zn3(PO4)2添加量改性的LiNi0.8Co0.1Mn0.1O2(NCM811)正极材料,深入探讨了Zn3(PO4)2改性对正极材料的晶体结构、形貌特征、元素状态及电化学性能的影响。在聚乙烯吡咯烷酮(PVP)的辅助下,Zn3(PO4)2均匀分布在颗粒表面,形成了均匀的包覆层。XRD图谱显示,包覆改性后正极材料的I(003)/I(104)值随Zn3(PO4)2添加量(质量分数)增加先增大后减少,添加量为3%时的改性样品NCM2的I(003)/I(104)值与c/a值比纯样的大,表明其相比NCM811纯样拥有更低的Li+/Ni2+混排。同时,Zn2+进入电极材料表面晶格,使晶面间距扩大,(003)平面内原子散射能力提升。改性材料NCM2在0.1C倍率下循环100周后容量保持率为92%,相比纯样有较大提升。在大电流密度(5C)下,改性后样品NCM2的放电比容量相比纯样提升43%。当放电倍率由0.1C逐步到5C后又恢复到0.1C时,NCM2样品的容量恢复率为87%,高于未改性样品NCM811的70%。电化学阻抗谱(EIS)结果表明,改性样品NCM2电极界面处的电化学极化降低,且具有较小的Rct阻抗,这可能是因为Zn3(PO4)2改性层抑制了界面副反应和颗粒表面的恶化,抑制了充电过程中Ni4+到Ni2+的转变。NCM2循环100周后的首周循环伏安(CV)曲线表明,改性后正极材料的氧化还原可逆性、电化学活性提高。Zn3(PO4)2包覆改性抑制了循环过程中电解液对正极材料的腐蚀和表面结构的离子重排,正极材料晶面间距扩大,Li+扩散速率提高,正极材料的循环性能和倍率性能得以提升。
