经皮肾通道顺行输尿管软镜技术处理回肠输出道术后输尿管回肠吻合处狭窄的临床应用
2021-09-14郭小林王少刚张加桥
崔 磊,郭小林,王少刚,杨 欢,李 聪,张加桥
(华中科技大学同济医学院附属同济医院泌尿外科,湖北武汉 430030)
膀胱根治性切除术结合回肠输出道术(Bricker术)是目前治疗肌层浸润性膀胱癌的最常用术式[1],而输尿管狭窄梗阻是Bricker术后并发症之一,发生率约为4%~8%[2],常见于输尿管回肠吻合处,其治疗方法主要包括开放手术和腔内手术。尽管开放手术效果更为确切,但由于此类患者以高龄者居多,且已经接受过膀胱根治性切除手术,再次手术的风险及难度均较高,患者的依从性也很差[3];腔内手术主要有经造口逆行途径和经皮肾穿刺顺行途径2种,逆行途径为常规入路[4],由于尿流改道后肠黏膜、肠皱襞的影响,经回肠输出道内逆行寻找输尿管口的难度大幅增加,手术成功率较低[5]。我们采用经皮肾通道顺行输尿管软镜联合输尿管硬镜的手术方式,配合多种手段处理Bricker术后输尿管回肠吻合处狭窄,取得了较好的疗效并总结出一定经验,现报道如下。
1 资料与方法
1.1 临床资料回顾2017年1月至2019年12月同济医院泌尿外科收治的Bricker术后发生输尿管回肠吻合处狭窄梗阻的患者16例,左侧10例,右侧4例,双侧狭窄2例,共计18侧手术。其中男性11例,女性5例,年龄61~79岁,平均(68.1±5.2)岁。所有患者发现输尿管回肠吻合处狭窄梗阻的时间在Bricker术后20~32个月之间,其中9例患者为常规术后复查时发现,7例患者因存在明显患侧腰痛的症状而发现。所有患者中11例患者出现肾功能不全,其肌酐平均值为(253.6±85.3)μmol/L。患者于术前结合B超、静脉尿路造影(intravenous pyelography,IVP)、泌尿系计算机断层扫描(computed tomography,CT)平扫三维重建、泌尿系CT增强(CT urography,CTU)、磁共振尿路成像(magnetic resonance urography,MRU)等多种检查明确患侧肾积水情况及狭窄梗阻部位,并排除相关手术禁忌证。
1.2 手术方法全身麻醉成功后取健侧斜卧位,尽可能架空暴露患侧腰部;结合术前影像资料在B超下观察患侧肾脏皮髄质、肾上下极、积水肾盏及肾周脏器,采用SVOF原则穿刺法建立经皮肾镜工作通道,SVOF原则图解见图1。尽量选择肾后组中、上盏,超声实时引导下经11肋间或12肋下经肾周/肾脏2步法对目标肾盏穹窿部最高点行垂直穿刺,逐级扩张通道至F18,输尿管硬镜进入经皮肾通道内,寻找到输尿管上段,留置亲水导丝,循导丝置入输尿管软镜输送鞘,利用输尿管软镜进入肾盂,沿顺行途径在输尿管内向下探查,寻找狭窄梗阻部位。根据狭窄部位情况,选择适当扩张方式,包括钬激光切开(200 μm,0.8~1.0 J/15~20 Hz)、球囊扩张(Bard,美国)、软镜输送鞘序贯扩张(F12/14,Cook,美国)。扩张完成后,将亲水导丝顺行置入回肠输出道内,由助手在输尿管硬镜经回肠输出道内直视下将导丝拉出造口并固定,顺行或逆行置入F6输尿管支架。输尿管软镜采用OLYMPUS URF-V型号,术后常规留置肾造瘘管。

A:短距原则,穿刺针经过肾实质路径最短;B:高点原则,穿刺点选择相对位置最高的肾盏;C:钝角原则,穿刺方向与肾盏开口方向呈钝角;D:穹隆原则,肾盏穹隆顶部进针,进针方向与肾盏穹窿垂直。
1.3 术后随访所有患者术后3~5 d拔除肾造瘘管,术后3 d复查腹部平片及泌尿系CT以检查输尿管支架管位置及肾积水情况,术后7 d复查血肌酐以检查肾功能恢复情况。术后2~3个月后经回肠输出道造口拔除输尿管支架管,每3个月复查1次,随访12个月。以患者症状明显减轻、患侧肾积水减轻或无明显加重、血肌酐明显下降并保持稳定为治疗有效的判定标准。
2 结 果
2.1 手术结果18侧手术中(16例患者,其中2例为双侧手术),17侧顺利完成,1侧因输尿管迂曲角度过大,反复多次尝试仍无法经腔内通过狭窄段而未能完成手术,后择期改行开放手术,手术完成率为94.4%。17侧手术完成病例中,2侧以钬激光切开狭窄段,3侧通过球囊扩张治疗,12侧采用输尿管软镜输送鞘序贯扩张吻合口狭窄处。手术时间为35~130 min,平均(53.7±16.5)min。
2.2 术后复查情况17侧手术完成病例中,患者腰痛症状于术后均得到有效缓解。术后3 d复查腹部平片及泌尿系CT,输尿管支架管位置良好,患侧肾积水均有不同程度缓解。术前11例肾功能不全患者于术后7 d再次复查血肌酐,其平均值为(133.7±21.5)μmol/L,较术前有明显改善。
2.3 术后并发症完成手术病例中,无患者出现诸如邻近脏器损伤、感染性休克、失血性休克、肾集合系统穿孔和撕裂伤、输尿管撕脱断裂、死亡等严重并发症发生。术后有3例患者出现发热,经抗生素合理治疗后好转;9例患者术后出现短暂持续性血尿,但血尿程度较轻,经对症处理后均好转。
2.4 术后随访结果17侧手术完成病例均在术后2~3个月内拔除输尿管支架管。术后随访12个月,13侧在随访期内患侧肾积水无明显加重,肾功能持续稳定。4侧术后出现狭窄复发,主要表现为患侧肾积水再次加重,复发时间在术后4~6个月。复发患者均择期行开放手术治疗,治疗成功率为76.5%。图2显示为其中1例患者术前、术后3个月及术后12个月影像学资料对比,效果显著。
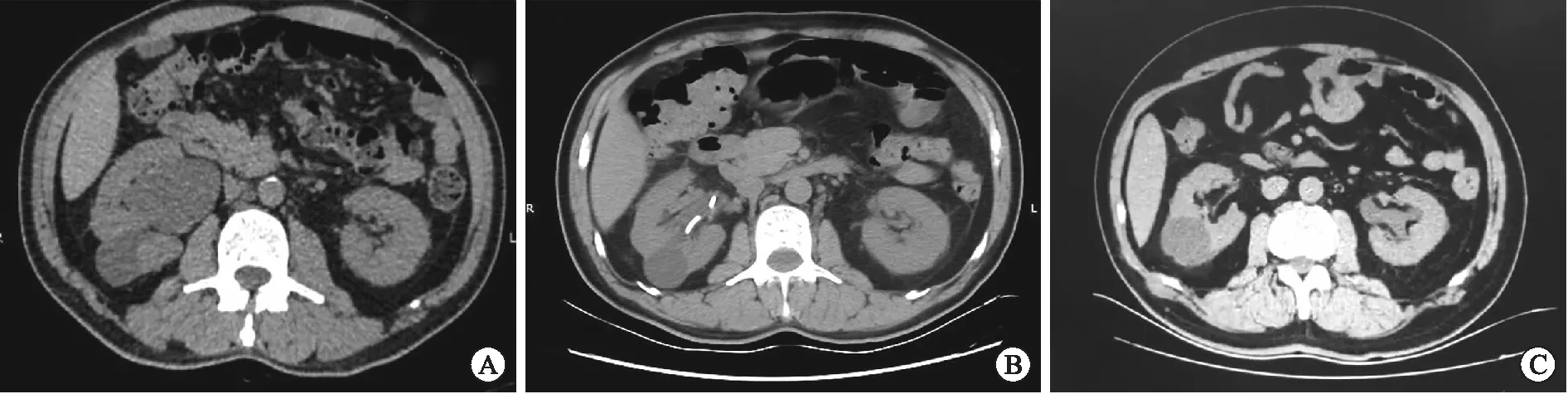
A:患者术前影像,显示右肾积水;B:患者术后3个月复查影像,右肾积水明显缓解,右侧输尿管支架管尚未拔除;C:患者术后12个月复查影像,输尿管支架管已拔除,肾积水未见明显复发。
3 讨 论
膀胱根治性切除术是目前治疗肌层浸润性膀胱癌最常用、最有效的手术方式,而与其相结合的尿流改道术后也有多种选择,无论是回肠输出道、结肠输出道、亦或是输尿管皮肤造口,都是被认可采用且行之有效的术式选择[6]。而尿流改道术的复杂程度与围手术期并发症具有相关性,研究报道显示不同术式的并发症发生率在30%~50%不等[2]。Bricker术具备较好的手术适应证、患者耐受较好、手术操作性较强等特点,目前仍是与膀胱根治性切除术联合进行的最常用的尿流改道术式之一。由于Bricker术需要将输尿管与游离的回肠段做吻合,因此术后输尿管狭窄梗阻是该术式的并发症之一,而梗阻发生部位常见于输尿管回肠吻合处,研究报道其发生率约为4%~8%,且该并发症是接受膀胱根治性切除术的患者术后出现肾功能减退、上尿路梗阻积水的重要危险因素[7]。Bricker术后输尿管回肠吻合处狭窄的典型临床表现是严重的患侧腰痛和反复的尿路感染,但有证据显示输尿管回肠吻合处狭窄的患者在前期也可表现为无明显临床症状,直至出现严重的肾功能不全[8]。本组病例中,有9例患者(9/16)是在常规术后复查随访时发现的,并无明显临床症状。Bricker术后出现输尿管回肠吻合处狭窄的主要原因是尿流改道术中输尿管周围的微循环受到不同程度的破坏,持续的缺血状态导致了输尿管黏膜及周围组织的纤维化改变,结缔组织瘢痕收缩、粘连、挤压最终导致狭窄梗阻[9]。另外,一些医源性的原因如吻合方法不当、输尿管医源性损伤,也可导致术后输尿管回肠吻合处狭窄的发生,而结石梗阻、局部肿瘤复发则是继发性输尿管回肠吻合处狭窄的常见原因[10]。
由于接受Bricker术的患者大多为肌层浸润性膀胱癌患者,因切除范围扩大、盆腔淋巴结清扫、综合治疗等原因都会在术后出现不同程度的腹腔、腹膜,甚至肠道的粘连,再次行腹腔探查手术的难度大幅增加[11]。有研究报道,腔内手术治疗Bricker术后输尿管回肠吻合处狭窄的成功率在10%~40%,而开放手术的成功率则达到了40%~90%[12]。尽管两者在手术效果上有明显的差异,但腔内手术在治疗Bricker术后输尿管回肠吻合处狭窄时,其患者整体耐受和依从性较好、手术难度相对较低、经自然腔道入路不受腹腔粘连的影响、手术风险较低。
Bricker术后患者的尿流输出道由回肠替代,其内部肠黏膜、肠绒毛、肠皱襞会对逆行途径的内镜视野造成严重影响,因此采用腔内手术治疗Bricker术后输尿管回肠吻合处狭窄时,经造口逆行途径在寻找输尿管吻合口时难度极大,这也是造成腔内手术治疗Bricker术后输尿管回肠吻合处狭窄成功率较低的原因之一[13]。经皮肾穿刺顺行途径则可以避免回肠输出道内肠黏膜对内镜探查视野的影响,结合输尿管软镜可增加顺行途径探查上尿路的适用范围,其主要难点在于术中患侧经皮肾穿刺的技巧以及狭窄治疗方式的选择上。通过分析本组病例,我们总结出具有广泛性的经验,以适用于经皮肾通道顺行输尿管软镜联合输尿管硬镜在Bricker术后输尿管回肠吻合处狭窄的治疗。其适应证主要包括:①Bricker术后输尿管回肠吻合处狭窄的初发患者;②患者高龄、开放手术风险较高,或患者自身暂不接受开放手术;③Bricker术后接受过肿瘤相关综合治疗,考虑腹腔粘连严重。而输尿管回肠吻合处狭窄多次复发、合并泌尿系感染未得到有效控制、术前检查考虑肿瘤复发导致狭窄等情况则应列为其行腔内治疗的禁忌证。
在经皮肾穿刺操作方面,传统方式为患者在俯卧位下经B超引导下穿刺,而斜仰卧位下穿刺与传统俯卧位下穿刺相比,操作需要更细致。在本组病例中,我们借鉴复杂性肾结石行经皮肾镜碎石术时的穿刺技巧,在斜仰卧位下依然可采用短距(short)、高点(vertex)、钝角(obtuse)、穹窿(fornix)4个方面相结合的SVOF原则来完成经皮肾穿刺[14]。
在输尿管狭窄腔内治疗方式的选择上,本组病例中,有2例以钬激光切开狭窄段,3例通过球囊扩张治疗,12例采用输尿管软镜输送鞘序贯扩张狭窄处。有研究显示采用球囊扩张治疗输尿管狭窄的有效率在15%~30%,而采用序贯扩张并于术后留置输尿管支架的方法其有效率在40%左右[15]。不同的治疗方式其效果虽各有差异,但与患者输尿管狭窄程度、狭窄段长度以及患者自身因素等也有着密切关系[16]。
在并发症方面,采用SVOF原则进行经皮肾穿刺可显著提高斜仰卧位下穿刺成功率、减少出血,同时以高点和钝角原则选择穿刺点和穿刺方向,避免因穿刺通道与输尿管角度过大而增加手术难度;而经皮肾通道的存在,使软镜术中的肾内灌注回流增加,降低肾盂内压力,在保证视野清晰的同时,降低肾内高压导致逆行感染的风险。本组病例中,术后有3例患者出现发热,经抗生素合理治疗后好转;9例患者术后出现短暂持续性血尿,但血尿程度较轻,经对症处理后均好转。
综上所述,经皮肾通道顺行输尿管软镜联合输尿管硬镜治疗Bricker术后输尿管回肠吻合处狭窄,通过腔内手术的方式解决肌层浸润性膀胱癌患者接受膀胱根治性切除术、尿流改道术后的并发症,具有较好的临床应用价值。尽管腔内手术治疗输尿管狭窄的远期效果不如开放手术,而且针对难治性、复发性输尿管狭窄仍然建议选择开放手术治疗,但腔内手术用于高龄患者时风险较低、患者耐受较好,可以延缓或降低需要行开放手术的可能性[17]。
