混合材料对废水中氨氮脱除的实验研究
2021-09-12孙菱翎李晓颖温新悦黄明秀熊宇玲王旭
孙菱翎 李晓颖 温新悦 黄明秀 熊宇玲 王旭
摘 要:为了更有效地脱除废水中的氨氮,选用人造沸石和活性炭混合作吸附剂,考察不同条件下废水中氨氮的脱除效果,包括比例、用量、pH值、反应时间、初始浓度、温度等,并通过等温吸附和吸附动力学研究了吸附机理。结果表明:当沸石/活性炭为2/3、吸附剂用量为2.5g、pH为8、反应时间20min、氨氮废水初始浓度为40mg/L、温度为20℃时,氨氮的脱除率较高,属于Langmuir吸附,符合拟二级动力学。
关键词:人造沸石;活性炭;氨氮废水;脱除率;动力学
中图分类号:X703.1 文献标识码:A 文章编号:1673-260X(2021)08-0070-05
引言
近年来,工农业发展突飞猛进,随之而来的是逐日剧增的污水排放,其中,化工、化肥农业、养殖业及催化剂厂等产生了大量的氨氮污水[1,2],排放进河流湖泊,使水体缺氧变质,富营养化加剧,致使水中动植物产生中毒现象,人类的饮用水也产生严重危害甚至危及生命健康。因此减少污水排放或是将污水中污染物降低到标准浓度以下目前是一种较可行的方法。
目前,国内外处理氨氮的方法主要有:生物法、折点氯化法、化学沉淀法、离子交换法、吹脱法和电渗析法等。黄婧[3-5]等人采用的生物法仍处于实验室阶段,生物反应器不能广泛应用。胡亮[6-8]等人用折点氯化法处理铅锌冶炼中产生的氨氮废水,效果良好,但是此过程对药剂的加入量要求较高,且会产生大量的余氯,不适合广泛使用。化学沉淀法[9-11]只适用于高浓度氨氮废水的处理,并且在强碱性条件下会发生副反应,不利于去除氨氮。离子交换法[12]的优点是成本低、工艺简单、易操控,但树脂再生困难,再生后仍含有大量氨氮,效果并不理想。吹脱法[13,14]用来处理高浓度的氨氮废水,吹脱后氨氮可回收利用,方便且易于操作,应用广泛,但用时较长,且氨氮剩余浓度并不是很低。余光亚[15]等人在电渗析过程中,对设备的设计、材料、不同条件的控制精度要求较高。
如何高效、快速、有效地处理氨氮废水,找寻成本低廉、稳定有利的处理技术是生态环境保护的一个重要的课题。此次主要研究以人造沸石和活性炭混合为吸附剂对废水中氨氮进行脱除,为氨氮废水的处理方面提供更多的经验数据,为环境保护方面贡献力量。
1 实验试剂及实验仪器
实验室模拟氨氮废水、人造沸石、活性炭、碘化钾、氯化铵、二氯化汞、酒石酸钾钠、氢氧化钾、试剂均为分析纯。紫外可见分光光度计、磁力搅拌器、pH计、标准检验筛、电子天平、电热鼓风干燥箱、超级恒温水浴锅。
2 实验方法
2.1 氨氮含量的测定
废水中氨氮含量的测定按照水质分析标准HJ535—009纳氏试剂分光光度法进行测定。
2.2 实验方法
2.2.1 氨氮脱除实验
取氨氮废水100ml,加入一定比例沸石和活性炭,调节温度、pH,反应一段时间后,静置过滤,取上清液测定吸光度。分别对吸附剂比例、用量、pH、反应时间、初始浓度、温度逐一进行梯度实验。
2.2.2 脱除率的计算
氨氮脱除率=[(初始氨氮浓度-剩余氨氮浓度)/初始氨氮浓度]*100%
由上式得到脱除率,作各个变量与脱除率的关系曲线图。
2.2.3 吸附等温实验
分别配制20mg/L、40mg/L、60mg/L、80mg/L、100mg/L、150mg/L、200mg/L氨氮废水溶液100mL,加入比例为2/3,质量共2.5g的沸石和活性炭,调节pH=8,温度为20℃,反应20min,静置,过滤。取上清液测定吸光度,计算剩余溶液中的氨氮浓度以及对应的吸附等温实验的数据。
2.3 标准曲线
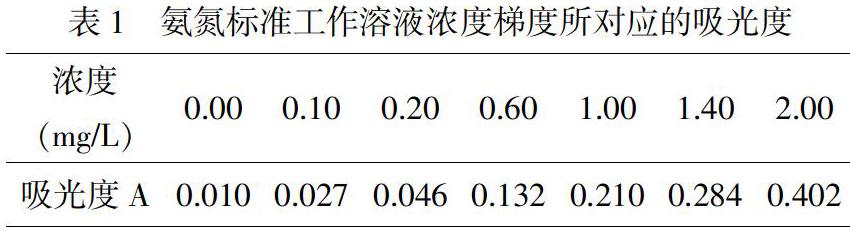
配制0.0mg/L、0.1mg/L、0.2mg/L、0.6mg/L、1.0 mg/L、1.4mg/L和2.0mg/L的氨氮标准溶液。静置20min,在420mm波长下,测量吸光度。数据如表1所示:
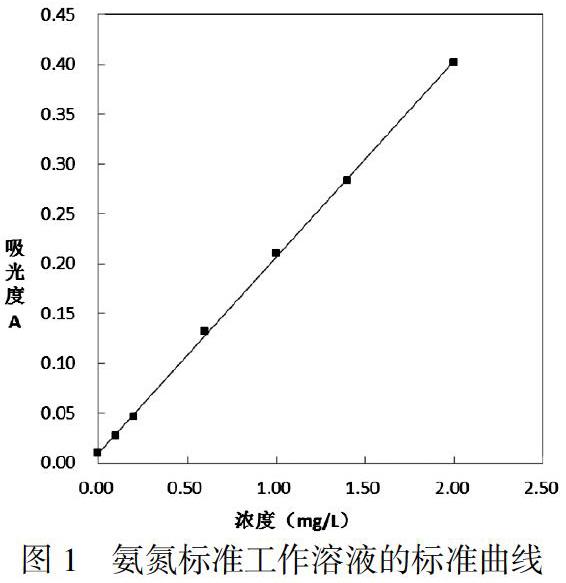
绘制校准曲线。横坐标为氨氮初始浓度,纵坐标为吸光度,其标准曲线方程为:y=0.197x+0.0095,R2=0.9996,标准曲线符合工作曲线的要求。如图1:
3 结果与讨论
3.1 兩种吸附剂比例对氨氮脱除的影响
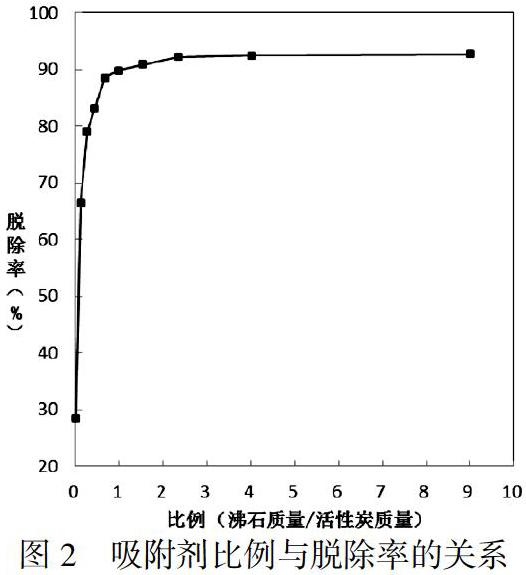
选用吸附剂用量5g、pH值=9、反应时间20min、氨氮废水初始浓度为40mg/L、温度为室温条件下,考察不同吸附剂比例下的氨氮脱除率。
由图2可以看出,随着比例(沸石质量/活性炭质量)的增加,脱除率先急剧上升,后趋势变缓至趋于稳定,这是因为比例增加,沸石比重增大,沸石与氨氮接触机会增多,故脱除率增大,当达到一定比例时,氨氮含量过低,不能被有效的吸附,趋势减缓。考虑图中趋势及市场上人造沸石高于活性炭价格等因素,因此选取比例(沸石质量/活性炭质量)2/3为较佳比例。并可以说明人造沸石吸附氨氮的能力大于活性炭。
3.2 吸附剂用量对氨氮脱除的影响
选用吸附剂比例(沸石质量/活性炭质量)2/3、pH值=9、反应时间20min、初始浓度为40mg/L、温度为室温条件下,考察不同的吸附剂用量对氨氮脱除率的影响。
由图3可以看出,随着吸附剂用量的增加,氨氮脱除率先快速增高后趋势减缓。这是因为吸附剂用量增加,增加了与氨氮的接触机会,使得氨氮迅速占据吸附剂孔隙,当达到一定脱除率时,吸附剂孔道减少,故脱除率减缓。所以考虑吸附剂成本及吸附趋势,选取吸附剂用量2.5g。
3.3 pH对氨氮脱除的影响
选用吸附剂比例(沸石质量/活性炭质量)2/3、吸附剂用量为2.5g、反应时间20min、氨氮初始浓度为40mg/L、温度为室温,观察不同pH对氨氮脱除效果的影响。
由图4可以看出,随着pH的增大,氨氮脱除率先缓慢增加,后呈下降趋势,说明次吸附剂在偏酸及中性环境下易于脱除氨氮,而在碱性环境不利于氨氮的脱除。这是因为,在强碱性条件下,沸石和活性炭对氨氮的吸附能力减弱,造成脱除率降低,相反则吸附能力强。因此由图中趋势,选取pH=8。
3.4 反应时间对氨氮脱除的影响
选用吸附剂比例(沸石质量/活性炭质量)2/3、吸附剂用量为2.5g、pH=8、氨氮初始浓度为40mg/L、温度为室温,观察不同的反应时间对氨氮脱除率的影响。
由图5可以看出,随着反应时间的增长,氨氮脱除率先急剧增加后趋于平缓。这是因为当反应时间小于20min时,反应较为剧烈;当反应时间在20min~50min时,反应过渡为稳定状态;而当反应时间大于50min,反应基本上达到平衡。所以考虑省时高效等因素,选择反应时间为20min。
3.5 初始浓度对氨氮脱除的影响
选用吸附剂比例(沸石质量/活性炭质量)2/3、吸附剂用量为2.5g、pH=8、反应时间为20min、温度为室温,考察不同的氨氮初始浓度为对氨氮脱除率的影响。
由图6可以看出,随初始浓度的增大,氨氮的脱除率不断下降。这是因为在低浓度时,氨氮分子与吸附剂接触的机会更多,而吸附剂的孔隙有限,所以在低浓度下更易进行吸附。说明吸附通常适用于低浓度氨氮废水的处理。
3.6 温度对氨氮脱除的影响
选用吸附剂比例(沸石质量/活性炭质量)2/3、吸附剂用量为2.5g、pH=8、反应时间为20min、氨氮初始浓度为40mg/L,考察不同的温度对氨氮脱除率的影响。
由图7可以看出,温度对氨氮脱除没有较大的影响,在温度较高时,溶液中水分蒸发会带出氨氮,所以一般情况下在室温进行反应即可。
3.7 吸附等温实验
通过吸附等温实验的数据,可计算出吸附平衡后氨氮溶液的残留浓度C以及平衡时氨氮的吸附量Q,根据Langmuir和Freundlich等温吸附数学表达式[16],即吸附等温方程,绘制出Langmuir和Freundlich吸附等温线。方程式如下:
Langmuir吸附等温式线性方程为:
Freundlich吸附等温性方程为:
式中:Q——平衡时氨氮吸附量,单位为mg·g-1;Qm——吸附剂表面所有吸附点均被吸附质覆盖时的吸附量,即饱和吸附量;单位为mg·g-1;C——吸附平衡后氨氮溶液的残留浓度,单位为mg·L-1;KL——Langmuir吸附等温式的吸附平衡常数;KF——Freundlich吸附等温式的吸附平衡常数;n——经验常数。
根据Langmuir方程(1)和Freundlich方程(2)作图8和9,计算出表2和表3的数据。
由上可以看出吸附过程中Langmuir的R2大于Freundlich,说明Langmuir的回归性较好,所以符合Langmuir等温吸附线。
3.8 吸附动力学实验
吸附動力学研究吸附的快慢,与接触时间相联系。拟用一级动力学方程和二级动力学方程[12]对数据进行模拟,关系式如下:
拟一级动力学模型:
拟二级动力学模型:
式中:qe——平衡时氨氮的吸附量,单位为mg·g-1;qt——t时刻氨氮的吸附量,单位为mg·g-1;k1——一级动力学速率常数;t——反应时刻,单位为min;k2——二级动力学速率常数。
根据拟一级动力学模型(3)、拟二级动力学模型(4)作图10以及图11,计算各模型参数如表4、表5。
经相关度对比,拟二级动力学的R2大于拟一级动力学的数值,说明拟二级动力学的回归性较好,故该吸附符合拟二级动力学。
4 结论
通过控制不同的条件,研究人造沸石、活性炭混合试剂对废水中氨氮的吸附,得出以下结论:
(1)使用混合试剂吸附废水中的氨氮较佳的吸附条件为:沸石质量、活性炭质量比例2/3;吸附剂用量为2.5g;pH=8;反应时间为20min;氨氮初始浓度为40mg/L;温度为室温。混合试剂通常适用于低浓度氨氮废水的吸附;符合Langmuir等温吸附线,及拟二级动力学模型。
(2)采用混合试剂可以有效地去除废水中的氨氮,且经济可行,可以为废水的处理提供一定的理论基础,对水的富营养化方面有一定的抑制作用。在今后,开发更高效且用途广泛的脱除剂具有广阔的发展空间。
参考文献:
〔1〕王兆熊,郭崇涛,张英,等.化工环境保护和三废处理技术[M].北京:化学工业出版社,1982.18-29.
〔2〕李天育,陈钰琦,张静,等.含氮废水的处理方法研究[J].广东化工,2020,47(24):82-83.
〔3〕Yaofeng Lu,Zhibin Ding,Kexin Gao,et al. The effect of hydraulic retention time on ammonia and nitrate bio-removal over nitrite process[J]. Environmental Technology, 2020, 41(10). 1275-1283.
〔4〕黄婧,吴若菁,贾晗,等.生物法处理养殖污水中氨氮的研究进展[J].福建畜牧兽医,2009,31(02):15-16.
〔5〕Long Liang,Yingqiao Shi,Guigan Fang, et al. The changes of bamboo pulping waste water residuals in biological treatment process[J]. Water and Environment Journal, 2019, 33(01): 14-20.
〔6〕赵振.折点加氯法去除氨氮应用于河道突发性污染中的试验研究及其应用[J].资源信息与工程,2021,36(01):118-121.
〔7〕刘恒嵩,彭玉玲,丁伟,等.折点氯化法处理废水中氨氮工艺研究[J].农村经济与科技,2016,27(02):145-146.
〔8〕胡亮,高联欢,等.折点氯化法去除铅锌冶炼废水中氨氮研究[C].云南曲靖:云南冶金集团驰宏锌锗股份有限公司,2014.1-5.
〔9〕刘国跃,王昶昊,施云海,等.化学沉淀法处理高浓度氨氮废水的实验研究[J].石油化工技术与经济,2013,29(06):31-35.
〔10〕孙菱翎,范晓静,罗冬梅,等.罚函数及高斯牛顿拟合优化磷酸铵镁法[J].辽宁石油化工大学学报,2018,38(06):26-30+53.
〔11〕张道斌,吕玉娟,张晖,等.化学沉淀法去除垃圾渗滤液中氨氮的试验研究[J].环境化学,2007,26(01):62-65.
〔12〕陶莉,许海青,刘晨明,等.离子交换树脂处理氨氮废水的研究现状[J].环境科技,2020,33(03):69-73.
〔13〕奥斯曼·吐尔地,杨令,安迪,等.吹脱法处理氨氮废水的研究和应用进展[J].石油化工,2014,43(11):1348-1353.
〔14〕姚淑华,张晓燕,石中亮,等.氨氮废水处理技术及研究进展[J].化工中间体,2010(11):24-30.
〔15〕余光亚,杨战社,呼世斌,等.氨氮废水的电渗析处理[J].西北农业学报,2008,17(03):332-335.
〔16〕Cheng J J, Shi L J, Lu J J, etal. Aminoionic liquids-modified magnetic core/shell nanocomposite as an effi-cient adsorbent for dye removal[J]. Journal of Industrialand Engineering Chemistry, 2016, 36: 206-214.