氟硅酸钾滴定法测定粗制氟化钠中二氧化硅
2021-09-09谢堂锋陈若葵巩勤学蔡罗蓉
谢堂锋,陈若葵,巩勤学,蔡罗蓉
(湖南邦普循环科技有限公司,湖南 长沙 410600)
氟化钠是一种重要的氟化盐,是许多氟化合物中氟离子的主要来源,广泛用于工业、农业、医药、国防等领域,主要用作木材防腐剂、金属助熔剂、农业杀虫剂、电解铝调整剂、饮水氟化处理剂等[1]。锂盐工业生产过程产生的副产品氟化钙,可回收用于生产粗制氟化钠产品。但是,在粗制氟化钠的生产过程中,分离、洗涤后所得的粗制氟化钠中仍夹杂有二氧化硅。因此,在粗制氟化钠的生产过程中二氧化硅含量的检测准确与否对氟化钠产品指标的监测至关重要。
目前,测定二氧化硅的方法主要有重量法[2]、氟硅酸钾滴定法[3]、钼蓝分光光度法[4]、X射线荧光光谱法[5]、电感耦合等离子体发射光谱法(ICP-AES)[6]等。其中氟硅酸钾滴定法因操作简便、准确、测定范围广等优点被广泛应用于各类试样中较高含量硅的测定。但是,该方法多采用碱性熔剂对试样进行高温熔融预处理,操作繁琐冗长,易污染环境,严重腐蚀熔融器皿(如镍坩埚、银坩埚、铂坩埚等),大大降低了日常生产中分析测试的速率及效率。微波消解技术是一种高效的样品预处理方法,具有操作简便、消解速度快、试剂用量少、低空白、节能高效等优点,克服了传统高温碱熔法的不足[7]。笔者拟采用HNO3-HF混合酸为消解溶剂,通过微波消解技术对氟化钠样品进行快速消解,以溴麝香草酚蓝-酚红为指示剂,优化测试条件,建立了氟硅酸钾滴定法测定氟化钠中二氧化硅的方法。该方法可大幅度缩短分解试样的时间,有效降低检测成本,结果较满意,能够满足氟化钠生产过程中的分析要求。
1 实验部分
1.1 主要仪器、试剂及溶液配制
仪器:MWD-600型密闭式智能微波消解仪;DT227型调压电热板。
试剂及溶液配制:50 g/L氯化钾-50%乙醇溶液(称取50 g氯化钾溶于500 mL水中,并加入500 mL乙醇,混匀);溴麝香草酚蓝-酚红指示剂(分别称取溴麝香草酚蓝、酚红指示剂各0.1 g,溶于100 mL乙醇中,混匀后滴加0.1 mol/L氢氧化钠溶液至呈鲜明紫色);0.5%硝氮黄指示剂(称取0.5 g硝氮黄溶于100 mL水中,混匀);1%酚酞指示剂(称取1.0 g酚酞溶于100 mL乙醇中,混匀);0.1 mol/L氢氧化钠标准溶液(称取4.0 g氢氧化钠溶于预先煮沸并冷却的1 000 mL水中,充分摇匀并贮存于塑料瓶中,以基准试剂邻苯二甲酸氢钾标定);中性水(向沸水中滴加溴麝香草酚蓝-酚红指示剂3滴,滴加0.1 mol/L氢氧化钠溶液至呈紫色);GBW(E)070102萤石标准物质[w(SiO2)=18.04%,国家标准物质]。所用试剂均为分析纯,水均为电阻率为18.2 MΩ·cm的超纯水。
1.2 实验原理及方法
1.2.1 工作原理
样品在微波电场下经浓硝酸-浓氢氟酸混合酸消解使硅以可溶性氟硅酸的形式存在,并在硝酸介质条件下与过量钾离子反应生成难溶的氟硅酸钾沉淀,经过滤、洗涤、中和残余酸,加沸水使氟硅酸钾沉淀水解,采用氢氧化钠标准溶液滴定水解后生成的氢氟酸。化学反应方程式:

1.2.2 样品测定
称取0.100 0 g(精确到0.000 1 g)试样置于Teflon消解罐中,加入8 mL浓HNO3和2 mL浓HF,摇匀后旋紧消解罐盖子,放入微波消解仪中,按表1所示的消解条件进行微波消解。消解结束后取出消解罐,放置在冷水浴中冷却至室温,拧开消解罐盖子将试样转移至300 mL塑料烧杯中,用纯水洗涤消解罐5~6次,控制体积在50 mL左右,加少量滤纸浆,不断搅拌下加入8 mL饱和氯化钾溶液,充分搅拌2~3 min,静置约15 min使沉淀完全。用快速滤纸和塑料漏斗过滤,用50 g/L氯化钾-50%乙醇溶液洗涤塑料烧杯及沉淀各3次,然后取下滤纸连同沉淀置于原塑料烧杯中,沿杯壁加20 mL 50 g/L氯化钾-50%乙醇溶液,将滤纸捣碎,加5滴溴麝香草酚蓝-酚红指示剂,滴加氢氧化钠标准溶液至呈稳定的紫红色,以中和沉淀和滤纸上的残余酸,不计读数。加入200 mL左右中性沸水,搅拌使沉淀水解,补加5滴混合酸碱指示剂,此时溶液变为黄色,用氢氧化钠标准滴定溶液滴定至稳定的紫红色为终点,记下读数,根据标准溶液的消耗量计算二氧化硅的含量。随同试样做空白试验。
1.2.3 结果计算
试样中二氧化硅的质量分数按式(1)计算:
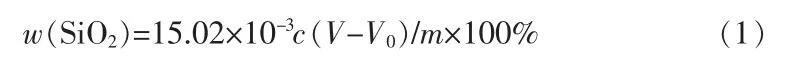
式中:w(SiO2)为试样中二氧化硅的质量分数,%;c为氢氧化钠标准溶液的浓度,mol/L;V为试样滴定消耗的氢氧化钠标准溶液的体积,mL;V0为空白滴定消耗的氢氧化钠标准溶液的体积,mL;m为试样质量,g。
2 结果与讨论
2.1 消解酸体系的选择
微波消解中常用的酸较多。对于完全消解,不同基质样品用酸也有很大不同。采用不同酸体系对GBW(E)070102萤石标准物质[w(SiO2)=18.04%]进行微波消解试验,结果见表2。由表2看出,采用王水体系消解定容后的溶液中还存在少量残渣,未达到完全消解,测定结果严重偏低,相对误差较大。这主要是因为王水体系中没有加入氢氟酸,二氧化硅晶格结构无法被完全破坏。采用硝酸-氢氟酸、盐酸-氢氟酸、硝酸-盐酸-氢氟酸体系消解定容后均得到澄清溶液,这表明氢氟酸的加入会与样品中的硅反应,促进样品溶解。但是引入盐酸的两种消解酸体系测定值相对偏低。这可能是因为生成的氟硅酸钾沉淀可溶于体系中的盐酸,且溶解度随温度的升高略有增加。因此,选择硝酸-氢氟酸体系作为消解溶剂。

表2 不同酸体系消解GBW(E)070102萤石标准物质的测定结果Table 2 Test results of GBW(E)070102 fluorite standard substance digested by different acid systems
2.2 饱和氯化钾溶液用量对萤石标准物质测定结果的影响
钾离子浓度是影响氟硅酸钾沉淀是否完全的主要因素。根据同离子效应,氟硅酸钾需在大量钾离子存在下才能完全沉淀,钾离子适当过量可以抑制氟硅酸钾沉淀的水解,有助于降低氟硅酸钾沉淀的溶解度[8]。很多文献选择直接加入固体氯化钾作为沉淀剂,但是固体氯化钾溶解度随环境温度的变化较大,在低温条件下易析出大量细小氯化钾晶体堵塞滤纸孔,不利于沉淀的过滤及洗涤,同时加入固体氯化钾可能引起溶液中局部钾离子浓度过高产生假过饱和现象而影响测定结果[9]。为排除温度的影响,拟采用饱和氯化钾溶液替代固体氯化钾作为沉淀剂,对GBW(E)070102萤石标准物质[w(SiO2)=18.04%]进行饱和氯化钾溶液用量试验,结果见图1。由图1可见,随着饱和氯化钾溶液用量增加,二氧化硅含量测定结果逐渐升高,当饱和氯化钾溶液用量为6~8 mL时,二氧化硅含量测定结果偏差较小,测定值比较接近标准物质中硅的参考值。这主要是因为,当饱和氯化钾溶液用量过低时,由于共同离子效应太弱,氟硅酸钾沉淀不完全,导致测定结果偏低;当饱和氯化钾溶液用量过高时,钛、铝等干扰元素的沉淀作用增大,使得测定结果偏高。为确保氟硅酸钾沉淀完全,选择饱和氯化钾溶液用量为8 mL。

图1 饱和氯化钾溶液用量对GBW(E)070102萤石标准物质测定结果的影响Fig.1 Effect of saturated potassium chloride dosage on the determination result of GBW(E)070102 fluorite standard substance
2.3 沉淀温度对萤石标准物质测定结果的影响
氟硅酸钾沉淀是放热反应,氟硅酸钾的溶解度随温度的升高而增加,降低温度有利于氟硅酸钾沉淀完全。对GBW(E)070102萤石标准物质[w(SiO2)=18.04%]进行沉淀温度试验,结果见图2。由图2看出,当沉淀温度为15~28℃时,测定结果稳定性较好。当沉淀温度低于15℃时,测定结果与标准物质硅含量相比普遍偏高,可能是由于吸附的杂质和共沉淀不易洗涤干净所致;当沉淀温度高于30℃时,氟硅酸钾沉淀的溶解度增大,导致氟硅酸钾沉淀不完全或复溶,使得测定结果偏低。因此,选择沉淀温度为20~25℃。

图2 沉淀温度对GBW(E)070102萤石标准物质测定结果的影响Fig.2 Effect of different precipitation temperature on the determinationresult of GBW(E) 070102 fluorite standard substance
2.4 沉淀放置时间对萤石标准物质测定结果的影响
沉淀放置时间是影响氟硅酸钾是否沉淀完全的一个重要因素。氟硅酸钾是一种无定形胶状沉淀,不需要经过长时间陈化,沉淀充分形成后应尽快过滤分离,以防止沉淀提前水解。对GBW(E)070102萤石标准物质[w(SiO2)=18.04%]进行沉淀放置时间试验,结果见图3。由图3看出,当沉淀放置时间为10~20 min时,测定结果与标准物质硅含量基本保持一致;放置时间过短造成氟硅酸钾沉淀不完全,使得测定结果偏低;放置时间过长,测定结果显著偏高。这可能是因为铝、钛等杂质离子以异质同晶现象共沉淀或氟硅酸钾沉淀部分水解而影响测定结果[10]。综合考虑,选择沉淀放置时间为15 min。

图3 沉淀放置时间对GBW(E)070102萤石标准物质测定结果的影响Fig.3 Digestion results of different precipitation time
2.5 沉淀洗涤及残余酸中和对萤石标准物质测定结果的影响
沉淀洗涤的效果及残余酸中和是否完全将直接影响测试结果的准确性。沉淀洗涤次数少,将不能充分洗净吸附在氟硅酸钾沉淀表面的杂质和残余游离酸,使得测定结果偏高;沉淀洗涤次数过多,则会引起氟硅酸钾沉淀提前水解,使得测定结果偏低。由于氟硅酸钾在水中的溶解度较大[Ksp(K2SiF6)=8.6×10-7,25℃时100 mL水中可溶解0.177 g氟硅酸钾],且其溶解度随着温度的升高而逐渐增大,为防止氟硅酸钾沉淀在洗涤时水解,采用50 g/L氯化钾-50%乙醇溶液作为洗液,洗涤烧杯及沉淀各3次,洗液体积为25~30 mL,其中乙醇可有效降低氟硅酸钾溶解度并加快洗去沉淀表面杂质和游离酸的速度。同时中和酸过程要迅速准确,中和时间过长可能会引起部分氟硅酸钾沉淀提前水解,使得分析结果偏低;残余酸中和不完全又会导致测定结果偏高[11]。
2.6 指示剂的选择
氟硅酸钾水解生成的两种酸的电离常数相差较大,氢氟酸是一元弱酸,其电离常数K(HF)=6.6×10-4,硅酸是二元弱酸,其电离常数K(H2SiO3)=1×10-9,由于K(HF)/K(H2SiO3)>105,可以进行分步滴定。而氢氧化钠滴定溶液为强碱滴混合弱酸,氢氟酸首先被滴定,当超过突越范围后部分硅酸被滴定[12]。为防止硅酸分解被氢氧化钠滴定,需控制滴定终点pH为7.5~8.0,否则会导致结果偏高。选择酚酞、硝氮黄、溴麝香草酚蓝、溴麝香草酚蓝-酚红等4种指示剂对GBW(E)070102萤石标 准物 质[w(SiO2)=18.04%]进行指示剂试验,结果见表3。

表3 不同指示剂对GBW(E)070102萤石标准物质测定结果的影响Table 3 Effect of different indicators on the determination result of GBW(E)070102 fluorite standard substance
实验中发现,使用酚酞指示剂滴定时,终点拖得太长,不易掌握且测定结果偏高;使用溴麝香草酚蓝指示剂滴定时,终点变色较迟缓,测定结果偏高;使用硝氮黄和溴麝香草酚蓝-酚红混合指示剂滴定时,终点变色敏锐,测定结果与标准物质参考值更为接近。因此,选择溴麝香草酚蓝-酚红指示剂滴定,将pH控制在7.5左右,滴定终点时可由黄色突越至浅紫色。
2.7 共存元素的干扰及消除
铝和钛是氟硅酸钾滴定法测定二氧化硅的主要干扰元素。当试样中铝、钛含量较高时,在氟硅酸钾沉淀过程中,铝、钛易生成相应的氟铝酸钾和氟钛酸钾夹杂在氟硅酸钾沉淀中,并在沸水加入后水解生成氢氟酸,使分析结果偏高。通常在沉淀前添加H2O2或用草酸钾代替氯化钾作沉淀剂使其生成可溶性络合物,消除其影响[13]。另外,由于氟铝酸钾和氟钛酸钾溶解度在硝酸中比在盐酸中大,采用硝酸作为消解酸也有利于减少铝和钛的干扰。
3 样品分析
3.1 精密度试验
对两个不同二氧化硅含量的粗制氟化钠样品按照实验方法分别进行了8次平行测定,进行精密度考察,结果见表4。由表4可知,在实验条件下试样分析结果相对标准偏差小于1%,方法精密度良好。

表4 方法精密度实验结果Table 4 Experiment result of precision of the method
3.2 准确度试验
目前粗制氟化钠暂无国家相应标准物质,对1号氟化钠粗制样品进行加标回收试验,结果见表5。由表5可知,二氧化硅的加标回收率为99.15%~100.63%,说明该方法具有较好的准确度。

表5 加标回收实验结果Table 5 Experiment result of recovery of standard addition
3.3 不同测定方法结果对照
按照实验方法测定了两个不同的粗制氟化钠样品,并与传统高温碱熔法测定结果进行比较,结果见表6。结果表明,该方法测试时间与传统高温碱熔法相比大大减少,而且测定结果相符,进一步说明该方法准确度较好,满足测定要求。

表6 不同测定方法结果对照Table 6 Comparison results of different methods
4 结语
提出了采用硝酸-氢氟酸混合酸作为消解溶剂,通过微波消解技术对粗制氟化钠样品进行前处理,并用氟硅酸钾滴定法测定其二氧化硅含量的方法。通过试验,选择了合适的消解酸体系,采用饱和氯化钾溶液取代固体氯化钾作为沉淀剂并确定了其用量,分析了沉淀温度、沉淀放置时间、沉淀洗涤和中和等条件对测定结果的影响,采用溴麝香草酚蓝-酚红混合指示剂滴定,终点变色敏锐。该方法应用于粗制氟化钠产品中二氧化硅含量的测定,加标回收率为99.15%~100.63%,相对标准偏差(RSD,n=8)小于1%,与传统高温碱熔法测定结果相符,方法准确度和精密度较好。
