增生性糖尿病视网膜病变患眼玻璃体切除手术后玻璃体再积血的临床特征分析
2021-09-06冯姝颖解正高杨婉笛华欣
冯姝颖 解正高 杨婉笛 华欣
经睫状体扁平部玻璃体切除术(pars plana vitrectomy,PPV)是治疗继发于增生性糖尿病视网膜病变(proliferative diabetic retinopathy,PDR)的玻璃体积血(vitreous hemorrhage,VH)和(或)牵拉性视网膜脱离(tractional retinal detachment ,TRD)的标准和有效手术方式。尽管PPV治疗PDR成功率很高,但手术并发症如术后玻璃体再积血(postoperative vitreous hemorrhage,PVH)、新生血管性青光眼和TRD等,通常会导致不良的视力预后[1]。PVH是PDR术后常见的并发症之一,影响术后视力恢复,部分患者需要二次玻璃体视网膜手术[2]。本研究观察并分析PDR患眼PPV术后玻璃体再积血的临床特征,并分析术后玻璃体再积血的全身与眼部危险因素,为减少术后PVH的发生提供思路。
资料与方法
一、对象
回顾性病例研究。2015年12月至2018年12月在苏北人民医院确诊为PDR并行PPV治疗的291例(353只眼)患者纳入本研究,其中男性138例(166只眼,47.03%),女性153例(187只眼,52.97%),年龄21~79岁,平均(52.40±9.59)岁。纳入标准:(1)符合PDR的诊断标准;(2)持续不吸收的VH超过1个月;(3)发生TRD和(或)纤维血管增生(fibrovascular proliferation,FVP)。除外既往曾行玻璃体视网膜手术者以及合并视网膜静脉阻塞、年龄相关性黄斑变性等其他眼底疾病者。
记录患者术前全身及眼部情况。糖尿病(diabetes mellitus,DM)病程0.5~30年,平均(11.53±6.43)年。合并肾损伤者(80只眼,22.66%),合并高血压病者(168只眼,47.59%),合并血管疾病者(204只眼,57.79%)。既往行全视网膜激光光凝(pan retinal photocoagulation,PRP)者(144只眼,40.79%),玻璃体切除术前行玻璃体腔注射抗血管内皮生长因子(vascular endothelial growth factor,VEGF)药物者(293只眼,83.00%)。患眼均行最佳矫正视力(best corrected visual acuity,BCVA)、眼压、裂隙灯显微镜、眼底彩色照相以及B型超声检查。根据我国1984年DR分期标准对PDR进行分期。患眼BCVA为光感至0.5,其中光感者20只眼,手动者115只眼,指数者145只眼,0.01~0.1者43只眼,>0.1者30只眼。
二、方法
所有患者均接受标准23G PPV,手术由同一位具有丰富玻璃体视网膜手术经验的医生完成,手术中彻底剥除增生膜、充分电凝止血,同时完成视网膜激光光凝。术中因晶状体混浊而联合白内障切除术者(66只眼,18.70%),术中发现玻璃体腔增生膜形成而未合并视网膜脱离者(118只眼,33.43%),合并视网膜脱离者(154只眼,43.63%)。根据术中视网膜脱离程度、是否合并医源性裂孔、激光数量及全身状况等综合考虑选择填充物,其中硅油填充者(195只眼,55.24%),空气填充者(137只眼,38.81%),留置灌注液者(21只眼,5.95%)。硅油填充者手术后3~6个月行硅油取出手术。
PVH是指PPV术后再次积血导致视力下降、间接检眼镜下视网膜细节不能窥清,手术后第1天积血未吸收即手术后持续积血者被排除。根据是否出现PVH,将患者分为PVH组和无PVH 组。根据PVH出现的时间,将术后1个月内出现的玻璃体出血纳入早期PVH组,1个月后出现的玻璃体出血纳入晚期PVH组[1]。
三、统计学分析方法
采用SPSS23.0软件行统计学分析,对年龄、糖尿病病程、手术时长采用独立样本t检验,对性别、是否合并肾损伤、是否合并高血压、是否合并血管疾病、是否合并虹膜新生血管、术前是否行抗VEGF治疗、眼内填充物、是否联合白内障手术、术中并发症采用χ2检验,对术前PDR分期、术前是否行视网膜激光、术中视网膜情况采用非参数检验(Mann-WhitneyU检验),分析评估全身、眼部和手术因素对PVH的影响。根据单因素分析结果,(P<0.05)为差异有统计学意义;将(P<0.2)的变量纳入二分类logistics回归分析,(P<0.05)为差异有统计学意义。
结 果
353只眼中,发生PVH组有(28只眼,7.93%),未发生PVH组有(325只眼,92.07%),将PVH组与未发生PVH组进行单因素分析,其中性别(P=0.742),眼别(P=0.343)、年龄(P=0.355),DM病程(P=0.623),合并肾损伤(P=0.115),合并高血压(P=0.898),合并血管疾病(P=0.261)等全身情况差异无统计学意义(表1)。术前PDR分期(P=0.519),术前合并NVI(P=1.000),术前进行PRP情况(P=0.094),术前抗VEGF治疗(P=0.689)等术前眼部情况差异无统计学意义(表2)。术中视网膜情况(P=0.524)、眼内填充物(P=0.271)、联合白内障手术(P=0.259)、术中并发症(P=1.000)等术中情况差异无统计学意义(表3)。将(P<0.2)的变量如术前行视网膜激光光凝术(P=0.094)、合并肾损伤(P=0.115)、术中视网膜情况(P=0.524),眼内填充物(P=0.271)纳入二分类logistics回归分析,术前行全视网膜激光光凝术(P=0.034,OR=0.267)有统计学意义(表4)。
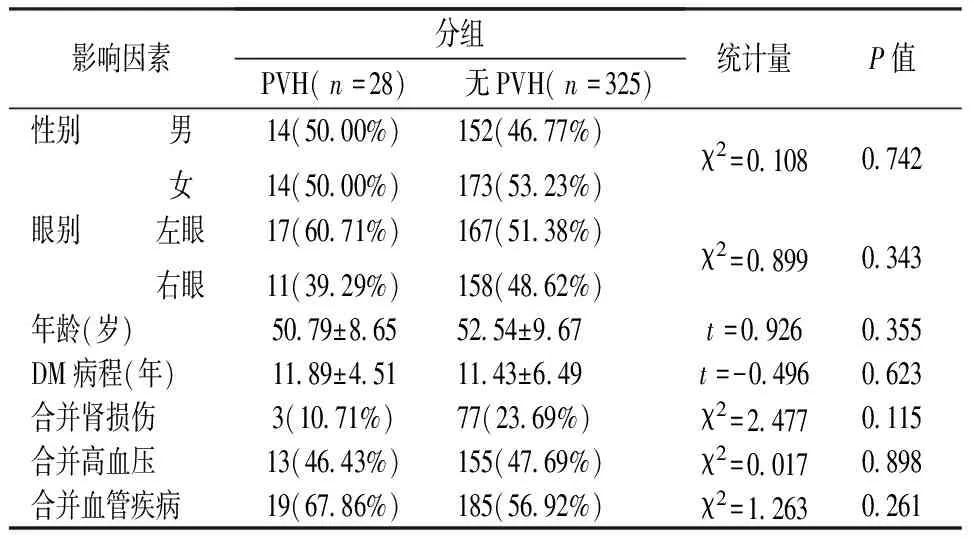
表1 PVH组与无PVH组术前全身情况对比
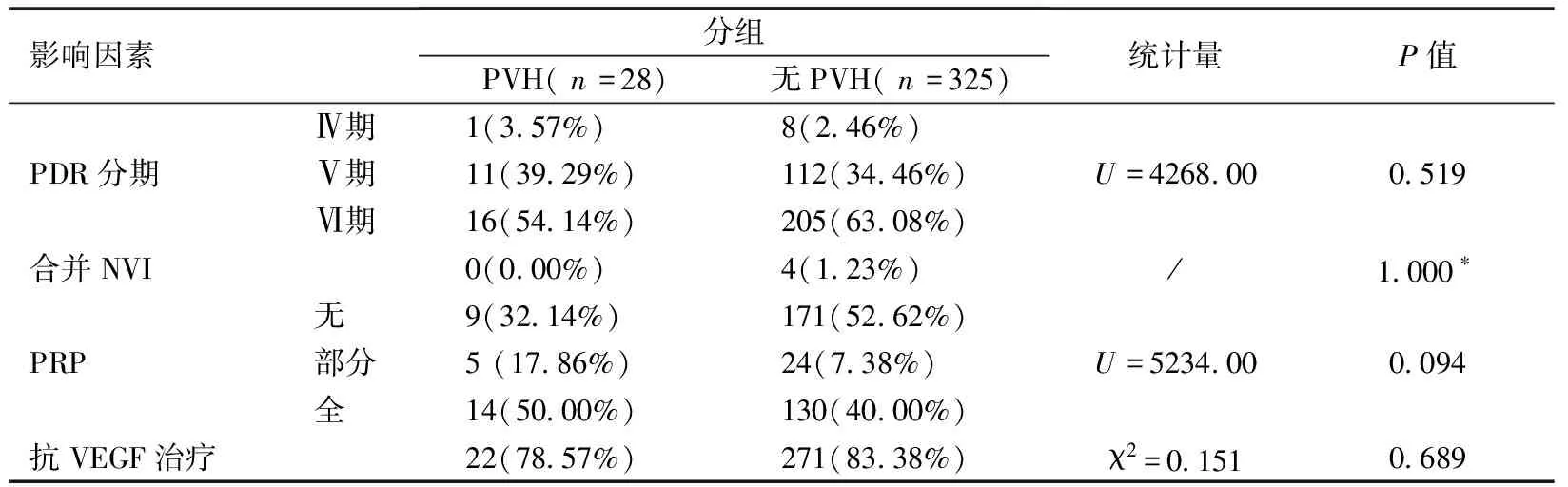
表2 PVH组与无PVH组术前眼部情况对比

表3 PVH组与无PVH组术中情况对比

表4 PVH的logistic回归分析
讨 论
糖尿病视网膜病变(diabetic retinopathy,DR)是工作年龄人群第一位的致盲疾病,增生期进展性DR的玻璃体手术的适应证为不吸收的玻璃体积血、增生性DR纤维增生膜、牵引性视网膜脱离等[3]。PVH是PDR术后常见的并发症,严重影响术后视力恢复,甚至可能需要二次玻璃体视网膜手术。根据PVH的发生时间,可分为早期PVH(PPV术后1个月内发生)和晚期PVH(PPV术后1个月至半年内发生)。造成PVH的原因包括玻璃体基底部残余血凝块出血、残余纤维血管组织出血和巩膜切口处的新生血管形成,因此,玻璃体腔填充长效气体预防出血、预防性的周边视网膜冷冻特别是巩膜切口处的冷冻、玻璃体腔注射抗VEGF药物和(或)曲安奈德(triamcinolone acetonide,TA)等方法早已应用于降低PVH的发生[2]。既往研究报道,DR患者PPV术后玻璃体积血的发生率为5%~45%[4],这与本研究中(28只眼,7.93%)相符。同时,PVH的发生也与术前全身及眼部因素、术中情况等相关。
赵通等[5]的研究显示,年龄、高血压病史、术前存在NVI、术前HbA1c水平高与PDR患者PPV联合硅油填充术后早期出血相关。Sato等[4]认为,晚期PVH患者的糖化血红蛋白水平明显高于非晚期PVH患者,因高糖化血红蛋白水平的患者可能更易产生新生血管,从而导致晚期PVH。但也有研究认为,大多数全身情况并不影响PVH的发生[6,7]。本研究显示,患者术前全身情况如性别、年龄、DM病程、是否合并肾损伤、是否合并高血压、是否合并血管疾病与是否发生PVH的发生无明显相关性。我们认为,这可能与本研究中PVH组样本量较小相关,而无法提示全身因素与发生PVH的相关性。
楚艳华等[6]发现, PVH的发生与眼底病变严重程度密切相关,因为术前合并TRD、FVP以及接受抗VEGF药物治疗等因素均与PDR的活跃程度相关,而这些在手术时可能更易残余玻璃体后皮质及新生血管膜,从而导致PVH。他们认为,手术中应重点关注残存或再生的纤维血管膜。高韶晖等[7]的研究显示,术中视盘新生血管(disc neovascularization,NVD)出血是PVH发生的危险因素。Sato等[4]认为,NVD是早期PVH的预测因素,NVD术中无法有效止血可能是PVH发生的原因,同时,重度PDR患者更易发生早期PVH,他们认为,早期PVH可能与玻璃体基底部和(或)视网膜表面残余血凝块出血有关,也可能与视盘新生血管出血有关。但本研究中,术前眼部情况如术前PDR分期、术前合并NVI差异无统计学意义,我们认为,术中尽可能完全切除积血、彻底剥除增生膜、充分电凝止血及完成全视网膜激光光凝可以减小术前不同眼部情况造成PVH发生的差异。然而,本研究发现,术前行视网膜激光光凝术可减少PVH的发生,这与Khuthaila等[8]的研究结果类似。他们发现,术前未行PRP的患者,发生PVH的概率是行PRP患者的二倍,因为术前PRP可以导致新生血管的消退,从而降低术中和术后出血的风险。我们认为,术前进行视网膜激光光凝术可以降低眼内VEGF水平,减少PVH的发生。因此,尽管部分患者因术前VH而无法完成PRP,也应尽可能行视网膜激光光凝术,同时在术中完善PRP。Wakabayashi等[1]的研究认为,眼内VEGF水平增高与晚期PVH相关,术前玻璃体腔高VEGF水平会导致术后产生更多VEGF,从而导致更广泛的新生血管膜形成而造成PVH。Comyn等[9]发现,术前进行玻璃体内注射雷珠单克隆抗体可以减少PVH。本研究发现,术前行抗VEGF治疗对PVH的发生差异无统计学意义。由于本研究为回顾性研究,我们对于术前较为严重的PDR均行抗VEGF治疗,因此术前行抗VEGF治疗存在人为选择治疗方案造成的偏倚,因此术前行抗VEGF治疗对PVH的发生是否有影响需要未来更合理的前瞻性研究。
Sato等[4]的研究显示,早期PVH与术中视网膜裂孔相关,同时,早期PVH患者手术时间更长。他们认为,医源性裂孔常常发生在玻璃体腔有着广泛形成的致密纤维血管膜眼中,且与视网膜粘连紧密,这也说明了重度PDR患者易发生PVH。Khuthaila等[8]的研究发现,有晶状体眼患者更易发生PVH,这可能是由于担心晶状体受损而未完全切除周边部玻璃体,导致术后玻璃体基底部残余血凝块出血。本研究发现,术中视网膜情况、术中联合白内障手术、术中出现并发症等术中情况与PVH的发生无明显关联。我们认为,由于发生PVH组样本量过小,一些因素的相关性在本研究中不一定能完全显现。Balakrishnan等[10]的认为,术中填充物的选择与PVH的发生无明显关联。这与本研究结果相符,硅油填充可能有助于视网膜的解剖复位以及对VEGF形成屏障作用,但随着PPV手术的进步,在非接触广角镜的帮助及良好的巩膜顶压下,基底部玻璃体清除更加彻底,因而对于填充物的选择可能比过去更加灵活。
本研究结果显示,术前行视网膜激光光凝术可减少PVH的发生,因此,术前应尽可能完成PRP,同时在术中完善PRP。由于本研究为回顾性研究,存在着人为选择治疗方案如术前抗VEGF治疗等对结果造成的偏倚,对PVH影响因素的分析存在一定局限性。同时,由于本研究样本量较小,未对早期PVH与晚期PVH进行进一步的分析,有待今后更为完善的大样本前瞻性研究。
