RP-HPLC法测定银菊感冒胶囊中氨基比林的含量
2021-09-05王喆朱正华张馨
王喆 朱正华 张馨
【摘 要】 目的:建立高效液相色谱法测定银菊感冒胶囊中氨基比林含量的方法。方法:色谱柱采用依利特Hypersil ODS2 C18(4.6 mm×250 mm,5 μm);流动相为乙腈-0.05 moL/l枸橼酸溶液(用三乙胺调节pH至3.5)(10∶90,V/V);流速为1.0 mL/min;进样量为10 μL;柱温为35℃;检测波长为285 nm。结果:氨基比林浓度在25.71~642.87 μg/mL范围内与峰面积线性关系良好,r=0.9999(n=5),平均回收率为101.3%(RSD为1.3%)。结论:本方法操作简单,结果准确,重复性良好,可用于银菊感冒胶囊中氨基比林的含量测定。
【关键词】 银菊感冒胶囊;氨基比林;反相高效液相色谱法
【中图分类号】R284.1 【文献标志码】 A 【文章编号】1007-8517(2021)15-0032-04
Abstract:Objective To establish a HPLC method for the determination of aminopyrine in Yinjuganmao capsules.Method The chromatographic column was Elite HYPERSIL ODS C18(4.6 mm×250 mm,5 μm),The mobile phase is acetonitrile -0.05mol/l citric acid soiution(adjust pH to 3.5 with triethylamine)(10∶90,V/V),t the flow rate was 1.0 ml/min,the injection volume was 10 μL,the column temperature was 35 ℃,and the detection wavelength was set at 285nm. Results The linear range of bergenin were 25.71~642.87 μg/mL(r=0.9999,n=5)with an average recovery of 101.3%(RSD=1.3%).Conclusions The method is simple,the result is accurate and reproducible.It can be used for the determination of aminopyrine in Yin Ju cold capsules.
Keywords:Yin Ju Cold Capsules; Aminopyrine; RP-HPLC
银菊感冒胶囊是由曲靖市中医医院研制的制剂,其主要成分为金银花、菊花、射干、氨基比林、马来酸氯苯那敏等,具清热解毒、解热镇痛的功效,用于治疗感冒、发烧、头痛、咽喉肿痛等。氨基比林属于吡唑酮类解热镇痛药,具有较强的解热镇痛效果,药效缓慢而持久;同时又具有一定的抗炎作用,多用于发热头痛、关节痛、神经痛、痛经及活动性风湿症等;但由于氨基比林能引起骨髓抑制,并可产生亚硝胺致癌物质,因此临床领域中单用制剂已被淘汰,而现在临床用药剂型一般为片剂、注射剂和复方制剂[1]。银菊感冒胶囊现行质量标准中尚未建立氨基比林的质量控制方法,为更有效控制银菊感冒胶囊的质量,本实验以氨基比林为定量控制指标,采用反向高效液相色谱法对氨基比林进行含量测定,并根据《中国药典》2015年版四部通则9101药品质量标准分析方法验证指导原则[2]的要求进行分析方法验证,以期为银菊感冒胶囊中氨基比林的质量控制寻找准确可靠且简便易行的方法。
1 仪器与试药
1.1 仪器 岛津LC40型高效液相色谱仪(配置LC-40DXR系列四元泵,SPD-M40检测器,CTO-40S柱温箱,SIL-40XR自动进样器);双频数控超声清洗器(KQ-300UDB型,购自昆山市超声仪器有限公司);电子天平(METTLE MS205DU,购自上海METTLER TOLEDO);Millipore超纯水機(德国默克集团)。
1.2 试药 氨基比林对照品(来源:中国食品药品检定研究院,批号:100503-201803,供含量测定用,含量以99.7%计);乙腈为色谱纯,德国默克公司提供;水为纯化水及超纯水,由Millipore超纯水机制备;银菊感冒胶囊由曲靖市中医医院制剂室提供,批号分别为:200102、200501、200802。
2 方法与结果
2.1 色谱条件 色谱柱为依利特Hypersil ODS2 C18柱(4.6 mm×250 mm,5 μm);流动相为乙腈-0.05 moL/l枸橼酸溶液(用三乙胺调节pH至3.5)(10∶90,V/V);流速为1.0 mL/min;进样量为10 μL;柱温为35 ℃;检测波长为285 nm。
2.2 溶液制备
2.2.1 供试品溶液制备 取银菊感冒胶囊内容物适量,混匀,取约0.1 g,精密称定,置25 mL容量瓶中,加入纯化水适量,超声(频率:45KHz;功率:300 W)30 min,取出,放冷,用纯化水稀释至刻度,摇匀,滤过,精密量取续滤液5 mL至50 mL容量瓶中,用纯化水稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液。
2.2.2 对照品溶液制备 精密称取氨基比林对照品16.12 mg,置25 mL容量瓶中,加水溶解并稀释至刻度,即得浓度为642.87 μg/mL的氨基比林对照品储备溶液。取储备液2.5 mL,置10 mL容量瓶中,用纯化水稀释至刻度,即得浓度为160.72 μg/mL的氨基比林对照品溶液。
2.2.3 阴性样品溶液的制备 按银菊感冒胶囊处方,分别称取除氨基比林以外的其他原辅料,按照银菊感冒胶囊制备工艺制作不含氨基比林成分的阴性样品,并按供试品溶液制备方法制备阴性样品溶液。
2.3 方法学考察
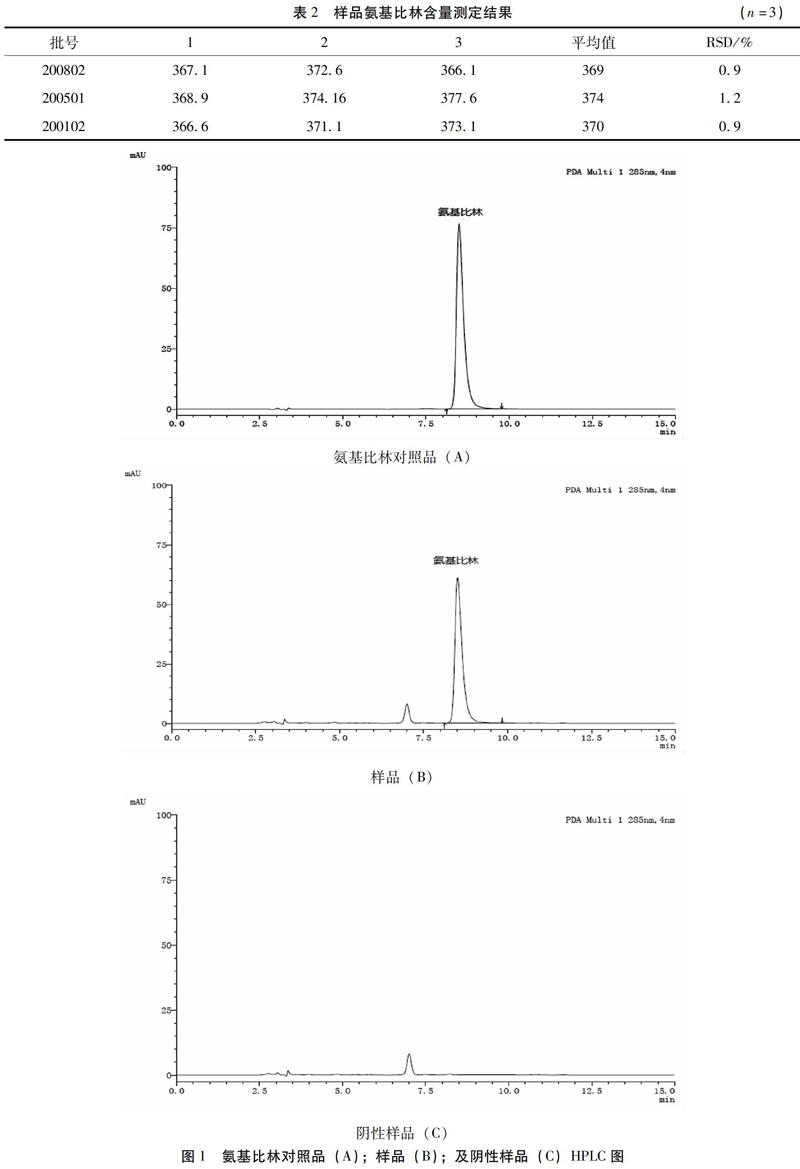
2.3.1 专属性试验 分别取2.2项下的供试品溶液、对照品溶液和阴性样品溶液, 按2.1项下色谱条件进样分析,记录色谱图,结果见图1(色谱图中在氨基比林相应出峰位置未出现干扰峰)。
2.3.2 線性关系考察 分别精密吸取浓度为642.87 μg/mL氨基比林对照品储备溶液适量,加水稀释制成含氨基比林分别为25.71、80.36、160.72、321.43、642.87 μg/mL 的系列对照品溶液。按2.1项下色谱条件进样分析,记录色谱图,以氨基比林对照品浓度为横坐标(X),峰面积为纵坐标(Y)绘制标准曲线,得回归方程为Y=5074.69X+8180.22(r=0.9999,n=5)。结果表明:氨基比林浓度在25.71~642.87 μg/mL范围内与峰面积具有良好线性关系。
2.3.3 精密度试验 精密吸取同一氨基比林对照品溶液(浓度为160.72 μg/mL)按2.1项下色谱条件连续进样6次,记录峰面积,峰面积值的RSD为0.5%,仪器精密度良好。
2.3.4 稳定性试验 取同一份供试品溶液(批号200802),分别于常温下放置0、2、4、8、12、24、48 h后进样分析,记录峰面积。结果的RSD为1.1%(n=7)。表明供试品溶液于室温下放置48 h基本稳定。
2.3.5 重复性试验 取同一批次银菊感冒胶囊(批号200802)20粒,混匀,按2.2.1项下的方法,分别精密称取6份,制备供试品溶液,按2.1 项下色谱条件进样测定,考察方法的重复性。结果的RSD为0.6%(n=6)。
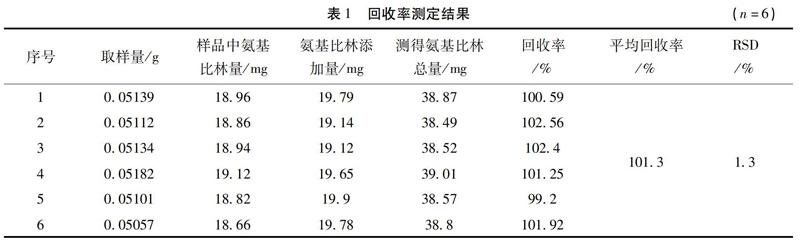
2.3.6 回收率试验 分别取已知含量的同一批银菊感冒胶囊(批号200802)约0.05 g,精密称定,共6份,分别精密加入对照品约19 mg, 置25 mL容量瓶中,按2.2.1项下的方法处理,制备供试品溶液,分别测定,计算回收率。平均回收率为101.3%,RSD为1.3%。见表1。
2.4 样品含量测定 分别取不同批号的供试品3批按2.2.1项下的方法处理,制备相应的供试品溶液,并根据2.1项下色谱条件依次进样测定,并记录峰面积,以外标法计算各供试品中的氨基比林含量。结果见表2。
3 讨论
3.1 流动相的选择 本试验首先试用文献[3]中甲醇-水(45:55,V/V)作为流动相测定,结果发现对照品及样品中氨基比林的峰形拖尾严重,后又参考文献[4-6]对流动相的比例进行调整,结果峰型仍然不太理想,最后试用文献[7]中的乙腈-0.05moL/l枸橼酸溶液(三乙胺调节pH至3.5)(10∶90,V/V)作为流动相,结果能得到对称性较好的氨基比林峰,并且样品中氨基比林峰与其它杂质峰的分离符合要求,故选用乙腈-0.05mol/l枸橼酸溶液(三乙胺调节pH至3.5)(10∶90,V/V)为流动相。
3.2 提取方式的选择 ①提取溶剂的确定:在查询氨基比林溶解度时发现氨基比林在水和乙醚中溶解[8],故选用纯化水作为提取溶剂;②提取方式的确定:通过查阅文献[3-5]发现,不同的文献提取方式各有不同,主要为直接溶解,振摇提取及超声提取,通过试验发现超声提取效果较好,且加标回收率较高,故选用超声提取。③超声时间的确定:精密称取样品(批号200802)4份,每份约0.1 g,置25 mL量瓶中,加入纯化水适量,分别超声(频率:45 KHz;功率:300 W)处理10 min、20 min、30 min、40 min后取出,依法操作测定氨基比林含量,结果显示超声20 min后, 氨基比林含量基本不再改变,证明样品超声处理20 min后,能将样品中的氨基比林提取完全,所以超声(频率:45 KHz;功率:300 W)时间确定为30 min。
本实验所建立的氨基比林含量测定方法准确、快速、简便可靠,结果稳定,可用于银菊感冒胶囊中氨基比林的含量测定。
参考文献
[1]温敏,刘景彬,刘永臣.氨基比林原料药含量测定方法的研究[J].中国现代药物应用,2012,6(15):1-3.
[2]国家药典委员会.中华人民共和国药典(四部)[M].北京:中国医药科技出版社,2015:374-377.
[3]国家药典委员会.国家食品药品监督管理局国家药品标准化学药品地方标准上升国家标准第十四册[M].北京:中国医药科技出版社.2003:14.
[4]谢桂芬,李照宏,李应芬.HPLC法测定金菊感冒胶囊中氨基比林的含量[J].中国民族民间医药,2008,17(12):22-23.
[5]刘晓哲.HPLC法同时测定酚氨咖敏颗粒中三组分的含量[J].药物分析杂志,2007,27(9):1487-1489.
[6]万莉.HPLC法测定复方金刚烷胺氨基比林片中氨基比林的含量[J].中国药师,2007,10(10):1001-1002.
[7]闫小峰,孙志文.高效液相色谱法测定安痛定注射液中氨基比林和安替比林含量[J].中国兽医杂志,2011,47(2):77-79.
[8]中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准-化学药品及制剂第一册[M].北京:人民卫生出版社,1989:79-123.
(收稿日期:2020-12-17 编辑:程鹏飞)
