HPLC法同时测定参莲颗粒中三种姜黄素的含量
2021-09-05张小折叶晓娅
张小折 叶晓娅
【摘 要】 目的:建立参莲颗粒中姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素的含量测定方法。方法:色谱柱,Agilent SB-C18色谱柱(4.6 mm×250 mm,5 μm),流动相甲醇-3%冰醋酸(35∶65,v/v);流速1.0 mL·min-1;柱温30℃,检测波长418 nm,进样量:10 μL。结果:参莲颗粒中姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素的进样质量分别在39.17 ~1530.0 ng(r=0.999 9)、48.90~1910.0 ng(r=1.000 0)、44.65~1744.0 ng(r=1.000 0)范围内线性良好,平均回收率分别为97.86%(RSD=1.01%)、95.46%(RSD=1.07%)和99.69%(RSD=0.46%)。结论:该方法经方法学验证具有操作简单、分析速度快,准确度高的优点,可以用于参莲颗粒中三种姜黄素类成分的含量测定。
【关键词】 参莲颗粒;姜黄素;高效液相色谱;含量测定;质量控制
【中图分类号】R284.1 【文献标志码】 A 【文章编号】1007-8517(2021)15-0023-04
Abstract:Objective To propose as method for determination of curcumin, demethoxycurcumin and bisdemethoxycurcumin in Shenlian granules by HPLC method. Methods The Agilent-C18 (4.6 mm×250 mm, 5 μm) chromatography column was performed for separation with methanol(A)–3% HAc(B) as the mobile phase (35∶65, V/V). The flow rate was 1.0 mL·min-1, detection wavelength was set at 412 nm, column temperature was maintained at 30℃ and the injection volume was 10 μL. Results The curcumin, demethoxycurcumin, and bisdemethoxycurcumin had good linearity with the range of 39.17 ~1530.0 ng(r=0.999 9), 48.90~1910.0 ng(r=1.000 0) and 44.65~1744.0 ng(r=1.000 0), respectively. The average recoveries were 97.86%(RSD=1.01%), 95.46%(RSD=1.07%) and 99.69%(RSD=0.46%), respectively. Conclusion The established method was verified by methodology which has a good advantage of simple operation, analysis rapidly and high accuracy which can be used for the determination of curcumin, demethoxycurcumin, and bisdemethoxycurcumin in Shenlian granules by HPLC.
Keywords:Shenlian Granules; Curcumin; HPLC; Content Determination; Quality Control
參莲颗粒是由苦参、山豆根、防己、三棱、莪术、丹参、补骨脂、苦杏仁、乌梅和白扁豆等七位药组成,具有活血化瘀、清热解毒和软坚散结的作用,临床主要用于气血瘀滞、热毒内阻而导致的中晚期肺癌和胃癌病患者[1]。方中三棱具有消积止痛、破血行气的作用[2],莪术具有行气破血、消积止痛的功效[3],二者合用共同为方中君药,有报道[4-5]称莪术的主要成分为姜黄素类和挥发油,姜黄素类是其主要活性成分,主要有姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素[6-7],这三种化合物结构相似,均具有抗动脉粥样硬化、抗癌、抗氧化、抗诱变和清除自由基的作用[8-10],且有报道称去甲氧基姜黄素可以抑制TPA (12—O—tetradecanoyl phorbol—13-acetate)引起的癌细胞增生以及多种癌细胞[11],作用大于其它两种姜黄素类,由于参莲颗粒主要是治疗癌症等症状,根据刘昌孝院士提出的中药质量标志物(Q-Marker)[12]的概念,把能够作为与中药功能主治和反映药品安全性和有效性的活性成分作为中药质量标志物从而对其进行质量控制。因此姜黄素类成分是其抗癌作用的有效活性成分,目前标准中未有对其进行控制,鉴于此本实验参考莪术以及含有姜黄类成分的中成药[13-15]建立参莲颗粒中姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素三种成分的含量测定,从而为改进和提高参莲颗粒的质量标准提供实验参考。
1 仪器与试药
1.1 仪器 高效液相色谱仪Waters e2695(美国Waters仪器公司);Empower 3 工作站;XPE204型十万分之一电子天平(瑞士Mettler ToleDo仪器公司);KQ-500DE型双频数控超声波清洗器(江苏昆山超声仪器有限公司)。Mili-Q超纯水机(美国密理博公司)。
1.2 试药 参莲颗粒是由市场所购,规格:4.5 g/袋);批号分别标记为1#、2#和3#,20180516,20190706,对照品:姜黄素(批号:110823-201706,含量98.9%),去甲氧基姜黄素(批号:112003-201501,含量98.5%、双去甲氧基姜黄素(批号:112004-201501,含量95.0%),对照品购于中国食品药品检定研究院,甲醇为色谱纯(美国Merck公司),冰醋酸为分析纯(天津科密欧化学试剂公司),水为超纯水。
2 方法与结果
2.1 色谱条件 色谱柱:Agilent SB-C18色谱柱(4.6 mm×250 mm,5 μm),流动相:(A)甲醇-3%冰醋酸(35∶65,v/v);流速1.0 mL·min-1;检测波长418 nm,柱温30 ℃,进样量:10 μL。
2.2 对照品溶液的配制 精密称取用五氧化二磷干燥12h后的姜黄素5.36 mg、去甲氧基姜黄素6.12 mg、双去甲氧基姜黄素5.58 mg分别置3个25 mL容量瓶中,加甲醇定容稀释至刻度,分别作为对照品储备溶液,然后分别精密吸取上述姜黄素对照品储备溶液2 mL,去甲氧基姜黄素和双去甲氧基姜黄素各1 mL置同一20 mL容量瓶中,加甲醇溶解并稀释至刻度,作为对照品混合溶液(每1 mL含姜黄素21.44 μg、去甲氧基姜黄素12.24 μg、双去甲氧基姜黄素11.16 μg)。
2.3 供试品溶液的配制 取批号为1#的参莲灵颗粉末约5.0 g,精密称定,平行制备2份样品,然后精密加入甲醇25 mL,称定重量,然后超声(频率40 kHz,功率300 W)处理30 min,用甲醇补足减失的重量,摇匀,用¢0.45 μm的微孔滤膜滤过,取续滤液作为供试品溶液。
2.4 阴性样品的制备 按照参莲颗粒的质量标准处方量及制备工艺,分别制备缺莪术、三棱药材的阴性样品,作为缺莪术、三棱的参莲阴性样品溶液。
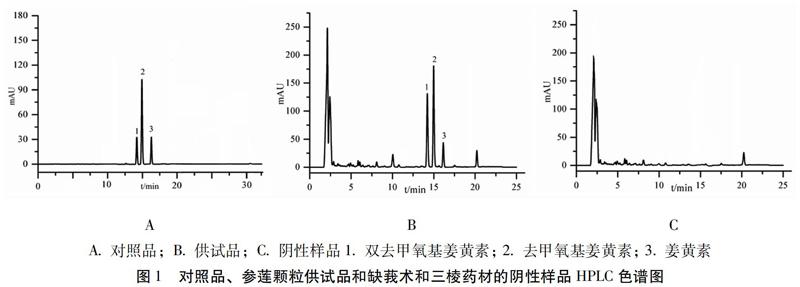
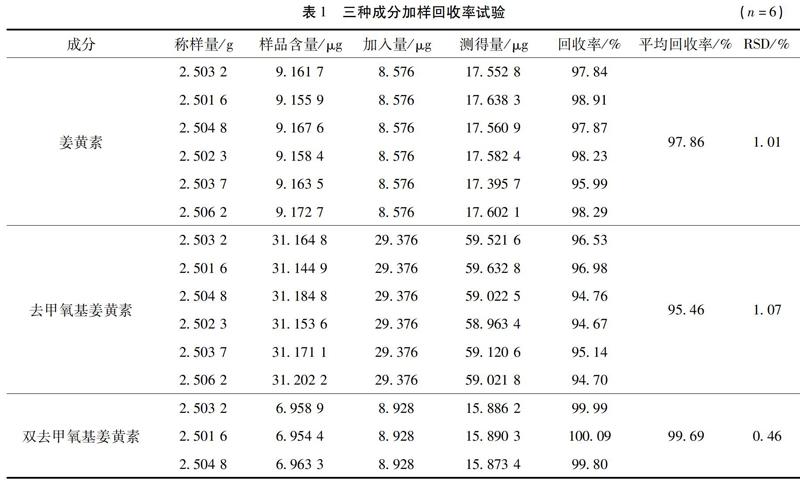
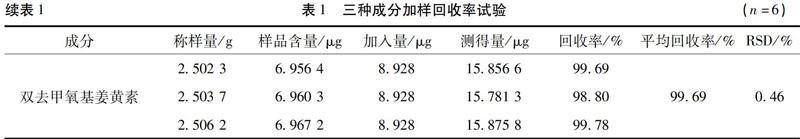
2.5 专属性实验 按照“2.1”项的色谱条件,分别取上述对照品和供试品溶液和阴性样品溶液进行测定,记录色谱图,结果发现阴性样品对姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素的测定无干扰。理论塔板数按姜黄素峰计算不低于5000,分离度均大于1.5,色谱图如图1所示。
2.6 线性关系的考察 精密称取姜黄素7.65 mg、去甲氧基姜黄素9.55 mg、双去甲氧基姜黄素8.72 mg分别置同一50 mL容量瓶中,加甲醇稀释至刻度,作为V号对照品混合溶液,然后采用逐级稀释法,精密吸取V号对照品溶液2 mL置5 mL量瓶中,加甲醇稀释至刻度,作为IV号对照品溶液,精密吸取上述IV号对照品溶液2 mL置5 mL量瓶中,加甲醇稀释至刻度,作为III号对照品溶液,精密吸取上述III号对照品溶液2 mL置5 mL量瓶中,加甲醇稀释至刻度,作为II号对照品溶液,精密吸取II号对照品溶液2 mL置5 mL量瓶中,加甲醇稀释至刻度,作为I号对照品溶液,分别吸取上述I~V号对照品溶液各10 μL,按照“2.1”项下的液相色谱条件进行测定,横坐标(X)为进样量的质量(ng),其相对应的峰面积(Y)为纵坐标,绘制标准工作曲线,进行线性回归,结果三种成分的线性方程如下:姜黄素Y=0.901 1X–3.072 3,r=0.999 9,线性范围为39.17~1530.0 ng;去甲氧基姜黄素Y=0.725 8X-1.108 2,r=1.000 0,线性范围为48.90~1910.0 ng;双去甲氧基姜黄素Y=0.561 9X+2.612 8,r=1.000 0,线性范围为44.65~1744.0 ng。
2.7 精密度試验 分别取“2.6”项下的I号、III号和V号三个不同浓度的对照品溶液,按照“2.1”项下的色谱条件各连续进样6次,进样量10 μL,结果I号对照品中姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素峰面积的RSD分别为1.98%、2.16%、和2.33%;III号对照品中各色谱峰面积的RSD为0.96%、1.12%、和1.07%;V号对照品中各色谱峰面积的RSD为0.35%、0.26%、和0.39%,结果说明该仪器的进样精密度良好。
2.8 稳定性试验 取“2.3”项下的供试品溶液,按照“2.1”项下的液相色谱条件,分别在0、1、2、4、8、12、24 h进行测定,连续考察24 h,记录各个时间的色谱峰面积,结果姜黄素峰面积的RSD分别为2.39%、去甲氧基姜黄素峰面积的RSD为2.72%、双去甲氧基姜黄素峰面积的RSD为2.96%,结果表明该参莲颗粒供试品溶液在24 h内稳定性良好。
2.9 重复性试验 取同一批号1#的参莲颗粒,研细,按照“2.3”项下的制备方法平行制备6份供试品溶液,按照“2.1”项下的液相色谱条件进行测定,结果参莲颗粒中姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素含量平均值为3.66 μg·g-1、12.45 μg·g-1和2.78 μg·g-1,RSD分别为0.86%、1.35%和0.79%,测定结果说明该方法的重复性良好。
2.10 中间精密度试验 在相同实验室,由不同操作者在不同时间、不同仪器,采用上述色谱条件和供试品溶液制备方法对同一批号的参莲颗粒进行测定,结果与重复性项下对比,两位操作者所测值得RSD均小于2.0%,因此表明该方法的中间精密度良好。
2.11 加样回收率试验 精密吸取“2.2”项下的1 mL、姜黄素对照品储备溶液、去甲氧基姜黄素3 mL、双去甲氧基姜黄素1 mL置同一25 mL量瓶中,作为待加混合对照品溶液,然后精密称取已知含量的参莲颗粒2.5 g置三角锥形瓶中,共6份,分别加入上述待加混合对照品溶液各1 mL,然后按照“2.3”项下的制备方法制备样品溶液,“2.1”项下的液相色谱条件进行测定,分别计算姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素的回收率,测定结果见表1。
2.12 样品的测定 取上述市场所购买的3批样品,按照“2.3项”下方法制备供试品溶液,按“2.1”项下的液相色谱条件进行测定,采用外标法计算测定结果。见表2。
3 讨论
3.1 供试品溶液的制备 供试品溶液的提取溶剂分别考察采用甲醇、50%甲醇和乙醇,结果发现甲醇作为提取溶剂时姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素三者含量最高,因此采用甲醇作为提取溶剂,接着考察回流、超声、索氏提取三种方法,结果发现三种提取方法时含量基本一致,无明显差异,由于超声操作简单,故选择超声作为提取方法。然后对时间(20 min、30 min、40 min)、超声功率(200 W、350 W、500 W)进行考察,结果发现当超声30 min,功率350 W为最佳提取工艺,因此选择该方法为供试品溶液的制备方法。
3.2 测定条件的选择 实验首先采用文献报道的270 nm作为检测波长,结果发现三者色谱峰干扰较大,分不开且基线不平稳,然后采用DAD检测器进行检测,发现姜黄素的最大吸收波长为420 nm,去甲氧基姜黄素的最大吸收波长为418 nm、双去甲氧基姜黄素的最大吸收波长为416 nm,由于三者中去甲氧基姜黄素的色谱峰较大,综合考虑,选择418 nm作为三者检测波长,结果发现三者色谱峰形良好,没有干扰,且可以很好的分离。流动相的选择先后采用甲醇—3%醋酸、乙腈—0.1%磷酸缓冲溶液、乙腈—水三者作为流动相,结果发现当甲醇—3%醋酸时三者峰形较好,分离度较高,因此选择甲醇—3%醋酸溶液作为流动相。
3.3 耐用性试验 本实验分别对不同柱温(20 ℃、25 ℃、30 ℃、35 ℃、40 ℃);不同流速(0.8 mL/min、0.9 mL/min、1.0 mL/min、1.1 mL/min、1.2 mL/min);不同流动性比例:甲醇—3%冰醋酸(31∶69)、(33∶67)(35∶65)(37∶63)(39∶61);不同检测波长(414 nm、416 nm、418 nm、420 nm和422 nm);不同色谱柱:Agilent SB-C18(250 mm×4.6 mm, 5 μm)、Waters Symmetry C18(250 mm×4.6 mm, 5 μm)和岛津Shim-Pack VP-ODS液相色谱柱(250mm×4.6 mm, 5 μm),各种条件微小变动下,系统适用性均符合要求,同时分别采用Agilent1260.Waters2695和岛津LC-2030液相色谱仪对同一批样品测定,结果三者测定值RSD<1.5%,因此该方法的耐用性良好。
4 结论
本实验对参莲颗粒中具有药理活性的指标性成分进行检测,在实验中发现姜黄和三棱均含有上述三种姜黄素成分,因此上述三个成分为两种药材的含量之和,且建立的同时测定参莲颗粒中姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素的含量HPLC法,具有分析速度快、灵敏度高、专属性强的优点,可以为该标准中三棱和莪术的质量控制提供一定的依据。
参考文献
[1]陈桂红,黄清松,曾繁涛.参莲颗粒抗突变和抑瘤作用研究[J].中国药房,2007,18(36):2809-2811.
[2]国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2015:31.
[3]陈晓军,韦洁,苏华,等.莪术药理作用的研究新进展[J].药学研究,2018,37(11):49-53,67.
[4]赖艳妮,严一文,徐培平,等.基于系统药理学探索莪术有效成分的药理作用机制[J].中国实验方剂学杂志,2017,23(14):185-190.
[5]冯娅茹,张文婷,李二文,等.三棱化学成分及药理作用研究进展[J].中草药,2017,48(22):4804-4818.
[6]崔语涵,安潇,王海峰,等.姜黄化学成分研究[J].中草药,2016,47(7):1074-1078.
[7]赵承光,梁广,邵丽丽,等.姜黄素类化合物抗炎和细胞保护作用的构效关系研究进展[J].中草药,2008,39(4):619-622.
[8]王玉玲,吴振,张喜轩.姜黄素类化合物的抗肿瘤活性[J].中国医科大学学报,2006,35(4):380-381.
[9]吴杰,李丹,沈秉正,等.姜黄素类化合物的药理活性研究进展[J].中国药师,2013,16(12):1918-1920.
[10]姜黄素类化合物的提取分离鉴定及其与化疗药的协同抗肿瘤作用研究[D].烟台:烟台大学,2009.
[11]苗久旺,荆雪宁,高荧,等.自噬对双去甲氧基姜黄素诱导肝癌HepG2细胞凋亡作用的影响[J].中国实验方剂学杂志,2018,24(17):167-171.
[12]刘昌孝,陈士林,肖小河,等.中药质量标志物(Q-Marker):中药产品质量控制的新概念[J].中草药,2016,47(9):1443-1457.
[13]史晶晶,馮素香,郝蕊,等.姜黄提取物中姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素的含量测定[J].中医学报,2015,30(6):853-855.
[14]李文兵,卢君蓉,胡麟,等.一测多评法测定姜黄中姜黄素、去甲氧基姜黄素和双去甲氧基姜黄素[J].中草药,2017,48(3):573-577.
[15]孙静,孙艳涛,张振秋.中药莪术中姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素的含量测定[J].中国医院药学杂志,2010,30(8):714-716.
(收稿日期:2020-12-24 编辑:程鹏飞)
