盐田卤水小型自然蒸发实验
2021-08-27薛玉婷
薛玉婷


摘 要:通过实验确定霍布逊矿区盐田原卤自然蒸发的结晶析出顺序和光卤石矿物的最佳分离点,获得母液中的KCl质量分数等基础数据,掌握盐田走水路线和各控制点参数。
关键词:原卤;自然蒸发;最佳分离点
1 实验原理
霍布逊矿区盐湖卤水化学类型为氯化物型,从KCl等组分的质量分数来看,属于低钾高钠高镁的卤水。对该类型卤水进行自然蒸发实验,确定盐类结晶析出顺序和光卤石矿物的最佳分离点,获得母液中的KCl质量分数等基础数据[1]。
2 实验目的
为了更好地指导盐田生产,选择合理的固液分离点,对东泵站原卤卤水进行实验室模拟盐田生产小型蒸发实验,用以指导盐田蒸发工作,进一步掌握盐田走水路线和各控制点参数。
3 实验器材
3.1 实验仪器
烧杯,波美计,分析天平,移液管,量瓶,三角瓶,温度计,滴定管,布氏漏斗,电子秤,光度计。
3.2 实验材料
实验所用原卤组分如表1所示。
4 实验方法
本实验将同一组分的原卤卤水分成两组,分别进行蒸发实验。第一组用电子秤准确称取1 218 g原卤,置于 2 000 mL烧杯中;第二组用电子秤准确称取5 000 g原卤,置于5 000 mL烧杯中,静置,在实验室内有自然光照射的地方进行自然蒸发,定时测定卤水温度和密度,观察蒸发过程中原卤中盐类结晶析出的变化,当波美度升至30.5 °Be′时,先称取烧杯内总物料的质量、测量物料温度,然后将烧杯内的物料固液分离,分别称量固液相各自的质量,并对固液相进行化验分析。再依次将波美度控制在31.5、32.5、36.5 °Be′进行固液分离,对固相和液相进行化验分析,计算相图指数,以相图理论为指导,预测结晶路线,探求光卤石矿物的最佳分离点。
5 分析方法
利用光度计测K+、Na+,采用容量法测Mg2+、Ca2+、Cl-。测量结果如表2所示。
6 结果与讨论
6.1 实验1(原卤KCl质量分数为0.73%)结果
1-1样品质量1 218 g,6月15日置于2 000 mL烧杯中,这一阶段气温不断升高,蒸发较快。实验过程中的取样分析结果表明,母液中的NaCl质量分数逐渐降低,KCl、MgCl2、CaCl2的质量分数不断提高,有石盐固体不断析出。6月22日,当波美度为30.0 °Be′、密度为1.250 8 g/mL(25 ℃)时,进行了本组实验的第一次固液分离,分离出固体70 g,主要物质是石盐。通过化学分析得到固相KCl质量分数为0.22%、NaCl质量分数为90.21%、MgCl2质量分数为2.93%、CaCl2质量分数为0.11%。此时母液中的KCl质量分数为1.00%,是原卤的1.37倍,蒸发水分276 g(含少量作业损失),占原卤的23%。
进行了第一次固液分离后,继续进行蒸发,母液组分的变化规律不变。6月25日,当波美度为31.5 °Be′、密度为 1.257 2 g/mL(22 ℃)时,进行第二次固液分离,分离出固体12 g,主要物质还是石盐。通过化学分析得到固相KCl质量分数为0.57%、NaCl质量分数为84.12%、MgCl2质量分数为2.82%、CaCl2质量分数为0.87%。此时母液中的KCl质量分数为1.02%,是原卤的1.4倍,蒸发水分70 g(含少量作业损失),占原卤的5.75%。
继续进行蒸发,6月28日,当波美度为32.5 °Be′、密度为1.280 5 g/mL(22 ℃)时,进行第三次固液分离,分离出固体14 g,主要物质还是石盐。通过化学分析得到固相KCl質量分数为0.50%、NaCl质量分数为87.37%、MgCl2质量分数为3.77%、CaCl2质量分数为1.14%。此时母液中的KCl质量分数为1.10%,是原卤的1.51倍,蒸发水分70 g(含少量作业损失),占原卤的5.75%。
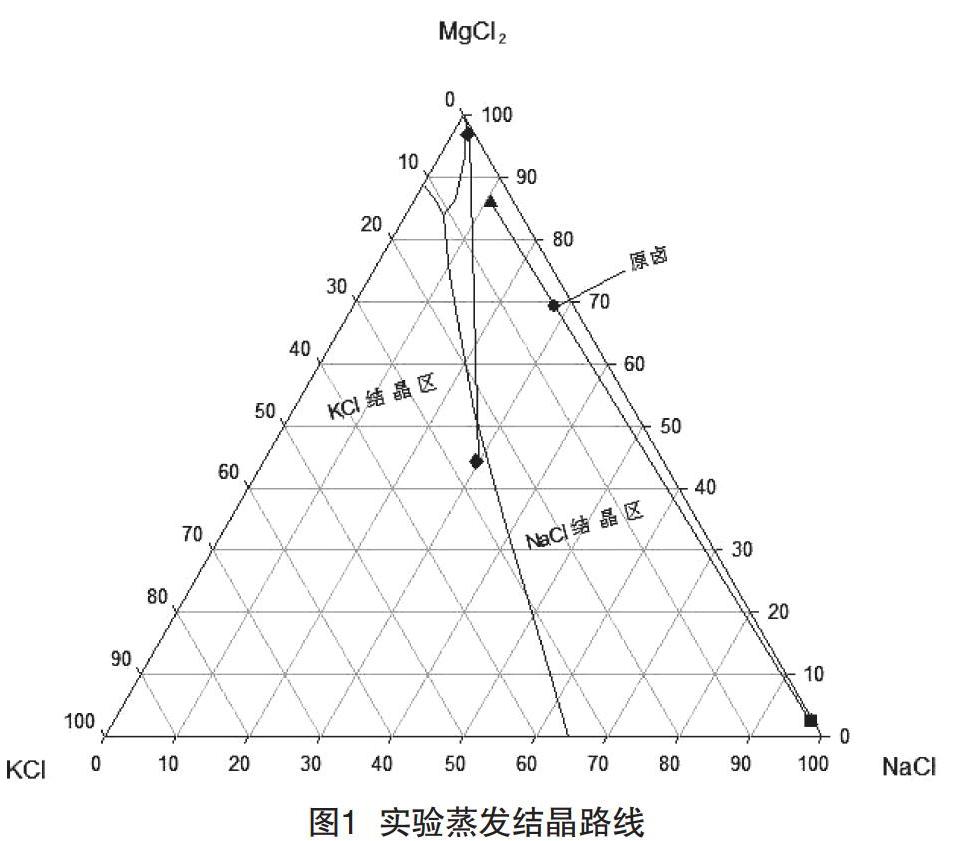
第三次分离后的钾饱和液母液为706 g,3次共分离出石盐96 g,继续蒸发。7月3日,当波美度为34.9 °Be′、密度为 1.309 7 g/mL(25 ℃)时,进行第四次固液分离,得到固体 40 g。通过化学分析得到固相KCl质量分数为16.29%、NaCl质量分数为21.46%、MgCl2质量分数为26.35%、CaCl2质量分数为1.21%,此时样品进入光卤石析出阶段。然后进行下一步蒸发,此时温度升高较快,蒸发量较大。7月5日,当波美度为36.6 °Be′、密度为1.322 2(31 ℃)时,进入老卤阶段,进行第五次固液分离,得到固体12 g,产率较低。通过化学分析得到固相KCl质量分数为12.25%、NaCl质量分数为19.54%、MgCl2质量分数为27.98%、CaCl2质量分数为1.92%。根据第四次和第五次的实验数据,当卤水波美度为34.9 °Be′、密度为1.309 7 g/mL时,光卤石的品质较好,产率较高。随着卤水密度的不断升高,光卤石品质变差,且产率变低,此组实验结束。实验蒸发结晶路线如图1所示。
6.2 实验2(原卤KCl质量分数为0.73%)结果
2-1样品于6月19日置于5 000 mL烧杯中进行自然蒸发,样品重5 000 g。与1-1样品相比,实验方法及实验过程完全相同,蒸发的表面积变大,卤水的深度也增加了,所以蒸发速度较慢。根据监测样本的分析结果,经过17天的蒸发,对本组实验进行了第一次固液分离,固相物为石盐。本组实验共进行了5次固液分离,前3次固液分离共产出石盐374 g,产率为7.48%,同时卤水进入光卤石阶段。实验于7月31日结束,光卤石阶段共进行了两次固液分离。第一次固液分离,产出了固相KCl质量分数为16.71%、NaCl质量分数为18.94%、MgCl2质量分数为26.89%、CaCl2质量分数为1.50%的光卤石178 g,产率为3.6%。第二次固液分离,产出了固相KCl质量分数为14.86%、NaCl质量分数为16.53%、MgCl2质量分数为28.70%、CaCl2质量分数1.36%的光卤石32 g,产率为0.6%。由此可见,当卤水刚进入光卤石阶段时,产出的光卤石品质好、产率高。随着卤水密度的不断增高,光卤石品质变差,且产率变低。
6.3 两组实验分析与讨论
虽然两组实验的蒸发面积和卤水深度不同,但原卤组分完全相同。分析固相石盐和光卤石的产率,1-1样品的固相石盐的产率为7.9%,光卤石的产率为4.3%。2-1样品的固相石盐的产率为7.5%,光卤石的产率为4.2%。由此可见,两组实验的石盐析出阶段较长,且产率较高,光卤石析出阶段较短,相应地产率也较低。
实验表明,在自然蒸发的析盐过程中,可以通过母液的波美度对分离点进行控制,还可以通过卤水表面漂浮的结晶物特征进行控制。根据两组实验化学分析数据,石盐析出阶段较长,不同阶段石盐夹带的KCl质量分数也不同,随着波美度的升高,母液中的KCl质量分数也不断增加,当波美度为32.5 °Be′、密度为1.280 5 g/mL(22 ℃)时,母液中的KCl达到饱和,波美度再升高,母液中的KCl质量分数不断降低,进入光卤石阶段。由表2可知,当波美度为32.5~34.9 °Be′时,形成的光卤石品质好且产率高。当波美度为34.9~36.6 °Be′时,形成的光卤石品质较差,产率也低。盐田生产可根据实验数据,控制最佳的固液分离点:钠盐池卤水波美度应控制在27.0~31.5 °Be′,调节池卤水波美度应控制在31.5~32.5 °Be′,一级矿池卤水波美度应控制在32.5~34.9 °Be′,二级矿池波美度应控制在34.9~36.6 °Be′。
[参考文献]
[1]张兆广,祁艳.察尔汗盐湖低品位卤水自然蒸发试验研究[J].盐湖研究,2006(1):17-23.
