托珠单抗治疗全身型幼年特发性关节炎疗效及安全性分析
2021-08-27蒋新辉邵晓珊李宇红宋锦洪漾谢偲陈双梅陈俊豪贵阳市妇幼保健院贵州贵阳550003
蒋新辉 邵晓珊 李宇红 宋锦 洪漾 谢偲 陈双梅 陈俊豪 (贵阳市妇幼保健院,贵州 贵阳 550003)
全身型幼年特发性关节炎(systemic juvenile idiopathic arthritis, sJIA)是幼年特发性关节炎(juvenile idiopathic arthritis, JIA)的一种亚型,占JIA的10%-20%,任何年龄均可发病,5岁以前略多见。目前认为sJIA是一种多源性自身炎症性疾病,固有免疫免疫系统异常导致炎症细胞因子的过量产生是sJIA的典型特征[1-5]。现将贵阳市妇幼保健院肾脏风湿免疫科自2018年1月至2020年5月期间应用托珠单抗治疗的sJIA患儿的临床资料总结。报告如下。
1 资料与方法
1.1临床资料 回顾性分析2018年1月至2020年5月住院的5例经TCZ治疗的sJIA患儿的临床资料作为研究对象,研究对象纳入标准见相关文献[5]。排除标准:排除感染性疾病、肿瘤性疾病和其他风湿性疾病。
1.2方法 (1)临床资料收集:收集入组患儿住院期间临床资料,包括性别、年龄、体温、皮疹、肝脾淋巴结肿大、血常规、血沉、C反应蛋白、血清铁蛋白、肝功能、血脂及TCZ治疗前病程、受累关节数、用药方案、MAS次数、复发次数等。(2)治疗及随访:开始治疗起点(0周)及首次给药后每2周静脉滴注托珠单抗注射液(罗氏公司,规格:80 mg/支 ,药品批号 :B1022B03)1次,3月后改为每4周给药1次,半年后改为每4-8周给药一次。具体方案 :体质量 ≥30 kg者剂量 8 mg/kg;体质量<30kg者剂量 12 mg/kg,溶媒为0.9%氯化钠注射液100 mL每次静脉滴注时间>1h;同时继续口服NSAIDs、激素或联合DMARDs。定期随访,观察 TCZ治疗前及治疗后4、8、12、24周临床及实验室指标变化。(3)JIA评估参数:采用国际通用的儿科用ACR疗效标准ACR Pedi 30/50/70/90标准[6], 它包括6个项目,即医师对疾病的总体评估 、患儿或患儿父母对病情的总体评估、儿童健康评估问卷(CHAQ)、活动性炎性关节计数 、活动受限关节计数 、ESR或CRP。治疗改善定义 :与治疗前相比,6项核心指标中至少3项有≥30%的改善 ,而且其余的任一项指标均不能有超过30%的加重 (此即ACR Pedi30疗效 )。(4)临床缓解评估:采用Wallace等[7]提出的标准。安全性评价:观察记录患儿用药期间及用药后出现的不良反应及是否出现感染等。每次TCZ治疗前进行血ALT、AST及血中性粒细胞绝对值检测。

2 结 果
2.1一般情况 共入选5例患儿,年龄6岁,最小1岁8月,男2例,女3例,短病程2例(病程小于6个月),长病程3例(病程大于6个月)。在托珠单抗治疗前2例合并巨噬细胞活化综合征、1例合并严重肝功能损害; 5例患儿均以NSAIDs、激素、DMARDs治疗为基础,其中联合甲氨蝶呤2例,联合环孢素1例,联合沙利度胺1例,联合益赛普和英夫利息单抗1例,所有患儿在TCZ治疗前均有多个关节受累。见表1。

表1 患儿一般资料及托珠单抗治疗前情况
2.2治疗前后临床表现比较 应用托珠单抗治疗前所有患儿均有发热,体温≥39℃,伴肝脾、淋巴结肿大,其中4例在高热时出现红色斑疹,热退后皮疹消退。所有患儿应用托珠单抗治疗24 h后体温均恢复正常,且在观察期内未再发热,体温恢复正常后皮疹亦未再出现。所有患儿治疗4周后肝脾、淋巴结肿大消失,关节肿痛减轻,与治疗前相比,托珠单抗治疗4周后,活动性关节炎的关节数目、活动受限的关节数目均有明显改善,ACR Ped达标率随着治疗时间延长持续改善。见表2。在治疗第12周时患儿的激素用量较治疗前明显减少[( 0.64±0.47) mg /( kg· d) vs ( 1.56± 0.44) mg /( kg·d) ,t= 5.93,P<0.01]。短病程组中,1例治疗3个月停用激素,另1例治疗9个月后停用激素,长病程组患儿观察期中无1例减停激素。
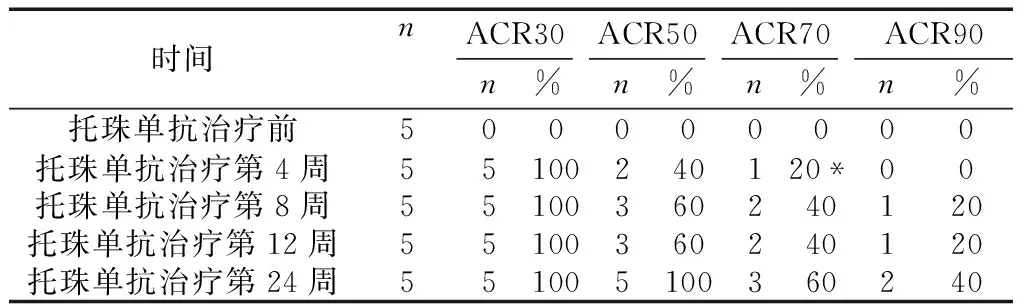
表2 托珠单抗注射液治疗前后JIA ACR Pedi30/50/70/90比较
2.3治疗前后实验室结果比较 与治疗前相比,治疗后的白细胞、CRP、ESR等实验室指标明显下降,血红蛋白明显升高 ,以上差异均有统计学意义(P<0.05)。见表3。

表3 托珠单抗注射液治疗前后主要实验室结果比较
2.4长病程组与短病程组临床缓解率比较 不管是长病程还是短病程,在全身症状、关节炎症状、实验室指标的改善方面疗效都明显,在治疗52周时5例均达到病情不活动(ID)、均未达到不用药维持的临床缓解(CR),短疗程组达到用药维持临床缓解的比例优于长病程组(短病程组2例占100%,长病程组1例占33.3%),但差异无统计学意义(χ2=0.833,P=0.600)。
2.5安全性评价 5例患儿共输注托珠单抗51次,发生可能与药物机制相关的不良事件1次,发生率为 1.96%,例3患儿第二次输注过程中出现一过性发热、寒战,予放慢输液速度、布洛芬口服、地塞米松静推等对症治疗后缓解。无1例出现ALT、AST增高及血中性粒细胞绝对值降低。病例4在TCZ治疗前合并MAS及严重肝功能损害,经甲基泼尼松龙冲击、口服CsA及保肝治疗,在肝功能恢复正常后加用TCZ治疗,观察期中未在出现肝功能损害。
3 讨 论
JIA是儿童时期最常见的慢性风湿病,2018年国际儿童风湿病试验组织(PRINTO)[5]制定的JIA新分类标准中,保留了sJIA这个术语,以符合当前国际公认的术语。但由于sJIA患儿体内缺乏特异性抗体,固有免疫系统异常导致巨噬细胞噬细胞过度活化,释放大量IL-1、IL-6、IL-18和促炎s100蛋白是其主要发病机制,目前国内外学者更倾向于将其归入自身炎症性疾病范畴。治疗上常需使用NSAIDs、大剂量糖皮质激素和cDMARDs,但往往难以控制疾病的活动性[8],与其他类型比较,sJIA有更高的致残率[9],尤其在合并多关节炎和MAS情况下治疗更为棘手。研究发现,JIA活动期患者的血液和关节液中IL-6水平的表达均增高[10]。本组资料中短病程2例,长病程3例,在托珠单抗治疗前2例合并巨噬细胞活化综合征、1例合并严重肝功能损害; 所有患儿在TCZ治疗前均使用了大剂量糖皮质激素、NSAIDs、cDMARDs或联合益赛普、英夫利昔单抗等治疗仍不能有效控制病情,sJIA疾病活动度高。应用托珠单抗治疗24小时后5例患儿体温均恢复正常,皮疹很快消失 ,且在观察周期内均未再出现发热和皮疹。治疗4周后肝脾、淋巴结肿大消失,关节肿痛明显减轻,白细胞、CRP、ESR等下降明显、血红蛋白明显升高 ,糖皮质激素用量明显减少,并随着治疗时间延长,激素持续减量,短病程组的2例患儿分别在治疗3个月和治疗9个月后停用激素,停用激素后均未出现疾病活动。提示托珠单抗能够迅速控制患儿的全身炎症反应,有利于减少糖皮质激素用量,甚至减停激素。托珠单抗治疗4周后,活动性关节炎的关节数目、活动受限的关节数目及ACR Ped达标率均有明显改善,随者TCZ疗程的延长,关节症状得到进一步改善,说明TCZ对缓解sJIA的关节症状亦有显著疗效。
托珠单抗给药间隔时间和停药时机也尚无定论,基于国内外的临床研究,结合患儿家庭经济条件,本组患儿开始每2周给药1次,3个月后改为每4周给药1次,半年后改为每4~8周给药一次,所有患儿均取得了明显疗效。不管是长病程组还是短病程组,TCZ治疗52周后均达到病情不活动(ID),短病程组达到临床缓解的比例优于长病程组,但差异无统计学意义(P>0.05)。短病程组中的2例患儿能减停激素,其中1例患儿停用TCZ半年后复查未见病情活动,是否能达到Wallace等[7]提出的不用药维持的临床缓解(CR)有待进一步随访观察。病例3患儿TCZ治疗前对NSAIDs、糖皮质激素、MTX治疗反应均不佳,给予TCZ输注1次后,体温即降至正常,关节肿痛减轻,因第2次输注时出现一过性发热且年龄小于2岁,停用托珠单抗,继续口服激素、NSAIDs,加用环孢素治疗,观察24周仍能达到疾病不活动。说明在炎症难以控制时,可以应用托珠单抗及时控制炎症 ,即使没有规律用药,对抑制炎症也能起到一定的作用。本组资料中的5例患儿输注TCZ共51次,发生可能与药物输注相关的不良事件1次,发生率为 1.96%,未见严重不良反应。无1例出现ALT、AST、血脂增高、血中性粒细胞绝对值降低和感染。考虑可能与病例数太少有关。
综上所述,托珠单抗治疗sJIA疗效显著,不良反应发生率小。在sJIA起病6个月内给予托珠单抗治疗,似乎更容易实现激素减停同时维持非疾病活动状态,诱导缓解后延长用药间隔仍能达到较好疗效。
