放射性皮肤损伤评估工具研究现状
2021-08-26吴晓月宋丽君韩宝瑾刘杰
吴晓月 宋丽君 韩宝瑾 刘杰
摘要 准确、标准的评估工具对肿瘤患者放射性皮肤损伤的诊断、防治均有重要意义。现对国内外开发的放射性皮肤损伤评估工具进行综述,并分析现有评估工具的特点、存在的问题。建议肿瘤诊治和研究时依据患病人群特点、干预效果、测量负担、是否在目标人群中应用或验证等选择适宜的量表。为全面评估放射性皮肤损伤症状表现及对患者生命质量的影响,开展高质量临床研究,合理实施针对性干预措施提供了方法和依据。
关键词 放射性皮炎;评估工具;肿瘤;患者报告的临床结局;放射性皮肤损伤;放射治疗;基于临床医生报告的臨床结局
Abstract Accurate and standard assessment tools are important for the diagnosis and interventions of radiation dermatitis(RD) in cancer patients.This paper reviews the radiation skin damage assessment tools developed at home and abroad,and analyzes the characteristics and problems of existing assessment tools.It is suggested that the appropriate scale should be selected according to the characteristics of the disease population,the intervention effect,the measurement burden,whether it is applied or verified in the target population,etc.during tumor diagnosis and research.This paper provides a method and basis for comprehensively assessing the symptoms of radiation-induced skin injury and the degree of quality of life,conducting high-quality clinical research,and rationally implementing targeted intervention measures.
Keywords Radioactive dermatitis; Assessment tool; Oncology; Patient Reported Outcome(PRO); Radiation skin injury; Radiotherapy; Clinician Reported Outcome(CRO)
中图分类号:R273;R275.9文献标识码:Adoi:10.3969/j.issn.1673-7202.2021.13.005
放射治疗是多种恶性肿瘤疾病的重要治疗方式,虽然目前技术进步和治疗方案的改变,减轻了放射治疗对皮肤的损伤,但放射性皮肤损伤仍然是放射治疗常见的不良事件之一[1]。其表现为不同程度的瘙痒、红斑、干湿性脱皮,继而引起水泡、溃疡、糜烂,甚至癌变。上述皮肤反应可能导致放射治疗中断,从而延长疗程,延误治疗,严重者会降低患者的生命质量。
针对预防和治疗放射性皮肤损伤,国内外开展了多项临床研究。放射性皮肤损伤的防治主要集中在降低皮肤表面照射剂量、抗炎抗氧化、促进创面愈合、水合保湿、改善微循环等有关机制和措施。另外,临床上用于预防和治疗放射性皮肤反应的药物较多,主要有植物提取物(芦荟凝胶、植物油)、维生素类(维生素C、B12、E)、乳膏类(激素类乳膏、比亚芬乳膏)、重组表皮生长因子(贝复济)和中药类等[2-3]。但是,目前尚缺乏公认的针对放射性皮肤损伤的标准化治疗方案。
2004年和2010年发表的2篇放射性皮肤损伤文献中均提到:由于缺乏一致且有效的评分方法,各个研究之间异质性较大[4-5]。另外,从患者和临床医生的角度来看,放射性皮肤损伤同样缺乏标准化的评估工具[6]。因此,寻找准确、标准的评估工具对放射性皮肤损伤的诊断、防治和护理均有重要意义。现就常用放射性皮肤损伤评估工具进行综述,旨在对未来的诊断提供依据。
1 放射性皮肤损伤评估工具
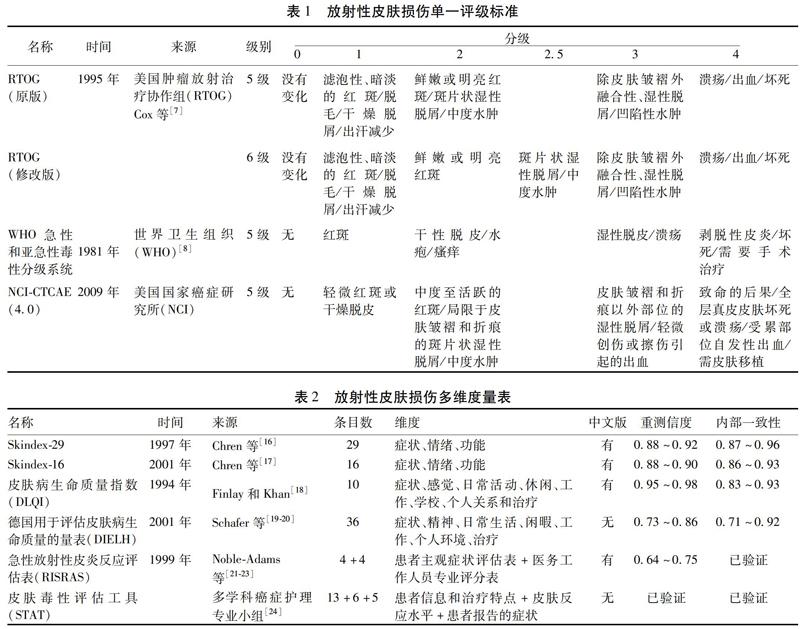
1.1 单一分级标准 急性放射性皮肤损伤的严重程度,通常是由临床医师根据不同临床评分标准进行评估和分级。最常用的评分标准是美国肿瘤放射治疗协作组(Radiation Therapy Oncology Group,RTOG)评分标准、美国国立癌症研究院通用毒性标准(National Cancer Institute Common Toxicity Criteria,NCI-CTC)评分标准、世界卫生组织(World Health Organization,WHO)不良反应评价标准。见表1。
3种评分标准各有优劣。RTOG标准是临床上最常用的急性放射性皮炎的评价标准。但是RTOG标准的缺点是,明亮的红斑和斑片状的湿性脱屑都被分级为2级,尽管从患者的角度来看,这些皮肤变化的严重性可能不相同。目前已有部分研究修改了RTOG评分标准,对原标准中的2级进行了进一步细分,将“鲜嫩或明亮的红斑”评分为2级,而将“斑片状湿脱屑”评分为2.5级[9-10]。美国国家癌症研究所不良事件通用术语标准(NCI-CTCAE)自1983年首次创建后,经过多次修订,1998年发布的CTC v2.0版本系统纳入了放射治疗急性影响的分级标准[11]。2003年发布的CTCAE 3.0版本已被证明可以对头颈部肿瘤患者的放射性皮肤损伤进行可靠地分级[12]。而WHO评分标准对皮肤损伤的症状分级不够详细,因此较少在临床中应用。
此外,3种评分标准之间存在差异。例如,RTOG和CTCAE标准可将红斑分为1级或2级,而WHO标准只能将红斑分为1级;在RTOG和CTCAE标准中,湿性脱屑可分为2级或3级,但在WHO标准中,湿性脱屑只能分为3级。在比较不同的临床医生评估时,使用RTOG和CTCAE标准评估放射治疗导致的2级反应比例高于WHO标准。Sharp等[9]分别使用RTOG和WHO标准评估了接受放射治疗的乳腺癌患者急性皮肤反应的频率和严重程度,发现使用RTOG标准评估出现2~4级反应的比例比WHO标准高近10%。
尽管这些标准经常用于临床和研究,但文献中尚未发表对评分系统的正式效度测试,目前仅有有效性验证[13]。Berthelet等[14]在1项41例乳腺癌患者接受辅助放射治疗的队列研究中,对RTOG评分系统在评估接受放射治疗患者急性皮肤毒性方面的有效性进行了验证。Huang等[15]采用RTOG、CTCAE和WHO临床评分标准对101例乳腺癌患者急性放射性皮炎的严重程度进行了分级,发现3种不同的临床医生评估评分标准(特别是RTOG和CTCAE标准)与放射治疗后皮肤血流变化相关性最强,并且与皮肤色素沉着变化也有中度相关性,这不仅证实了3种评分标准的有效性,也表明RTOG和CTCAE标准比WHO标准更适合评估急性放射性皮炎。
1.2 多维度量表 我们描述了6种放射性皮肤损伤多维度量表。见表2。
1.2.1 Skindex-29和Skindex-16 Chren等[25]于1996年研发了Skindex量表,并进行了信度和效度验证。初始版本共61个条目,但由于Skindex量表填写时间较长(15 min)、区分能力不强,后期逐渐简化为Skindex-16、Skindex-29、Skindex-17等3个版本[16-17,26]。其中Skindex-29、Skindex-16版本应用最广泛。
Skindex-29是Chren等[16]于1997年研究简化的版本,该量表使用开放式问题评估患者对其过去4周皮肤状况的困扰程度的频率,从“从不”(1)到“一直”(5)分为5个等级(1~5)。从症状、情绪、功能3个方面进行评估,其中7项针对症状,10项针对情绪,12项针对功能,平均需要5 min完成。Skindex-29的结果报告为评定情绪、身体症状和功能的3个量表得分,得分越高表示健康相关生命质量(Health-related Quality of Life,HRQoL)越差。692例皮肤病患者参与了调查,证明了Skindex-29的判别效度、聚合效度等,重测信度为0.88~0.92,内部一致性为0.87~0.96。
Skindex-16是Chren等[17]于2001年研究简化的版本。Skindex-16使用問题来评估患者对其过去1周皮肤状况的困扰程度,共分为从“从未困扰”(0)到“总是困扰”(6)7个等级(0~6),并根据3个方面评估HRQoL:症状、情绪和功能。第1~4项属于症状,第5~11项属于情绪,第12~16项属于功能。Skindex-16结果以总分和3个方面分数报告。Skindex-16已经在包括痤疮和银屑病在内的皮肤疾病中进行了信度和效度测试,541例皮肤病患者参与了调查,内部一致性为0.86~0.93[症状量表、情绪量表和功能量表的克朗巴哈系数法(Cronbach′s α)=0.86、0.93、0.92],重测信度为0.88~0.90。
Skindex-29已被翻译成德国版[27]、意大利版[28]、西班牙版[29]等多个版本,其中德国、西班牙、意大利均进行了大样本患者调查。Skindex-16也被翻译成日本版[30]、阿拉伯版[31]等多个版本。Skindex-29和Skindex-16的中文版已经被开发出来,并被证明是评估中国皮肤病患者HRQoL可靠有效的工具。He等[32]在225例皮肤病患者中进行了调查,Skindex-29内部一致性为0.85~0.97,Skindex-16内部一致性为0.86~0.96。
Skindex-29和Skindex-16各有优劣。Skindex-29在了解HRQoL的详细影响方面更全面,其中包含各种皮肤状况的评估。Skindex-16评估的是被调查者各症状的“困扰”程度,而不是各症状发生的“频率”。因此,Skindex-16可以更直接地评估HRQoL的各种症状[33]。
1.2.2 皮肤病生命质量指数 皮肤病生命质量指数(Dermatology Life Quality Index,DLQI)是由Finlay和Khan[18]于1994年共同研制的量表,该量表包括10个问题,用来评估患者过去1周的皮肤状况,涉及症状、感觉、日常活动、休闲、工作、学校、个人关系和治疗。每个问题分为4个等级:“一点也不”“一点”“很多”或“非常”。每个问题的得分从0到3,将得分相加,范围从0(对生命质量没有损害)到30(最大损害)。作为第一个皮肤特异性HRQoL评估工具,DLQI的主要优势是有大量可用的临床研究数据。此外,DLQI非常易于使用和评分,分数解释也相对容易(例如超过10分通常意味着非常严重)[34]。
DLQI已被用于32个国家的33种不同的皮肤状况,并被翻译为55种语言[35]。2004年王晓玲等[36]将其翻译为简体中文版,并被证实具有较好的信度和效度。115个研究描述了DLQI的效度、信度、对变化的反应性、因子结构和最小重要差异等内容[35]。在5项考察DLQI内部一致性的研究中,Cronbach′s α得分范围为0.83~0.93,重测信度为0.95~0.98[18,37]。但是,DLQI仅适用于15岁以上成年人,5~16岁可使用儿童版本的DLQI,即儿童皮肤病学生命质量指数(the Children′s Dermatology Life Quality Index,CDLQI)[38]。2003年,Loo等[39]和Holme等[40]又分别在DLQI和CDLQI基础上配上图片,制成图解版和卡通版。
1.2.3 德国用于评估皮肤病生命质量的量表 德国用于评估皮膚病生命质量的量表(Deutschen Instruments zur Erfassung der Lebensqualitt bei Hauterkrankungen,DIELH)由Schfer等[19-20]于2001年研制,其中包括了7方面(症状、精神、日常生活、闲暇、工作、个人环境、治疗)的36个问题,已在一般皮肤病和特应性皮炎中进行了内部一致性、信度和效度的验证,内部一致性为0.71~0.92,重测信度为0.73~0.86。
1.2.4 急性放射性皮炎反应评估表 急性放射性皮炎反应评估表(the Radiation-Induced Skin Reaction Assessent Scale,RISRAS)是Noble-Adams等[21-23]于1999年研发的,该量表分为2部分,第一部分为患者主观症状评估表,由患者填写,包括放射野皮肤的紧绷不适、疼痛、痒或灼热感,以及各反应或症状影响患者日常活动的程度。研究对象的回答从“一点都没有”“一点点”“有一些”到“非常”依次计0~3分,总分为0~12分,分值越高,患者症状越严重;第二部分为医务工作人员专业评分表,包括红斑、干性脱皮、湿性脱皮、坏死4项。红斑根据患者照射野皮肤颜色的改变来评分,干性脱皮、湿性脱皮、坏死则根据患者放射野发生皮炎的面积占整个放射野皮肤的比例来评估,总分为0~16分。2个评分表的得分汇总即为总分,总分为0~28分。RISRAS在急性放射性皮炎中进行了信度和效度测试,结果是令人满意的,重测信度为0.64~0.75。RISRAS已被应用于国内外多项防治放射性皮肤损伤及探索放射性皮肤损伤影响因素的临床研究中[41-44]。
1.2.5 皮肤毒性评估工具 皮肤毒性评估工具(Skin Toxicity Assessment Tool,STAT)[24]是由一个多学科癌症护理专业人员组成的小组所研发的,是评估放射性急性皮肤毒性的特异性评估工具。皮肤毒性评估工具(STAT)包括3个部分。第1部分记录患者信息和治疗特点;第2部分包括以下皮肤反应水平的评分:皮肤完整、轻度红斑、严重红斑、干燥脱屑、潮湿脱屑、渗出物等,记录皮肤受累面积(以平方厘米计);第3个部分为患者报告症状的评分:对灼烧、瘙痒、拉扯感、压痛和其他不适的症状进行评分。STAT在乳腺癌患者中进行了信度和效度测试。Miller等[45]在一项Ⅲ期双盲随机试验中,应用STAT评估了糠酸莫米松对接受放射治疗的乳腺癌患者急性皮肤毒性的影响。
2 常用量表的选择
2.1 维度及研究目的 单一评级标准仅能评估放射性皮损的严重程度,而多维度量表则在评估范围方面更具有优势。但是,针对多维度量表应包含哪些维度至今未有统一标准。如果研究目的仅仅是探索放射性皮损的损伤情况及严重程度,可选择单一的、基于临床医生报告的临床结局(Clinician Reported Outcome,CRO)评级标准。如果侧重于皮肤损伤对患者生命质量等更多维度的评价,可选择多维度的基于患者报告的临床结局(Patient Reported Outcome,PRO)量表,Skindex-29、Skindex-16、DLQI、DIELH、RISRAS和STAT均从多方面进行了患者的自我报告,且信度、效度均得到了验证。如果研究目的兼顾CRO及PRO,可选用RISRAS、STAT,或选择单一的CRO评级标准再联合某个多维度PRO量表。RISRAS和STAT不仅有患者生命质量的报告,且有皮肤反应症状的评估。但是,与STAT不同,RISRAS使用累积分数,将CRO和PRO相加。而CRO与PRO之间的相关系数通常较低,将二者合并为累积评分的方法可能具有自限性。除此之外,它还有另一个限制——评价皮肤损伤情况的是临床照片而不是直接与患者接触。这限制了有关该工具在临床环境中的易用性的结论[24]。
2.2 研究人群 放射性皮肤损伤研究一般针对于肿瘤患者,Skindex-29、Skindex-16、DLQI和DIELH虽然为应用于各种皮肤病的评估工具,但均在单种癌症种类患者中进行了信度及效度检验。而RISRAS和STAT是仅应用于放射性皮肤损伤的评估工具,RTOG评分标准、WHO评分标准、NCI-CTCAE评分标准均是用于肿瘤患者的评估工具。
另外,根据研究人群的年龄和行为能力进行选择。若研究人群为儿童,可选择CDLQI、卡通版或单一CRO评分标准。若研究人群无法配合填写量表(例如影响表达能力的肿瘤患者),可选择单一CRO评分标准。
2.3 干预效果和测量负担 临床研究中,施加干预措施的时间点、起效时间、疗效持续时间等可决定选择量表的回忆期和测量频次。研究者使用的单一CRO评估工具相对而言对患者的测量负担较小,只是增加患者就诊的负担。维度多、条目多的PRO评估工具测量负担往往较重,但可以借助ePRO平台减少患者就诊负担。因此,研究者应在考虑干预效果的同时,结合具体研究需求,综合考虑选择评估工具,尽可能减少测量负担,这有助于提高数据质量和研究效率。
3 存在问题与展望
根据放射性皮肤损伤的临床表现,评估放射性皮肤损伤主要采用的标准包括红斑和鳞片等信号的视觉测量,如RTOG、WHO和CTCAE。这些量表的一个局限性是研究者自身判定放射性皮损分级中可能出现的主观性,导致在多中心研究中对放射性皮损的评价存在显著的偏差[46]。
急性皮肤毒性评价方法除采用肉眼观察对放射皮肤变化进行评分外,还包括分光光度法[47]、反射率计算机彩色分析仪[48]、超声成像[49]、激光多普勒血流法[50-53]和使用介电法测量皮肤水化[54-55]。虽然这些技术可以提供客观的皮肤反应测量方法,但测量负担重。刘成伟等[56]在2020年研发了一个包含2个1级指标、10个2级指标、35个3级指标的放射性皮肤溃疡评估工具,但尚未进行临床验证。现有皮肤评估工具的另一个局限性是——它们通常强调研究者对皮肤反应的评估,但不关注患者报告的症状和功能结果。而且,研究者报告的结果与患者报告的结果往往不一致。据报道,患者和医生对常见CTCAE项目的症状等级的严重程度评价并不一致[7]。虽然用于评估放射性皮肤反应的单一数字评分易于管理和使用,但是它们的结构倾向于是刚性的,并且没有考虑到不同程度的皮肤反应所伴随的症状[24]。
此外,中醫干预往往以多症状管理为目标,以整体观念和辨证论治为基本原则。中医认为辐射是一种火热邪毒,放射治疗所致损伤为热邪入侵、内外热毒、化火耗气灼津,为气阴两虚的病机,治疗宜清热润燥、益气养阴。放射性皮肤损伤除热蕴肌腠而致的红斑、脱皮、溃疡、疼痛外,往往伴有疲乏、睡眠障碍、焦虑等症状[57-58]。为了评估中医药对放射治疗引起的局部和全身反应的综合疗效,可以应用现有的经过验证的局部皮肤PRO工具和全身症状PRO工具,如安德森症状评估量表(MD Anderson Symptom Inventory,MDASI),或研制症状群评估工具,以更好评估中医药对肿瘤放射治疗人群中放射治疗相关症状群的作用。这既可以使中医临床研究更科学、规范,又可以使研究结果能够支持中医理论应用于临床实践[59]。
放射性损伤是放射治疗中常见的除皮肤反应外伴随多种症状的不良反应,其诊断、预防、治疗和护理目前无规范标准,临床工作者和研究者可通过上述合理选择放射性皮肤损伤的评估工具。针对目前放射性皮肤损伤评估工具的研究现状,未来应进一步完善和验证现有评估量表,开发适宜本土的放射性皮肤损伤特异性评估工具或中医多症状评估工具,为放射性皮肤损伤的诊断、合理化治疗、改善症状、提高疗效和生命质量提供依据,推动高质量的临床研究,支撑中医药优势的科学阐释和新药研发。
参考文献
[1]Bray FN,Simmons BJ,Wolfson AH,et al.Acute and Chronic Cutaneous Reactions to Ionizing Radiation Therapy[J].Dermatol Ther(Heidelb),2016,6(2):185-206.
[2]徐敏,李建彬,田世禹.放射性皮炎的防治研究现状[J].中华肿瘤防治杂志,2007,14(17):1354-1357.
[3]关靓,郑佳彬,李冰雪,等.放射性皮肤损伤的药物治疗现状[J].中华中医药杂志,2020,35(7):3550-3552.
[4]Gosselin TK,Schneider SM,Plambeck MA,et al.A prospective randomized,placebo-controlled skin care study in women diagnosed with breast cancer undergoing radiation therapy[J].Oncol Nurs Forum,2010,37(5):619-626.
[5]Wickline MM.Prevention and treatment of acute radiation dermatitis:a literature review[J].Oncol Nurs Forum,2004,31(2):237-247.
[6]Lam E,Yee C,Wong G,et al.A systematic review and meta-analysis of clinician-reported versus patient-reported outcomes of radiation dermatitis[J].Breast,2020,50:125-134.
[7]Cox JD,Stetz J,Pajak TF.Toxicity criteria of the Radiation Therapy Oncology Group(RTOG) and the European Organization for Research and Treatment of Cancer(EORTC)[J].Int J Radiat Oncol Biol Phys,1995,31(5):1341-1346.
[8]Miller AB,Hoogstraten B,Staquet M,et al.Reporting results of cancer treatment[J].Cancer,1981,47(1):207-214.
[9]Sharp L,Johansson H,Landin Y,et al.Frequency and severity of skin reactions in patients with breast cancer undergoing adjuvant radiotherapy,the usefulness of two assessment instruments-a pilot study[J].Eur J Cancer,2011,47(18):2665-2672.
[10]Porock D,Kristjanson L.Skin reactions during radiotherapy for breast cancer:the use and impact of topical agents and dressings[J].Eur J Cancer Care(Engl),1999,8(3):143-153.
[11]Trotti A,Colevas AD,Setser A,et al.CTCAE v3.0:development of a comprehensive grading system for the adverse effects of cancer treatment[J].Semin Radiat Oncol,2003,13(3):176-181.
[12]Palazzi M,Tomatis S,Orlandi E,et al.Effects of treatment intensification on acute local toxicity during radiotherapy for head and neck cancer:prospective observational study validating CTCAE,version 3.0,scoring system[J].Int J Radiat Oncol Biol Phys,2008,70(2):330-337.
[13]Feight D,Baney T,Bruce S,et al.Putting Evidence Into Practice[J].Clin J Oncol Nurs,2011,15(5):481-492.
[14]Berthelet E,Truong P,Chung C,et al.37 Preliminary Validation of the RTOG Acute Skin Toxicity Scoring System in Patients Undergoing Adjuvant Radiotherapy for Breast Cancer[J].Radiotherapy and oncology,2005,76:S12.
[15]Huang CJ,Hou MF,Luo KH,et al.RTOG,CTCAE and WHO criteria for acute radiation dermatitis correlate with cutaneous blood flow measurements[J].Breast,2015,24(3):230-236.
[16]Chren MM,Lasek RJ,Flocke SA,et al.Improved discriminative and evaluative capability of a refined version of Skindex,a quality-of-life instrument for patients with skin diseases[J].Arch Dermatol,1997,133(11):1433-1440.
[17]Chren MM,Lasek RJ,Sahay AP,et al.Measurement properties of Skindex-16:a brief quality-of-life measure for patients with skin diseases[J].J Cutan Med Surg,2001,5(2):105-110.
[18]Finlay AY,Khan GK.Dermatology Life Quality Index(DLQI)--a simple practical measure for routine clinical use[J].Clin Exp Dermatol,1994,19(3):210-216.
[19]T.Schfer,A.Staudt,J.Ring.Deutsches Instrument zur Erfassung der Lebensqualitt bei Hauterkrankungen(DIELH)Interne Konsistenz,Reliabilitt,konvergente und diskriminante Validitt und Vernderungssensitivitt[J].Der Hautarzt,2001,52(7):624-628.
[20]T.Schfer,A.Staudt,J.Ring.Entwicklung des Deutschen Instruments zur Erfassung der Lebensqualitt bei Hauterkrankungen(DIELH)[J].Der Hautarzt,2001,52(6):492-498.
[21]Noble-Adams R.Radiation-induced reactions.1:An examination of the phenomenon[J].Br J Nurs,1999,8(17):1134-1140.
[22]Noble-Adams R.Radiation-induced skin reactions.2:Development of a measurement tool[J].Br J Nurs,1999,8(18):1208-1211.
[23]Noble-Adams R.Radiation-induced skin reactions.3:Evaluating the RISRAS[J].Br J Nurs,1999,8(19):1305-1312.
[24]Berthelet E,Truong PT,Musso K,et al.Preliminary reliability and validity testing of a new Skin Toxicity Assessment Tool(STAT) in breast cancer patients undergoing radiotherapy[J].Am J Clin Oncol,2004,27(6):626:631.
[25]Chren MM,Lasek RJ,Quinn LM,et al.Skindex,a quality-of-life measure for patients with skin disease:reliability,validity,and responsiveness[J].J Invest Dermatol,1996,107(5):707-713.
[26]Nijsten TE,Sampogna F,Chren MM,et al.Testing and reducing skindex-29 using Rasch analysis:Skindex-17[J].J Invest Dermatol,2006,126(6):1244-1250.
[27]Augustin M,Wenninger K,Amon U,et al.German adaptation of the Skindex-29 questionnaire on quality of life in dermatology:validation and clinical results[J].Dermatology,2004,209(1):14-20.
[28]Abeni D,Picardi A,Pasquini P,et al.Further evidence of the validity and reliability of the Skindex-29:an Italian study on 2,242 dermatological outpatients[J].Dermatology,2002,204(1):43-49.
[29]Jones-Caballero M,Peas PF,García-Díez A,et al.The Spanish version of Skindex-29[J].Int J Dermatol,2000,39(12):907-912.
[30]Sahori U,Hiroshi U,Syoko O,et al.Measurement of QoL of 1,202 New Japanese Outpatients Using the Japanese Version of Skindex16[J].The Japanese Journal of Dermatology,2009,119(3):337-343.
[31]D.O.Diakité,S.El Fakir,F.Z.Mernissi,et al.Adaptation transculturelle et validation du questionnaire SKINDEX 16 dans la version dialectale arabe marocaine[J].Revue d′Epidemiologie et de Santé Publique,2014,62.S153-S153.
[32]He Z,Lu C,Chren MM,et al.Development and psychometric validation of the Chinese version of Skindex-29 and Skindex-16[J].Health Qual Life Outcomes,2014,12:190.
[33]Chren MM.The Skindex instruments to measure the effects of skin disease on quality of life[J].Dermatol Clin,2012,30(2):231-236,xiii.
[34]Finlay AY,Basra M,Piguet V,et al.Dermatology life quality index(DLQI):a paradigm shift to patient-centered outcomes[J].J Invest Dermatol,2012,132(10):2464-2465.
[35]Basra MK,Fenech R,Gatt RM,et al.The Dermatology Life Quality Index 1994-2007:a comprehensive review of validation data and clinical results[J].Br J Dermatol,2008,159(5):997-1035.
[36]王晓玲,赵天恩,张喜芹.简体中文版皮肤病生命质量指标信度和效度初探[J].中华流行病学杂志,2004,25(9):791-793.
[37]Lewis V,Finlay AY.10 years experience of the Dermatology Life Quality Index(DLQI)[J].J Investig Dermatol Symp Proc,2004,9(2):169-180.
[38]Lewis-Jones MS,Finlay AY.The Children′s Dermatology Life Quality Index(CDLQI):initial validation and practical use[J].Br J Dermatol,1995,132(6):942-949.
[39]Loo WJ,Diba V,Chawla M,et al.Dermatology Life Quality Index:influence of an illustrated version[J].Br J Dermatol,2003,148(2):279-284.
[40]Holme SA,Man I,Sharpe JL,et al.The Children′s Dermatology Life Quality Index:validation of the cartoon version[J].Br J Dermatol,2003,148(2):285-290.
[41]王珍,陳鹏飞,王伟.医用三氧橄榄油防治鼻咽癌急性放射性皮炎的临床疗效观察[J].中国医药科学,2019,9(12):208-211.
[42]Yan J,Yuan L,Wang J,et al.Mepitel Film is superior to Biafine cream in managing acute radiation-induced skin reactions in head and neck cancer patients:a randomised intra-patient controlled clinical trial[J].J Med Radiat Sci,2020,67(3):208-216.
[43]Sabater S,Leon R,Esteban C,et al.Patients′ view of the differences in topical creams for radiation dermatitis prevention.A pilot study of cosmetic properties[J].Rep Pract Oncol Radiother,2019,24(4):347-354.
[44]Sutherland AE,Bennett NC,Herst PM.Psychological stress affects the severity of radiation-induced acute skin reactions in breast cancer patients[J].Eur J Cancer Care(Engl),2017,26(6):e12737.
[45]Miller RC,Schwartz DJ,Sloan JA,et al.Mometasone furoate effect on acute skin toxicity in breast cancer patients receiving radiotherapy:a phase Ⅲ double-blind,randomized trial from the North Central Cancer Treatment Group N06C4[J].Int J Radiat Oncol Biol Phys,2011,79(5):1460-1466.
[46]Ferreira EB,Vasques CI,Gadia R,et al.Topical interventions to prevent acute radiation dermatitis in head and neck cancer patients:a systematic review[J].Support Care Cancer,2017,25(3):1001-1011.
[47]Porock D,Kristjanson L.Skin reactions during radiotherapy for breast cancer:the use and impact of topical agents and dressings[J].Eur J Cancer Care(Engl),1999,8(3):143-153.
[48]Russell NS,Knaken H,Bruinvis IA,et al.Quantification of patient to patient variation of skin erythema developing as a response to radiotherapy[J].Radiother Oncol,1994,30(3):213-221.
[49]Warszawski A,Rttinger EM,Vogel R,et al.20 MHz ultrasonic imaging for quantitative assessment and documentation of early and late postradiation skin reactions in breast cancer patients[J].Radiother Oncol,1998,47(3):241-247.
[50]Amols HI,Goffman TE,Komaki R,et al.Acute radiation effects on cutaneous microvasculature:evaluation with a laser Doppler perfusion monitor[J].Radiology,1988,169(2):557-560.
[51]Nystrm J,Geladi P,Lindholm-Sethson B,et al.Objective measurements of radiotherapy-induced erythema[J].Skin Res Technol,2004,10(4):242-250.
[52]Nystrm J,Svensk AC,Lindholm-Sethson B,et al.Comparison of three instrumental methods for the objective evaluation of radiotherapy induced erythema in breast cancer patients and a study of the effect of skin lotions[J].Acta Oncol,2007,46(7):893-899.
[53]Doll C,Durand R,Grulkey W,et al.Functional assessment of cutaneous microvasculature after radiation[J].Radiother Oncol,1999,51(1):67-70.
[54]Nuutinen J,Lahtinen T,Turunen M,et al.A dielectric method for measuring early and late reactions in irradiated human skin[J].Radiother Oncol,1998,47(3):249-254.
[55]Jensen JM,Gau T,Schultze J,et al.Treatment of acute radiodermatitis with an oil-in-water emulsion following radiation therapy for breast cancer:a controlled,randomized trial[J].Strahlenther Onkol,2011,187(6):378-384.
[56]刘成伟,刘亦凡,黄瑶,等.放射性皮肤溃疡评估工具的构建[J].上海交通大学学报:医学版,2020,40(12):1687-1692.
[57]张娜,宋金霞,王宏桥,等.鼻咽癌同步放化学药物治疗患者症状群的纵向研究[J].护理学报,2019,26(23):6-10.
[58]陈婷婷,王应天,田甜.数据挖掘法浅析中医治疗肺癌用药规律及相关机制[J].中国实验方剂学杂志,2018,24(11):206-210.
[59]Liu J,Mao JJ,Wang XS,et al.Evaluation of Traditional Chinese Medicine Herbs in Oncology Clinical Trials[J].Cancer J,2019,25(5):367-371.
(2021-04-23收稿 責任编辑:王明)
