体外膜肺氧合在院外急救救援现场和转运后送中的应用
2021-08-26樊毫军李文莉哈力旦阿布都蔡金霞陈原森刘燕青刘子泉
樊毫军,李文莉,哈力旦·阿布都,蔡金霞,陈原森,刘燕青,刘子泉
近年来,世界范围内各种自然灾害、军事冲突、恐怖事件、交通事故、传染病等时有发生,特别是2019年底爆发的新型冠状病毒肺炎(Corona Virus Disease 2019,COVID-19)疫情,目前仍在全球范围内蔓延,对人类生命安全构成极大的威胁。上述情况下重症循环呼吸衰竭的发生率大大增加,常规治疗技术难以满足现场紧急救治需求,若不能及时采取有效的生命支持策略,患者死亡率可高达40%~60%[1-2],因此迅速、有效的循环呼吸辅助支持成为首选。
体外膜肺氧合(Extracorporeal Membrane Oxygenation,ECMO)作为一种呼吸循环支持技术,又被称为体外生命支持(Extracorporeal Life Support,ECLS),是针对常规治疗无效的循环和(或)呼吸衰竭的抢救性辅助治疗措施。ECMO能够快速改善危重症患者的低氧血症和循环衰竭状态,可在相对时间内部分替代患者的心肺功能,为心肺功能的恢复赢得时间。研究表明,ECMO辅助支持可有效降低患者的死亡率[3],近年来该技术在危重症救治领域发挥了重要作用,特别是自2009年甲型H1N1流感大流行开始,全球接受ECMO辅助治疗的患者数量呈现跨越式的增长。由体外生命支持组织(Extracorporeal Life Support Organization,ELSO)提供的数据显示,截至2020年,超过150 000例患者接受过ECMO治疗,总体生存率约为69%[4],见图1。
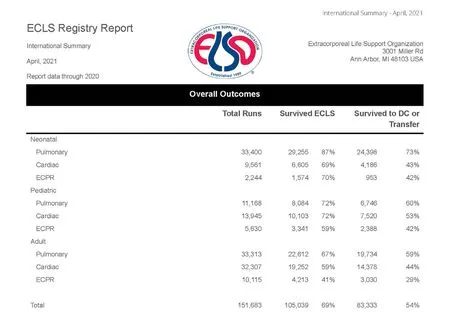
图1 ELSO 2021-04的统计报表
近年来,便携式ECMO系统的出现使ECMO救援现场紧急启动成为可能。研究表明,该装置可为重症心肺衰竭患者院前现场紧急救治和转运后送途中提供生命支持,可提高危重症患者的救治率,降低病死率[5-8],极大拓展了ECMO的应用范围。本文对国内外便携式ECMO应用现状进行综述,以期未来能更好地利用ECMO技术救治危重症患者。
1 便携式ECMO设备的研究进展
ECMO具有循环和呼吸支持功能,其原理是将静脉血引流至体外,经膜肺氧合和二氧化碳排出后,再经血泵输送回体内,以暂时性替代心脏和(或)肺脏完成气体交换和血液循环功能;还可通过变温水箱维持和调节患者体温。ECMO系统的主要部件包括血泵,氧合器(膜肺),血管内插管,配套管路包以及各种监测装置[9]。传统的ECMO设备体积较大,便携性差,操作较复杂,需要外接电源,不适用于紧急医疗救援现场或救护车等移动运输工具,不能满足院前急救和转运的需求。
近年来,移动式ECMO和便携式ECMO系统的出现使ECMO救援现场紧急启动成为可能。目前,国外已经有多个品牌的便携式ECMO成功用于院前急救。Lifebridge B2T治疗系统(Lifebridge Medizintechnik AG,Ampfing,德国)是一种便携式模块化的微型心肺支持系统,其包含患者模块,控制模块和基础模块。由于该系统体积较小,总重量相对较轻(18 kg),内置电池可提供2 h续航,因此常用于院外患者的急救和转运[10-11]。但其模块化设计的不足是当患者模块单一组件出现故障时,需更换整个模块。Novalung系统(Inspiration Healthcare Ltd, Leicester,英国)是基于无泵型体外肺辅助技术(Pumpless Extracorporeal Lung Assist,PECLA),专为急性呼吸衰竭患者研制的生命支持系统,其使用前提是患者的心脏功能正常,并利用机体动脉压驱动血液流经膜肺进行氧合。由于无需血泵驱动,该系统大小仅为13.5 cm×13.5 cm×4.0 cm,已被用于多起反恐行动中伤员的院前救治和转运[12-13]。由于该系统只适用于心脏功能正常、能维持稳定血压的患者,因此不宜作为院外生命支持设备的首要选择。Cardiohelp系统(Maquet Cardiopulmonary GmbH,德国)是目前世界上最小的便携式ECMO系统,重量仅为10 kg,内置电池可续航90 min[14],可将该系统安装于转运工具上(救护车、直升机或固定翼飞机),与车载电源相连。该系统已经成功用于院外现场急救、转运后送以及院内行走支持。
国内便携式ECMO研究也取得了一定进展[15-16]。沈阳军区总医院和中国科学院沈阳自动化研究所[17]研制了便携式体外生命支持系统并与Maquet公司Rota flow系统进行动物实验对照研究,结果表明两者具有相似的稳定性。深圳汉诺医疗科技有限公司已经完成了ECMO核心部件以及功能样机的设计。目前,国内产品与国外同类产品相比在血泵、热交换器等的性能指标上仍存在一定差距,同时国内生产的ECMO系统一些关键部件如氧合器,抗凝管路包等仍依赖进口。
2 ECMO救援现场应用现状
2.1 ECMO现场救援的宏观调控国外从20世纪90年代开始实行由ECMO团队在救援现场紧急启动ECMO,再转运至ECMO医疗中心的方案。此外,建立病例筛选与转运流程,可减少患者的致残率和致死率,且不增加诊疗费用[18-20]。目前,国外较大的ECMO医疗中心现场急救和转运流程已经比较成熟。例如法国为了更快、更及时地对院外心脏骤停患者实施体外心肺复苏(对可逆病因的心脏骤停患者,在常规心肺复苏无效时及时启动ECMO辅助支持),设计并使用了分级调度系统,将基础生命支持团队、移动重症监护团队及体外心肺复苏团队根据患者疾病进展状况进行统一调配:当目击到70岁以下院外心脏骤停患者后,首先由基础生命支持和移动重症监护团队到达现场联合救治患者,同时体外心肺复苏团队会接到警报并处于待命状态,如救治成功则体外心肺复苏团队取消待命;反之,10 min后便调配体外心肺复苏团队到达现场准备救援,这样可有效缩短团队准备时间、人员到位时间、物品准备时间和管路预充时间等,及早为患者实施ECMO辅助支持[21]。我国的ECMO现场急救和转运起步较晚,目前尚未建立完善的ECMO协作网络和转运流程,需要借鉴国外经验来建立和完善适合我国特点的转运流程。
2.2 ECMO院前现场救治和转运现状目前,便携式ECMO主要用于院外发生的常规治疗无效的重症心肺功能衰竭的抢救性支持治疗,主要适应症包括:创伤导致的急性呼吸窘迫综合征(Acute Respiratory Distress Syndrome,ARDS)和失血性休克,各种原因导致的心脏骤停,重度失温症,火场气体吸入、溺水等。
在便携式ECMO系统辅助支持下,将危重患者从院外现场或普通医院转运至更高级ECMO医疗中心,能够提高危重症患者的救治率,降低其死亡率。目前,国外较大的ECMO医疗中心已开展ECMO转运服务,单程转运距离可达上万公里,转运人群包括新生儿、儿童、成人,积累了较丰富的急救和转运经验。例如,2015年Kaliyev等[22]报道在便携式ECMO系统的辅助支持下,首次成功对一例严重呼吸衰竭孕妇进行1 155 km远距离转运。此外,便携式ECMO还可应用于战场急救,为危重伤员提供迅速有效的体外生命支持。例如,2005年,美军最大海外医疗机构-德国兰施图尔医疗中心(Landstuhl Regional Medical Center,LRMC)接收来自美国中央司令部行动区(包括伊拉克和阿富汗)的伤员,采用移动式体外肺支持系统对严重呼吸衰竭伤员进行抢救,4名伤员在战区内紧急置管,6名伤员在撤离到德国LRMC后置管,所有伤员的低氧血症和高碳酸血症均得到改善,最终9名伤者成功撤机,1名死于多器官功能衰竭,生存率高达90%[23]。
目前,我国已有重症患儿在专业ECMO转运团队监护下成功进行院间转运的报道。例如,湖南省内首例重症甲型流感患儿的ECMO转诊,并于转诊入院后第9天成功撤机,但该患儿因前期心肺复苏时间过长造成严重的缺血性脑损伤,最终家属放弃治疗后死亡,这也提示ECMO中心应制定完善的病例筛选和转诊流程,并定期进行转诊的预演及培训,从而能在最短的时间内给予患者ECMO支持治疗[24]。研究表明ECMO转运能降低病死率及减少并发症的发生率,最大程度地提高患儿的生存率[25]。此外,ECMO转运在成人危重症患者中也有应用,例如,2019年安徽医科大学第一附属医院收治的1例ARDS患者,患者远距离转运中应用ECMO支持取得了良好的效果[26]。2019年四川省人民医院急诊重症监护病房(Intensive Care Unit,ICU)收治的高原性肺水肿所致呼吸、心脏骤停患者,采用ECMO支持联合航空转运,转运顺利、疗效明确且预后良好[27]。这些成功案例都说明ECMO转运在危重症患者救治中的巨大应用前景。
2.3 ECMO救治团队为了应对院外突发事件及病人病情的变化,及时地维持患者的生命,安全转运到ECMO医疗中心,为进一步的治疗赢得时间,应建立一支快速反应ECMO救治团队。当团队接到现场急救或转运通知后,应在短时间内完成系统的组装,通常便携式ECMO管路较短且均为预充状态,能够在路途中完成管路的连接。团队的人员组成一般根据ECMO服务所涵盖的范围来确定。ELSO指南[28]规定,典型的ECMO转运小组应包括重症医学医师、外科医师、护士、呼吸治疗师、ECMO专业治疗师、急诊医疗服务人员,且队员具有经皮穿刺和血管内插管置入经验。此外,在规划超远距离转运时,应考虑增加队员。目前法国的院外体外心肺复苏团队只由三人组成:一名医生(麻醉师-重症监护医生或急诊医生)、一名麻醉护士和一名护理人员[21]。国内也有单位组建ECMO团队。例如,2017-12华中科技大学同济医学院附属协和医院建立了ECMO团队,包括教育培训小组,质量监控小组,循环建立小组,应急转运小组和护理小组。其中应急转运组包括五名ICU主治医生(同时是循环建立小组成员),五名ICU高级护士[29]。一个良好的ECMO团队的建立可为患者康复争取更多的宝贵时间,同时也提高了重症患者的撤机成功率。
2.4 转运工具的选择最初ECMO转运主要用于呼吸衰竭的新生儿,随着转运经验的积累和ECMO技术的发展,其应用领域不断扩大。过去认为病情严重不能转运的危重患者,现在可通过动脉-静脉ECMO同时提供呼吸循环支持,一旦建立起体外循环,病人病情可迅速稳定下来,这就使得ECMO转运成为从院外救治现场或医疗单位转运危重患者到ECMO医疗中心的最有效的办法。但是也需要考虑ECMO转运的必要性和可行性,对病情危重的患者越早建立ECMO支持,发生多器官功能衰竭和死亡的概率越小。另外,需要考虑到转运工具的安全性,途中是否可进行紧急抢救。在法国,运输方式以空中转运结合陆地转运(50%)和陆地转运结合陆地转运(42%)为主,地面救护车、直升机和固定翼飞机是ECMO运输的三种转运工具,平均运输距离为189 km[30],国外直升机和固定翼飞机紧急ECMO救援发展较早,而国内主要以陆地运输为主,即一般通过救护车运送到ECMO救治中心,远距离的患者可选择直升机和固定翼飞机。
3 局限性和展望
3.1 局限性目前ECMO技术尚不完善,可出现多种机械系统并发症,如血栓形成、插管问题、氧合器功能异常及空气栓塞等;此外,还有出血、溶血、感染及中枢神经系统功能异常等机体并发症。同时,在ECMO运输过程中可能会发生不良事件,大多数不良事件是由于患者在运输过程中的病情不稳定(如潮气量不足或血流动力学衰竭)所致,其他不良事件包括运输延误、ECMO装置遗忘或泵故障、运输停电、现场插管问题、运输过程中严重低温等[30]。
有研究对2010-2015年间的452次转运进行了回顾性调查[31],其中115次(25.4%)转运过程中共发生165次不良事件。在救护车转运(4%)中,由于救护车转运技术不成熟和缺乏经验导致ECMO转运过程中发生了两例心力衰竭死亡事件。目前还没有研究发现不良事件与转运距离或平均转运时间之间的联系[30],并且使用ECMO转运的患者的存活率与未转运的ECMO患者的存活率相当[19]。因此,ECMO支持的远、近距离转运均是安全可行的,但是需要经验丰富的ECMO团队才能减少不良事件的发生,从而为患者争取更多的治疗时间。另外,设备耗材价格昂贵,核心部件需要进口等困难都限制了ECMO转运技术的进一步发展。
3.2 展望便携式ECMO系统国产化,小型化、智能化,将是今后ECMO技术的革新方向。该技术将急危重症患者救治关口整体前移,在“黄金时间”或“白金时间”内对患者实施紧急救治,不仅可用于战时医疗、重大自然灾害、应急医疗救援体系,还可用于平时院外急危重症患者救治和转运,具有广阔的应用前景。此外,危重患者ECMO现场紧急救治和转运需要一支训练有素的ECMO团队,在中国心肺复苏培训中心建立ECMO模拟培训单元,秉承中国特色心肺复苏生存环理念,将院外救援现场与转运后送,融入心肺复苏融入全生命周期系统管理中[32-33]。
