炎症性肠病与非酒精性脂肪性肝病关系的研究
2021-08-24司彤彤李娅董新华程晓寒杨笑瑞朱琳徐峰
司彤彤 李娅 董新华 程晓寒 杨笑瑞 朱琳 徐峰△
郑州大学第一附属医院 1)消化内科 2)胃肠外科 郑州 450052
炎症性肠病(inflammantory bowel disease,IBD)主要包括溃疡性结肠炎(Ulcerative colitis,UC)和克罗恩病(Crohn's disease,CD),是一类多种病因引起的异常免疫介导的肠道慢性及复发性炎症,有终身复发倾向。若病情迁延,常因出现并发症或内科治疗失败而需要肠切除等外科干预[1]。IBD患者常出现皮肤、关节、肝胆等肠外表现,其中肝胆表现最为常见[2]。脂肪性肝病,特别是非酒精性脂肪性肝病( nonalcoholic fatty liver disease,NAFLD),占IBD诊断肝脏改变的40.8%[3]。据报道,与仅患有IBD的患者比较,患有IBD并伴有慢性肝病住院患者的病死率高出两倍[4]。国外已有不少关于IBD合并NAFLD的报道,但我国相关研究较少。本研究初步探讨了IBD与NAFLD间的关系,报告如下。
1 资料与方法
1.1一般资料选取2019-01—2019-12就诊于我院的163例IBD患者作为研究对象,其中UC 119例、CD 44例。均符合“炎症性肠病诊断与治疗的共识意见”中的诊断标准[5]。排除其他肝损伤原因、严重的精神疾病、孕妇,以及合并有心肺脑肾等严重疾病的患者。所有入选者均自愿行肝胆胰脾超声或上腹部CT检查,均签署知情同意书,并通过我院伦理委员会批准。
1.2研究方法记录所有入选者的一般资料、血清学指标、IBD临床特征。将163例IBD患者作为IBD组,根据有无NAFLD分为单纯IBD组(125例)、IBD+NAFLD组(38例)。另选取同期进行健康体检的150例非IBD者作为非IBD对照组,其中20例存在NAFLD的患者为单纯NAFLD组。IBD组与非IBD对照组的性别、年龄差异无统计学意义(P>0.05)。
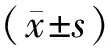
2 结果
2.1IBD组与非IBD对照组NAFLD阳性率比较IBD组和非IBD对照组的NAFLD阳性率分别为23.3%(38/163)和13.3%(20/150),差异有统计学意义(χ2=5.153,P<0.05)。IBD组中UC患者的NAFLD阳性率为24.4%(29/119),CD患者为20.45%(9/44),差异无统计学意义(χ2=0.275,P>0.05)。
2.2单纯IBD组与IBD+NAFLD组患者临床特征比较单纯IBD组与IBD+NAFLD组患者的BMI、高血压病史、既往是否行肠道手术、IBD复发>1次/a,以及ALT、AST、TC、TG的差异有统计学意义(P<0.05),见表1。

表1 单纯IBD组和IBD+NAFLD组患者临床特征比较
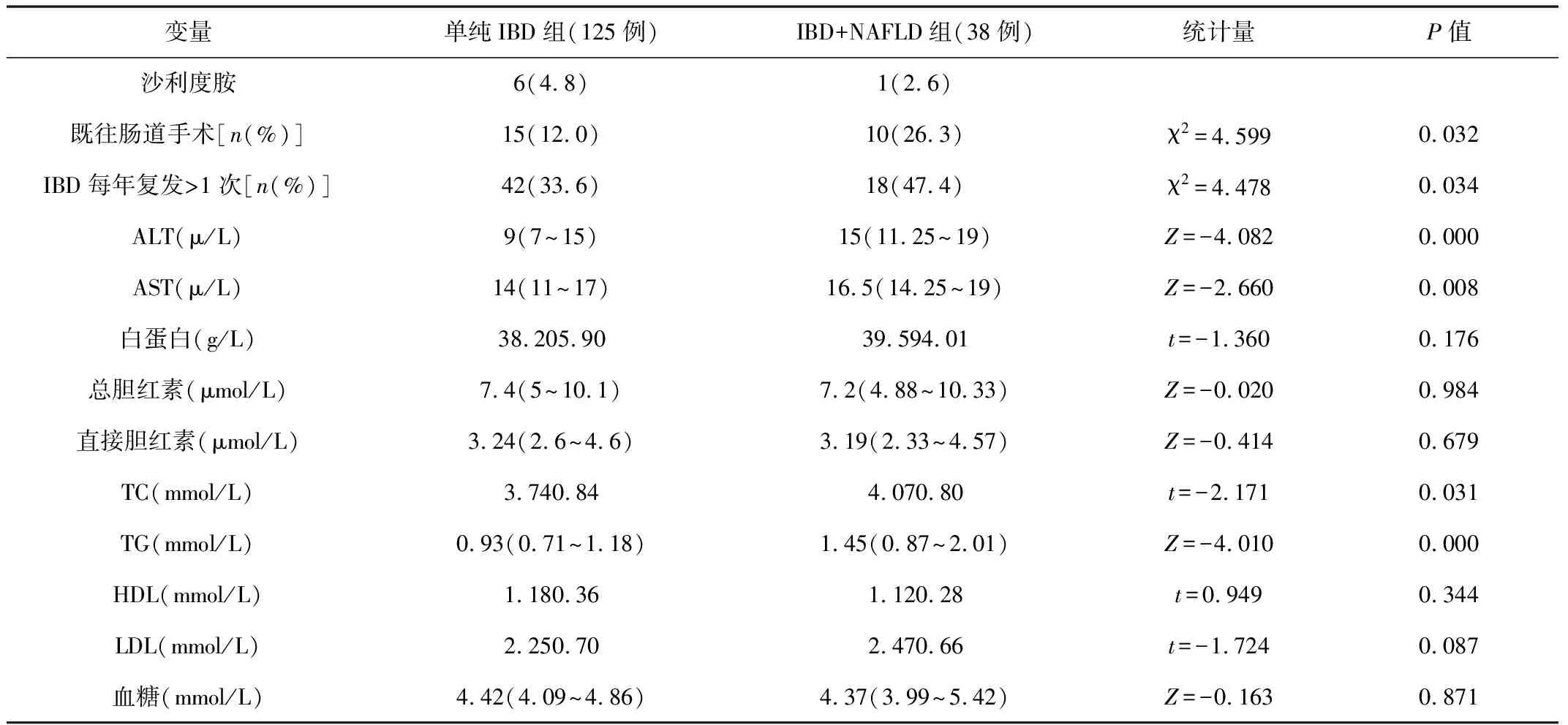
续表1 单纯IBD组和IBD+NAFLD组患者临床特征比较
2.3单纯NAFLD组与IBD+NAFLD组患者临床特征比较单纯NAFLD组与NAFLD+IBD组的年龄、BMI、TG、LDL差异均有统计学意义(P<0.05)。见表2。
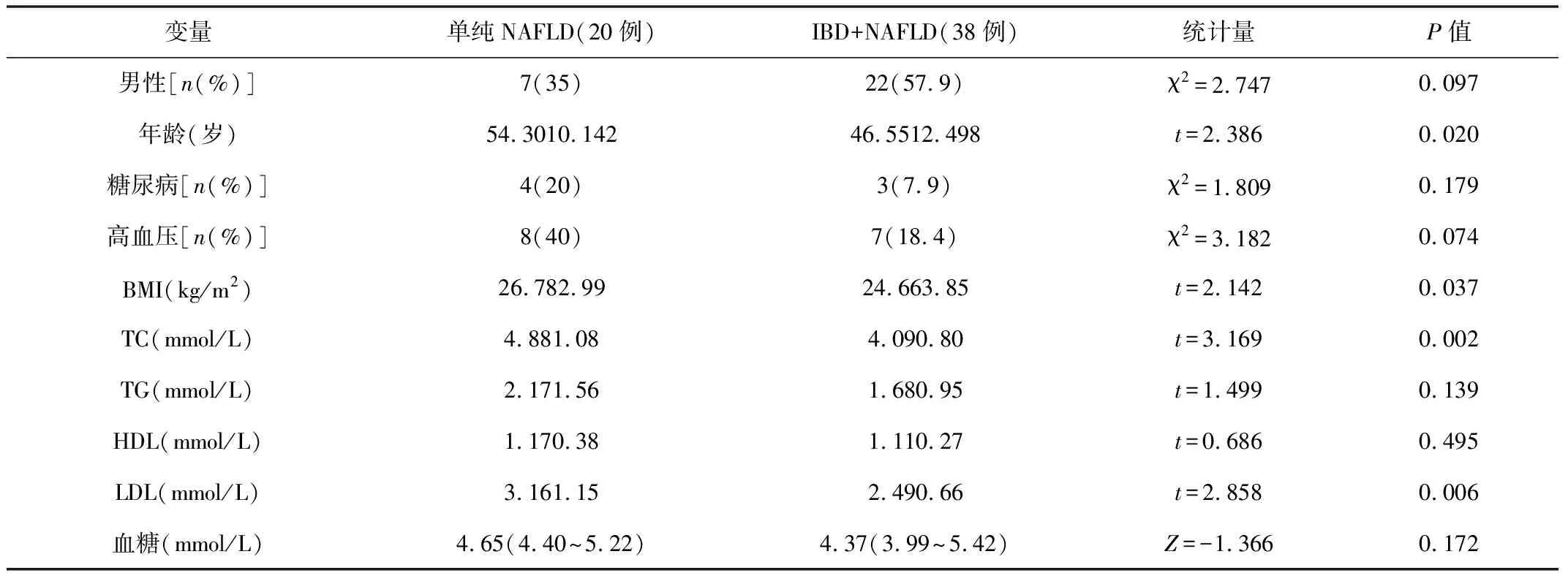
表2 单纯NAFLD组和NAFLD+IBD组的患者临床特征比较
2.4IBD患者发生NAFLD影响因素分析在IBD组中,二元Logistic回归分析显示NAFLD发生与BMI、既往是否行肠道手术、TG独立相关。见表3。
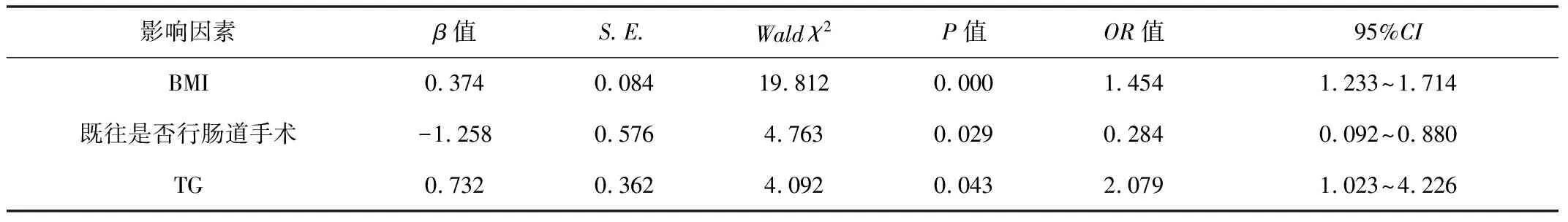
表3 IBD患者发生NAFLD影响因素的Logistic 回归分析
3 讨论
NAFLD是一种影响大约四分之一普通人群的疾病,与巨大的临床和经济负担有关。由于肠道疾病相关疾病,IBD患者患NAFLD的风险可能更高,这些疾病与NAFLD有相同的生理病理特征,如慢性复发性炎症和免疫激活、潜在的肝毒性药物、手术和肠外营养[6-7]等。NAFLD与IBD的共存给管理患者带来了挑战,因此,对IBD合并NAFLD的危险因素分析有重要意义。
虽然IBD并发NAFLD的发病率很高,但是关于这一方面的研究相对较少。既往研究显示NAFLD在IBD中的患病率为8%~40%[3,6],与本研究结果相一致,IBD患者与非IBD人群比较,患NAFLD的风险更高。
高BMI、TG是IBD患者中发生NAFLD的独立危险因素。这与Principi Mariabeatrice[8]等的研究结果相一致。在肥胖状态下,过量的游离脂肪酸(FFA)通过门脉循环进入肝脏,肝细胞甘油三酯合成增加,引起肝细胞内脂质过量沉积,促进NAFLD发生。多项研究表明[9-10],高脂血症是NAFLD的危险因素,患有高脂血症患者合并NAFLD的发生率远高于正常人。
Saroli等[11]的研究结果显示,IBD患者是否合并NAFLD,与IBD用药方面的差异无统计学意义。而Sourianarayanane[6]等发现,类固醇是IBD人群NAFLD的独立危险因素。Vernon W等[12]认为,虽然一些药物可能会导致NAFLD,如糖皮质激素可能通过上调脂肪酸合成酶和乙酰辅酶A羧化酶1和2等几种机制诱导肝细胞脂肪生成和脂肪变性,但没有证据表明单靠药物就能起作用,对用药剂量和用药时间的仔细研究可能会揭示在某些情况下与NAFLD的发展更密切的联系。既往行肠道手术是IBD患者发生NAFLD的独立危险因素,与Sartini[13]等的结果相一致。诊断水平的提高、手术技术的发展和围手术期药物效能的改善,始终成为过去一百年来推动炎性肠病学术研究进步的三大重点领域[14]。虽然内科药物治疗的进步,使IBD手术率降低或手术时间推迟,但仍有30%~40%的CD患者及20%~30%的UC患者最终需手术干预[15]。IBD相关手术,特别是小肠手术,被广泛认为是发生NAFLD的主要预测因素[6]。即使在普通人群中,大量的小肠切除也被发现与NAFLD有关[16]。已有合理的机制被报道,如小肠细菌过度生长,肠道Toll样受体4(TLR4)激活导致的全身炎症反应,以及肠切除相关的代谢综合征[16-18]等。
合并NAFLD的IBD患者较单纯IBD患者血脂更高,但较单纯NAFLD患者,其血脂含量却偏低,表明与单纯NAFLD患者相比,合并NAFLD的IBD患者代谢相关危险因素更少。另外,与单纯NAFLD患者相比,合并NAFLD的IBD患者更年轻。
综上所述,IBD患者中发生NAFLD较健康人更为隐匿,更加年轻化。IBD治疗不应仅限于肠道疾病,还应包括代谢干预,对于肥胖、有行肠道手术病史的患者应通过促进健康的生活方式和正确的饮食方案,减少慢性肝病的发生。
