高铁酸盐对水中H2受体拮抗剂的降解特性
2021-08-21方智煌刘祥余阳钱雅洁薛罡
方智煌,刘祥,余阳,钱雅洁,薛罡
(东华大学环境科学与工程学院,上海 201620)
在药企、临床和生活里被广泛使用的H2受体拮抗类药品(HRAs)主要包括法莫替丁(FMTD)、雷尼替丁(RNTD)、罗沙替丁(RXTD)、西咪替丁(CMTD)和尼扎替丁(NZTD),因其在人体中具有抑制胃酸和胃蛋白酶活性的作用,在医学领域广泛用于治疗消化性溃疡等肠胃问题[1]。然而,由于人体吸收该药物的能力有限,大部分HRAs药物会经过人体的排泄系统重新进入水环境中,且HRAs具有持久性、生物难降解、毒性大等特点,易对水环境造成严重的生态污染[2-4]。Radjenović等[2]在WWTPs的主要排泄物中检测到RNTD浓度在70~540ng/L;Kolpin等[5]在地表水(SW)中检测到CMTD浓度范围为74~580ng/L。传统的紫外消毒法和臭氧氧化法无法实现RNTD和NZTD两种硝基类药物的有效去除,还会生成毒性更强的卤代硝基甲烷和N-亚硝基二甲胺的前体[6-7]。FMTD在制药工业中的常规水处理过程中只是部分被降解,易对水域生态造成危害[8-9]。Hoppe等[10]发现CMTD高达60%的原始剂量可以作为母体化合物排出体外对生态环境造成污染。HRAs在水生环境中的频繁出现表明需要更加清洁高效的水处理技术来应对HRAs对水环境造成的不良影响。
由于HRAs在水体中具有使用广、浓度低、难降解和持久性等特点,传统的处理工艺(混凝、过滤、吸附和消毒等)以及生物降解工艺并不能有效将其去除[2-3,7-9]。Karpińska等[9]用H2O2、UV和Fe2+联用于最佳降解条件下降解50μmol/L FMTD,在80min的去除效果仅为80.2%;Dong等[6]用UV降解雷尼替丁(RNTD)和尼扎替丁(NZTD),容易生成强毒性卤代硝基甲烷,且降解反应速率难以提高。K2FeO4是一种新型、绿色的环境友好材料,与传统的氧化剂如氯系消毒剂和臭氧相比,其氧化还原电位最高[11],在氧化降解污染物过程中集氧化、吸附、絮凝等作用为一体而在水处理领域备受关注[12]。目前,K2FeO4广泛用于去除水中个人护理品、内分泌干扰物和医药品等新兴微污染物以及部分难降解有机污染物。高铁酸盐[Fe(Ⅵ)]与含硫有机物具有较高的反应性,10mg/LK2FeO4降解含硫有机物的半衰期在ms到s的范围内[13];K2FeO4与β-内酰胺抗生素阿莫西林和氨苄西林以摩尔化学计量比分别为3.5和4.5反应时,可将污染物完全去除[14]。Gombos等[15]在对K2FeO4和氯的氧化降解进行试验对比,发现K2FeO4在去除有机物及其副产物方面呈现出很大优势,反应不会产生溴酸盐等有害副产物。
本文考察了K2FeO4对HRAs的降解特性,通过控制K2FeO4投加量和反应pH,探究了K2FeO4氧化HRAs的降解动力学;通过控制共存离子及腐殖酸(HA),探究了不同水体基质对K2FeO4降解HRAs的影响,并在超纯水、地表水、二沉池出水和医疗废水体系中进行了验证;通过大肠杆菌的菌落生长情况,探究了K2FeO4降解HRAs过程中目标污染物的毒性变化,研究结果可以为水体中HRAs的控制提供理论依据和技术支撑。
1 材料与方法
1.1 试剂与仪器
试剂:西咪替丁(Cimetidine,CMTD)、法莫替 丁 (Famotidine,FMTD)、 罗 沙 替 丁(Roxatidine,RXTD)、雷 尼 替 丁(Ranitidine,RNTD)、尼扎替丁(Nizatidine,NZTD)的标准化学品均来自Sigma Aldrich或ANPEL实验室技术(上海)有限公司,为分析纯级别,物质结构如图1所示。磷酸二氢钠、磷酸氢二钠、硫代硫酸钠、氯化钠、碳酸氢钠、乙酸铵、腐殖酸、氢氧化钠、磷酸均来自阿拉丁,为分析纯级别。甲醇、乙醇、乙腈均为色谱纯,来自Sigma Aldrich。试验过程中取用的超纯水来自Milli-Q超纯水制备机(EMD Millipore,Billerica,MA,USA)。
仪器:高效液相色谱仪(1260,Agilent Technology,USA)、Zorbax SB-C18色 谱 柱(4.6mm×250mm×5μm)、紫外分光光度计(UV-1600PC,Shanghai Mapada Instruments)、pH计(FE28K,Mettler Toledo)、磁力搅拌器(84-1A上海司乐仪器有限公司)、电子天平(AW120,Shimadzu)、高压灭菌锅(OMY SX-500,日本)、振荡培养箱(MaxQ6000,Thermo Scientific)。
1.2 试验过程
1.2.1 反应动力学试验
所有试验操作均在室温条件下(25℃±2℃)进行,将10μmol/L HRAs等目标污染物溶解于玻璃血清瓶中,用10mmol/L磷酸盐缓冲液(PB)调节反应pH,加入相应浓度的K2FeO4溶液,在转速为200r/min的恒温磁力搅拌器上充分搅拌,于一定的时间取样1mL并经过0.45μm滤膜过滤于液相棕色进样瓶,并立即用0.1mL浓度为300mmol/L的Na2S2O3进行猝灭,最后置于高效液相色谱仪进行定量分析测定浓度。通过控制试验中的变量关系,分别研究K2FeO4投加量、pH、共存离子等对反应降解效果的影响和降解动力学。所有的试验重复3次。
1.2.2 毒性评估试验
本试验的采抗菌性和毒性由大肠杆菌(ATCC 25922)作为参考菌株进行测试,细菌在37.5℃的肉汤培养基中培养24h,而后稀释涂布,进而得出在最适宜梯度下的菌落数,稀释过程中使用振荡器振荡3min,以保证菌液和水可以完全混合,所有试验器材均在120℃的高压灭菌锅灭菌后使用。选用稀释倍数为106和107,显微镜观察大肠杆菌在K2FeO4氧化RNTD和RXTD过程中菌落的变化。
1.3 分析方法
1.3.1 K2FeO4浓度的标定
K2FeO4浓度标定用ABST分光光度法。在25mL比色管中加入体积V1为1mL的2mmol/L的[ABST],加入5mL的ABST缓冲溶液(由0.6mol/L的乙酸和0.2mol/L的磷酸盐制成),取体积为V2的K2FeO4于比色管中后,定容摇匀取样后在415nm波长下测量吸光度值A1。同理,测定不含K2FeO4下的吸光度值A0,查知ABST+的摩尔吸光系数ε=3.4×104mol-1‧s-1。由此,K2FeO4的浓度[K2FeO4]可由式(1)求得。

1.3.2 目标污染物的测定
FMTD、RNTD、RXTD、CMTD、NZTD的浓度采用配备紫外检测器的高效液相色谱仪(HPLC,1260,Agilent Technology,USA)进行定量分析。使用ZORBAX SB-C18色谱柱(2.4mm×150mm×5μm)进行分离,洗脱方式为等度洗脱。FMTD、RNTD、RXTD、CMTD和NZTD的检测波长分别设置为208nm、242nm、218nm、218nm和315nm,流动相分别为V(甲醇)/V(水)=45/55、V(乙腈)/V(乙酸铵)=15/85、V(乙腈)/V(乙酸铵)=20/80、V(甲醇)/V(水)=40/60和V(乙腈)/V(乙酸铵)=20/80。所有目标污染物的进样量、柱温和流速分别为15μL、35℃和1.0mL/min,流动相中乙酸铵水溶液为50mmol/L。
1.4 反应动力学分析
K2FeO4降解HRAs的动力学方程如式(2)表示。

式中,kapp为表观速率常数,mol-1‧s-1;[HRAs]、[K2FeO4]分别为HRAs和K2FeO4的平衡浓度,μmol/L;n为HRAs的反应级数;m为K2FeO4的反应级数。
当反应体系中[K2FeO4]∶[HRAs]≥5∶1,可近似认为式(2)中的[K2FeO4]m为常数,则可简化成式(3)表示。

式中,kobs为一级反应速率常数,s-1,按式(4)计算。

半衰期按式(5)计算。

2 结果与讨论
2.1 K2FeO4投加量的影响
考察了不同K2FeO4投加量对HRAs降解的影响,结果如图2所示。不同浓度的K2FeO4降解HRAs呈现较高的一致性,即HRAs的降解效率随着K2FeO4投加量的增加而变高。特别地,在0.5mmol/L K2FeO4的投加量下,HRAs于0~90s内均迅速反应,除RXTD外,在300s时HRAs的降解率均达到98.4%,而RXTD降解率为59.4%。对所有HRAs的降解进行动力学分析,ln([HRAs]/[HRAs]0)与反应时间t的反应关系如图2所示,在0.5mmol/L K2FeO4投加量下均呈现良好的线性关系(R2>0.91),故可推出式(3)中的n=1,即K2FeO4对HRAs的降解满足一级反应动力学规律。再将lnkobs对ln[K2FeO4]0作图,其结果如图3所示,R2均大于0.96,可知两者也呈现明显的线性关系,故式(4)中的m=1。由此,m+n=2,表明K2FeO4与HRAs的反应符合二级动力学。

图2 不同K2FeO4投加量下HRAs的降解动力学

图3 不同HRAs中ln kobs与ln[K2FeO4]0的关系
与其他HRAs相比,RXTD没有硫醚键结构(图1),已有研究证实过一硫酸盐(PMS)可以攻击HRAs(除RXTD外)而生成亚砜产物[16],而K2FeO4可通过氧转移机制攻击含硫醚键的污染物而生成硫酸盐和亚砜产物[11,14,17-22]。另外,由于HRAs上芳香环中的取代基具有富电子特征且有较强的供电子作用[21,23-24]而能和K2FeO4快速反应,但RXTD含有的羧基结构为吸电子基团,会影响K2FeO4获取电子而降低其氧化性能。已有试验证明布洛芬、双氯芬酸和恩诺沙星等含有羧基结构的物质,二级反应速率常数明显低于磺胺类抗生素、环丙沙星和卡马西平等污染物[11]。综上,RXTD因结构中缺乏硫醚键,且含有吸电子基团的羧基结构,导致其降解速率远小于其他4种HRAs。
2.2 p H的影响
探究K2FeO4在不同pH的条件下对HRAs的降解情况,试验结果如图4所示。5类HRAs降解反应呈现较高的一致性,在体系pH为7、8时均符合一级反应动力学特性,相关系数R2>0.90。pH对K2FeO4的降解效果影响较大,在pH=7条件下HRAs的降解反应速率最高,半衰期最短,除RXTD外,去除率达到99%。其次是pH=6,碱性条件下降解速率最差,并且随着pH增大而减小。以FMTD为例,pH=6条件下去除率为76%,高于pH=8时64.8%和pH=9时42.2%的去除率。现有众多的报道表明,pH对K2FeO4降解污染物会产生较大的影响[17-18,24],反应速率通常随着pH的增加而降低,kapp与pH的相关性可以归因于K2FeO4和污染物形态的双重效应[21]。

图4 不同pH下HRAs的降解动力学

2.3 Cl-、HCO3-和HA的影响

图5 不同pH下高铁酸盐的形态分布

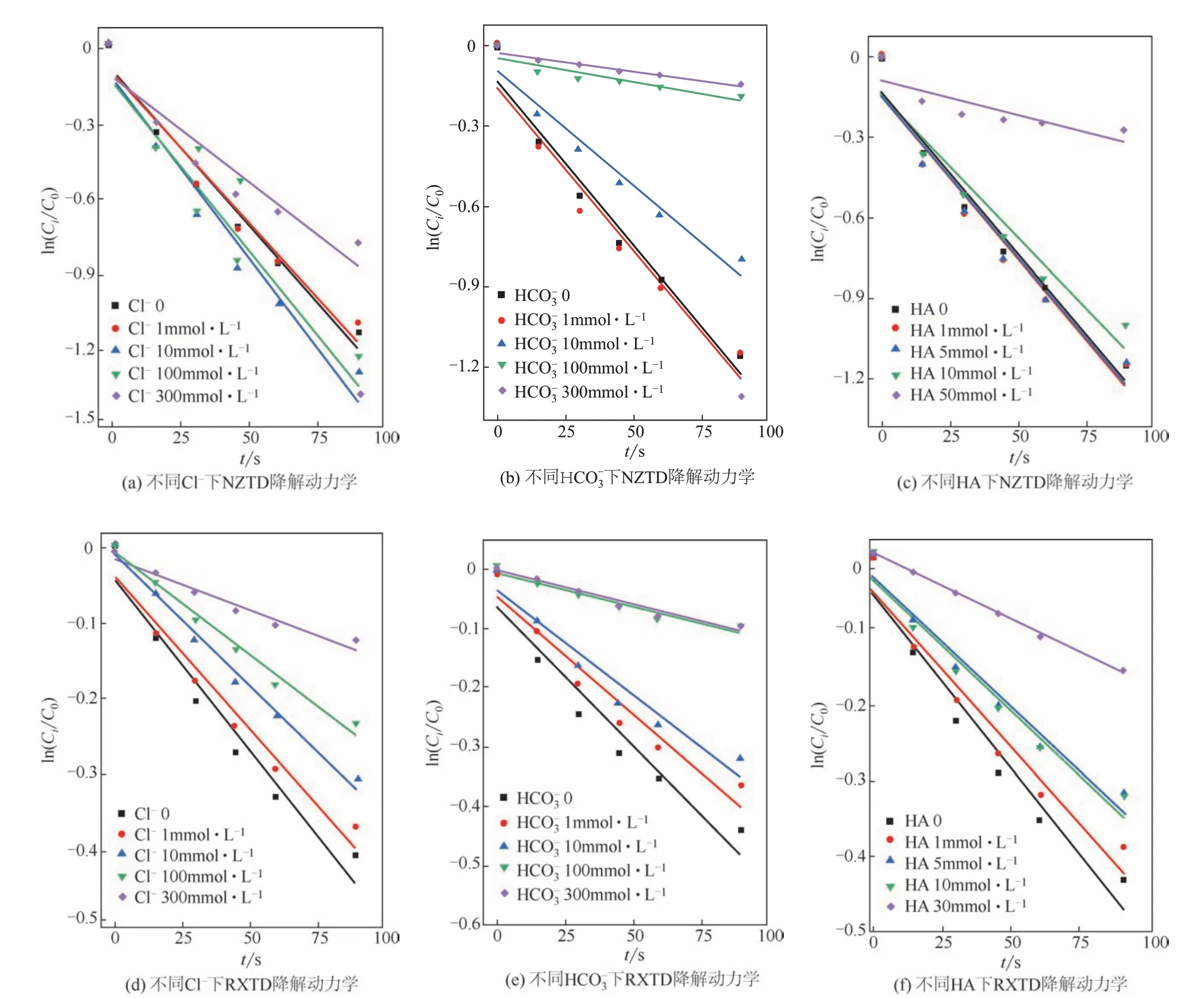
图6 Cl-、HCO3-和HA影响下NZTD和RXTD的降解动力学

2.4 实际水体中HRAs的降解
实际水样复杂的背景基质在不同程度上会影响氧化剂的氧化效果,本文选择实际二沉池出水、地表水以及模拟医院废水为背景水样,其水质组分分别见表1和表2。为考察K2FeO4在实际水体中对HRAs的去除效果,选用RNTD和RXTD作为目标污染物,研究其在不同水样中的降解效果,结果如图7所示。两者的降解均呈现出超纯水>地表水>二沉池出水>医疗废水。RNTD和RXTD在超纯水中的去除率分别为99%和46%,而在医疗废水中RNTD和RXTD的去除率分别为65%和20%。另外,相比于地表水,二沉池出水(RNTD和RXTD的降解率分别为85%和34%)对两个污染物的抑制降解效果更为明显,而地表水下的降解效果略差于超纯水。

图7 RNTD和RXTD在不同实际水样中的降解

表1 实际水样的性质
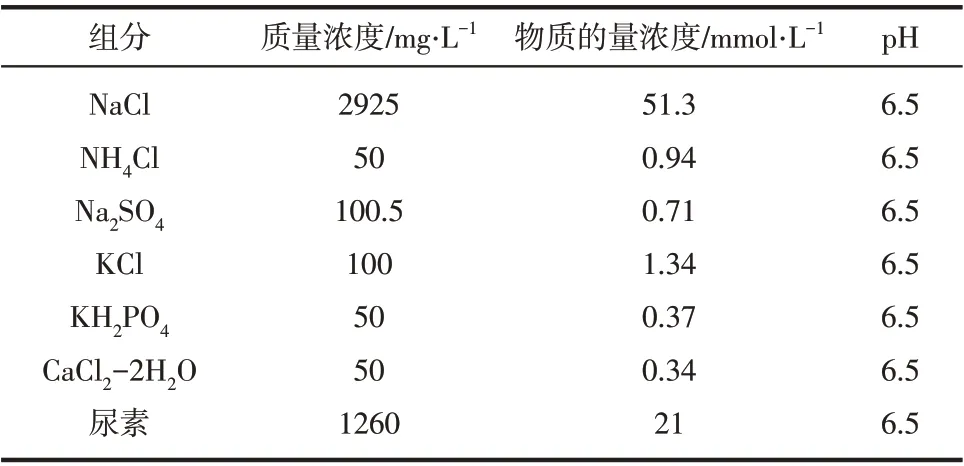
表2 医院废水组分
试验结果表明,K2FeO4在实际水体中能够对RNTD起到良好的去除作用,而RXTD因其本身不具有硫醚键和羧基结构,其降解效果较低。由于二沉池出水中含有的Cl-和溶解性有机质(DOC)浓度较高,因此抑制了HRAs的降解,相对地表水来说RNTD和RXTD的去除率均有所下降。医院废水中成分复杂,含盐量较高,因此在医院废水中RNTD和RXTD的降解受到的抑制率更高。实际水体中不同的水质成分对K2FeO4氧化降解污染物均会有一定的影响,因此K2FeO4作用的发挥仍需通过不同的控制条件优化来进一步提高效率。
2.5 HRAs降解过程中的毒性评估
为了进一步研究K2FeO4氧化HRAs及其产物的毒性变化,选用大肠杆菌的生长状况作为判断毒性的依据,结果如图8所示。在单独RNTD、RXTD样品中大肠杆菌的生长受到明显抑制,而当RNTD、RXTD被K2FeO4降解后,体系中大肠杆菌的生长得到极大促进。以稀释106倍下的RNTD组为例,在0~120s内,RNTD和K2FeO4/RNTD=50/1组的菌落数在70~90区间起伏,在120s时两者的菌落个数分别为75和76,数值相差不大。而单独RNTD组的细菌数量在150s后缓慢升高,这可能是体系中的K2FeO4被消耗完,在300s菌落个数仅为82。K2FeO4/RNTD=50/1的细菌在120s后生长快速,到300s菌落个数达到105。

图8 RNTD和RXTD氧化后对大肠杆菌毒性的变化
大肠杆菌的生长曲线进一步证实了RNTD、RXTD具有抗菌能力,且对体系中的微生物具有毒害作用,这对污水的生化处理也提出了挑战。K2FeO4具有强氧化性,在处理RNTD和RXTD等HRAs后反应体系抗菌活性显著降低,因此高铁酸盐作为绿色的水处理剂,能够广泛应用于污废水处理和饮用水安全保障。
3 结论
(1)HRAs的降解速率随着K2FeO4投加量的增大而加快,0~90s内符合二级反应动力学规律。在0.5mmol/L的K2FeO4投加量、pH=7条件下,0.01mmol/L的CMTD、RNTD、FMTD、NZTD能与K2FeO4充分反应,300s内降解率能达到99%。而RXTD由于不具有特殊的硫醚键以及羧基结构,降解率为59%。
(2)pH可以通过改变K2FeO4和HRAs的形态而影响HRAs的降解效果,降解反应速率为pH 7>pH 6>pH 8>pH 9。高浓度的HCO3-和HA对NZTD和RXTD的氧化降解具有抑制作用,低剂量Cl-对NZTD的降解具有轻微的促进作用。
(3)在不同实际水质中,RXTD和RNTD的降解受到不同程度的抑制,具体的降解效果呈现超纯水>地表水>二沉池出水>医疗废水。单独RNTD和RXTD对体系中的污染物具有毒害作用,经K2FeO4降解后体系毒性显著降低。
