颈椎后路椎板切除融合手术后相关并发症的独立风险因素
2021-08-13李国伟李文霞仝允辉王乐乐
李国伟,李文霞,仝允辉,王乐乐
(1.河南省洛阳正骨医院/河南省骨科医院,河南洛阳 471000;2.洛阳市栾川县人民医院骨科,河南洛阳 471500)
脊髓型颈椎病(cervical spondylotic myelopathy,CSM)是脊柱外科的常见病,患者以颈肩痛、头晕呕吐、上肢麻木无力乃至行走有踩棉花感等为主要表现[1],导致其功能受限、生活能力明显下降。在临床上,CSM的治疗方案有保守和手术治疗,但多数患者保守治疗效果较差,手术减压是解除脊髓压迫、缓解临床症状的主要手段[2]。颈椎后路椎板切除融合术(posterior cervical laminectomy and fusion,PCLF)是治疗多节段CSM的经典术式,患者术后的减压效果较好,颈椎功能障碍可获得良好改善,且重建了手术节段的稳定性。但据文献报道,约12.5%-16.9%的CSM患者接受PCLF术后出现相关并发症[3-5]。本研究试通过回顾性分析多节段CSM手术患者的相关资料,以确定PCLF术后30 d内出现并发症的潜在风险因素。
1 材料与方法
1.1 研究对象
共纳入2015年7月-2019年7月接受PCLF手术的多节段CSM患者196例,其纳入标准如下:①有四肢麻木无力、下肢行走时出现踩棉花感、胸部束带感等颈脊髓损害表现,X线片提示存在颈椎管前后径狭窄、椎体后缘骨质增生,MRI提示颈脊髓受压;②多节段CSM病变;③手术方式为PCLF;④临床资料齐全,无重大缺失。排除标准:①非CSM患者,如颈椎肿瘤或急性椎体骨折等;②采用颈前路手术或其他术式者;③临床和影像学资料缺失,围手术期记录不全者。
1.2 手术方法
患者全麻,俯卧于手术床上,以头架钉做头部固定后,常规行术野皮肤消毒和铺巾,作后正中切口,沿棘突切开皮肤、皮下组织和筋膜后,电刀将项韧带切开,加深切口并将椎板上肌肉剥离,向两侧牵开软组织,以尖嘴钳将拟减压节段的颈椎棘突两侧椎板于反折处开槽,术中注意以冰生理盐水冲洗以确保术野的脊髓处于低温条件下。将减压节段的黄韧带切开,并切除椎板、棘突,剔除软组织,将减压切除的自体骨制备成颗粒状备用。术野中可见病变节段的脊髓呈明显受压变细表现,脊髓搏动消失;减压后可见脊髓恢复搏动,且向后膨隆,受压解除。对神经根管作探查、扩大处理。将2根长度合适的钛棒预弯成形后,于减压节段两侧椎弓根各拧入螺钉,X线透视确认螺钉位置理想,将钛棒与螺钉连接固定并作后外侧植骨。确认钉棒固定稳固、无松动后,留置引流管,逐层缝合切口,术毕。患者术后应卧床休息1~2周,并以颈围保护1~3个月左右。
1.3 相关资料收集
(1)人口学资料:包括年龄,性别,吸烟状况(吸烟,从不吸烟,既往吸烟者)、保险类型(商业保险,医疗保险或未参保),以及是否为翻修手术,术前麻醉风险ASA分级。(2)神经功能:行走状态(可独立步行,需辅助步行,不能步行),是否存在运动障碍。(3)术前合并症情况:包括糖尿病,冠心病,精神障碍,慢性肾脏疾病,慢性肺部疾病。(4)术前用药情况:肌松剂,抗抑郁药、抗焦虑药,以及阿片类镇痛药的使用情况。(5)手术情况:包括融合椎体数,术中失血量,手术时间等。
1.4 并发症统计
统计患者术后30 d内的并发症发生情况,内科并发症包括:尿路感染、贫血、血栓事件、心律失常、心跳骤停、肺炎、败血症和死亡。外科并发症包括:术后吞咽困难、硬膜撕裂、手术部位感染、血肿形成、新的神经功能缺损、植入物移位和30 d内手术翻修等。总体并发症被定义为存在内科并发症、外科并发症或两者兼而有之。
1.5 研究方法
采用单因素分析和多因素回归分析确定术后并发症的预测因素。其中,单因素分析中,采用例数和百分率表示分类资料,采用卡方检验和Fisher精确检验进行分析;采用“均数±标准差”表示定量资料,采用t检验进行分析。多因素分析采用Logistic回归模型进行处理,得出其P值、OR值和95%CI范围。统计学工具采用SPSS 20.0软件,以P<0.05为差异有统计学意义。
2 结果
196例患者术后30 d内,共发生相关并发症51例,占比26.0%。急性失血性贫血7例(3.6%),尿路感染5例(2.6%),心律失常4例(2.0%),肺炎2例(1.0%),心脏骤停1例(0.5%),术后30 d内死亡1例(0.5%);术后新发神经功能缺损16例(8.2%)、硬膜囊撕裂11例(5.6%),切口感染7例(3.6%),3例(1.5%)内植物移位、需30 d内行翻修手术,其中6例同时合并有两种并发症。
将51例术后30 d内出现并发症者作为并发症组,另145例作为无并发症组。两组患者的行走状态、术前服用阿片类镇痛药和术中失血量、手术时间比较,差异均有统计学意义(P<0.05);两组的性别、年龄、吸烟、保险类型、翻修手术、术前ASA分级、合并症、术前其他用药情况和融合椎体数等资料比较,差异均无统计学意义(P>0.05),见表1。
对单因素分析中具备统计学意义的四项相关性因素进行赋值:行走状态(独立行走=1,辅助行走=2,不能行走=3),服用阿片类镇痛药(无=0,有=1),失血量和手术时间为连续数值。赋值后,引入Logistic回归模型进行多因素分析,表2提示:术前服用阿片类镇痛药(OR=5.150)、术中失血量(OR=4.872)、手术时间(OR=5.181)是术后30 d内出现并发症的独立风险因素;独立行走(OR=0.216)则是一项独立保护因素。

表1 术后并发症的单因素分析
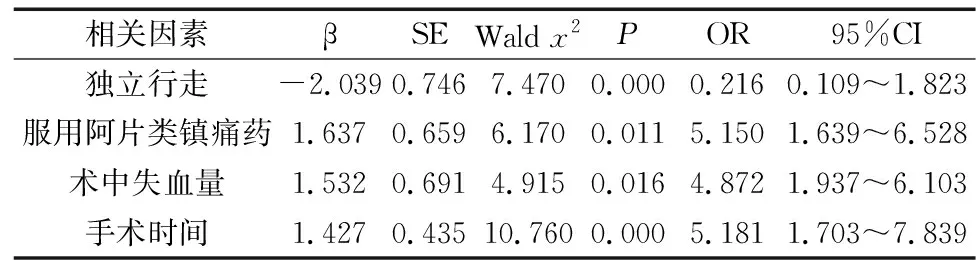
表2 Logistic回归分析
3 讨论
CSM是脊柱外科常见病,保守治疗对患者临床症状的缓解有限,当脊髓压迫较重或症状呈进行性加重时,临床一般建议尽早采取手术减压治疗[6-7]。PCLF是多节段CSM较为经典的后路手术方案,在确保多节段减压效果的同时,通过植骨内固定对颈椎局部稳定性进行了重建,远期疗效较好[8]。但据研究报道,PCLF术后可出现轴性疼痛、C5神经根麻痹和硬膜撕裂、内植物移位、切口或其他部位感染、急性失血性贫血等并发症[9-10]。本文中所见的总体发生率为26.0%,高于文献报道[11-12]。考虑原因为:作者将术后相关的急性失血性贫血、尿路感染、心律失常、肺炎等内科并发症也计算在内,导致总发生率偏高。上述并发症虽然为外科手术中的共有常见问题,然而PCLF术后亦无法避免,对患者的康复进程也存在明显影响,因此将其纳入探讨范畴亦实属必要。
本研究结果发现,术前服用阿片类镇痛药、术中失血量、手术时间均是独立的风险因素;独立行走则是一项独立保护因素。其中,阿片类镇痛药的OR=5.150,引起术后并发症的风险相对较高。Jain等[13]的研究证实,术前服用阿片类药物可导致腰椎融合术后并发症的风险增高8倍。同时研究认为,阿片类受体被激活可干扰血管生成,使中性粒细胞与巨噬细胞向手术部位募集的过程受到延迟和抑制,并影响切口愈合所必需的神经肽分泌[14-15],这可能是阿片类镇痛药对PCLF术后并发症产生独立影响的潜在机制。术中大量失血是脊柱围手术期并发症的公认危险因素[16-17],本研究中,术中失血量的OR=4.872,提示风险系数也相对较高。大量失血对术后并发症的不良影响可能通过以下途径实现:(1)影响心脏、肺和肾脏的供血状态,乃至对免疫系统造成不良影响,从而增加内科感染或心血管不良事件的风险;(2)术中大量失血是引起术后急性失血性贫血的主因之一;(3)此外,术中大量失血也提示手术造成的创伤性较大,术中引起硬膜撕裂或神经损伤等风险也较高。手术时间(OR=5.181)对PCLF术后的不良影响在于:手术时间较久,则术野的暴露时间久,可增加术后切口深部或浅部感染的风险;此外,手术时间较长则术中出血也相对较多,与前述观点中的术中失血量所致风险产生明显关联;另外,手术时间较长者,提示手术操作较复杂,增加了术中不当操作导致的相关并发症。
在本文中,步行状态是一项独立的保护因素,术前能独立步行则可使PCLF术后并发症的风险降低至0.216倍。既往研究也支持这一观点[18],该研究发现,术前行走障碍将增加脊柱手术后静脉血栓事件的发生风险;虽然行走功能障碍是CSM的一项典型症状,但也可能是患者体质虚弱的一项观察指标,此类人群术后易出现感染等并发症。另外,部分CSM导致行走障碍的患者常伴有神经源性膀胱功能障碍,虽然PCLF手术可减压脊髓神经受压,从而使膀胱功能得以恢复,但若术后不完全减压可能导致残留排便障碍,增加术后尿路感染的概率。
综上所述,术前服用阿片类镇痛药和术中大量失血、手术时间较长,均是PCLF术后30 d内并发症的风险因素;术前给予“阿片类药物洗脱”,提高手术熟练度、尽量减少手术时间和注意降低出血量,将有助于减少并发症的发生。此外,术前独立步行是降低术后并发症发生率的有利因素,对于术前存在步行功能障碍者,制定合理的术后康复计划可能是一项有益措施。
