缺碳预还原MoO3+氢气深脱氧工艺制备超细钼粉
2021-08-13张国华周国治
张 勇,张国华,周国治
北京科技大学钢铁冶金新技术国家重点实验室,北京 100083
钼是目前应用最广泛的难熔金属之一。由于钼及钼合金具有高熔点(2610 ℃)、高强度、低热膨胀系数等一系列优良性质,在电子、冶金、航空航天和电气工业等领域被广泛应用[1-4]。由于钼的熔点较高,以钼粉为原料的粉末冶金法成为生产钼及其合金的主要方法。根据Hall-Petch理论[5-6],金属颗粒细化可以显著改善合金的强度、硬度、耐磨性等力学性能。相比于微米钼粉,超细/纳米钼粉具有更高的烧结活性,可以在较低的温度下烧结成高相对密度的细晶材料。比如纳米钼粉可以在1200 ℃烧结1 h得到相对密度为95%的样品,烧结后晶粒的粒径为1.4 μm,而微米钼粉需要在1500 ℃的高温下保温3 h才能达到同样的相对密度,且烧结后晶粒的粒径为6.2 μm[7]。因此,超细/纳米钼粉的制备显得尤为重要。
目前,工业上制备钼粉的主要工艺是两段氢还原MoO3[8-9]。首先在600~700 ℃将MoO3还原为MoO2,然后在800~1100 ℃将MoO2还原为高纯Mo粉。该方法制备的钼粉虽纯度高,但氢还原过程中会生成气相中间产物MoO2(OH)2,导致钼颗粒可以通过化学气相迁移机理生长,因此使用该方法难以制备出超细钼粉[10-13]。而碳热还原工艺可以制备超细钼粉,但却存在难以精准控制碳含量的问题[14-16]。这是由于碳热还原过程既会产生CO2,又有CO,且两者比例受温度、料层厚度、气流等因素的影响,导致无法精准配碳,从而使得使用该方法制备的钼粉碳含量较高[14]。
本课题组一直致力于超细/纳米钼粉的研究。Wang等[2,17-18]以工业MoO3为原料,采用高温升华-低温冷凝法制备出了超细球形单晶β-MoO3,然后在440~560 ℃氢气气氛下制备出了超细MoO2,最后通过在590~800 ℃氢气还原超细MoO2制备出纳米钼粉。Wang等[19]考虑到高温下MoO3可以以蒸气的形式存在,在950 ℃直接通过氢气还原MoO3蒸汽也成功制备了纳米钼粉。基于辅助形核的思路,研究者通过在MoO2中以“喷雾法”掺杂少量碱金属的碳酸盐、氯盐[3,20-22],或者加入少量超细钼粉作为核心[23],通过氢气还原也实现了超细钼粉的制备。由于碳还原工艺具有生产成本低、产品粒度细等优点,Sun等[13,24-25]提出了“缺碳预还原+氢气深脱氧”工艺制备超细钼粉,即先缺碳还原MoO3制备出含有少量MoO2的Mo粉,之后在氢气气氛下对剩余的MoO2进行还原。Sun[25]利用该工艺,以炭黑作为碳源,通过热分析仪作为实验设备,系统研究了炭黑与MoO3的反应过程和机理以及不同钼源(MoO3和MoO2)对钼产品的影响,制备出残碳量(质量分数)为0.02%的纳米钼粉。温度对碳热还原钼粉的粒度和纯度具有重要影响,温度越低,钼粉粒度越细,但是残余碳含量(质量分数)越高。为了制备高质量的超细钼粉,很有必要研究较低还原温度下产物情况。本文在更大的温度范围内(950、1000、1100、1150 ℃)详细研究了温度和配碳量(C/MoO3摩尔比)对还原过程及产物的影响规律。
1 实验材料及方法
实验所用原料为商业MoO3(纯度大于99.9%,金堆城钼业股份有限公司)和炭黑(MA100,三菱化工)。MoO3原料的X射线衍射(X-ray diffraction,XRD)分析和扫描电子显微镜(scanning electron microscopy,SEM)形貌如图1(a)和图1(b)所示,其中MoO3平均粒径为1.45 μm。图1(c)是炭黑的显微形貌,其平均粒径为24 nm。实验装置示意图如图2所示,具体实验过程如下:首先将MoO3与炭黑混合40 min,得到均匀的混合物,如图1(d)所示,其中C/MoO3摩尔比为2.1、2.2、2.3;将混合后的样品取出5 g装入氧化铝坩埚,放置于石英管中,通入氩气(400 mL/min)排净空气;将石英管放入炉内恒温区,并以5 ℃/min的升温速率先加热到600 ℃并保温1 h,之后继续加热到目标温度(950~1150 ℃)并保温2 h,待石英管冷却后取出还原产物。氢气深脱氧阶段是将预还原的Mo粉在800 ℃下氢气气氛中(200 mL/min)保温1.5 h。
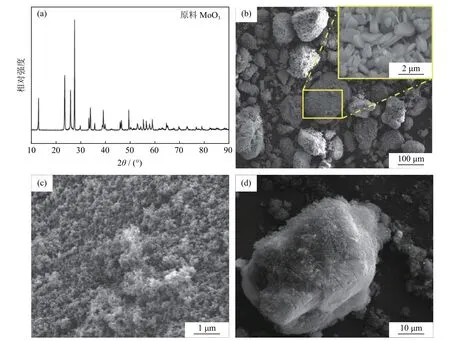
图1 原料XRD分析和微观形貌:(a)MoO3XRD分析;(b)MoO3显微形貌;(c)炭黑显微形貌;(d)MoO3和炭黑混合物显微形貌Fig.1 XRD patterns and SEM images of the raw materials: (a)XRD pattern of MoO3;(b)SEM image of MoO3;(c)SEM image of carbon black;(d)SEM image of MoO3 and carbon black mixture

图2 实验装置示意图Fig.2 Schematic diagram of the experimental apparatus
利用X射线衍射仪(Model TTRIII,Rigaku,Japan)对还原产物物相进行分析。通过场发射扫描电子显微镜对碳还原和氢还原产物的形貌进行表征(ZEISS SUPRA 55,Germany)。使用红外碳-硫分析仪(EMIA-920 V2,HORIBA,Japan)测定了氢还原产物的残余碳含量(质量分数)。采用纳米粒度分析软件(Nano-measurer)对产物的粒度进行测定。每个样品用3张电镜图片进行粒度测量,每张图片至少测量100个晶粒。
2 实验结果
2.1 碳热预还原过程
图3所示是不同C/MoO3摩尔比的样品在不同还原温度下反应产物的X射线衍射分析。从图3(a)可以看到,当还原温度为950 ℃、C/MoO3比为2.0时,产物为MoO2和Mo;随着C/MoO3比增加到2.1时,产物依然只有MoO2和Mo两种衍射峰存在,但MoO2的衍射峰强度减小;当C/MoO3比增加到2.2时,MoO2的衍射峰消失,物相变为Mo和Mo2C。图3(b)为还原温度1000~1150 ℃下制备产物的X射线衍射分析,其主要趋势和图3(a)一致,当C/MoO3摩尔比从2.0增加到2.1时,MoO2的衍射峰强度减弱;当C/MoO3摩尔比为2.1时,不同还原温度下产物的MoO2衍射峰强度几乎相同。
图4所示是在不同C/MoO3摩尔比和还原温度下碳热还原产物的显微形貌。图4(c)所示产物的形貌有所不同,除了Mo以外还出现了粒径更小的Mo2C纳米颗粒,这与图3中X射线衍射分析结果一致。其他条件下产物的形貌没有很大不同,所制备的颗粒均匀细小并具有很好的分散性。当C/MoO3摩尔比为2.1时,产物的平均粒径随着温度的升高而有所增加。在同一还原温度下,C/MoO3摩尔比从2.0增加到2.1时,产物的粒径变化很小。
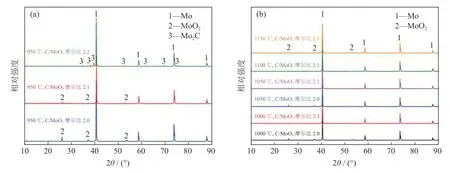
图3 碳热还原产物X射线衍射分析Fig.3 XRD patterns of the carbothermic reduction products

图4 不同温度和不同C/MoO3摩尔比的碳热还原产物显微形貌:(a)950 ℃,2.0;(b)950 ℃,2.1;(c)950 ℃,2.2;(d)1000 ℃,2.0;(e)1000 ℃,2.1;(f)1050 ℃,2.0;(g)1050 ℃,2.1;(h)1100 ℃,2.1;(i)1150 ℃,2.1Fig.4 SEM images of the carbothermic reduction products at different temperatures and C/MoO3 ratios by mole: (a)950 ℃,2.0;(b)950 ℃,2.1;(c)950 ℃,2.2;(d)1000 ℃,2.0;(e)1000 ℃,2.1;(f)1050 ℃,2.0;(g)1050 ℃,2.1;(h)1100 ℃,2.1;(i)1150 ℃,2.1
2.2 氢气深脱氧过程
图5是预还原Mo粉在800 ℃下氢气深度还原1.5 h后X射线衍射分析和显微形貌。产物的X射线衍射分析如图5(a)所示,可以看到产物的物相都是Mo,说明经过氢气还原后,样品已经被完全还原成金属Mo。图5(b)所示的是氢还原后产物平均粒径,当温度为950 ℃时,随着C/MoO3摩尔比从2.0增加到2.1,钼粉的平均粒径从99 nm增加到100 nm。当温度增加到1000 ℃和1050 ℃时,随着C/MoO3摩尔比从2.0增加到2.1,钼粉的平均粒径分别从115 nm增加到117 nm、141 nm增加到142 nm。当C/MoO3摩尔比由2.0增加到2.1时,产物粒径的增加不明显。当C/MoO3摩尔比都为2.1时,随着温度从950 ℃增加到1150 ℃,此时Mo颗粒的平均粒径分别为100、117、142、177和190 nm。因此,温度对产物粒径的影响更显著,这与碳热还原的结果是一致的。当C/MoO3摩尔比为2.1时,在950 ℃碳还原和800 ℃氢气还原之后,Mo粉残碳量(质量分数)为0.030%;当碳热还原温度增加到1150 ℃时,钼粉的残碳量可以降低到0.009%。
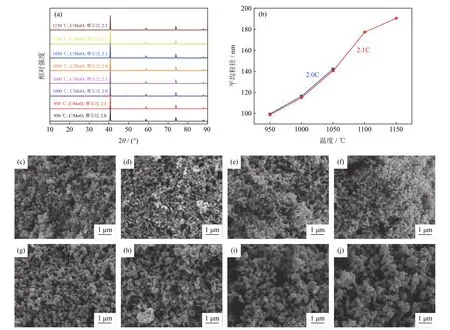
图5 不同温度和不同C/MoO3摩尔比的氢气还原产物X射线衍射分析、平均粒径及显微形貌:(a)X射线衍射分析;(b)平均粒径;(c)950 ℃,C/MoO3摩尔比2.0产物显微形貌;(d)950 ℃,C/MoO3摩尔比2.1产物显微形貌;(e)1000 ℃,C/MoO3摩尔比2.0产物显微形貌;(f)1000 ℃,C/MoO3摩尔比2.1产物显微形貌;(g)1050 ℃,C/MoO3摩尔比2.0产物显微形貌;(h)1050 ℃,C/MoO3摩尔比2.1产物显微形貌;(i)1100 ℃,C/MoO3摩尔比2.1产物显微形貌;(j)1150 ℃,C/MoO3摩尔比2.1产物显微形貌;
3 分析与讨论
3.1 热力学分析
Sun等[25]指出MoO3的碳热还原包含三个阶段:MoO3→MoO2→MoO2+Mo2C→Mo。在第一个阶段,MoO3被直接还原为MoO2,如式(1)所示。第二阶段的主要反应如式(2)~(4)所示。当C/MoO3摩尔比为2.0和2.1时,反应物中剩余的炭黑会继续与MoO2反应,如式(2)所示,从而生成稳定的Mo2C。本工艺在碳还原之后保留少量的MoO2,是为了将Mo2C全部消耗掉,从而降低产物中残余碳含量。在1个标准大气压下,根据热力学分析可知,MoO2和Mo2C只能在温度高于1090 ℃才会发生反应[24-25],而在本文950 ℃温度下就已经反应生成Mo。其原因是反应生成的CO被流动的氩气(400 mL/min)带走,从而导致CO分压相对较低,使得MoO2和Mo2C即便在较低的温度下也可以发生反应。随着温度的升高,式(4)进行的更加彻底,因此随着温度升高,产物的残碳量更低。

3.2 形核和生长机理分析
图6所示的是炭黑还原MoO3制备超细钼粉的反应机理。制备超细钼粉的关键是调控钼的形核以获得足够多分散的核心,并控制核心的生长[3,13,23,25]。纯氢气还原氧化钼时,不可避免的生成水蒸气和气相水合物MoO2(OH)2,当MoO2(OH)2浓度较高时,形成的钼晶核可以通过化学气相迁移的方式进行生长,导致制备的钼粉粒度较大[10-13]。而炭黑作为还原剂,避免了MoO2(OH)2的形成,限制了钼原子的迁移。炭黑粒径小(24 nm),当MoO3与炭黑均匀混合后,大量的炭黑纳米颗粒为碳热反应提高了许多形核点,从而形成了大量的MoO2纳米片。在MoO2形成之后,会继续与剩余的炭黑形成粒径更小的Mo2C,直到炭黑完全消耗。形成的Mo2C纳米颗粒和剩余的MoO2纳米片将会反应生成Mo晶核。在从MoO2纳米片、Mo2C纳米颗粒到Mo颗粒的形成过程中,由于没有气体传输相的存在,产物只能依靠原子沉积的方式生长。但随着反应的进行和反应界面的远离,Mo颗粒的生长将会受到限制。如表1所示,MoO3和Mo的摩尔体积分别为30.68 cm3/mol和9.41 cm3/mol,随着反应的进行,在还原过程中体积的减少和碳的消耗,将在形成的产物间形成大量的空隙,使得粉体疏松,颗粒之间难以烧结长大。

图6 炭黑还原MoO3机理示意图Fig.6 Schematic diagram of the MoO3 reduction by carbon black
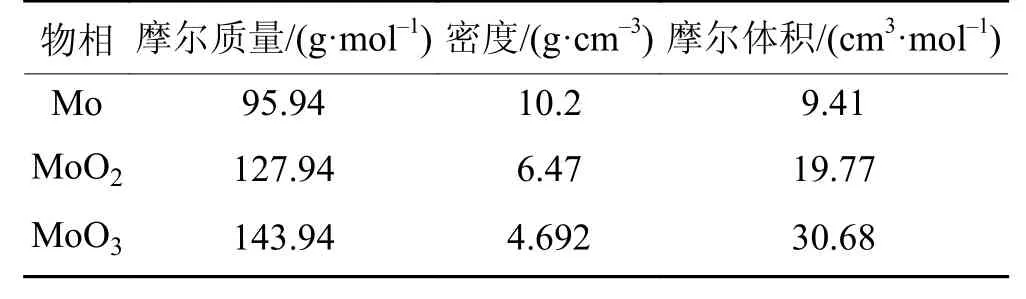
表1 Mo、MoO2和MoO3的基本物理性能参数[8,17-18]Table 1 Physical property parameters of Mo,MoO2,and MoO3
在随后的氢气还原阶段,因为预还原的Mo粉中仅剩少量的MoO2,还原生成的Mo核很难通过化学气相迁移的方式生长成很大的Mo颗粒。大量Mo超细颗粒的存在,也可以在反应时作为形核点[13,23],因此氢还原对后续Mo粉平均粒径的影响并不显著。
4 结论
以炭黑和MoO3为原料,采用“缺碳预还原+氢气深脱氧”工艺成功制备出了粒径在99~190 nm超细钼粉,研究配碳量和温度等因素对还原过程、产物粒度和残碳量的影响。
(1)当C/MoO3摩尔比为2.0和2.1时,碳热还原产物为Mo和MoO2;C/MoO3摩尔比增加到2.2时,产物变为Mo和Mo2C。
(2)在同一还原温度下,C/MoO3摩尔比从2.0增加到2.1时,对产物的粒径的影响不明显。
(3)碳热还原温度对产物粒径有显著影响,当C/MoO3摩尔比为2.1时,随着还原温度从950 ℃增加到1150 ℃,氢还原产物的平均粒径从100 nm增加到190 nm,且残碳量(质量分数)由0.030%降低到0.009%。
